2023年中考化学专题复习课件(04) 工艺流程题(共31张PPT)(鲁教版)
文档属性
| 名称 | 2023年中考化学专题复习课件(04) 工艺流程题(共31张PPT)(鲁教版) |

|
|
| 格式 | pptx | ||
| 文件大小 | 600.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-29 00:00:00 | ||
图片预览







文档简介
(共31张PPT)
专题(四) 工艺流程题
工艺流程题的特点是给出某个生产实际问题的解决流程,把书本知识糅合在整个流程中对学生进行考查。题目有的以操作名称作为框图形成流程主线,有的以物质作框,有的以设备作框。最常见的是以操作名称为主线,物质随着操作流程发生变化。题目中通常还包含简单的实验设计,一般为物质的制备、提纯或对样品的定性、定量分析实验。
1.资源背景
(1)海水资源:海水制盐、氯碱工业、海水提镁等。
(2)制碱与石灰石工业。
(3)空气资源:合成氨工艺流程等。
(4)矿产资源:冶炼钢铁、制取铜等。
(5)化石燃料:有机合成工艺。
(6)化工(实验)废液:提取金属或盐等
2.考查内容
(1)化学反应原理(化学方程式的书写及反应类型)。
(2)实验操作的名称及要点(过滤、蒸发、结晶等)。
(3)流程中的物质转化与循环。
(4)工艺流程评估及改进。
3.方法点拨
(1)步骤:读正文,找信息,明确目的;精读流程,弄懂原理,理解操作;先局部,后全盘,逐步深入。
(2)涉及混合物的除杂、分离、提纯等有关实验基础知识及操作时,要认真在流程图中找到主要物质和混有的杂质,分析当加入某一试剂后能与什么物质反应,产物是什么,用什么方法才能除去杂质,真正理解每步所加试剂或操作的目的。
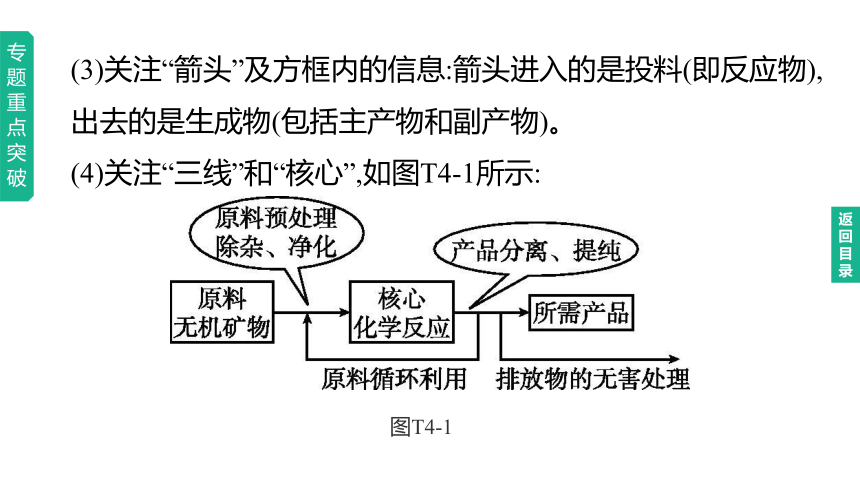
(3)关注“箭头”及方框内的信息:箭头进入的是投料(即反应物),出去的是生成物(包括主产物和副产物)。
(4)关注“三线”和“核心”,如图T4-1所示:
图T4-1
角度1 粗盐提纯 (8年1考,2021.12)
例1 [2022·重庆B]重庆多地都曾出现过盐井,从天然盐井水中获取的粗盐(含泥沙、CaCl2、MgCl2、
Na2SO4等杂质)。为除去以上杂质
得到精盐,小明设计如下实验:
提示:杂质含量较少,不考虑
微溶物形成沉淀。
类型一
提纯回收类
图T4-2
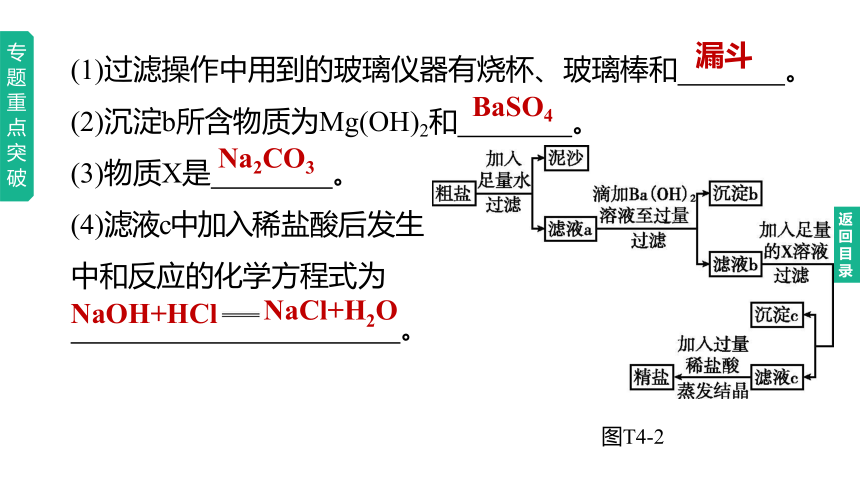
(1)过滤操作中用到的玻璃仪器有烧杯、玻璃棒和 。
(2)沉淀b所含物质为Mg(OH)2和 。
(3)物质X是 。
(4)滤液c中加入稀盐酸后发生
中和反应的化学方程式为
。
图T4-2
漏斗
BaSO4
Na2CO3
NaOH+HCl
NaCl+H2O
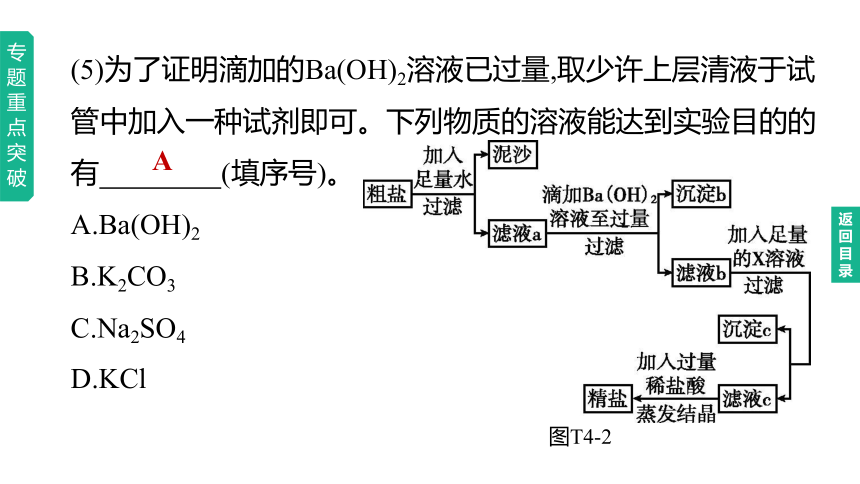
(5)为了证明滴加的Ba(OH)2溶液已过量,取少许上层清液于试管中加入一种试剂即可。下列物质的溶液能达到实验目的的有 (填序号)。
A.Ba(OH)2
B.K2CO3
C.Na2SO4
D.KCl
图T4-2
A
角度2 海水制镁 (8年2考,2021.12/2018.13)
例2 [宿迁]海洋是人类巨大的资源宝库。图T4-3为从海水中提取金属镁的简易流程图。
请回答下列问题。
(1)海洋中含量最多的
物质是 。
(2)实验室中进行操作Ⅰ时,
玻璃棒的作用是 。
图T4-3
水
引流
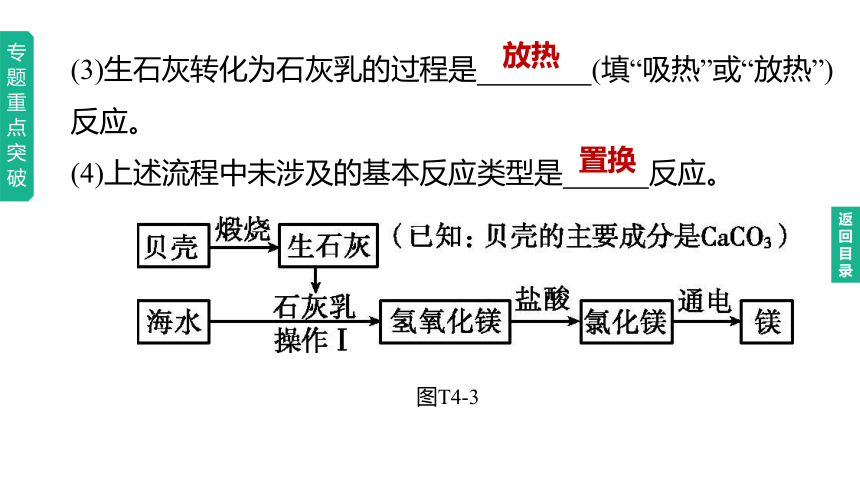
(3)生石灰转化为石灰乳的过程是 (填“吸热”或“放热”)反应。
(4)上述流程中未涉及的基本反应类型是 反应。
图T4-3
放热
置换
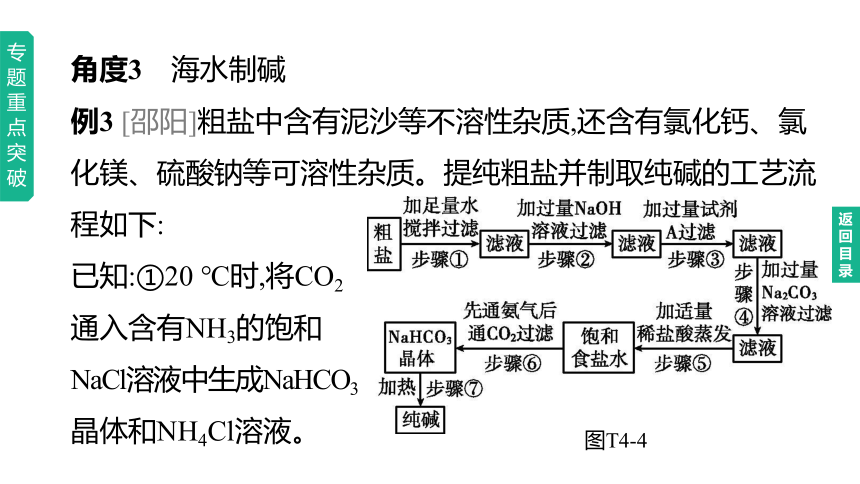
角度3 海水制碱
例3 [邵阳]粗盐中含有泥沙等不溶性杂质,还含有氯化钙、氯化镁、硫酸钠等可溶性杂质。提纯粗盐并制取纯碱的工艺流程如下:
已知:①20 ℃时,将CO2
通入含有NH3的饱和
NaCl溶液中生成NaHCO3
晶体和NH4Cl溶液。
图T4-4
②20 ℃时,几种物质在水中的溶解度:
物质 NaCl NH4Cl NaHCO3
溶解度/g 36.0 37.2 9.6
请根据上述题中有关信息,回答下列问题。
(1)步骤③中加入试剂A的化学式是__________。
(2)步骤④中加入过量Na2CO3溶液的目的是_______________
___________。
BaCl2
除去氯化钙和过
量的氯化钡
(3)在步骤⑥反应中,有NaHCO3晶体析出,而没有NH4Cl和NaCl析出的原因是_____________________________。
(4)步骤⑦中NaHCO3转化为纯碱的化学反应方程式是2NaHCO3 Na2CO3+
CO2↑+H2O,该化学反应
属于 (填基本
反应类型)反应。
20 ℃时,碳酸氢钠的溶解度最小
分解
角度4 金属化合物的回收
例4 某工厂的废水中含有MgSO4和FeCl3,技术人员逐渐加入NaOH溶液调节废水的pH,先后分离出两种沉淀,并通过系列处理得到有价值的产品。操作流程如图T4-5所示。
图T4-5
(1)固体A与某酸反应的化学方程式为____________________
。操作②时,当 即可停止加热。
图T4-5
Mg(OH)2+H2SO4
MgSO4+2H2O
蒸发皿中出现大量固体时
(2)固体B加热的产物是两种常见氧化物,则另一种氧化物的化学式为 。
(3)溶液a除了可能含有NaOH外,还一定含有的溶质是_______
______(填化学式)。
图T4-5
H2O
NaCl
Na2SO4、
角度1 单质的制备
例5 [2022·贵港]“太阳能光伏发电”能有效推进“碳中和”,发展“低碳经济”,其关键的材料是高纯硅。以下是高纯硅的简易生产流程。
类型二
制备类
图T4-6
请回答:
(1)石英砂的主要成分是 。四氯化硅(SiCl4)中硅元素的化合价为 。
(2)“精馏”是蒸馏的一种,其原理是利用混合物各成分的 不同,将物质分离出来。
二氧化硅
+4
图T4-6
沸点
(3)上述流程中可循环使用的物质是 。
(4)流程⑤中发生反应的化学方程式为____________________
。
图T4-6
HCl和H2
SiHCl3+H2 Si+
3HCl
角度2 化合物的制备 (8年1考,2015.12)
例6 [2022·深圳]某科学兴趣小组,用废渣(主要为CaCO3,还含有C、Fe2O3、MgO等少量杂质)制作CaCl2,反应过程如图T4-7所示。
(1)Ⅰ过程中加过量稀盐酸的目的是__________________________
__________。
图T4-7
使碳酸钙、氧化铁、氧化镁
完全反应
(2)Ⅰ过程中MgO发生反应的化学反应方程式为____________
,此反应为 (填基本反应类型)反应。
(3)滤渣一的成分为 (填化学式)。
图T4-7
MgO+2HCl
MgCl2+H2O
复分解
C
(4)X溶液为 (填化学式)溶液。
(5)NaCl在生活中的用处: (写一例)。
(6)已知CaCl2与焦炭、BaSO4在高温下生成BaCl2、CO和CaS,写出该反应的化学方程
式:_________________
。
图T4-7
NaOH
用作调味品(合理即可)
CaCl2+4C+BaSO4
BaCl2+4CO↑+CaS
角度3 化工生产 (8年1考,2021.12)
例7 [2022·广西北部湾]某工厂生产高锰酸钾的流程如图T4-8所示。请回答下列问题。
图T4-8
(1)“混合加热室”发生的主要是 (填“物理变化”或“化学变化”)。
(2)“电解室”反应中,反应前后化合价发生变化的元素有______
(写元素符号)。
图T4-8
物理变化
Mn、H
(3)生产流程中可循环利用的物质是 (写化学式)。
(4)写出氧化室中发生反应的化学方程式:_________________
。
图T4-8
KOH
2MnO2+4KOH+O2
2K2MnO4+2H2O
(5)取47.4 g高锰酸钾,加热一段时间后停止,共收集到3.2 g氧气。计算剩余固体中氧元素的质量分数是 (计算结果保留到0.1%)
图T4-8
36.2%
例8 [2022·沈阳]合成氨是人类科学技术上的一项重大突破,对社会发展与科技进步作出了巨大贡献。合成氨工艺的主要流程如图T4-9:
(1)合成塔中的反应在高温、高压、催化剂条件下进行,其化学方程式是 。
(2)上述反应中,一定发生改变的
是 (填序号)。
A.元素种类 B.分子种类
C.原子种类
图T4-9
N2+3H2
2NH3
B
(3)生产过程中可循环使用的物质是 。
(4)根据表中的数据回答问题。
物质 H2 N2 NH3
沸点/℃(1.01×105 Pa) -252 -195.8 -33.35
在1.01×105 Pa时,要将工业合成氨的产物氨气(NH3)从它的反应物氮气和氢气的混合物中分离开来,最适宜的温度应该控制在 ℃≤T< ℃。
N2、H2
-195.8
-33.35
例9 [宿迁]燃煤产生的烟气中含有二氧化硫,二氧化硫会形成酸雨污染环境。科研小组设计利用海水除去二氧化硫,工艺流程如图T4-10:
类型三
环境污染类 (8年1考,2016.13)
请回答下列问题。
(1)二氧化硫中硫、氧元素的质量比m(S)∶m(O)= 。
图T4-10
1∶1
(2)亚硫酸(H2SO3)能被空气中的氧气氧化为硫酸,写出反应的化学方程式: 。
(3)用熟石灰中和稀硫酸是利用了熟石灰的 (填序号)。
A.酸性 B.碱性 C.氧化性
图T4-10
2H2SO3+O2
2H2SO4
B
专题(四) 工艺流程题
工艺流程题的特点是给出某个生产实际问题的解决流程,把书本知识糅合在整个流程中对学生进行考查。题目有的以操作名称作为框图形成流程主线,有的以物质作框,有的以设备作框。最常见的是以操作名称为主线,物质随着操作流程发生变化。题目中通常还包含简单的实验设计,一般为物质的制备、提纯或对样品的定性、定量分析实验。
1.资源背景
(1)海水资源:海水制盐、氯碱工业、海水提镁等。
(2)制碱与石灰石工业。
(3)空气资源:合成氨工艺流程等。
(4)矿产资源:冶炼钢铁、制取铜等。
(5)化石燃料:有机合成工艺。
(6)化工(实验)废液:提取金属或盐等
2.考查内容
(1)化学反应原理(化学方程式的书写及反应类型)。
(2)实验操作的名称及要点(过滤、蒸发、结晶等)。
(3)流程中的物质转化与循环。
(4)工艺流程评估及改进。
3.方法点拨
(1)步骤:读正文,找信息,明确目的;精读流程,弄懂原理,理解操作;先局部,后全盘,逐步深入。
(2)涉及混合物的除杂、分离、提纯等有关实验基础知识及操作时,要认真在流程图中找到主要物质和混有的杂质,分析当加入某一试剂后能与什么物质反应,产物是什么,用什么方法才能除去杂质,真正理解每步所加试剂或操作的目的。
(3)关注“箭头”及方框内的信息:箭头进入的是投料(即反应物),出去的是生成物(包括主产物和副产物)。
(4)关注“三线”和“核心”,如图T4-1所示:
图T4-1
角度1 粗盐提纯 (8年1考,2021.12)
例1 [2022·重庆B]重庆多地都曾出现过盐井,从天然盐井水中获取的粗盐(含泥沙、CaCl2、MgCl2、
Na2SO4等杂质)。为除去以上杂质
得到精盐,小明设计如下实验:
提示:杂质含量较少,不考虑
微溶物形成沉淀。
类型一
提纯回收类
图T4-2
(1)过滤操作中用到的玻璃仪器有烧杯、玻璃棒和 。
(2)沉淀b所含物质为Mg(OH)2和 。
(3)物质X是 。
(4)滤液c中加入稀盐酸后发生
中和反应的化学方程式为
。
图T4-2
漏斗
BaSO4
Na2CO3
NaOH+HCl
NaCl+H2O
(5)为了证明滴加的Ba(OH)2溶液已过量,取少许上层清液于试管中加入一种试剂即可。下列物质的溶液能达到实验目的的有 (填序号)。
A.Ba(OH)2
B.K2CO3
C.Na2SO4
D.KCl
图T4-2
A
角度2 海水制镁 (8年2考,2021.12/2018.13)
例2 [宿迁]海洋是人类巨大的资源宝库。图T4-3为从海水中提取金属镁的简易流程图。
请回答下列问题。
(1)海洋中含量最多的
物质是 。
(2)实验室中进行操作Ⅰ时,
玻璃棒的作用是 。
图T4-3
水
引流
(3)生石灰转化为石灰乳的过程是 (填“吸热”或“放热”)反应。
(4)上述流程中未涉及的基本反应类型是 反应。
图T4-3
放热
置换
角度3 海水制碱
例3 [邵阳]粗盐中含有泥沙等不溶性杂质,还含有氯化钙、氯化镁、硫酸钠等可溶性杂质。提纯粗盐并制取纯碱的工艺流程如下:
已知:①20 ℃时,将CO2
通入含有NH3的饱和
NaCl溶液中生成NaHCO3
晶体和NH4Cl溶液。
图T4-4
②20 ℃时,几种物质在水中的溶解度:
物质 NaCl NH4Cl NaHCO3
溶解度/g 36.0 37.2 9.6
请根据上述题中有关信息,回答下列问题。
(1)步骤③中加入试剂A的化学式是__________。
(2)步骤④中加入过量Na2CO3溶液的目的是_______________
___________。
BaCl2
除去氯化钙和过
量的氯化钡
(3)在步骤⑥反应中,有NaHCO3晶体析出,而没有NH4Cl和NaCl析出的原因是_____________________________。
(4)步骤⑦中NaHCO3转化为纯碱的化学反应方程式是2NaHCO3 Na2CO3+
CO2↑+H2O,该化学反应
属于 (填基本
反应类型)反应。
20 ℃时,碳酸氢钠的溶解度最小
分解
角度4 金属化合物的回收
例4 某工厂的废水中含有MgSO4和FeCl3,技术人员逐渐加入NaOH溶液调节废水的pH,先后分离出两种沉淀,并通过系列处理得到有价值的产品。操作流程如图T4-5所示。
图T4-5
(1)固体A与某酸反应的化学方程式为____________________
。操作②时,当 即可停止加热。
图T4-5
Mg(OH)2+H2SO4
MgSO4+2H2O
蒸发皿中出现大量固体时
(2)固体B加热的产物是两种常见氧化物,则另一种氧化物的化学式为 。
(3)溶液a除了可能含有NaOH外,还一定含有的溶质是_______
______(填化学式)。
图T4-5
H2O
NaCl
Na2SO4、
角度1 单质的制备
例5 [2022·贵港]“太阳能光伏发电”能有效推进“碳中和”,发展“低碳经济”,其关键的材料是高纯硅。以下是高纯硅的简易生产流程。
类型二
制备类
图T4-6
请回答:
(1)石英砂的主要成分是 。四氯化硅(SiCl4)中硅元素的化合价为 。
(2)“精馏”是蒸馏的一种,其原理是利用混合物各成分的 不同,将物质分离出来。
二氧化硅
+4
图T4-6
沸点
(3)上述流程中可循环使用的物质是 。
(4)流程⑤中发生反应的化学方程式为____________________
。
图T4-6
HCl和H2
SiHCl3+H2 Si+
3HCl
角度2 化合物的制备 (8年1考,2015.12)
例6 [2022·深圳]某科学兴趣小组,用废渣(主要为CaCO3,还含有C、Fe2O3、MgO等少量杂质)制作CaCl2,反应过程如图T4-7所示。
(1)Ⅰ过程中加过量稀盐酸的目的是__________________________
__________。
图T4-7
使碳酸钙、氧化铁、氧化镁
完全反应
(2)Ⅰ过程中MgO发生反应的化学反应方程式为____________
,此反应为 (填基本反应类型)反应。
(3)滤渣一的成分为 (填化学式)。
图T4-7
MgO+2HCl
MgCl2+H2O
复分解
C
(4)X溶液为 (填化学式)溶液。
(5)NaCl在生活中的用处: (写一例)。
(6)已知CaCl2与焦炭、BaSO4在高温下生成BaCl2、CO和CaS,写出该反应的化学方程
式:_________________
。
图T4-7
NaOH
用作调味品(合理即可)
CaCl2+4C+BaSO4
BaCl2+4CO↑+CaS
角度3 化工生产 (8年1考,2021.12)
例7 [2022·广西北部湾]某工厂生产高锰酸钾的流程如图T4-8所示。请回答下列问题。
图T4-8
(1)“混合加热室”发生的主要是 (填“物理变化”或“化学变化”)。
(2)“电解室”反应中,反应前后化合价发生变化的元素有______
(写元素符号)。
图T4-8
物理变化
Mn、H
(3)生产流程中可循环利用的物质是 (写化学式)。
(4)写出氧化室中发生反应的化学方程式:_________________
。
图T4-8
KOH
2MnO2+4KOH+O2
2K2MnO4+2H2O
(5)取47.4 g高锰酸钾,加热一段时间后停止,共收集到3.2 g氧气。计算剩余固体中氧元素的质量分数是 (计算结果保留到0.1%)
图T4-8
36.2%
例8 [2022·沈阳]合成氨是人类科学技术上的一项重大突破,对社会发展与科技进步作出了巨大贡献。合成氨工艺的主要流程如图T4-9:
(1)合成塔中的反应在高温、高压、催化剂条件下进行,其化学方程式是 。
(2)上述反应中,一定发生改变的
是 (填序号)。
A.元素种类 B.分子种类
C.原子种类
图T4-9
N2+3H2
2NH3
B
(3)生产过程中可循环使用的物质是 。
(4)根据表中的数据回答问题。
物质 H2 N2 NH3
沸点/℃(1.01×105 Pa) -252 -195.8 -33.35
在1.01×105 Pa时,要将工业合成氨的产物氨气(NH3)从它的反应物氮气和氢气的混合物中分离开来,最适宜的温度应该控制在 ℃≤T< ℃。
N2、H2
-195.8
-33.35
例9 [宿迁]燃煤产生的烟气中含有二氧化硫,二氧化硫会形成酸雨污染环境。科研小组设计利用海水除去二氧化硫,工艺流程如图T4-10:
类型三
环境污染类 (8年1考,2016.13)
请回答下列问题。
(1)二氧化硫中硫、氧元素的质量比m(S)∶m(O)= 。
图T4-10
1∶1
(2)亚硫酸(H2SO3)能被空气中的氧气氧化为硫酸,写出反应的化学方程式: 。
(3)用熟石灰中和稀硫酸是利用了熟石灰的 (填序号)。
A.酸性 B.碱性 C.氧化性
图T4-10
2H2SO3+O2
2H2SO4
B
同课章节目录
