化学人教版九下分层练习:10.2 酸和碱的中和反应第1课时 中和反应(含解析)
文档属性
| 名称 | 化学人教版九下分层练习:10.2 酸和碱的中和反应第1课时 中和反应(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 148.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-29 00:00:00 | ||
图片预览

文档简介
10.2 酸和碱的中和反应
第1课时 中和反应
【基础练习】
1.下列物质不能与NaOH发生中和反应的是( )
A.盐酸 B.氯化钠
C.醋酸 D.硫酸
2.下列反应属于中和反应的是( )
A. B.
C. D.
3.山药中含有碱性皂角素,有些人皮肤沾上会奇痒难忍,涂抹下列厨房中的某物质能明显缓解不适,该物质是( )
A.食醋 B.花生油
C.酱油 D.面粉
4.中和反应在生产、生活中应用广泛。下列应用的主要原理不涉及中和反应的是( )
A. 生石灰用于加热即热食品 B. 氢氧化铝用于治疗胃酸过多
C. 熟石灰用于改良酸性土壤 D. 硼酸用于处理皮肤上沾有的碱
5.向装有一定量盐酸的密闭隔热容器中,逐滴滴加氢氧化钠溶液,利用数字传感器测出反应时间与溶液温度的变化如图所示。下列说法正确的是( )
A. 由该图像可知该反应先放热后吸热
B. a点所示溶液中,溶质只有NaCl
C. b点表示盐酸和氢氧化钠溶液恰好完全反应
D. 向70 s时的溶液中滴加紫色石蕊溶液,溶液不变色
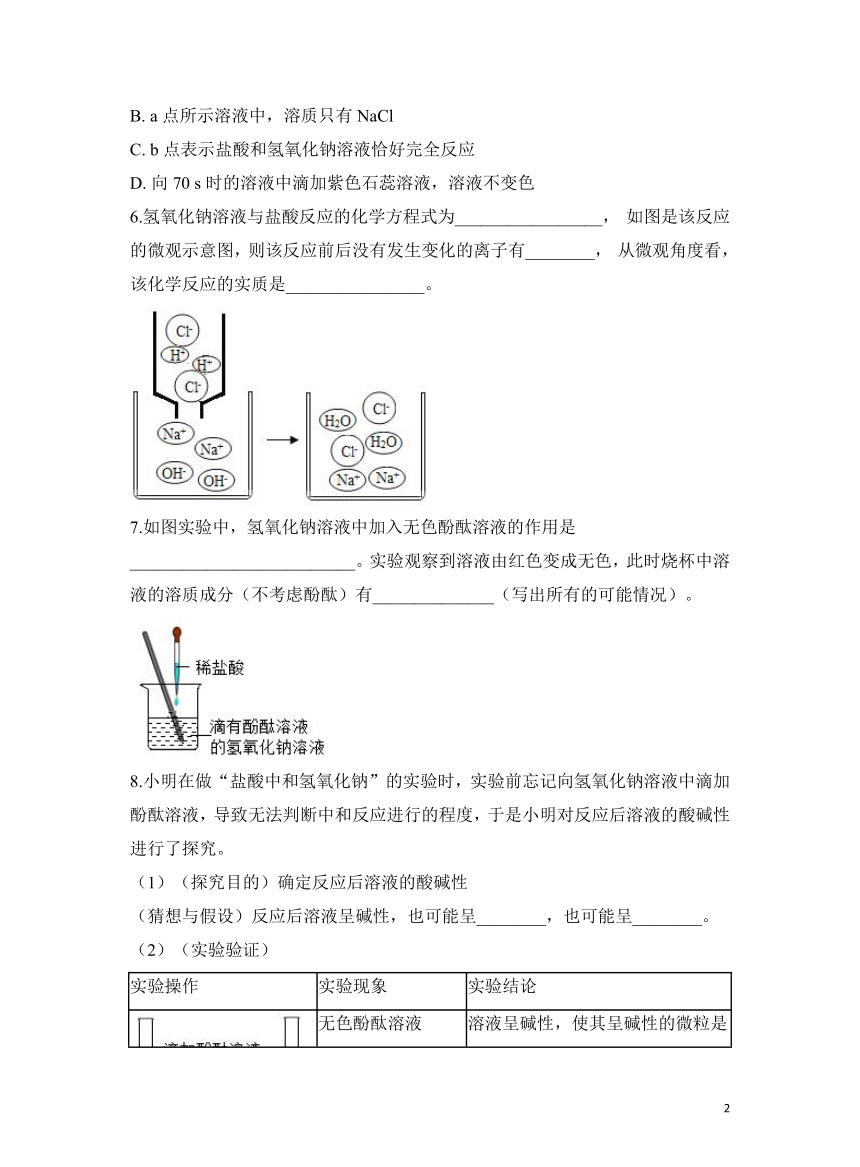
6.氢氧化钠溶液与盐酸反应的化学方程式为_________________, 如图是该反应的微观示意图,则该反应前后没有发生变化的离子有________, 从微观角度看,该化学反应的实质是________________。
7.如图实验中,氢氧化钠溶液中加入无色酚酞溶液的作用是__________________________。实验观察到溶液由红色变成无色,此时烧杯中溶液的溶质成分(不考虑酚酞)有______________(写出所有的可能情况)。
8.小明在做“盐酸中和氢氧化钠”的实验时,实验前忘记向氢氧化钠溶液中滴加酚酞溶液,导致无法判断中和反应进行的程度,于是小明对反应后溶液的酸碱性进行了探究。
(1)(探究目的)确定反应后溶液的酸碱性
(猜想与假设)反应后溶液呈碱性,也可能呈________,也可能呈________。
(2)(实验验证)
实验操作 实验现象 实验结论
无色酚酞溶液________ 溶液呈碱性,使其呈碱性的微粒是________
无色酚酞溶液不变色 溶液呈________
(继续验证)
实验操作 实验现象 实验结论
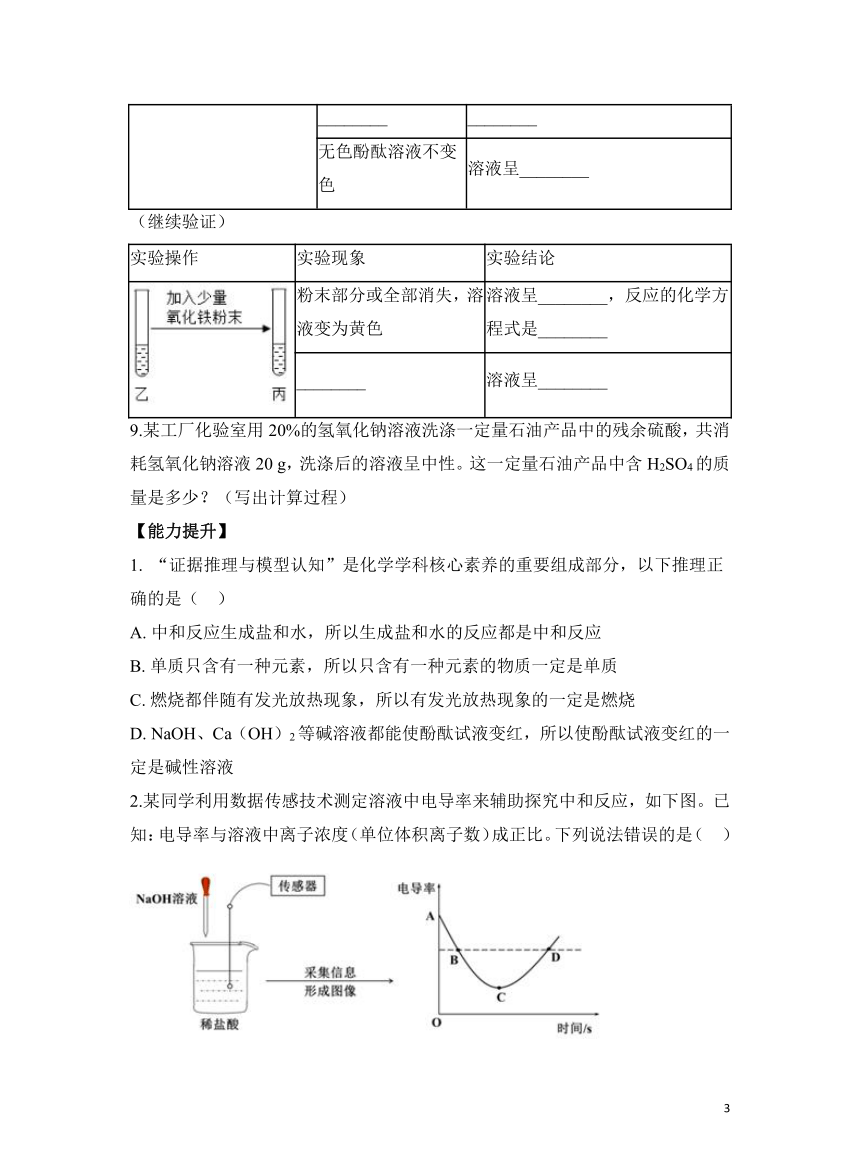
粉末部分或全部消失,溶液变为黄色 溶液呈________,反应的化学方程式是________
________ 溶液呈________
9.某工厂化验室用20%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液20 g,洗涤后的溶液呈中性。这一定量石油产品中含H2SO4的质量是多少?(写出计算过程)
【能力提升】
1. “证据推理与模型认知”是化学学科核心素养的重要组成部分,以下推理正确的是( )
A. 中和反应生成盐和水,所以生成盐和水的反应都是中和反应
B. 单质只含有一种元素,所以只含有一种元素的物质一定是单质
C. 燃烧都伴随有发光放热现象,所以有发光放热现象的一定是燃烧
D. NaOH、Ca(OH)2等碱溶液都能使酚酞试液变红,所以使酚酞试液变红的一定是碱性溶液
2.某同学利用数据传感技术测定溶液中电导率来辅助探究中和反应,如下图。已知:电导率与溶液中离子浓度(单位体积离子数)成正比。下列说法错误的是( )
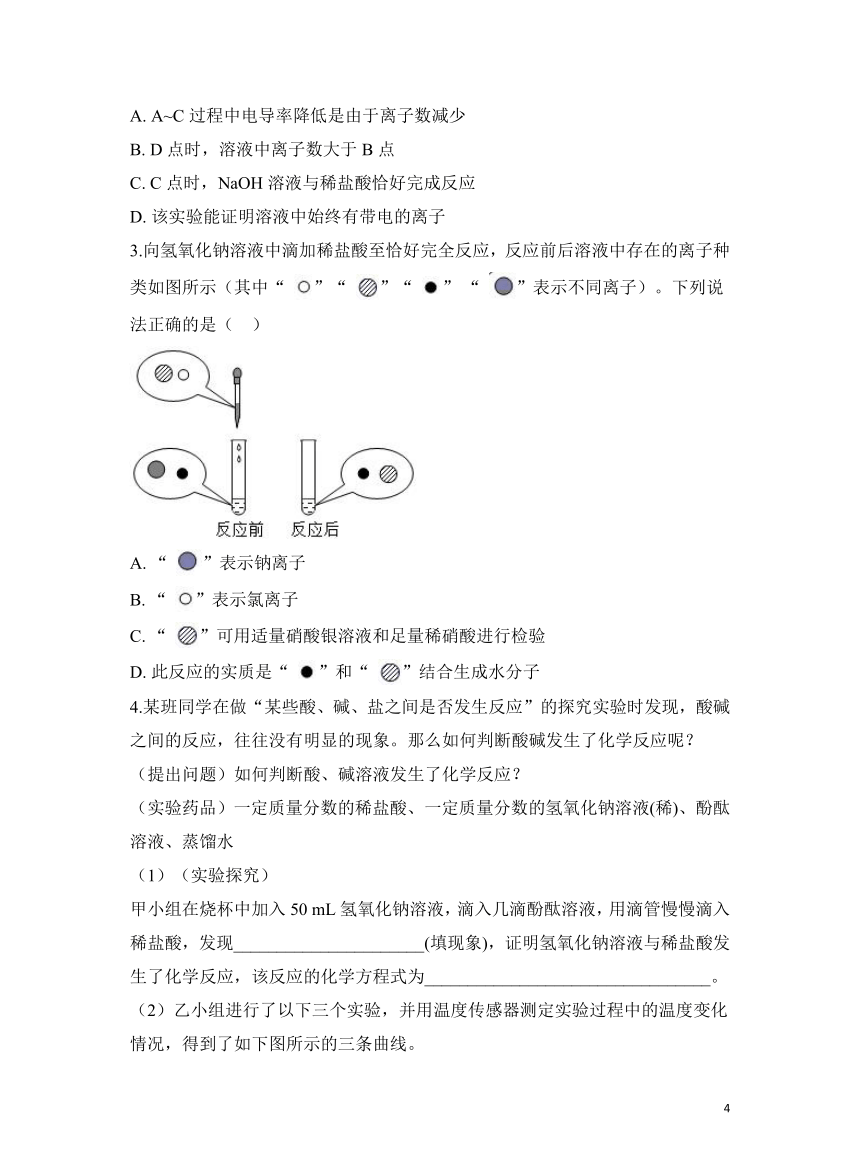
A. A~C过程中电导率降低是由于离子数减少
B. D点时,溶液中离子数大于B点
C. C点时,NaOH溶液与稀盐酸恰好完成反应
D. 该实验能证明溶液中始终有带电的离子
3.向氢氧化钠溶液中滴加稀盐酸至恰好完全反应,反应前后溶液中存在的离子种类如图所示(其中“ ”“ ”“ ” “ ”表示不同离子)。下列说法正确的是( )
A. “ ”表示钠离子
B. “ ”表示氯离子
C. “ ”可用适量硝酸银溶液和足量稀硝酸进行检验
D. 此反应的实质是“ ”和“ ”结合生成水分子
4.某班同学在做“某些酸、碱、盐之间是否发生反应”的探究实验时发现,酸碱之间的反应,往往没有明显的现象。那么如何判断酸碱发生了化学反应呢?
(提出问题)如何判断酸、碱溶液发生了化学反应?
(实验药品)一定质量分数的稀盐酸、一定质量分数的氢氧化钠溶液(稀)、酚酞溶液、蒸馏水
(1)(实验探究)
甲小组在烧杯中加入50 mL氢氧化钠溶液,滴入几滴酚酞溶液,用滴管慢慢滴入稀盐酸,发现______________________(填现象),证明氢氧化钠溶液与稀盐酸发生了化学反应,该反应的化学方程式为_________________________________。
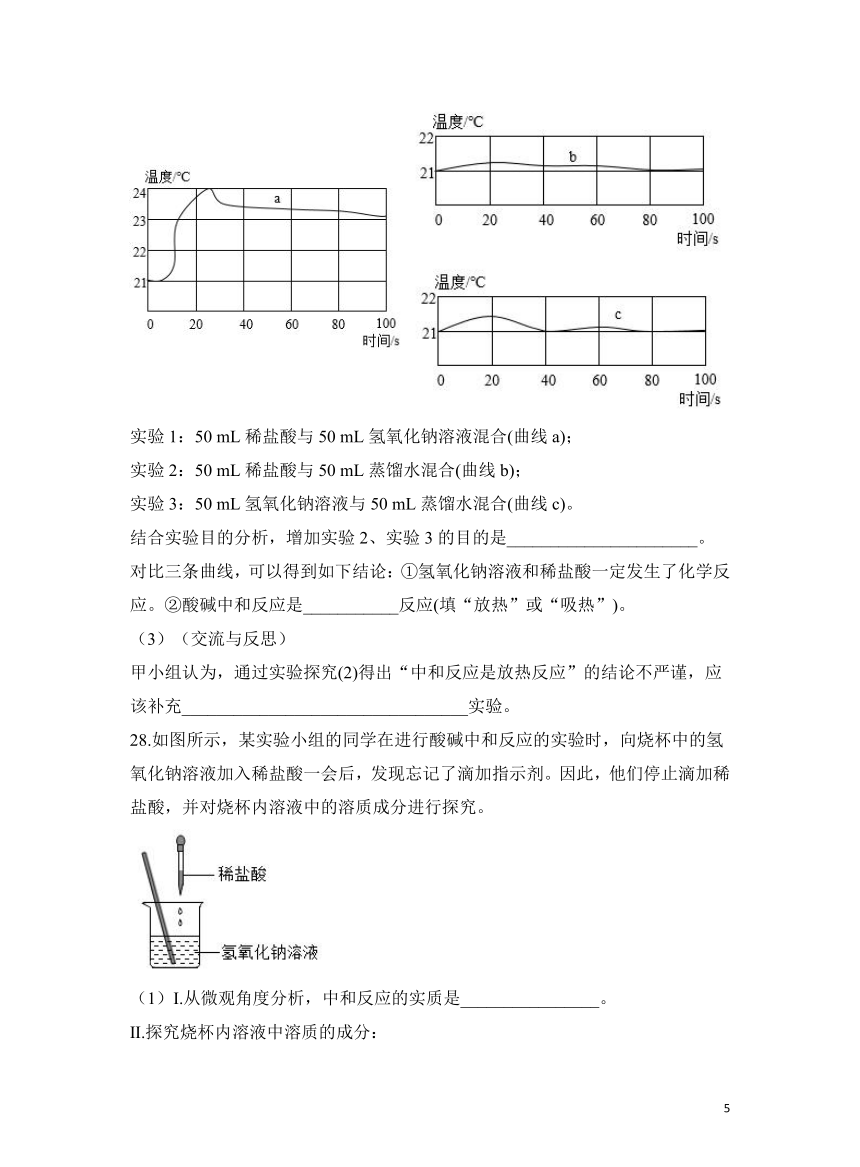
(2)乙小组进行了以下三个实验,并用温度传感器测定实验过程中的温度变化情况,得到了如下图所示的三条曲线。
实验1:50 mL稀盐酸与50 mL氢氧化钠溶液混合(曲线a);
实验2:50 mL稀盐酸与50 mL蒸馏水混合(曲线b);
实验3:50 mL氢氧化钠溶液与50 mL蒸馏水混合(曲线c)。
结合实验目的分析,增加实验2、实验3的目的是______________________。
对比三条曲线,可以得到如下结论:①氢氧化钠溶液和稀盐酸一定发生了化学反应。②酸碱中和反应是___________反应(填“放热”或“吸热”)。
(3)(交流与反思)
甲小组认为,通过实验探究(2)得出“中和反应是放热反应”的结论不严谨,应该补充_________________________________实验。
28.如图所示,某实验小组的同学在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液加入稀盐酸一会后,发现忘记了滴加指示剂。因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究。
(1)Ⅰ.从微观角度分析,中和反应的实质是________________。
Ⅱ.探究烧杯内溶液中溶质的成分:
(2)(提出问题)该烧杯内溶液中的溶质是什么?
(猜想)猜想①:可能是NaCl和NaOH;
猜想②:可能只有NaCl;
猜想③:可能是________。
(3)(查阅资料)氯化钠溶液呈中性。
(进行实验)
实验方案 实验操作 实验现象 实验结论
方案一 取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡 溶液________色 猜想①不正确
方案二 取少量烧杯内溶液于另一支试管中,逐滴加入碳酸钠溶液至过量 ________ 猜想②不正确, 猜想③正确
方案二发生反应的化学方程式是________________。
(4)(反思与拓展)
在分析化学反应后所得物质成分时,除考虑生成物外还需考虑________。
(5)根据所学化学知识,验证烧杯内溶液中的溶质含有HCl,除以上方案外,下列哪些物质单独使用也能完成该实验?________(填序号)。
A. pH试纸 B. 铜 C. 紫色石蕊溶液
参考答案
【基础训练】
1.【答案】 B
【解析】盐酸、醋酸和硫酸均属于酸,均能与氢氧化钠发生中和反应;氯化钠属于盐,不能与氢氧化钠发生中和反应。
故答案为:B。
2.【答案】C
【解析】A.,该反应的反应物是碱和非金属氧化物,不属于中和反应,不符合题意;
B. ,氧化镁属于金属氧化物,该反应的反应物是酸和金属氧化物,不属于中和反应,不符合题意;
C. ,该反应的反应物是酸和碱,生成物是盐和水,属于中和反应,符合题意;
D. ,该反应的反应物是酸和盐,不属于中和反应,不符合题意。
故答案为:C。
3.【答案】 A
【解析】山药中含有碱性皂角素,有些人皮肤沾上会奇痒难忍,所选的物质应是能与碱性皂角素反应的酸性物质,且对皮肤无副作用,厨房中的食醋中含有醋酸,显酸性,符合要求。
故答案为:A。
4.【答案】 A
【解析】A. 生石灰用于加热即热食品,是因为氧化钙能与水反应生成氢氧化钙,不涉及中和反应,故符合题意;
B. 氢氧化铝用于治疗胃酸,是因为氢氧化铝能与稀盐酸反应生成氯化铝和水,属于中和反应,不符合题意;
C. 熟石灰用于改良酸性土壤,是因为氢氧化钙能与土壤中的酸反应生成盐和水,属于中和反应,不符合题意;
D. 硼酸用于处理皮肤上沾有的碱,是因为硼酸能与碱反应生成盐和水,属于中和反应,不符合题意。
故答案为:A。
5.【答案】C
【解析】A. 在密闭隔热容器中逐滴滴加氢氧化钠溶液,由该图像可知:溶液的温度升高,说明该反应是放热反应,充分反应后,继续滴加氢氧化钠溶液,溶液的温度下降,故A不符合题意;
B. a点所示溶液中,容器中还有未反应完的盐酸,所以溶质有NaCl和HCl,故B不符合题意;
C. b点时刻温度达到最高,表示盐酸和氢氧化钠溶液恰好完全反应,故C符合题意;
D. 70 s时的溶液中含有过量的氢氧化钠,溶液呈碱性,滴加紫色石蕊溶液,溶液变蓝色,故D不符合题意。
故答案为:C。
6.【答案】 ;Na+、Cl-;氢离子与氢氧根离子结合生成水(或 )
【解析】氢氧化钠溶液与盐酸反应生成氯化钠和水,反应的化学方程式为:NaOH+HCl=NaCl+H2O,如图是该反应的微观示意图,则该反应前后没有发生变化的离子Na+、Cl-, 从微观角度看,该化学反应的实质是氢离子与氢氧根离子结合生成水或者H++OH-=H2O。
7.【答案】 借助酚酞试液判断氢氧化钠能与稀盐酸发生反应;氯化钠或氯化钠和氯化氢
【解析】氢氧化钠与稀盐酸反应无现象,借助酚酞试液的颜色变化判断氢氧化钠能与稀盐酸反应。
酚酞试液遇碱性溶液变红,遇酸性溶液或中性溶液不变色,当观察到溶液由红色变成无色时,说明溶液不是碱性,溶液可能是中性或酸性。当溶液显中性时,溶质是氯化钠。当溶液显酸性时,溶质是氯化钠和氯化氢。
8.【答案】 (1)酸性;中性
(2)变红色;OH-;中性或酸性;酸性;Fe2O3+6HCl=2FeCl3+3H2O;无明显现象;中性
【解析】(1)猜想与假设:
氢氧化钠溶液与稀盐酸反应生成氯化钠和水,可能恰好完全反应,也可能是稀盐酸有剩余,也可能是氢氧化钠有剩余,故可假设可能呈酸性后中性。
(2)实验验证:
向反应后的溶液中滴加无色酚酞溶液,实验结论是显碱性,则无色酚酞溶液变红色;使其呈碱性的微粒是氢氧根离子。
无色酚酞溶液不变色,说明溶液显酸性或中性。
继续验证:
加入氧化铁后现象为粉末部分或全部消失,溶液变为黄色,是因为盐酸能与氧化铁反应生成氯化铁和水,说明溶液呈酸性;反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O。
若无明显现象,说明溶液显中性。
9.【答案】 解:设这一定量石油产品中含H2SO4的质量是x
=
解得x=4.9 g
答:这一定量石油产品中含H2SO4的质量是4.9 g。
【解析】由氢氧化钠的质量根据化学方程式的计算求出消耗的硫酸的质量。
【能力提升】
1.【答案】 D
【解析】A. 中和反应生成盐和水,生成盐和水的反应不都是中和反应,例如氢氧化钙和二氧化碳生成盐和水,故不符合题意;
B. 单质只含有一种元素,只含有一种元素的物质不一定是单质,例如氧气和臭氧组成的混合物,故不符合题意;
C. 燃烧都伴随有发光放热现象,有发光放热现象的不一定是燃烧,例如白炽灯发光发热,故不符合题意;
D. NaOH、Ca(OH)2等碱溶液都能使酚酞试液变红,所以使酚酞试液变红的一定是碱性溶液,故符合题意。
故答案为:D。
2.【答案】A
【解析】A.由题干信息“在相同条件下,电导率与离子浓度(单位体积内的离子数)成正比”可知,电导率减小不是由于溶液中离子数量逐渐减少,而是离子浓度减小造成的,说法符合题意;
B.D点时溶液的电导率与B点时相同,但是D点时溶液的体积大于B点时溶液的体积,说明D点时溶液中的离子数大于B点,说法不符合题意;
C.C点时溶液的电导率最小,即溶液中离子浓度最小,即NaOH溶液与稀盐酸恰好完全反应,说法不符合题意;
D.在该反应过程中,溶液始终具有导电性,即该实验证明溶液中始终含有带电的粒子,说法不符合题意。
故答案为:A。
3.【答案】 C
【解析】A. 氢氧化钠与稀盐酸反应生成氯化钠和水,该反应的实质是氢离子与氢氧根离子结合为水分子,“ ”表示氢氧根离子,故不符合题意;
B. “ ”表示氢离子,故不符合题意;
C. “ ”表示氯离子,可用适量硝酸银溶液和足量稀硝酸进行检验,故符合题意;
D. 此反应的实质是“ ”和“ ”结合生成水分子,故不符合题意。
故答案为:C。
4.【答案】 (1)溶液先变为红色,后变为无色;NaOH+HCl=NaCl+H2O
(2)盐酸、氢氧化钠溶液稀释时也会放出少量热,通过对比可证明中和反应放热;放热
(3)一个其他酸和碱发生的中和反应
【解析】[实验探究]
(1)甲小组在烧杯中加入50 mL氢氧化钠溶液,滴入几滴酚酞溶液,氢氧化钠溶液呈碱性,能使酚酞变红,用滴管慢慢滴入稀盐酸,因为生成的氯化钠呈中性,酚酞在中性时呈无色,所以当氢氧化钠完全反应时,溶液就会由红色变为无色,故整个实验中观察到的现象是:溶液先变为红色,后变为无色,该现象证明氢氧化钠溶液与稀盐酸发生了化学反应。氢氧化钠和盐酸反应生成氯化钠和水,化学方程式为:NaOH+HCl=NaCl+H2O。
(2)乙小组进行了三个实验,并用温度传感器测定实验过程中的温度变化情况,得到了题中所示的三条曲线。
因为实验目的是通过中和反应时放出热量,从而判断酸、碱溶液发生了化学反应,所以增加实验2、实验3的目的是:盐酸、氢氧化钠溶液稀释时也会放出少量热,通过对比可证明中和反应放热。
对比三条曲线可知,实验1中20多秒后溶液的温度达到最高24℃,此时反应结束,而实验2、实验3中最高温度都低于22℃,因此可得到的结论②是:酸碱中和反应是放热反应。
[交流与反思]
(3)因为氢氧化钠和盐酸反应只是中和反应中的一个,不具有普遍意义,所以通过实验探究(2)得出“中和反应是放热反应”的结论不严谨,应该补充一个其他酸和碱发生的中和反应实验(如稀硫酸和氢氧化钾的反应)。如果通过补充实验也得出反应中放热的结果,就能得出“中和反应是放热反应”的结论。
28.【答案】 (1)氢离子和氢氧根离子反应生成水分子
(2)NaCl和HCl
(3)不变;溶液中有气泡产生;
(4)反应物是否有剩余
(5)AC
【解析】(1)Ⅰ.中和反应是酸与碱反应生成盐和水,从微观角度分析,实质是氢离子和氢氧根离子反应生成水分子。
(2)[猜想]
猜想①:当氢氧化钠过量时,则烧杯内溶液中的溶质可能是NaCl和NaOH;
猜想②:当氢氧化钠与盐酸刚好完全反应时,则烧杯内溶液中的溶质可能只有NaCl;
猜想③:当盐酸过量时,则烧杯内溶液中的溶质可能是NaCl和HCl。
(3)[进行实验]
方案一:若猜想①不正确,则溶液中不存在氢氧化钠。取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡,溶液不变色,说明溶液呈中性或酸性,溶液不含氢氧化钠;
方案二:若猜想②不正确,猜想③正确,则溶液中存在盐酸和氯化钠。取少量烧杯内溶液于另一支试管中,逐滴加入碳酸钠溶液至过量,溶液中有气泡产生,说明溶液中含有盐酸,碳酸钠与盐酸反应生成氯化钠、水和二氧化碳发生反应的化学方程式是 。
(4)[反思与拓展]
在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物是否有剩余。
(5)验证烧杯内溶液中的溶质含有HCl。
A.用pH试纸测定溶液的pH值,如果溶液pH小于7 ,溶液中含有HCl,正确;
B.铜不与稀酸反应,无法检验溶液是否含有HCl,不正确;
C.把紫色石蕊溶液滴到溶液中,如果变红色,则溶液中含有HCl,正确。
故答案为:AC。
1
第1课时 中和反应
【基础练习】
1.下列物质不能与NaOH发生中和反应的是( )
A.盐酸 B.氯化钠
C.醋酸 D.硫酸
2.下列反应属于中和反应的是( )
A. B.
C. D.
3.山药中含有碱性皂角素,有些人皮肤沾上会奇痒难忍,涂抹下列厨房中的某物质能明显缓解不适,该物质是( )
A.食醋 B.花生油
C.酱油 D.面粉
4.中和反应在生产、生活中应用广泛。下列应用的主要原理不涉及中和反应的是( )
A. 生石灰用于加热即热食品 B. 氢氧化铝用于治疗胃酸过多
C. 熟石灰用于改良酸性土壤 D. 硼酸用于处理皮肤上沾有的碱
5.向装有一定量盐酸的密闭隔热容器中,逐滴滴加氢氧化钠溶液,利用数字传感器测出反应时间与溶液温度的变化如图所示。下列说法正确的是( )
A. 由该图像可知该反应先放热后吸热
B. a点所示溶液中,溶质只有NaCl
C. b点表示盐酸和氢氧化钠溶液恰好完全反应
D. 向70 s时的溶液中滴加紫色石蕊溶液,溶液不变色
6.氢氧化钠溶液与盐酸反应的化学方程式为_________________, 如图是该反应的微观示意图,则该反应前后没有发生变化的离子有________, 从微观角度看,该化学反应的实质是________________。
7.如图实验中,氢氧化钠溶液中加入无色酚酞溶液的作用是__________________________。实验观察到溶液由红色变成无色,此时烧杯中溶液的溶质成分(不考虑酚酞)有______________(写出所有的可能情况)。
8.小明在做“盐酸中和氢氧化钠”的实验时,实验前忘记向氢氧化钠溶液中滴加酚酞溶液,导致无法判断中和反应进行的程度,于是小明对反应后溶液的酸碱性进行了探究。
(1)(探究目的)确定反应后溶液的酸碱性
(猜想与假设)反应后溶液呈碱性,也可能呈________,也可能呈________。
(2)(实验验证)
实验操作 实验现象 实验结论
无色酚酞溶液________ 溶液呈碱性,使其呈碱性的微粒是________
无色酚酞溶液不变色 溶液呈________
(继续验证)
实验操作 实验现象 实验结论
粉末部分或全部消失,溶液变为黄色 溶液呈________,反应的化学方程式是________
________ 溶液呈________
9.某工厂化验室用20%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液20 g,洗涤后的溶液呈中性。这一定量石油产品中含H2SO4的质量是多少?(写出计算过程)
【能力提升】
1. “证据推理与模型认知”是化学学科核心素养的重要组成部分,以下推理正确的是( )
A. 中和反应生成盐和水,所以生成盐和水的反应都是中和反应
B. 单质只含有一种元素,所以只含有一种元素的物质一定是单质
C. 燃烧都伴随有发光放热现象,所以有发光放热现象的一定是燃烧
D. NaOH、Ca(OH)2等碱溶液都能使酚酞试液变红,所以使酚酞试液变红的一定是碱性溶液
2.某同学利用数据传感技术测定溶液中电导率来辅助探究中和反应,如下图。已知:电导率与溶液中离子浓度(单位体积离子数)成正比。下列说法错误的是( )
A. A~C过程中电导率降低是由于离子数减少
B. D点时,溶液中离子数大于B点
C. C点时,NaOH溶液与稀盐酸恰好完成反应
D. 该实验能证明溶液中始终有带电的离子
3.向氢氧化钠溶液中滴加稀盐酸至恰好完全反应,反应前后溶液中存在的离子种类如图所示(其中“ ”“ ”“ ” “ ”表示不同离子)。下列说法正确的是( )
A. “ ”表示钠离子
B. “ ”表示氯离子
C. “ ”可用适量硝酸银溶液和足量稀硝酸进行检验
D. 此反应的实质是“ ”和“ ”结合生成水分子
4.某班同学在做“某些酸、碱、盐之间是否发生反应”的探究实验时发现,酸碱之间的反应,往往没有明显的现象。那么如何判断酸碱发生了化学反应呢?
(提出问题)如何判断酸、碱溶液发生了化学反应?
(实验药品)一定质量分数的稀盐酸、一定质量分数的氢氧化钠溶液(稀)、酚酞溶液、蒸馏水
(1)(实验探究)
甲小组在烧杯中加入50 mL氢氧化钠溶液,滴入几滴酚酞溶液,用滴管慢慢滴入稀盐酸,发现______________________(填现象),证明氢氧化钠溶液与稀盐酸发生了化学反应,该反应的化学方程式为_________________________________。
(2)乙小组进行了以下三个实验,并用温度传感器测定实验过程中的温度变化情况,得到了如下图所示的三条曲线。
实验1:50 mL稀盐酸与50 mL氢氧化钠溶液混合(曲线a);
实验2:50 mL稀盐酸与50 mL蒸馏水混合(曲线b);
实验3:50 mL氢氧化钠溶液与50 mL蒸馏水混合(曲线c)。
结合实验目的分析,增加实验2、实验3的目的是______________________。
对比三条曲线,可以得到如下结论:①氢氧化钠溶液和稀盐酸一定发生了化学反应。②酸碱中和反应是___________反应(填“放热”或“吸热”)。
(3)(交流与反思)
甲小组认为,通过实验探究(2)得出“中和反应是放热反应”的结论不严谨,应该补充_________________________________实验。
28.如图所示,某实验小组的同学在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液加入稀盐酸一会后,发现忘记了滴加指示剂。因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究。
(1)Ⅰ.从微观角度分析,中和反应的实质是________________。
Ⅱ.探究烧杯内溶液中溶质的成分:
(2)(提出问题)该烧杯内溶液中的溶质是什么?
(猜想)猜想①:可能是NaCl和NaOH;
猜想②:可能只有NaCl;
猜想③:可能是________。
(3)(查阅资料)氯化钠溶液呈中性。
(进行实验)
实验方案 实验操作 实验现象 实验结论
方案一 取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡 溶液________色 猜想①不正确
方案二 取少量烧杯内溶液于另一支试管中,逐滴加入碳酸钠溶液至过量 ________ 猜想②不正确, 猜想③正确
方案二发生反应的化学方程式是________________。
(4)(反思与拓展)
在分析化学反应后所得物质成分时,除考虑生成物外还需考虑________。
(5)根据所学化学知识,验证烧杯内溶液中的溶质含有HCl,除以上方案外,下列哪些物质单独使用也能完成该实验?________(填序号)。
A. pH试纸 B. 铜 C. 紫色石蕊溶液
参考答案
【基础训练】
1.【答案】 B
【解析】盐酸、醋酸和硫酸均属于酸,均能与氢氧化钠发生中和反应;氯化钠属于盐,不能与氢氧化钠发生中和反应。
故答案为:B。
2.【答案】C
【解析】A.,该反应的反应物是碱和非金属氧化物,不属于中和反应,不符合题意;
B. ,氧化镁属于金属氧化物,该反应的反应物是酸和金属氧化物,不属于中和反应,不符合题意;
C. ,该反应的反应物是酸和碱,生成物是盐和水,属于中和反应,符合题意;
D. ,该反应的反应物是酸和盐,不属于中和反应,不符合题意。
故答案为:C。
3.【答案】 A
【解析】山药中含有碱性皂角素,有些人皮肤沾上会奇痒难忍,所选的物质应是能与碱性皂角素反应的酸性物质,且对皮肤无副作用,厨房中的食醋中含有醋酸,显酸性,符合要求。
故答案为:A。
4.【答案】 A
【解析】A. 生石灰用于加热即热食品,是因为氧化钙能与水反应生成氢氧化钙,不涉及中和反应,故符合题意;
B. 氢氧化铝用于治疗胃酸,是因为氢氧化铝能与稀盐酸反应生成氯化铝和水,属于中和反应,不符合题意;
C. 熟石灰用于改良酸性土壤,是因为氢氧化钙能与土壤中的酸反应生成盐和水,属于中和反应,不符合题意;
D. 硼酸用于处理皮肤上沾有的碱,是因为硼酸能与碱反应生成盐和水,属于中和反应,不符合题意。
故答案为:A。
5.【答案】C
【解析】A. 在密闭隔热容器中逐滴滴加氢氧化钠溶液,由该图像可知:溶液的温度升高,说明该反应是放热反应,充分反应后,继续滴加氢氧化钠溶液,溶液的温度下降,故A不符合题意;
B. a点所示溶液中,容器中还有未反应完的盐酸,所以溶质有NaCl和HCl,故B不符合题意;
C. b点时刻温度达到最高,表示盐酸和氢氧化钠溶液恰好完全反应,故C符合题意;
D. 70 s时的溶液中含有过量的氢氧化钠,溶液呈碱性,滴加紫色石蕊溶液,溶液变蓝色,故D不符合题意。
故答案为:C。
6.【答案】 ;Na+、Cl-;氢离子与氢氧根离子结合生成水(或 )
【解析】氢氧化钠溶液与盐酸反应生成氯化钠和水,反应的化学方程式为:NaOH+HCl=NaCl+H2O,如图是该反应的微观示意图,则该反应前后没有发生变化的离子Na+、Cl-, 从微观角度看,该化学反应的实质是氢离子与氢氧根离子结合生成水或者H++OH-=H2O。
7.【答案】 借助酚酞试液判断氢氧化钠能与稀盐酸发生反应;氯化钠或氯化钠和氯化氢
【解析】氢氧化钠与稀盐酸反应无现象,借助酚酞试液的颜色变化判断氢氧化钠能与稀盐酸反应。
酚酞试液遇碱性溶液变红,遇酸性溶液或中性溶液不变色,当观察到溶液由红色变成无色时,说明溶液不是碱性,溶液可能是中性或酸性。当溶液显中性时,溶质是氯化钠。当溶液显酸性时,溶质是氯化钠和氯化氢。
8.【答案】 (1)酸性;中性
(2)变红色;OH-;中性或酸性;酸性;Fe2O3+6HCl=2FeCl3+3H2O;无明显现象;中性
【解析】(1)猜想与假设:
氢氧化钠溶液与稀盐酸反应生成氯化钠和水,可能恰好完全反应,也可能是稀盐酸有剩余,也可能是氢氧化钠有剩余,故可假设可能呈酸性后中性。
(2)实验验证:
向反应后的溶液中滴加无色酚酞溶液,实验结论是显碱性,则无色酚酞溶液变红色;使其呈碱性的微粒是氢氧根离子。
无色酚酞溶液不变色,说明溶液显酸性或中性。
继续验证:
加入氧化铁后现象为粉末部分或全部消失,溶液变为黄色,是因为盐酸能与氧化铁反应生成氯化铁和水,说明溶液呈酸性;反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O。
若无明显现象,说明溶液显中性。
9.【答案】 解:设这一定量石油产品中含H2SO4的质量是x
=
解得x=4.9 g
答:这一定量石油产品中含H2SO4的质量是4.9 g。
【解析】由氢氧化钠的质量根据化学方程式的计算求出消耗的硫酸的质量。
【能力提升】
1.【答案】 D
【解析】A. 中和反应生成盐和水,生成盐和水的反应不都是中和反应,例如氢氧化钙和二氧化碳生成盐和水,故不符合题意;
B. 单质只含有一种元素,只含有一种元素的物质不一定是单质,例如氧气和臭氧组成的混合物,故不符合题意;
C. 燃烧都伴随有发光放热现象,有发光放热现象的不一定是燃烧,例如白炽灯发光发热,故不符合题意;
D. NaOH、Ca(OH)2等碱溶液都能使酚酞试液变红,所以使酚酞试液变红的一定是碱性溶液,故符合题意。
故答案为:D。
2.【答案】A
【解析】A.由题干信息“在相同条件下,电导率与离子浓度(单位体积内的离子数)成正比”可知,电导率减小不是由于溶液中离子数量逐渐减少,而是离子浓度减小造成的,说法符合题意;
B.D点时溶液的电导率与B点时相同,但是D点时溶液的体积大于B点时溶液的体积,说明D点时溶液中的离子数大于B点,说法不符合题意;
C.C点时溶液的电导率最小,即溶液中离子浓度最小,即NaOH溶液与稀盐酸恰好完全反应,说法不符合题意;
D.在该反应过程中,溶液始终具有导电性,即该实验证明溶液中始终含有带电的粒子,说法不符合题意。
故答案为:A。
3.【答案】 C
【解析】A. 氢氧化钠与稀盐酸反应生成氯化钠和水,该反应的实质是氢离子与氢氧根离子结合为水分子,“ ”表示氢氧根离子,故不符合题意;
B. “ ”表示氢离子,故不符合题意;
C. “ ”表示氯离子,可用适量硝酸银溶液和足量稀硝酸进行检验,故符合题意;
D. 此反应的实质是“ ”和“ ”结合生成水分子,故不符合题意。
故答案为:C。
4.【答案】 (1)溶液先变为红色,后变为无色;NaOH+HCl=NaCl+H2O
(2)盐酸、氢氧化钠溶液稀释时也会放出少量热,通过对比可证明中和反应放热;放热
(3)一个其他酸和碱发生的中和反应
【解析】[实验探究]
(1)甲小组在烧杯中加入50 mL氢氧化钠溶液,滴入几滴酚酞溶液,氢氧化钠溶液呈碱性,能使酚酞变红,用滴管慢慢滴入稀盐酸,因为生成的氯化钠呈中性,酚酞在中性时呈无色,所以当氢氧化钠完全反应时,溶液就会由红色变为无色,故整个实验中观察到的现象是:溶液先变为红色,后变为无色,该现象证明氢氧化钠溶液与稀盐酸发生了化学反应。氢氧化钠和盐酸反应生成氯化钠和水,化学方程式为:NaOH+HCl=NaCl+H2O。
(2)乙小组进行了三个实验,并用温度传感器测定实验过程中的温度变化情况,得到了题中所示的三条曲线。
因为实验目的是通过中和反应时放出热量,从而判断酸、碱溶液发生了化学反应,所以增加实验2、实验3的目的是:盐酸、氢氧化钠溶液稀释时也会放出少量热,通过对比可证明中和反应放热。
对比三条曲线可知,实验1中20多秒后溶液的温度达到最高24℃,此时反应结束,而实验2、实验3中最高温度都低于22℃,因此可得到的结论②是:酸碱中和反应是放热反应。
[交流与反思]
(3)因为氢氧化钠和盐酸反应只是中和反应中的一个,不具有普遍意义,所以通过实验探究(2)得出“中和反应是放热反应”的结论不严谨,应该补充一个其他酸和碱发生的中和反应实验(如稀硫酸和氢氧化钾的反应)。如果通过补充实验也得出反应中放热的结果,就能得出“中和反应是放热反应”的结论。
28.【答案】 (1)氢离子和氢氧根离子反应生成水分子
(2)NaCl和HCl
(3)不变;溶液中有气泡产生;
(4)反应物是否有剩余
(5)AC
【解析】(1)Ⅰ.中和反应是酸与碱反应生成盐和水,从微观角度分析,实质是氢离子和氢氧根离子反应生成水分子。
(2)[猜想]
猜想①:当氢氧化钠过量时,则烧杯内溶液中的溶质可能是NaCl和NaOH;
猜想②:当氢氧化钠与盐酸刚好完全反应时,则烧杯内溶液中的溶质可能只有NaCl;
猜想③:当盐酸过量时,则烧杯内溶液中的溶质可能是NaCl和HCl。
(3)[进行实验]
方案一:若猜想①不正确,则溶液中不存在氢氧化钠。取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡,溶液不变色,说明溶液呈中性或酸性,溶液不含氢氧化钠;
方案二:若猜想②不正确,猜想③正确,则溶液中存在盐酸和氯化钠。取少量烧杯内溶液于另一支试管中,逐滴加入碳酸钠溶液至过量,溶液中有气泡产生,说明溶液中含有盐酸,碳酸钠与盐酸反应生成氯化钠、水和二氧化碳发生反应的化学方程式是 。
(4)[反思与拓展]
在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物是否有剩余。
(5)验证烧杯内溶液中的溶质含有HCl。
A.用pH试纸测定溶液的pH值,如果溶液pH小于7 ,溶液中含有HCl,正确;
B.铜不与稀酸反应,无法检验溶液是否含有HCl,不正确;
C.把紫色石蕊溶液滴到溶液中,如果变红色,则溶液中含有HCl,正确。
故答案为:AC。
1
同课章节目录
