云南省大理州重点中学2022-2023学年高二下学期3月月考化学试题(含答案)
文档属性
| 名称 | 云南省大理州重点中学2022-2023学年高二下学期3月月考化学试题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 870.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-29 00:00:00 | ||
图片预览




文档简介
大理州重点中学2022-2023学年高二下学期3月月考
化学试卷
1.本试卷分选择题和非选择题两部分,共100分。考试时间90分钟。
2.请将各题答案填写在答题卡上。
3.可能用到的相对原子质量:
第Ⅰ卷(选择题,共48分)
一、选择题(本题共16小题,每小题3分,共48分。每小题只有一个选项符合题目要求。)
1.化学与生产、生活密切相关,下列说法正确的是( )
A.热的纯碱溶液可用于除铁锈
B.葡萄糖、淀粉和纤维素在酸性条件下均可水解
C.铅酸蓄电池、镍氢电池、锂离子电池均属于二次电池
D.工业上常采用电解饱和食盐水来获得金属钠
2.下列说法不正确的是( )
A.乙醇和丙三醇互为同系物
B.和互为同位素
C.和互为同素异形体
D.丙酮()和环氧丙烷()互为同分异构体
3.下列各离子组在指定条件下一定能大量共存的是( )
A.某无色透明溶液中:、、、
B.使甲基橙显红色的溶液中:、、、
C.常温下,的溶液中:、、、
D.常温下,的溶液中:、、、
4.设为阿伏加德罗常数的值,下列说法正确的是( )
A.足量浓盐酸与在加热条件下充分反应,生成的分子总数为
B.的溶液中,所含的氧原子总数为
C.溶液中,物质的量为
D.标准状况下,中所含的分子总数为
5.补骨脂素对白血病细胞有较强的杀伤作用,其结构如图所示,下列有关补骨脂素的说法正确的是( )
A.分子式为 B.含有四种官能团
C.不能与氢氧化钠溶液反应 D.能使酸性高锰酸钾溶液褪色
6.短周期主族元素、、、的原子序数依次增大,原子的最外层有6个电子,是迄今发现的非金属性最强的元素,在元素周期表中位于第IA族,与属于同一主族。下列说法正确的是( )
A.简单离子半径:
B.最简单氢化物的沸点:
C.的单质与的最简单氢化物反应,可得到的单质
D.溶液中,所含的物质的量为
7.下列离子方程式书写正确的是( )
A.澄清石灰水与过量的小苏打溶液反应:
B.乙酸乙酯与溶液共热:
C.溶液中通入少量:
D.氯化亚铁溶液中滴加铁氰化钾:
8.若将铜丝插入热 硫酸中进行如图(均为浸有相应试液的棉花)所示的探究实验,下列分析正确的是( )
A.与浓硫酸反应,只体现的酸性
B.处变红,说明是酸性氧化物
C.或处褪色,均说明具有漂白性
D.试管底部出现白色固体,说明反应中无生成
9.在分析试剂、医药、电子工业中用途广泛。下列有关说法正确的是( )
A.属于弱电解质,其溶液导电性较弱
B.溶液中水解产生的促进水解
C.中部分离子浓度大小顺序为
D.常温下稀溶液中滴加氨水至中性时,
10.下列实验操作和现象所得结论正确的是( )
选项 实验操作 现象 结论
A 向漂白粉溶液中通入 产生白色沉淀 能与反应生成
B 向砖红色的沉淀中滴加溶液 砖红色沉淀逐渐 转化为白色沉淀 相同温度下,溶度积常数:
C 向胶体中滴加溶液 产生红褐色沉淀 发生了胶体聚沉
D 将氨水滴加到红色石蕊试纸上 试纸变蓝 氨气属于碱性电解质
11.已知: ,不同条件下反应进程的能量变化如图所示。下列说法正确的是( )
A.升高温度,该反应的平衡常数增大
B.由可知,该反应低温能自发进行
C.过程使用了催化剂,使反应的减小
D.恒温恒容条件下通入氦气,使单位体积内的活化分子数增大
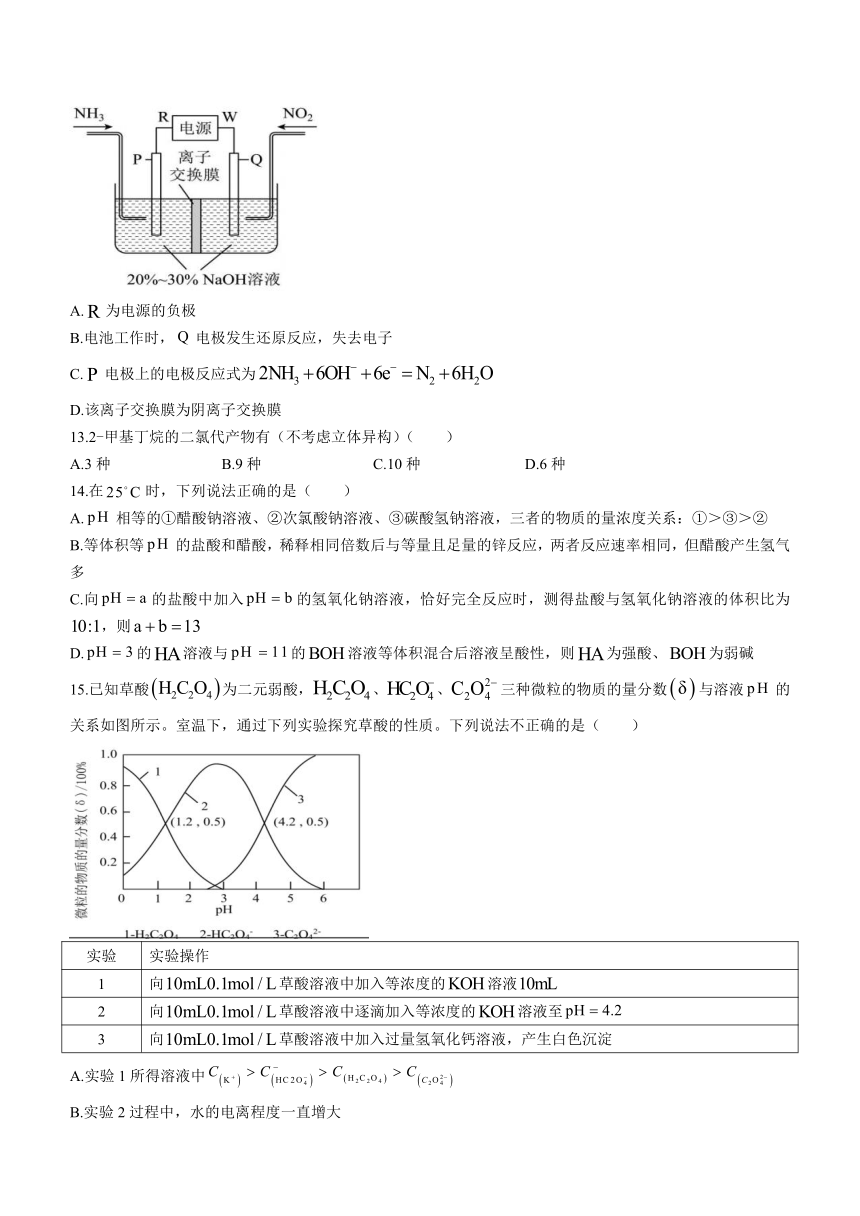
12.利用反应消除的简易装置如图所示(、)(电极均为惰性电极),下列说法正确的是( )
A.为电源的负极
B.电池工作时,电极发生还原反应,失去电子
C.电极上的电极反应式为
D.该离子交换膜为阴离子交换膜
13.2-甲基丁烷的二氯代产物有(不考虑立体异构)( )
A.3种 B.9种 C.10种 D.6种
14.在时,下列说法正确的是( )
A.相等的①醋酸钠溶液、②次氯酸钠溶液、③碳酸氢钠溶液,三者的物质的量浓度关系:①>③>②
B.等体积等的盐酸和醋酸,稀释相同倍数后与等量且足量的锌反应,两者反应速率相同,但醋酸产生氢气多
C.向的盐酸中加入的氢氧化钠溶液,恰好完全反应时,测得盐酸与氢氧化钠溶液的体积比为,则
D.的溶液与的溶液等体积混合后溶液呈酸性,则为强酸、为弱碱
15.已知草酸为二元弱酸,、、三种微粒的物质的量分数与溶液的关系如图所示。室温下,通过下列实验探究草酸的性质。下列说法不正确的是( )
实验 实验操作
1 向草酸溶液中加入等浓度的溶液
2 向草酸溶液中逐滴加入等浓度的溶液至
3 向草酸溶液中加入过量氢氧化钙溶液,产生白色沉淀
A.实验1所得溶液中
B.实验2过程中,水的电离程度一直增大
C.实验2所得溶液中:
D.实验3反应静置后的上层清液中
16.常温下,用的溶液滴定醋酸,滴定曲线如图所示,下列说法正确的是( )
已知:。
A.点溶液中,
B.点溶液中,
C.点溶液中含有5种不同的微粒
D.点溶液中
第Ⅱ卷(非选择题,共52分)
二、填空题
17.(14分)Ⅰ、在一定的条件下,天然气脱硫工艺中会发生以下反应:
(1)则相同条件下反应的______(用含、和的代数式表示)。
Ⅱ、三氯化硅是制备硅烷、多晶硅的重要原料。已知在催化剂作用下发生反应:。一定条件下,向容积为的恒容密闭容器中充入,分别在温度为、条件下反应,测得反应体系中的物质的量分数随时间变化的关系如图所示(2)在温度下,的平衡转化率______%。若想进一步提高的转化率,除改变温度外还可以采取的措施是______。
(3)在温度下,经后反应达到平衡。
①内,的反应速率______。
②在温度下,该反应的平衡常数______(已知,压强平衡常数用各气体组分的分压代替物质的量浓度计算)。
(4)下列不能判断该反应达到平衡状态的是______(填标号)。
a. b.混合气体的密度不再发生变化
c.与的浓度之比不再改变 d.混合气体的平均摩尔质量不再发生变化
(5)温度为的平衡常数______
18.(12分)亚硝酸钠外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。某化学兴趣小组设计实验制备并探究其性质。
查阅资料信息:①;.
②酸性溶液可将低价氮的氧化物或酸根离子氧化为。
(1)的制备(夹持装置和加热装置均已略,已检查装置气密性)。
①若没有装置,则装置中与水发生反应:______(写化学方程式)。
②制得的固体中混有的杂质主要为,改进措施是在装置、间添加______,提高的纯度。
③装置中发生的主要反应的离子方程式为______。
(2)验证亚硝酸钠与70%硫酸反应的气体产物为和的混合气体。
已知:溶液可吸收;的沸点为21℃,熔点为。
①为了检验装置中生成的气体产物,装置的连接顺序是______。(按气流方向从左到右)
②反应前应打开弹簧夹1,先通入一段时间氮气,目的是______。
(3)测定某亚硝酸钠样品的纯度。
设该样品的杂质均不与酸性溶液反应,可用酸性溶液测定的含量。
称取亚硝酸钠样品溶于水配成溶液,取出溶液于锥形瓶中,再用的酸性标准溶液进行滴定,消耗酸性标准溶液的体积如表:
实验组 第一组 第二组 第三组 第四组
消耗酸性标准溶液的体积 9.97 10.02 12.01 10.01
该亚硝酸钠样品中的质量分数为______。
19.(12分)镍是一种常用的催化剂。以红土镍矿(主要含有、、、等)为原料,制取纳米镍粉,同时获得净水剂黄钠铁矾的工艺流程如下:
回答下列问题:
(1)黄钠铁矾中,铁的化合价为______价。
(2)过滤操作1时滤渣的化学式为______
(3)“沉铁”过程加入的目的是______,控制不同的条件可以得到不同的沉淀,所得沉淀与温度、的关系如图所示(图中阴影部分表示的是黄钠铁矾稳定存在区域)。若反应在120℃时进行,加入的偏多,则所得黄钠铁矾中混有的杂质是______(填化学式)。
(4)“转化”过程,向“过滤Ⅱ”所得滤液(富含)中加入,控制溶液中的浓度,可得到不同晶态物质(、或二者的混合物)。当生成和的物质的量之比为时,该反应的离子方程式为______。
(5)化学镀镍是金属表面镀镍的常用方法,以为镀液,次亚磷酸钠为还原剂,在90℃的酸性溶液中发生反应,被氧化为弱酸亚磷酸。写出化学镀镍反应的离子方程式:______。
20.(14分)苯是工业上常用的化工原料,可以用于合成安息香酸苄酯和高分化合物(部分反应条件略去),流程如下所示,请回答下列问题:
(1)的化学名称是______,中的官能团名称是______。
(2)生成的反应类型为______。
(3)生成的化学方程式为______。
(4)是的同分异构体,分子中含有酯基,有两个苯环且不直接相连,符合上述条件的结构有______种,其中核磁共振氢谱图有6组峰,且面积比为的同分异构体的结构简式为______(写出一种即可)。
(5)参照上述合成路线,以2-氯丙烷为原料,其它无机试剂和有机溶剂任选,设计2-甲基-2-丙醇的合成路线______。
参考答案
一、选择题(每题3分,共48分)
1 2 3 4 5 6 7 8
C A C A D C B B
9 10 11 12 13 14 15 16
C C B D C A A B
二、填空题(每空2分,共52分)
17.(1)// (2)①.20 ②.及时移出产物
(3)①. ②. (4)bd (5)
18.(1)①
②一个装有蒸馏水的洗气瓶,将转化成
③
(2)①C、E、D、B
②排尽装置中的空气,防止生成的被氧化,干扰气体产物的检验
(3)86.25%
19(1) (2) (3)①.调节溶液的 ②.
(4)
(5)
20.(1)①.苯甲酸钠(安息香酸钠) ②.羧基 (2)取代反应
(3)
(4)①.11 ②.或
(5)
化学试卷
1.本试卷分选择题和非选择题两部分,共100分。考试时间90分钟。
2.请将各题答案填写在答题卡上。
3.可能用到的相对原子质量:
第Ⅰ卷(选择题,共48分)
一、选择题(本题共16小题,每小题3分,共48分。每小题只有一个选项符合题目要求。)
1.化学与生产、生活密切相关,下列说法正确的是( )
A.热的纯碱溶液可用于除铁锈
B.葡萄糖、淀粉和纤维素在酸性条件下均可水解
C.铅酸蓄电池、镍氢电池、锂离子电池均属于二次电池
D.工业上常采用电解饱和食盐水来获得金属钠
2.下列说法不正确的是( )
A.乙醇和丙三醇互为同系物
B.和互为同位素
C.和互为同素异形体
D.丙酮()和环氧丙烷()互为同分异构体
3.下列各离子组在指定条件下一定能大量共存的是( )
A.某无色透明溶液中:、、、
B.使甲基橙显红色的溶液中:、、、
C.常温下,的溶液中:、、、
D.常温下,的溶液中:、、、
4.设为阿伏加德罗常数的值,下列说法正确的是( )
A.足量浓盐酸与在加热条件下充分反应,生成的分子总数为
B.的溶液中,所含的氧原子总数为
C.溶液中,物质的量为
D.标准状况下,中所含的分子总数为
5.补骨脂素对白血病细胞有较强的杀伤作用,其结构如图所示,下列有关补骨脂素的说法正确的是( )
A.分子式为 B.含有四种官能团
C.不能与氢氧化钠溶液反应 D.能使酸性高锰酸钾溶液褪色
6.短周期主族元素、、、的原子序数依次增大,原子的最外层有6个电子,是迄今发现的非金属性最强的元素,在元素周期表中位于第IA族,与属于同一主族。下列说法正确的是( )
A.简单离子半径:
B.最简单氢化物的沸点:
C.的单质与的最简单氢化物反应,可得到的单质
D.溶液中,所含的物质的量为
7.下列离子方程式书写正确的是( )
A.澄清石灰水与过量的小苏打溶液反应:
B.乙酸乙酯与溶液共热:
C.溶液中通入少量:
D.氯化亚铁溶液中滴加铁氰化钾:
8.若将铜丝插入热 硫酸中进行如图(均为浸有相应试液的棉花)所示的探究实验,下列分析正确的是( )
A.与浓硫酸反应,只体现的酸性
B.处变红,说明是酸性氧化物
C.或处褪色,均说明具有漂白性
D.试管底部出现白色固体,说明反应中无生成
9.在分析试剂、医药、电子工业中用途广泛。下列有关说法正确的是( )
A.属于弱电解质,其溶液导电性较弱
B.溶液中水解产生的促进水解
C.中部分离子浓度大小顺序为
D.常温下稀溶液中滴加氨水至中性时,
10.下列实验操作和现象所得结论正确的是( )
选项 实验操作 现象 结论
A 向漂白粉溶液中通入 产生白色沉淀 能与反应生成
B 向砖红色的沉淀中滴加溶液 砖红色沉淀逐渐 转化为白色沉淀 相同温度下,溶度积常数:
C 向胶体中滴加溶液 产生红褐色沉淀 发生了胶体聚沉
D 将氨水滴加到红色石蕊试纸上 试纸变蓝 氨气属于碱性电解质
11.已知: ,不同条件下反应进程的能量变化如图所示。下列说法正确的是( )
A.升高温度,该反应的平衡常数增大
B.由可知,该反应低温能自发进行
C.过程使用了催化剂,使反应的减小
D.恒温恒容条件下通入氦气,使单位体积内的活化分子数增大
12.利用反应消除的简易装置如图所示(、)(电极均为惰性电极),下列说法正确的是( )
A.为电源的负极
B.电池工作时,电极发生还原反应,失去电子
C.电极上的电极反应式为
D.该离子交换膜为阴离子交换膜
13.2-甲基丁烷的二氯代产物有(不考虑立体异构)( )
A.3种 B.9种 C.10种 D.6种
14.在时,下列说法正确的是( )
A.相等的①醋酸钠溶液、②次氯酸钠溶液、③碳酸氢钠溶液,三者的物质的量浓度关系:①>③>②
B.等体积等的盐酸和醋酸,稀释相同倍数后与等量且足量的锌反应,两者反应速率相同,但醋酸产生氢气多
C.向的盐酸中加入的氢氧化钠溶液,恰好完全反应时,测得盐酸与氢氧化钠溶液的体积比为,则
D.的溶液与的溶液等体积混合后溶液呈酸性,则为强酸、为弱碱
15.已知草酸为二元弱酸,、、三种微粒的物质的量分数与溶液的关系如图所示。室温下,通过下列实验探究草酸的性质。下列说法不正确的是( )
实验 实验操作
1 向草酸溶液中加入等浓度的溶液
2 向草酸溶液中逐滴加入等浓度的溶液至
3 向草酸溶液中加入过量氢氧化钙溶液,产生白色沉淀
A.实验1所得溶液中
B.实验2过程中,水的电离程度一直增大
C.实验2所得溶液中:
D.实验3反应静置后的上层清液中
16.常温下,用的溶液滴定醋酸,滴定曲线如图所示,下列说法正确的是( )
已知:。
A.点溶液中,
B.点溶液中,
C.点溶液中含有5种不同的微粒
D.点溶液中
第Ⅱ卷(非选择题,共52分)
二、填空题
17.(14分)Ⅰ、在一定的条件下,天然气脱硫工艺中会发生以下反应:
(1)则相同条件下反应的______(用含、和的代数式表示)。
Ⅱ、三氯化硅是制备硅烷、多晶硅的重要原料。已知在催化剂作用下发生反应:。一定条件下,向容积为的恒容密闭容器中充入,分别在温度为、条件下反应,测得反应体系中的物质的量分数随时间变化的关系如图所示(2)在温度下,的平衡转化率______%。若想进一步提高的转化率,除改变温度外还可以采取的措施是______。
(3)在温度下,经后反应达到平衡。
①内,的反应速率______。
②在温度下,该反应的平衡常数______(已知,压强平衡常数用各气体组分的分压代替物质的量浓度计算)。
(4)下列不能判断该反应达到平衡状态的是______(填标号)。
a. b.混合气体的密度不再发生变化
c.与的浓度之比不再改变 d.混合气体的平均摩尔质量不再发生变化
(5)温度为的平衡常数______
18.(12分)亚硝酸钠外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。某化学兴趣小组设计实验制备并探究其性质。
查阅资料信息:①;.
②酸性溶液可将低价氮的氧化物或酸根离子氧化为。
(1)的制备(夹持装置和加热装置均已略,已检查装置气密性)。
①若没有装置,则装置中与水发生反应:______(写化学方程式)。
②制得的固体中混有的杂质主要为,改进措施是在装置、间添加______,提高的纯度。
③装置中发生的主要反应的离子方程式为______。
(2)验证亚硝酸钠与70%硫酸反应的气体产物为和的混合气体。
已知:溶液可吸收;的沸点为21℃,熔点为。
①为了检验装置中生成的气体产物,装置的连接顺序是______。(按气流方向从左到右)
②反应前应打开弹簧夹1,先通入一段时间氮气,目的是______。
(3)测定某亚硝酸钠样品的纯度。
设该样品的杂质均不与酸性溶液反应,可用酸性溶液测定的含量。
称取亚硝酸钠样品溶于水配成溶液,取出溶液于锥形瓶中,再用的酸性标准溶液进行滴定,消耗酸性标准溶液的体积如表:
实验组 第一组 第二组 第三组 第四组
消耗酸性标准溶液的体积 9.97 10.02 12.01 10.01
该亚硝酸钠样品中的质量分数为______。
19.(12分)镍是一种常用的催化剂。以红土镍矿(主要含有、、、等)为原料,制取纳米镍粉,同时获得净水剂黄钠铁矾的工艺流程如下:
回答下列问题:
(1)黄钠铁矾中,铁的化合价为______价。
(2)过滤操作1时滤渣的化学式为______
(3)“沉铁”过程加入的目的是______,控制不同的条件可以得到不同的沉淀,所得沉淀与温度、的关系如图所示(图中阴影部分表示的是黄钠铁矾稳定存在区域)。若反应在120℃时进行,加入的偏多,则所得黄钠铁矾中混有的杂质是______(填化学式)。
(4)“转化”过程,向“过滤Ⅱ”所得滤液(富含)中加入,控制溶液中的浓度,可得到不同晶态物质(、或二者的混合物)。当生成和的物质的量之比为时,该反应的离子方程式为______。
(5)化学镀镍是金属表面镀镍的常用方法,以为镀液,次亚磷酸钠为还原剂,在90℃的酸性溶液中发生反应,被氧化为弱酸亚磷酸。写出化学镀镍反应的离子方程式:______。
20.(14分)苯是工业上常用的化工原料,可以用于合成安息香酸苄酯和高分化合物(部分反应条件略去),流程如下所示,请回答下列问题:
(1)的化学名称是______,中的官能团名称是______。
(2)生成的反应类型为______。
(3)生成的化学方程式为______。
(4)是的同分异构体,分子中含有酯基,有两个苯环且不直接相连,符合上述条件的结构有______种,其中核磁共振氢谱图有6组峰,且面积比为的同分异构体的结构简式为______(写出一种即可)。
(5)参照上述合成路线,以2-氯丙烷为原料,其它无机试剂和有机溶剂任选,设计2-甲基-2-丙醇的合成路线______。
参考答案
一、选择题(每题3分,共48分)
1 2 3 4 5 6 7 8
C A C A D C B B
9 10 11 12 13 14 15 16
C C B D C A A B
二、填空题(每空2分,共52分)
17.(1)// (2)①.20 ②.及时移出产物
(3)①. ②. (4)bd (5)
18.(1)①
②一个装有蒸馏水的洗气瓶,将转化成
③
(2)①C、E、D、B
②排尽装置中的空气,防止生成的被氧化,干扰气体产物的检验
(3)86.25%
19(1) (2) (3)①.调节溶液的 ②.
(4)
(5)
20.(1)①.苯甲酸钠(安息香酸钠) ②.羧基 (2)取代反应
(3)
(4)①.11 ②.或
(5)
同课章节目录
