人教版(2019)高中化学必修第二册学案(含答案) 核心素养提升_无机推断题的解题突破口
文档属性
| 名称 | 人教版(2019)高中化学必修第二册学案(含答案) 核心素养提升_无机推断题的解题突破口 |

|
|
| 格式 | doc | ||
| 文件大小 | 261.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-30 00:00:00 | ||
图片预览

文档简介
核心素养提升(五) 无机推断题的解题突破口
1.常见的特征转化关系
(1)直线转化关系
①非金属酸性氧化物酸盐:满足此关系的有C、N、S等。
②ABC(酸或碱):满足此关系的有NH3、S、N2、H2S、C、Na等。
(2)三角转化关系
①铁三角
涉及的化学方程式:
a.FeO+COFe+CO2
Fe2++Zn==Fe+Zn2+
b.Fe+2H+=Fe2++H2↑
2Fe+O22FeO
c.2Fe3++Fe==3Fe2+
d.2Fe2++Cl2==2Fe3++2Cl-
4FeO+O2==2Fe2O3
e.Fe2O3+3CO2Fe+3CO2
2Fe3++3Zn==2Fe+3Zn2+
f.2Fe+3Cl2==2FeCl3
Fe+NO+4H+==Fe3++NO↑+2H2O
②氮三角[]
涉及的化学方程式:
a.2NO+O2==2NO2
b.3NO2+H2O==2HNO3+NO
c.Cu+4HNO3(浓)==Cu(NO3)2+2NO2↑+2H2O
d.4NO+3O2+2H2O==4HNO3[]
e.3Cu+8HNO3(稀)==3Cu(NO3)2+2NO↑+4H2O
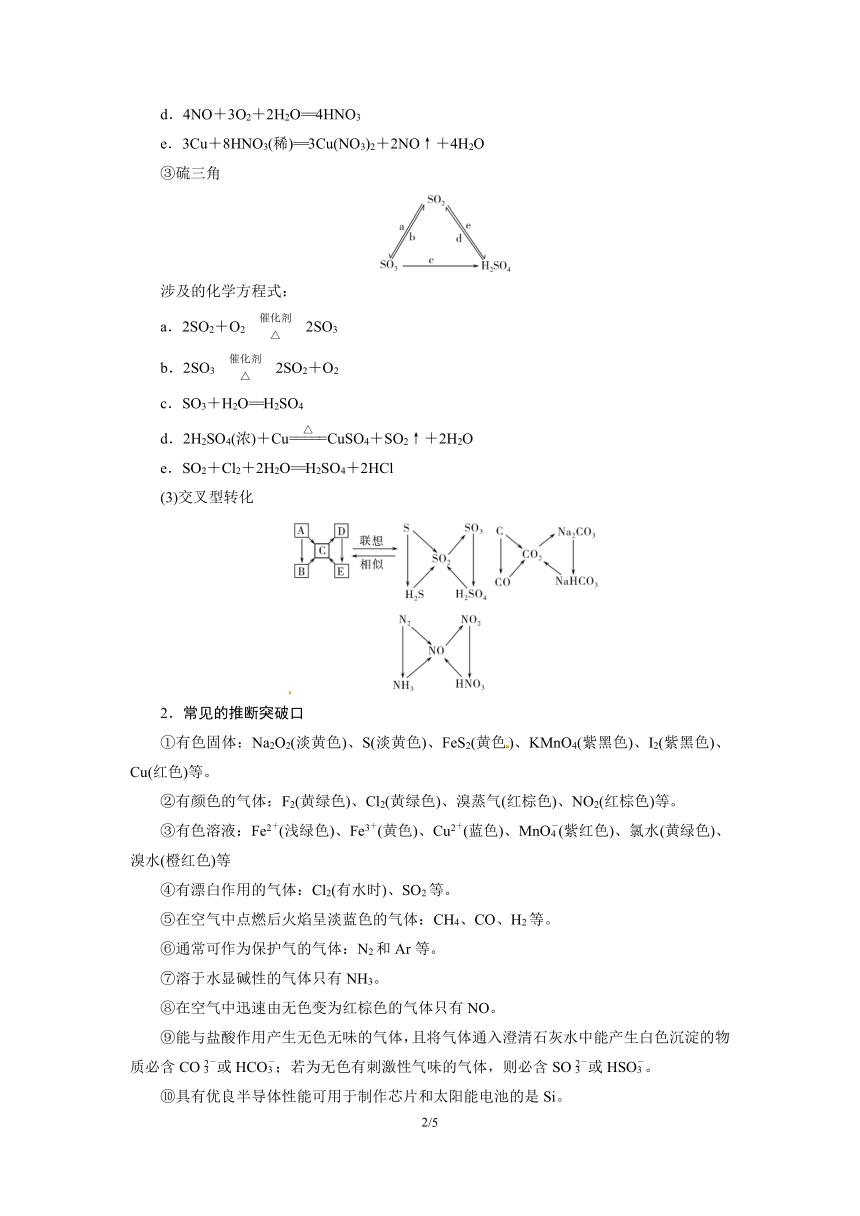
③硫三角
涉及的化学方程式:
a.2SO2+O22SO3
b.2SO32SO2+O2
c.SO3+H2O==H2SO4
d.2H2SO4(浓)+CuCuSO4+SO2↑+2H2O
e.SO2+Cl2+2H2O==H2SO4+2HCl
(3)交叉型转化
2.常见的推断突破口
①有色固体:Na2O2(淡黄色)、S(淡黄色)、FeS2(黄色)、KMnO4(紫黑色)、I2(紫黑色)、Cu(红色)等。
②有颜色的气体:F2(黄绿色)、Cl2(黄绿色)、溴蒸气(红棕色)、NO2(红棕色)等。
③有色溶液:Fe2+(浅绿色)、Fe3+(黄色)、Cu2+(蓝色)、MnO(紫红色)、氯水(黄绿色)、溴水(橙红色)等
④有漂白作用的气体:Cl2(有水时)、SO2等。
⑤在空气中点燃后火焰呈淡蓝色的气体:CH4、CO、H2等。
⑥通常可作为保护气的气体:N2和Ar等。
⑦溶于水显碱性的气体只有NH3。
⑧在空气中迅速由无色变为红棕色的气体只有NO。
⑨能与盐酸作用产生无色无味的气体,且将气体通入澄清石灰水中能产生白色沉淀的物质必含CO或HCO;若为无色有刺激性气味的气体,则必含SO或HSO。
⑩具有优良半导体性能可用于制作芯片和太阳能电池的是Si。
能够高效传输光信号可用于生产光导纤维的是SiO2。
3.根据特征反应推断
(1)常见特征反应条件:
2KClO32KCl+3O2↑;
2H2O22H2O+O2↑;
2SO2+O22SO3;
4NH3+5O24NO+6H2O;
N2+3H22NH3。
(2)常见特征反应
①与碱性溶液反应→气体:
2Al+2NaOH+2H2O==2NaAlO2+3H2↑;[]
②与H2O反应→气体:
2Na+2H2O==2NaOH+H2↑;
2Na2O2+2H2O==4NaOH+O2↑。
③与酸或碱都反应:
单质:Al;化合物:Al2O3、Al(OH)3、弱酸弱碱盐、弱酸铵盐、弱酸酸式盐。
(3)最高价氧化物对应水化物与气态氢化物反应生成盐的元素为N。
1.A、B、C、D、E都是中学化学中常见物质,它们均含有同一种元素,在一定条件下可发生如图所示的转化,其中A是单质,B在常温下是气态氢化物,C、D是氧化物,E是D和水反应的产物。下列判断中不合理的是( )[]
A.A不可能是金属
B.由C生成D肯定发生了电子转移
C.A生成C肯定属于离子反应
D.B和E可能会发生反应生成一种盐
C [根据图示转化关系,B为A的气态氢化物,因此A不可能为金属,A正确;根据C、D为A的不同氧化物,则由C生成D为氧化还原反应,B正确;根据图示关系,A有变价氧化物,可以推断A可能为N2、S等,此时A生成C的反应为单质和氧气的反应,肯定不是离子反应,C错误;当A为N2时,B为NH3,E为HNO3,NH3与HNO3反应生成NH4NO3,D正确。]
2.甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系:甲乙丙。下列有关物质的推断不正确的是( )
A.若甲为焦炭,则丁可能是O2
B.若甲为SO2,则丁可能是氨水
C.若甲为Fe,则丁可能是盐酸
D.若甲为NaOH溶液,则丁可能是CO2
C [A正确,若甲为C,丁为O2,乙为CO,丙为CO2。B正确,若甲为SO2,丁为氨水,乙为NH4HSO3,丙为(NH4)2SO3。C不正确,若甲为Fe,丁为盐酸,乙为FeCl2,FeCl2与盐酸不反应。D正确,若甲为NaOH溶液,丁为CO2,乙为Na2CO3,丙为NaHCO3。]
3.A、B、C、X是中学化学中常见的物质,它们之间的转化关系如图所示(部分产物已略去):
请回答下列问题:
(1)若X是强氧化性单质,则A不可能是__________(填序号)。
a.C B.N2
C.S D.Na e.Mg
(2)若A能使湿润的红色石蕊试纸变蓝色,C为红棕色气体,则A转化为B的化学方程式为_______________________________________________________。
(3)若A、B、C三种化合物的水溶液均呈酸性,写出A和B反应的化学方程式________________________________________________________________________。
(4)若X是金属单质,向B、C的溶液中分别滴加AgNO3溶液和稀硝酸均产生白色沉淀,则B的化学式是___________________________________________________,
保存C溶液常加少量的X,其目的是______________________________________。
解析 (1)C、N、S均为变价元素,当X为O2时均符合图示转化关系;Na与O2常温下生成Na2O,Na2O在加热条件下与O2反应生成Na2O2,也符合图示转化关系。Mg的化合价只有+2价,不符合图示转化关系。(2)A为NH3,C为NO2,则B为NO。(3)A为H2S,B为SO2,C为SO3。X为变价金属单质Fe,B、C的溶液中均含有Cl-,B为FeCl3,C为FeCl2,A为Cl2。保存FeCl2溶液时需加铁粉防止Fe2+被氧化成Fe3+。
答案 (1)e (2)4NH3+5O24NO+6H2O
(3)2H2S+SO2==3S↓+2H2O (4)FeCl3 防止Fe2+被氧化成Fe3+
4.黑色固体A加热至红热投入到无色溶液B中发生如图转化关系。
(1)由此可以推断:A为__________(填化学式,下同),B为__________,X为__________,C为__________,E为__________。
(2)写出A与B反应的化学方程式:________________________________________。
解析 结合框图,根据D(无色溶液)+F(单质)→G(蓝色溶液)+E(无色气体)可知F为Cu,则D为稀硝酸,E为NO,G为Cu(NO3)2溶液,继而推出气体X中有NO2,则气体C中有NO。气体C与澄清石灰水反应产生白色沉淀,A为黑色固体,所以气体C中还有CO2,X由NO2和CO2组成,A为C,B为浓硝酸。
答案 (1)C HNO3(浓) NO2和CO2 NO和CO2 NO (2)C+4HNO3(浓)4NO2↑+CO2↑+2H2O
5.如图所示为A、B、C、D、E五种含氮物质之间的相互转化关系。其中A、B、C、D在常温下都是气体,且B为红棕色气体。
(1)写出各物质的化学式:A__________,B__________,
C__________,D__________,E__________。
(2)写出各步反应的化学方程式。
①A→C:_______________________________________________________________。
②B→E:_________________________________________________________________。
③C→B:________________________________________________________________。
解析 由B为红棕色气体可知,B是NO2;C与O2反应能生成气体B,故C为NO;NO2与H2O反应生成E,且E与Cu能反应,故E为HNO3;由图中转化关系进一步分析,可知,A必为N2。[]
答案 (1)N2 NO2 NO NH3 HNO3
(2)N2+O22NO 3NO2+H2O==2HNO3+NO
2NO+O2==2NO2
1/5
1.常见的特征转化关系
(1)直线转化关系
①非金属酸性氧化物酸盐:满足此关系的有C、N、S等。
②ABC(酸或碱):满足此关系的有NH3、S、N2、H2S、C、Na等。
(2)三角转化关系
①铁三角
涉及的化学方程式:
a.FeO+COFe+CO2
Fe2++Zn==Fe+Zn2+
b.Fe+2H+=Fe2++H2↑
2Fe+O22FeO
c.2Fe3++Fe==3Fe2+
d.2Fe2++Cl2==2Fe3++2Cl-
4FeO+O2==2Fe2O3
e.Fe2O3+3CO2Fe+3CO2
2Fe3++3Zn==2Fe+3Zn2+
f.2Fe+3Cl2==2FeCl3
Fe+NO+4H+==Fe3++NO↑+2H2O
②氮三角[]
涉及的化学方程式:
a.2NO+O2==2NO2
b.3NO2+H2O==2HNO3+NO
c.Cu+4HNO3(浓)==Cu(NO3)2+2NO2↑+2H2O
d.4NO+3O2+2H2O==4HNO3[]
e.3Cu+8HNO3(稀)==3Cu(NO3)2+2NO↑+4H2O
③硫三角
涉及的化学方程式:
a.2SO2+O22SO3
b.2SO32SO2+O2
c.SO3+H2O==H2SO4
d.2H2SO4(浓)+CuCuSO4+SO2↑+2H2O
e.SO2+Cl2+2H2O==H2SO4+2HCl
(3)交叉型转化
2.常见的推断突破口
①有色固体:Na2O2(淡黄色)、S(淡黄色)、FeS2(黄色)、KMnO4(紫黑色)、I2(紫黑色)、Cu(红色)等。
②有颜色的气体:F2(黄绿色)、Cl2(黄绿色)、溴蒸气(红棕色)、NO2(红棕色)等。
③有色溶液:Fe2+(浅绿色)、Fe3+(黄色)、Cu2+(蓝色)、MnO(紫红色)、氯水(黄绿色)、溴水(橙红色)等
④有漂白作用的气体:Cl2(有水时)、SO2等。
⑤在空气中点燃后火焰呈淡蓝色的气体:CH4、CO、H2等。
⑥通常可作为保护气的气体:N2和Ar等。
⑦溶于水显碱性的气体只有NH3。
⑧在空气中迅速由无色变为红棕色的气体只有NO。
⑨能与盐酸作用产生无色无味的气体,且将气体通入澄清石灰水中能产生白色沉淀的物质必含CO或HCO;若为无色有刺激性气味的气体,则必含SO或HSO。
⑩具有优良半导体性能可用于制作芯片和太阳能电池的是Si。
能够高效传输光信号可用于生产光导纤维的是SiO2。
3.根据特征反应推断
(1)常见特征反应条件:
2KClO32KCl+3O2↑;
2H2O22H2O+O2↑;
2SO2+O22SO3;
4NH3+5O24NO+6H2O;
N2+3H22NH3。
(2)常见特征反应
①与碱性溶液反应→气体:
2Al+2NaOH+2H2O==2NaAlO2+3H2↑;[]
②与H2O反应→气体:
2Na+2H2O==2NaOH+H2↑;
2Na2O2+2H2O==4NaOH+O2↑。
③与酸或碱都反应:
单质:Al;化合物:Al2O3、Al(OH)3、弱酸弱碱盐、弱酸铵盐、弱酸酸式盐。
(3)最高价氧化物对应水化物与气态氢化物反应生成盐的元素为N。
1.A、B、C、D、E都是中学化学中常见物质,它们均含有同一种元素,在一定条件下可发生如图所示的转化,其中A是单质,B在常温下是气态氢化物,C、D是氧化物,E是D和水反应的产物。下列判断中不合理的是( )[]
A.A不可能是金属
B.由C生成D肯定发生了电子转移
C.A生成C肯定属于离子反应
D.B和E可能会发生反应生成一种盐
C [根据图示转化关系,B为A的气态氢化物,因此A不可能为金属,A正确;根据C、D为A的不同氧化物,则由C生成D为氧化还原反应,B正确;根据图示关系,A有变价氧化物,可以推断A可能为N2、S等,此时A生成C的反应为单质和氧气的反应,肯定不是离子反应,C错误;当A为N2时,B为NH3,E为HNO3,NH3与HNO3反应生成NH4NO3,D正确。]
2.甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系:甲乙丙。下列有关物质的推断不正确的是( )
A.若甲为焦炭,则丁可能是O2
B.若甲为SO2,则丁可能是氨水
C.若甲为Fe,则丁可能是盐酸
D.若甲为NaOH溶液,则丁可能是CO2
C [A正确,若甲为C,丁为O2,乙为CO,丙为CO2。B正确,若甲为SO2,丁为氨水,乙为NH4HSO3,丙为(NH4)2SO3。C不正确,若甲为Fe,丁为盐酸,乙为FeCl2,FeCl2与盐酸不反应。D正确,若甲为NaOH溶液,丁为CO2,乙为Na2CO3,丙为NaHCO3。]
3.A、B、C、X是中学化学中常见的物质,它们之间的转化关系如图所示(部分产物已略去):
请回答下列问题:
(1)若X是强氧化性单质,则A不可能是__________(填序号)。
a.C B.N2
C.S D.Na e.Mg
(2)若A能使湿润的红色石蕊试纸变蓝色,C为红棕色气体,则A转化为B的化学方程式为_______________________________________________________。
(3)若A、B、C三种化合物的水溶液均呈酸性,写出A和B反应的化学方程式________________________________________________________________________。
(4)若X是金属单质,向B、C的溶液中分别滴加AgNO3溶液和稀硝酸均产生白色沉淀,则B的化学式是___________________________________________________,
保存C溶液常加少量的X,其目的是______________________________________。
解析 (1)C、N、S均为变价元素,当X为O2时均符合图示转化关系;Na与O2常温下生成Na2O,Na2O在加热条件下与O2反应生成Na2O2,也符合图示转化关系。Mg的化合价只有+2价,不符合图示转化关系。(2)A为NH3,C为NO2,则B为NO。(3)A为H2S,B为SO2,C为SO3。X为变价金属单质Fe,B、C的溶液中均含有Cl-,B为FeCl3,C为FeCl2,A为Cl2。保存FeCl2溶液时需加铁粉防止Fe2+被氧化成Fe3+。
答案 (1)e (2)4NH3+5O24NO+6H2O
(3)2H2S+SO2==3S↓+2H2O (4)FeCl3 防止Fe2+被氧化成Fe3+
4.黑色固体A加热至红热投入到无色溶液B中发生如图转化关系。
(1)由此可以推断:A为__________(填化学式,下同),B为__________,X为__________,C为__________,E为__________。
(2)写出A与B反应的化学方程式:________________________________________。
解析 结合框图,根据D(无色溶液)+F(单质)→G(蓝色溶液)+E(无色气体)可知F为Cu,则D为稀硝酸,E为NO,G为Cu(NO3)2溶液,继而推出气体X中有NO2,则气体C中有NO。气体C与澄清石灰水反应产生白色沉淀,A为黑色固体,所以气体C中还有CO2,X由NO2和CO2组成,A为C,B为浓硝酸。
答案 (1)C HNO3(浓) NO2和CO2 NO和CO2 NO (2)C+4HNO3(浓)4NO2↑+CO2↑+2H2O
5.如图所示为A、B、C、D、E五种含氮物质之间的相互转化关系。其中A、B、C、D在常温下都是气体,且B为红棕色气体。
(1)写出各物质的化学式:A__________,B__________,
C__________,D__________,E__________。
(2)写出各步反应的化学方程式。
①A→C:_______________________________________________________________。
②B→E:_________________________________________________________________。
③C→B:________________________________________________________________。
解析 由B为红棕色气体可知,B是NO2;C与O2反应能生成气体B,故C为NO;NO2与H2O反应生成E,且E与Cu能反应,故E为HNO3;由图中转化关系进一步分析,可知,A必为N2。[]
答案 (1)N2 NO2 NO NH3 HNO3
(2)N2+O22NO 3NO2+H2O==2HNO3+NO
2NO+O2==2NO2
1/5
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
