第三单元 溶液 综合素质评价试题(含答案)
文档属性
| 名称 | 第三单元 溶液 综合素质评价试题(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 410.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-31 00:00:00 | ||
图片预览



文档简介
第三单元 溶液 综合素质评价
一、选择题(每小题3分,共30分)
1.[2022·湘西]“油、盐、酱、醋、糖”是家庭常用的厨房用品,其中与水混合不能形成溶液的是( )
A.植物油 B.食盐 C.米醋 D.白砂糖
2.[2022·福建]从植物“地不容”中提取抑制某病毒的新药——千金藤素,需用到5%的Na2CO3溶液。若配制100 g该溶液,需要称取Na2CO3的质量为( )
A.95 g B.90 g C.20 g D.5 g
3.[2022·德阳]实验室配制50 g 16%的氯化钠溶液的步骤有计算、称量、溶解和装瓶等。如图所示仪器在配制该溶液的过程中不会用到的是( )
INCLUDEPICTURE"5HX190.EPS" INCLUDEPICTURE \d "D:\\马银钏\\23秋 典中点 9 化学 LJ六三(马银钏\\5HX190.EPS" \* MERGEFORMATINET
4.[2022·龙东改编]下列有关溶液的说法正确的是( )
A.均一、稳定的液体都是溶液
B.硝酸铵溶于水会放出大量的热
C.汽油和洗涤剂除油污的原理是相同的
D.加入溶质能使不饱和溶液变为饱和溶液
5.[2022·贵港]下列有关配制50 g溶质质量分数为10%的氯化钠溶液的操作中,正确的是( )
6.下列有关水与溶液的说法错误的是( )
A.电解水时,负极产生的是氢气
B.溶液是均一、稳定的混合物
C.饱和溶液就是不能再溶解任何物质的溶液
D.天然淡水生产自来水需要经过沉降、过滤、杀菌消毒等净化过程
7.[2023·济南模拟]用MgCl2溶液喷洒路面可融雪、防尘。20 ℃时,按下表数据配制溶液。
序号 ① ② ③ ④
MgCl2的质量/g 30 40 50 60
水的质量/g 100 100 100 100
(已知:20 ℃时,MgCl2在100 g水中的最大溶解量为54.6 g)
①中溶质的质量分数约为( )
A.23% B.30% C.35% D.43%
8.下列有关溶液的说法不正确的是( )
A.洗涤剂去油污主要利用了乳化作用
B.溶液一定是无色的,且溶剂一定是水
C.NH4NO3固体溶于水时会出现吸热现象
D.一种溶剂可同时溶解多种溶质
9.下列关于溶液的说法错误的是( )
A.固体、液体、气体都可以作溶质
B.NH4NO3溶解过程中吸热,溶液温度降低
C.欲使100 g KNO3溶液的质量分数由5%变成10%,可向其中加入5 g KNO3固体
D.25 ℃时,将某KNO3溶液蒸发10 g水析出a g晶体,再蒸发10 g水析出b g晶体,a与b不一定相等
10.将30 g固体物质X(不含结晶水)投入盛有20 g水的烧杯中,搅拌,测得0 ℃、t1 ℃、t2 ℃、t3 ℃时烧杯中溶液的质量分别如图中甲、乙、丙、丁四点所示。下列判断不正确的是( )
A.0 ℃时,甲溶液中物质X的质量为4 g
B.t1 ℃时,物质X的溶解量比0 ℃时大
C.t2 ℃时,丙溶液一定是饱和溶液
D.t3 ℃时的丁溶液降温到t2 ℃时,没有晶体析出
二、填空题(32分)
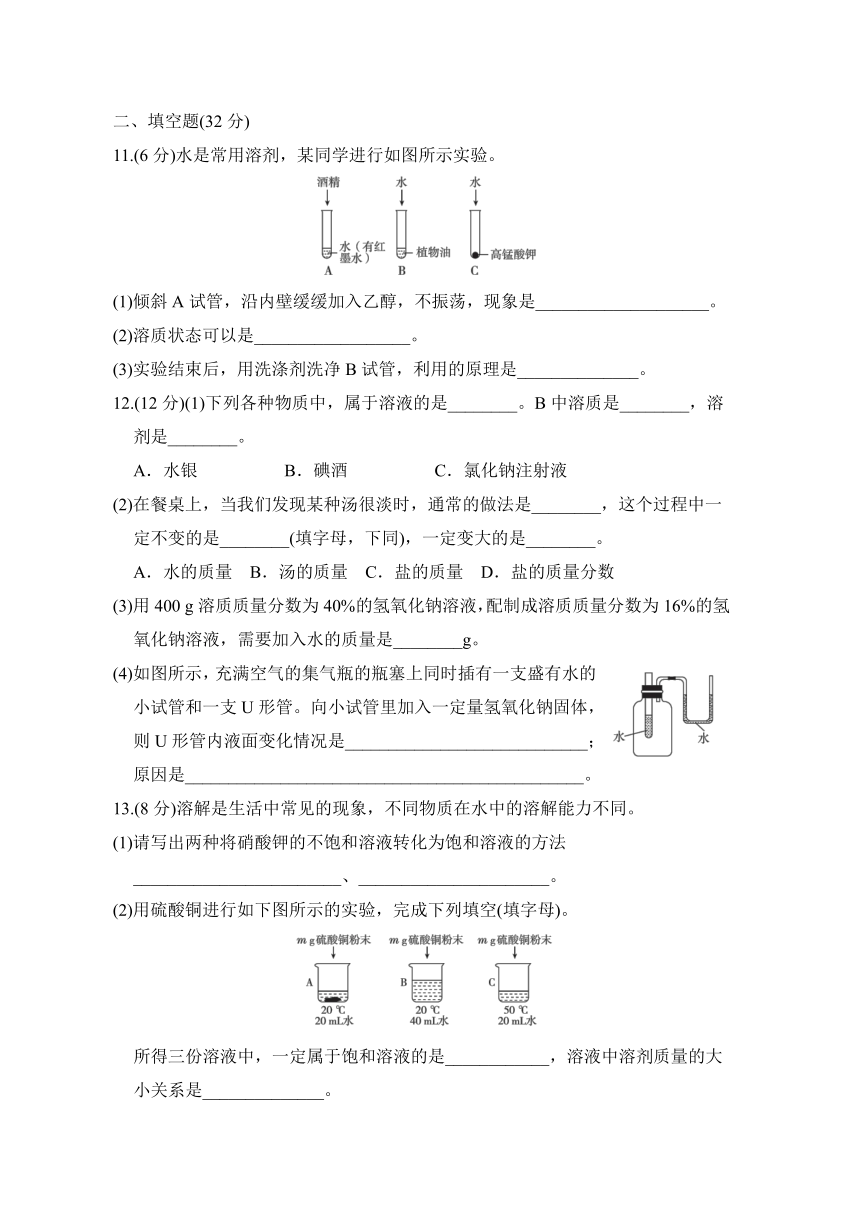
11.(6分)水是常用溶剂,某同学进行如图所示实验。
INCLUDEPICTURE"ZX110.EPS" INCLUDEPICTURE \d "D:\\马银钏\\23秋 典中点 9 化学 LJ六三(马银钏\\ZX110.EPS" \* MERGEFORMATINET
(1)倾斜A试管,沿内壁缓缓加入乙醇,不振荡,现象是____________________。
(2)溶质状态可以是__________________。
(3)实验结束后,用洗涤剂洗净B试管,利用的原理是______________。
12.(12分)(1)下列各种物质中,属于溶液的是________。B中溶质是________,溶剂是________。
A.水银 B.碘酒 C.氯化钠注射液
(2)在餐桌上,当我们发现某种汤很淡时,通常的做法是________,这个过程中一定不变的是________(填字母,下同),一定变大的是________。
A.水的质量 B.汤的质量 C.盐的质量 D.盐的质量分数
(3)用400 g溶质质量分数为40%的氢氧化钠溶液,配制成溶质质量分数为16%的氢氧化钠溶液,需要加入水的质量是________g。
(4)如图所示,充满空气的集气瓶的瓶塞上同时插有一支盛有水的
小试管和一支U形管。向小试管里加入一定量氢氧化钠固体,
则U形管内液面变化情况是____________________________;
原因是______________________________________________。
13.(8分)溶解是生活中常见的现象,不同物质在水中的溶解能力不同。
(1)请写出两种将硝酸钾的不饱和溶液转化为饱和溶液的方法________________________、______________________。
(2)用硫酸铜进行如下图所示的实验,完成下列填空(填字母)。
INCLUDEPICTURE"EE114.EPS" INCLUDEPICTURE \d "D:\\马银钏\\23秋 典中点 9 化学 LJ六三(马银钏\\EE114.EPS" \* MERGEFORMATINET
所得三份溶液中,一定属于饱和溶液的是____________,溶液中溶剂质量的大小关系是______________。
14.(6分)烧杯中盛有一定质量、温度为80 ℃、溶质为M的溶液,将其置于室温环境中,测定不同温度时析出固体M的质量。测定结果记录如下表。
溶液的温度/℃ 75 65 50 35 20
析出固体M的质量/g 0 0 2.0 4.5 8.4
若不考虑水蒸发对实验的影响,请回答下列问题:
(1)65 ℃时,该溶液是否为饱和溶液?____________(填“是”“否”或“无法判断”)。
(2)将40 ℃时接近饱和的M溶液变成饱和溶液,下列方法中一定能达到目的的有________(填序号)。
①升温 ②降温 ③加溶质M ④加水 ⑤加另一种固体N ⑥恒温蒸发水
⑦与40 ℃时M的饱和溶液混合
(3)20 ℃时,用固体粉末M和水配制100 g溶质质量分数为5%的M溶液,必须用到的仪器有:托盘天平(带砝码盒)、烧杯、_________________________________。
三、探究实验题(16分)
15.(6分)学习开启了我们认识物质之旅。我们知道了物质在溶解过程中会发生能量变化。如图所示,同学们设计了不同的实验方案进行探究:
INCLUDEPICTURE"ZX111.EPS" INCLUDEPICTURE \d "D:\\马银钏\\23秋 典中点 9 化学 LJ六三(马银钏\\ZX111.EPS" \* MERGEFORMATINET
(1)实验一中的硝酸铵溶解后,溶液温度________(填“升高”“降低”或“不变”)。
(2)实验二所加试剂及用量如图所示,将分液漏斗中的水全部加入试管后,立即关闭分液漏斗的活塞,此时观察到________________________,由此小明得出“氢氧化钠溶于水时放出热量”的结论,你是否同意小明的结论并写出你的理由
__________________________________________________________________。
16.(10分)某兴趣小组利用NaCl配制100 g溶质质量分数为15%的氯化钠溶液(假设称量氯化钠时1 g以下用游码)。请完成下列问题:
(1)配制时,除图中提供的仪器外,还需要试剂瓶和__________(填一种仪器名称)。
(2)称量氯化钠时如果发现指针偏向右侧,正确的操作是________________________________________________________________;
如果称量时氯化钠和砝码位置颠倒了,其他操作步骤均正确,则所配制溶液的溶质质量分数________(填“大于”“等于”或“小于”)15%。
(3)量取水时应选择量筒的规格是________(填“10”“50”或“100”)mL。
【反思拓展】
(4)经检测所配溶液的溶质质量分数偏小,原因可能是__________________(列举一条即可)。
四、计算题(22分)
17.(12分)20 ℃时,将10 g氯化钠完全溶于40 g水中,求:
(1)所得溶液中溶质的质量分数是多少?
(2)若欲使原溶液的溶质质量分数减少一半,需加水多少克?
18.(10分)若配制100 g溶质质量分数为20%的稀硫酸,需溶质质量分数为98%的浓硫酸的体积是多少?(已知:溶质质量分数为98%的浓硫酸的密度为1.84 g/mL,结果保留整数)
答案
一、1.A 【点拨】植物油难溶于水,不能和水形成均一、稳定的混合物,即不能形成溶液。
2.D 【点拨】配制100 g 5%的Na2CO3溶液,需碳酸钠的质量=100 g×5%=5 g。
3.B 【点拨】配制溶液的过程中量筒用于准确量取水,天平称量固体氯化钠的质量,烧杯用于完成溶解操作,不需要使用锥形瓶。故选B。
4.D 【点拨】溶液是均一、稳定的混合物,均一、稳定的液体不一定是溶液,如水,A错误;硝酸铵溶于水会吸收大量的热,B错误;汽油能溶解油污,汽油除油污是利用溶解原理;洗涤剂有乳化作用,二者除油污原理不同,C错误;不饱和溶液还能继续溶解溶质,加入溶质可使不饱和溶液变为饱和溶液,D正确。
5.C 【点拨】取用固体粉末状药品时,瓶塞要倒放,A错误;托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了,B错误;量取液体时,视线应与液体的凹液面的最低处保持水平,C正确;配制氯化钠溶液时,溶解操作应在烧杯中进行,不能在量筒内进行,D错误。
6.C 【点拨】饱和溶液还能再溶解其他物质,如一定温度下的蔗糖的饱和溶液不能再溶解蔗糖,但还能溶解氯化钠。
7.A 【点拨】20 ℃时,将30 g氯化镁放入100 g水中,充分搅拌后得到的是该温度下氯化镁的不饱和溶液,溶液中溶质的质量分数为×100%≈23%。
8.B 【点拨】溶液不一定是无色的,如硫酸铜溶液显蓝色;且溶剂不一定是水,汽油、酒精等也可以作溶剂。
9.C 【点拨】溶质可以是固体、液体、气体,溶剂一般是液体,A正确;NH4NO3溶解过程中吸热,溶液温度降低,B正确;加入5 g KNO3固体后溶质质量分
数=×100%≈9.5%,C错误;如果原硝酸钾溶液是不饱和溶液, 则a与b一定不相等,D正确。
10.C 【点拨】丙、丁对应的溶液质量均为50 g,溶剂质量均为20 g,溶质质量均为50 g-20 g=30 g,故t3 ℃时的丁溶液降温到t2 ℃时,没有晶体析出,D
正确。
二、11.(1)液体分层,上层无色,下层红色 (2)固体或液体或气体 (3)乳化原理
【点拨】(1)倾斜A试管,沿内壁缓缓加入乙醇,不振荡,现象是液体分层,上层无色,下层红色。
(2)由实验可知,溶质状态可以是固体、液体或气体。
(3)实验结束后,用洗涤剂洗净B试管,原理是利用洗涤剂能够乳化植物油。
12.(1)B、C;碘;酒精 (2)加食盐;A;B、C、D (3)600
(4)左侧液面下降,右侧液面上升;氢氧化钠溶于水放热,使集气瓶内气体温度升高,压强增大
【点拨】(1)水银常温下为液体,属于纯净物,不属于溶液;碘酒是均一、稳定的混合物,属于溶液,其溶质为碘,溶剂为酒精;氯化钠注射液是均一、稳定的混合物,属于溶液。
(2)汤很淡时加入食盐,食盐溶解在汤中,增加汤的咸味。此过程中不改变水的质量,但溶液中盐的质量增加,汤的质量也随之增加,盐的质量分数也增加。
(3)设需要加入水的质量为x,则400 g×40%=(400 g+x)×16%,解之得x=
600 g。
(4)氢氧化钠溶于水放出大量热,瓶内气体受热膨胀,气体压强增大,U形管内左侧液面下降,右侧液面上升。
13.(1)降低温度至刚好有固体析出;加入硝酸钾固体至不再溶解(或恒温蒸发溶剂至刚好有固体析出)
(2)A;B>C=A
【点拨】(1)将硝酸钾的不饱和溶液转化为饱和溶液,可以采用加入硝酸钾、恒温蒸发溶剂、降低温度等方法。(2)A中有固体剩余,一定属于饱和溶液;A、C中溶剂均为20 mL ,B中溶剂为40 mL,则溶液中溶剂质量的大小关系是
B>C=A。
14.(1)无法判断 (2)②③⑥
(3)药匙、量筒(100 mL)、胶头滴管、玻璃棒
【点拨】(1)温度降至65 ℃时无晶体析出,无法判断溶液是否饱和。
(3)配制一定溶质质量分数的溶液的步骤有计算、称量(量取)、溶解,称量固体时需用到托盘天平和药匙,量取液体时需用到量筒(100 mL)和胶头滴管,溶解时需用到烧杯和玻璃棒。
三、15.(1)降低
(2)U形管内的液面左侧下降,右侧上升;不同意,因为加入试管中的10 mL水占据一定体积,导致试管中的气体被挤压,也会导致U形管内液面左侧下降,右侧上升
【点拨】(1)硝酸铵溶于水,溶液温度降低;(2)加入10 mL水后试管中的部分空气被排出,也会使U形管中液面左低右高,无法得到小明的结论。
16.(1)胶头滴管
(2)在左盘添加氯化钠至天平平衡;等于
(3)100 (4)量取水时仰视读数(合理即可)
【点拨】(1)配制溶液的步骤是计算、称量、量取、溶解、装瓶贴标签。配制过程中除图中提供的仪器外,还需要试剂瓶和胶头滴管。
(2)称量氯化钠时如果发现指针偏向右侧,说明氯化钠取少了,故应继续添加氯化钠直至天平平衡;配制100 g溶质质量分数为15%的氯化钠溶液,需要氯化钠的质量=100 g×15%=15 g。如果称量时氯化钠和砝码的位置颠倒了,但此称量过程中不需要移动游码,故所配制溶液的溶质质量分数不变,等于15%。
(3)所配溶液的溶质质量分数偏小,可能是溶质质量偏小或溶剂质量偏大,故原因可能有将氯化钠倒入烧杯时有撒落或配制溶液的烧杯中有水或量取水时仰视读数等(合理即可)。
四、17.【解】(1)所得溶液中溶质的质量分数为×100%=20%;
(2)设需要加水的质量为x,则:
×100%=20%× x=50 g
答:(1)所得溶液中溶质的质量分数是20%;(2)若欲使原溶液的溶质质量分数减少一半,需加50 g水。
18.【解】设需要浓硫酸的体积为V。
1.84 g/mL×V×98%=100 g×20%
V≈11 mL
答:需要溶质质量分数为98%的浓硫酸的体积约为11 mL。
一、选择题(每小题3分,共30分)
1.[2022·湘西]“油、盐、酱、醋、糖”是家庭常用的厨房用品,其中与水混合不能形成溶液的是( )
A.植物油 B.食盐 C.米醋 D.白砂糖
2.[2022·福建]从植物“地不容”中提取抑制某病毒的新药——千金藤素,需用到5%的Na2CO3溶液。若配制100 g该溶液,需要称取Na2CO3的质量为( )
A.95 g B.90 g C.20 g D.5 g
3.[2022·德阳]实验室配制50 g 16%的氯化钠溶液的步骤有计算、称量、溶解和装瓶等。如图所示仪器在配制该溶液的过程中不会用到的是( )
INCLUDEPICTURE"5HX190.EPS" INCLUDEPICTURE \d "D:\\马银钏\\23秋 典中点 9 化学 LJ六三(马银钏\\5HX190.EPS" \* MERGEFORMATINET
4.[2022·龙东改编]下列有关溶液的说法正确的是( )
A.均一、稳定的液体都是溶液
B.硝酸铵溶于水会放出大量的热
C.汽油和洗涤剂除油污的原理是相同的
D.加入溶质能使不饱和溶液变为饱和溶液
5.[2022·贵港]下列有关配制50 g溶质质量分数为10%的氯化钠溶液的操作中,正确的是( )
6.下列有关水与溶液的说法错误的是( )
A.电解水时,负极产生的是氢气
B.溶液是均一、稳定的混合物
C.饱和溶液就是不能再溶解任何物质的溶液
D.天然淡水生产自来水需要经过沉降、过滤、杀菌消毒等净化过程
7.[2023·济南模拟]用MgCl2溶液喷洒路面可融雪、防尘。20 ℃时,按下表数据配制溶液。
序号 ① ② ③ ④
MgCl2的质量/g 30 40 50 60
水的质量/g 100 100 100 100
(已知:20 ℃时,MgCl2在100 g水中的最大溶解量为54.6 g)
①中溶质的质量分数约为( )
A.23% B.30% C.35% D.43%
8.下列有关溶液的说法不正确的是( )
A.洗涤剂去油污主要利用了乳化作用
B.溶液一定是无色的,且溶剂一定是水
C.NH4NO3固体溶于水时会出现吸热现象
D.一种溶剂可同时溶解多种溶质
9.下列关于溶液的说法错误的是( )
A.固体、液体、气体都可以作溶质
B.NH4NO3溶解过程中吸热,溶液温度降低
C.欲使100 g KNO3溶液的质量分数由5%变成10%,可向其中加入5 g KNO3固体
D.25 ℃时,将某KNO3溶液蒸发10 g水析出a g晶体,再蒸发10 g水析出b g晶体,a与b不一定相等
10.将30 g固体物质X(不含结晶水)投入盛有20 g水的烧杯中,搅拌,测得0 ℃、t1 ℃、t2 ℃、t3 ℃时烧杯中溶液的质量分别如图中甲、乙、丙、丁四点所示。下列判断不正确的是( )
A.0 ℃时,甲溶液中物质X的质量为4 g
B.t1 ℃时,物质X的溶解量比0 ℃时大
C.t2 ℃时,丙溶液一定是饱和溶液
D.t3 ℃时的丁溶液降温到t2 ℃时,没有晶体析出
二、填空题(32分)
11.(6分)水是常用溶剂,某同学进行如图所示实验。
INCLUDEPICTURE"ZX110.EPS" INCLUDEPICTURE \d "D:\\马银钏\\23秋 典中点 9 化学 LJ六三(马银钏\\ZX110.EPS" \* MERGEFORMATINET
(1)倾斜A试管,沿内壁缓缓加入乙醇,不振荡,现象是____________________。
(2)溶质状态可以是__________________。
(3)实验结束后,用洗涤剂洗净B试管,利用的原理是______________。
12.(12分)(1)下列各种物质中,属于溶液的是________。B中溶质是________,溶剂是________。
A.水银 B.碘酒 C.氯化钠注射液
(2)在餐桌上,当我们发现某种汤很淡时,通常的做法是________,这个过程中一定不变的是________(填字母,下同),一定变大的是________。
A.水的质量 B.汤的质量 C.盐的质量 D.盐的质量分数
(3)用400 g溶质质量分数为40%的氢氧化钠溶液,配制成溶质质量分数为16%的氢氧化钠溶液,需要加入水的质量是________g。
(4)如图所示,充满空气的集气瓶的瓶塞上同时插有一支盛有水的
小试管和一支U形管。向小试管里加入一定量氢氧化钠固体,
则U形管内液面变化情况是____________________________;
原因是______________________________________________。
13.(8分)溶解是生活中常见的现象,不同物质在水中的溶解能力不同。
(1)请写出两种将硝酸钾的不饱和溶液转化为饱和溶液的方法________________________、______________________。
(2)用硫酸铜进行如下图所示的实验,完成下列填空(填字母)。
INCLUDEPICTURE"EE114.EPS" INCLUDEPICTURE \d "D:\\马银钏\\23秋 典中点 9 化学 LJ六三(马银钏\\EE114.EPS" \* MERGEFORMATINET
所得三份溶液中,一定属于饱和溶液的是____________,溶液中溶剂质量的大小关系是______________。
14.(6分)烧杯中盛有一定质量、温度为80 ℃、溶质为M的溶液,将其置于室温环境中,测定不同温度时析出固体M的质量。测定结果记录如下表。
溶液的温度/℃ 75 65 50 35 20
析出固体M的质量/g 0 0 2.0 4.5 8.4
若不考虑水蒸发对实验的影响,请回答下列问题:
(1)65 ℃时,该溶液是否为饱和溶液?____________(填“是”“否”或“无法判断”)。
(2)将40 ℃时接近饱和的M溶液变成饱和溶液,下列方法中一定能达到目的的有________(填序号)。
①升温 ②降温 ③加溶质M ④加水 ⑤加另一种固体N ⑥恒温蒸发水
⑦与40 ℃时M的饱和溶液混合
(3)20 ℃时,用固体粉末M和水配制100 g溶质质量分数为5%的M溶液,必须用到的仪器有:托盘天平(带砝码盒)、烧杯、_________________________________。
三、探究实验题(16分)
15.(6分)学习开启了我们认识物质之旅。我们知道了物质在溶解过程中会发生能量变化。如图所示,同学们设计了不同的实验方案进行探究:
INCLUDEPICTURE"ZX111.EPS" INCLUDEPICTURE \d "D:\\马银钏\\23秋 典中点 9 化学 LJ六三(马银钏\\ZX111.EPS" \* MERGEFORMATINET
(1)实验一中的硝酸铵溶解后,溶液温度________(填“升高”“降低”或“不变”)。
(2)实验二所加试剂及用量如图所示,将分液漏斗中的水全部加入试管后,立即关闭分液漏斗的活塞,此时观察到________________________,由此小明得出“氢氧化钠溶于水时放出热量”的结论,你是否同意小明的结论并写出你的理由
__________________________________________________________________。
16.(10分)某兴趣小组利用NaCl配制100 g溶质质量分数为15%的氯化钠溶液(假设称量氯化钠时1 g以下用游码)。请完成下列问题:
(1)配制时,除图中提供的仪器外,还需要试剂瓶和__________(填一种仪器名称)。
(2)称量氯化钠时如果发现指针偏向右侧,正确的操作是________________________________________________________________;
如果称量时氯化钠和砝码位置颠倒了,其他操作步骤均正确,则所配制溶液的溶质质量分数________(填“大于”“等于”或“小于”)15%。
(3)量取水时应选择量筒的规格是________(填“10”“50”或“100”)mL。
【反思拓展】
(4)经检测所配溶液的溶质质量分数偏小,原因可能是__________________(列举一条即可)。
四、计算题(22分)
17.(12分)20 ℃时,将10 g氯化钠完全溶于40 g水中,求:
(1)所得溶液中溶质的质量分数是多少?
(2)若欲使原溶液的溶质质量分数减少一半,需加水多少克?
18.(10分)若配制100 g溶质质量分数为20%的稀硫酸,需溶质质量分数为98%的浓硫酸的体积是多少?(已知:溶质质量分数为98%的浓硫酸的密度为1.84 g/mL,结果保留整数)
答案
一、1.A 【点拨】植物油难溶于水,不能和水形成均一、稳定的混合物,即不能形成溶液。
2.D 【点拨】配制100 g 5%的Na2CO3溶液,需碳酸钠的质量=100 g×5%=5 g。
3.B 【点拨】配制溶液的过程中量筒用于准确量取水,天平称量固体氯化钠的质量,烧杯用于完成溶解操作,不需要使用锥形瓶。故选B。
4.D 【点拨】溶液是均一、稳定的混合物,均一、稳定的液体不一定是溶液,如水,A错误;硝酸铵溶于水会吸收大量的热,B错误;汽油能溶解油污,汽油除油污是利用溶解原理;洗涤剂有乳化作用,二者除油污原理不同,C错误;不饱和溶液还能继续溶解溶质,加入溶质可使不饱和溶液变为饱和溶液,D正确。
5.C 【点拨】取用固体粉末状药品时,瓶塞要倒放,A错误;托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了,B错误;量取液体时,视线应与液体的凹液面的最低处保持水平,C正确;配制氯化钠溶液时,溶解操作应在烧杯中进行,不能在量筒内进行,D错误。
6.C 【点拨】饱和溶液还能再溶解其他物质,如一定温度下的蔗糖的饱和溶液不能再溶解蔗糖,但还能溶解氯化钠。
7.A 【点拨】20 ℃时,将30 g氯化镁放入100 g水中,充分搅拌后得到的是该温度下氯化镁的不饱和溶液,溶液中溶质的质量分数为×100%≈23%。
8.B 【点拨】溶液不一定是无色的,如硫酸铜溶液显蓝色;且溶剂不一定是水,汽油、酒精等也可以作溶剂。
9.C 【点拨】溶质可以是固体、液体、气体,溶剂一般是液体,A正确;NH4NO3溶解过程中吸热,溶液温度降低,B正确;加入5 g KNO3固体后溶质质量分
数=×100%≈9.5%,C错误;如果原硝酸钾溶液是不饱和溶液, 则a与b一定不相等,D正确。
10.C 【点拨】丙、丁对应的溶液质量均为50 g,溶剂质量均为20 g,溶质质量均为50 g-20 g=30 g,故t3 ℃时的丁溶液降温到t2 ℃时,没有晶体析出,D
正确。
二、11.(1)液体分层,上层无色,下层红色 (2)固体或液体或气体 (3)乳化原理
【点拨】(1)倾斜A试管,沿内壁缓缓加入乙醇,不振荡,现象是液体分层,上层无色,下层红色。
(2)由实验可知,溶质状态可以是固体、液体或气体。
(3)实验结束后,用洗涤剂洗净B试管,原理是利用洗涤剂能够乳化植物油。
12.(1)B、C;碘;酒精 (2)加食盐;A;B、C、D (3)600
(4)左侧液面下降,右侧液面上升;氢氧化钠溶于水放热,使集气瓶内气体温度升高,压强增大
【点拨】(1)水银常温下为液体,属于纯净物,不属于溶液;碘酒是均一、稳定的混合物,属于溶液,其溶质为碘,溶剂为酒精;氯化钠注射液是均一、稳定的混合物,属于溶液。
(2)汤很淡时加入食盐,食盐溶解在汤中,增加汤的咸味。此过程中不改变水的质量,但溶液中盐的质量增加,汤的质量也随之增加,盐的质量分数也增加。
(3)设需要加入水的质量为x,则400 g×40%=(400 g+x)×16%,解之得x=
600 g。
(4)氢氧化钠溶于水放出大量热,瓶内气体受热膨胀,气体压强增大,U形管内左侧液面下降,右侧液面上升。
13.(1)降低温度至刚好有固体析出;加入硝酸钾固体至不再溶解(或恒温蒸发溶剂至刚好有固体析出)
(2)A;B>C=A
【点拨】(1)将硝酸钾的不饱和溶液转化为饱和溶液,可以采用加入硝酸钾、恒温蒸发溶剂、降低温度等方法。(2)A中有固体剩余,一定属于饱和溶液;A、C中溶剂均为20 mL ,B中溶剂为40 mL,则溶液中溶剂质量的大小关系是
B>C=A。
14.(1)无法判断 (2)②③⑥
(3)药匙、量筒(100 mL)、胶头滴管、玻璃棒
【点拨】(1)温度降至65 ℃时无晶体析出,无法判断溶液是否饱和。
(3)配制一定溶质质量分数的溶液的步骤有计算、称量(量取)、溶解,称量固体时需用到托盘天平和药匙,量取液体时需用到量筒(100 mL)和胶头滴管,溶解时需用到烧杯和玻璃棒。
三、15.(1)降低
(2)U形管内的液面左侧下降,右侧上升;不同意,因为加入试管中的10 mL水占据一定体积,导致试管中的气体被挤压,也会导致U形管内液面左侧下降,右侧上升
【点拨】(1)硝酸铵溶于水,溶液温度降低;(2)加入10 mL水后试管中的部分空气被排出,也会使U形管中液面左低右高,无法得到小明的结论。
16.(1)胶头滴管
(2)在左盘添加氯化钠至天平平衡;等于
(3)100 (4)量取水时仰视读数(合理即可)
【点拨】(1)配制溶液的步骤是计算、称量、量取、溶解、装瓶贴标签。配制过程中除图中提供的仪器外,还需要试剂瓶和胶头滴管。
(2)称量氯化钠时如果发现指针偏向右侧,说明氯化钠取少了,故应继续添加氯化钠直至天平平衡;配制100 g溶质质量分数为15%的氯化钠溶液,需要氯化钠的质量=100 g×15%=15 g。如果称量时氯化钠和砝码的位置颠倒了,但此称量过程中不需要移动游码,故所配制溶液的溶质质量分数不变,等于15%。
(3)所配溶液的溶质质量分数偏小,可能是溶质质量偏小或溶剂质量偏大,故原因可能有将氯化钠倒入烧杯时有撒落或配制溶液的烧杯中有水或量取水时仰视读数等(合理即可)。
四、17.【解】(1)所得溶液中溶质的质量分数为×100%=20%;
(2)设需要加水的质量为x,则:
×100%=20%× x=50 g
答:(1)所得溶液中溶质的质量分数是20%;(2)若欲使原溶液的溶质质量分数减少一半,需加50 g水。
18.【解】设需要浓硫酸的体积为V。
1.84 g/mL×V×98%=100 g×20%
V≈11 mL
答:需要溶质质量分数为98%的浓硫酸的体积约为11 mL。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
