6.1.3 设计原电池 化学电源 学案(共一课时) 高中化学人教版(2019)必修第二册
文档属性
| 名称 | 6.1.3 设计原电池 化学电源 学案(共一课时) 高中化学人教版(2019)必修第二册 |

|
|
| 格式 | docx | ||
| 文件大小 | 156.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-02 00:00:00 | ||
图片预览

文档简介
《设计原电池 化学电源》学案
一、学习目标
1.会设计简单的原电池。
2.知道干电池、充电电池、燃料电池等化学电源的特点。
3.掌握构成电池的要素,了解不同电极材料对电池性能的影响。
二、学习过程
环节 学习活动 记录
环节一: 设计原电池 1.回忆原电池的构成要素
2.P37探究(小组实验)
3.通过P37探究,得到了哪些启示?(提示:可从水果的作用,电极材料的注意事项,不同材料做电极的效果等进行汇报)
4.完成评价任务1、2、3
环节二: 化学电源 1.列举生活中常见的电池
2.学习一次电池、二次电池、发展中的燃料电池等
3.完成评价任务4、5
环节三: 课堂小结 整理笔记:原电池的工作原理
三、课堂测评
1.某兴趣小组设计的简易原电池装置如图所示。该电池工作时,下列说法正确的是
A.锌片作正极
B.铜片上有气泡产生
C.将电能转化为化学能
D.电子由铜片经导线流向锌片
2.几位同学以相同大小的铜片和锌片为电极研究水果电池,得到的实验数据如下表所示:
(1)该实验的目的是探究水果种类和_____对水果电池电流大小的影响。
(2)该实验所用装置中,负极的材料是____ ,该装置将 转化为电能。
(3)能表明水果种类对电流大小有影响的实验编号是___和 。
(4)请你再提出一个可能影响水果电池电流大小的因素: 。
3.铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式:___________________。
(2)若将(1)中的反应设计成原电池,请在方框内画出原电池的装置图,标出正、负极,并写出电极反应式。
正极反应式:_____________________________________
负极反应式:_____________________________________
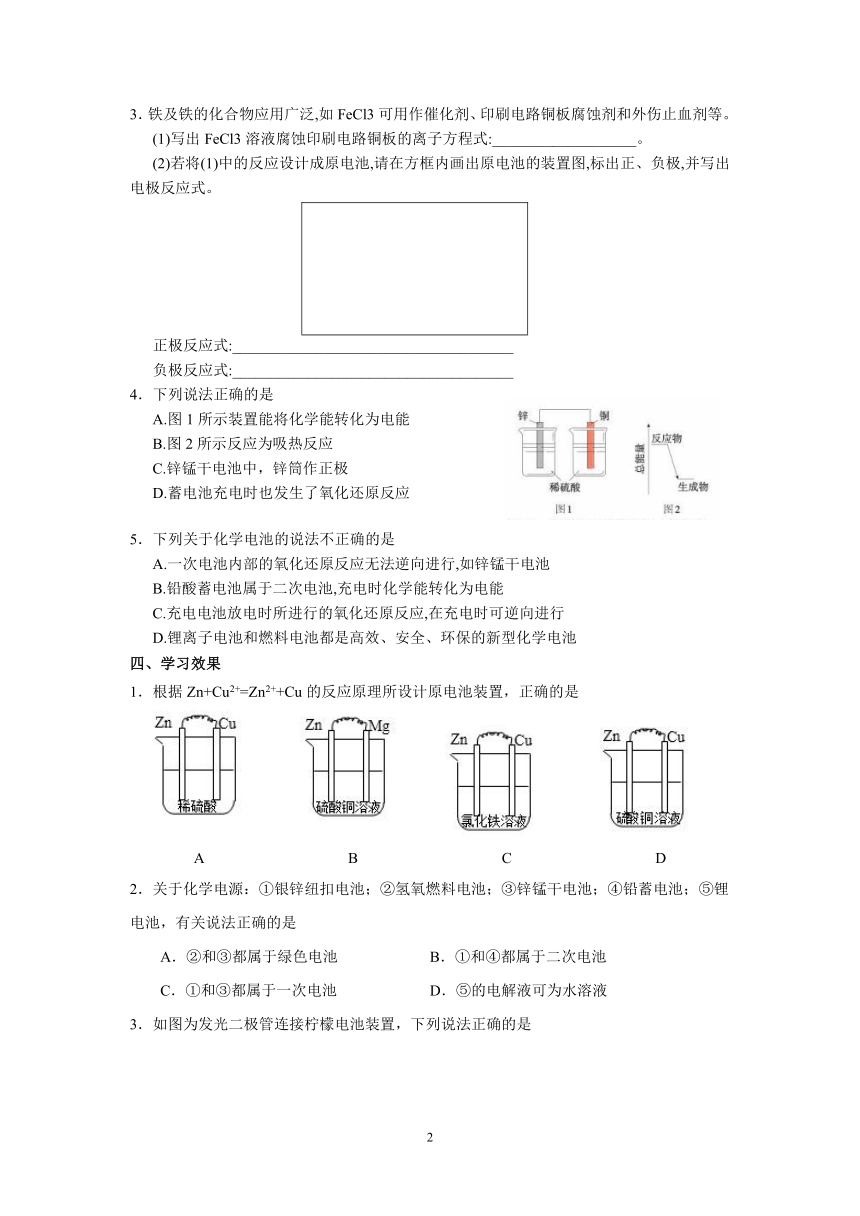
4.下列说法正确的是
A.图1所示装置能将化学能转化为电能
B.图2所示反应为吸热反应
C.锌锰干电池中,锌筒作正极
D.蓄电池充电时也发生了氧化还原反应
5.下列关于化学电池的说法不正确的是
A.一次电池内部的氧化还原反应无法逆向进行,如锌锰干电池
B.铅酸蓄电池属于二次电池,充电时化学能转化为电能
C.充电电池放电时所进行的氧化还原反应,在充电时可逆向进行
D.锂离子电池和燃料电池都是高效、安全、环保的新型化学电池
四、学习效果
1.根据Zn+Cu2+=Zn2++Cu的反应原理所设计原电池装置,正确的是
A B C D
2.关于化学电源:①银锌纽扣电池;②氢氧燃料电池;③锌锰干电池;④铅蓄电池;⑤锂电池,有关说法正确的是
A.②和③都属于绿色电池 B.①和④都属于二次电池
C.①和③都属于一次电池 D.⑤的电解液可为水溶液
3.如图为发光二极管连接柠檬电池装置,下列说法正确的是
A.该装置实现了电能转化为化学能 B.电子由铜经发光二极管流向铁环
C.可将柠檬替换成盛装酒精溶液的装置 D.负极的电极反应为:
4.下列有关电池的说法中,不正确的是
A.燃料电池是一种高效且对环境友好的新型电池,燃料储存在电池内部
B.铅蓄电池是可充电电池,电极的正极材料为PbO2
C.手机上用的锂离子电池收于二次电池
D.锌铜原电池在工作时,电子沿外电路从锌电极流向铜电极
5.原电池是直接把化学能转化为电能的装置。
(1)如图所示:按照构成原电池的基本要素来看,Zn的作用是(填字母,下同)____;稀硫酸的作用是________。
a.负极反应物 b.负极材料 c.正极反应物
d.正极材料 e.离子导体 f.电子导体
(2) ①在Cu-Zn原电池中,Zn片上发生________反应(填“氧化”或“还原”)。Cu片上发生的电极反应为________。
②外电路中电子流向_____极;内电路溶液中SO移向___极。
③能证明化学能转化为电能的实验现象为________。
(3)某原电池的总反应为Zn+Cu2+=Cu+Zn2+,该原电池正确的组成是__。
(4)从化学的角度分析,原电池装置产生电流的原因是:原电池可将________,并通过能导电的物质形成闭合回路,产生电流。
参考答案:
题号 1 2 3 4
答案 D C D A
5.
ab 、 ce
①氧化 2H+ + 2e- = H2↑ ②正、负 ③Cu片上有气泡或电流计指针发生偏转
AC
将氧化反应和还原反应分开在不同区域进行
1
一、学习目标
1.会设计简单的原电池。
2.知道干电池、充电电池、燃料电池等化学电源的特点。
3.掌握构成电池的要素,了解不同电极材料对电池性能的影响。
二、学习过程
环节 学习活动 记录
环节一: 设计原电池 1.回忆原电池的构成要素
2.P37探究(小组实验)
3.通过P37探究,得到了哪些启示?(提示:可从水果的作用,电极材料的注意事项,不同材料做电极的效果等进行汇报)
4.完成评价任务1、2、3
环节二: 化学电源 1.列举生活中常见的电池
2.学习一次电池、二次电池、发展中的燃料电池等
3.完成评价任务4、5
环节三: 课堂小结 整理笔记:原电池的工作原理
三、课堂测评
1.某兴趣小组设计的简易原电池装置如图所示。该电池工作时,下列说法正确的是
A.锌片作正极
B.铜片上有气泡产生
C.将电能转化为化学能
D.电子由铜片经导线流向锌片
2.几位同学以相同大小的铜片和锌片为电极研究水果电池,得到的实验数据如下表所示:
(1)该实验的目的是探究水果种类和_____对水果电池电流大小的影响。
(2)该实验所用装置中,负极的材料是____ ,该装置将 转化为电能。
(3)能表明水果种类对电流大小有影响的实验编号是___和 。
(4)请你再提出一个可能影响水果电池电流大小的因素: 。
3.铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式:___________________。
(2)若将(1)中的反应设计成原电池,请在方框内画出原电池的装置图,标出正、负极,并写出电极反应式。
正极反应式:_____________________________________
负极反应式:_____________________________________
4.下列说法正确的是
A.图1所示装置能将化学能转化为电能
B.图2所示反应为吸热反应
C.锌锰干电池中,锌筒作正极
D.蓄电池充电时也发生了氧化还原反应
5.下列关于化学电池的说法不正确的是
A.一次电池内部的氧化还原反应无法逆向进行,如锌锰干电池
B.铅酸蓄电池属于二次电池,充电时化学能转化为电能
C.充电电池放电时所进行的氧化还原反应,在充电时可逆向进行
D.锂离子电池和燃料电池都是高效、安全、环保的新型化学电池
四、学习效果
1.根据Zn+Cu2+=Zn2++Cu的反应原理所设计原电池装置,正确的是
A B C D
2.关于化学电源:①银锌纽扣电池;②氢氧燃料电池;③锌锰干电池;④铅蓄电池;⑤锂电池,有关说法正确的是
A.②和③都属于绿色电池 B.①和④都属于二次电池
C.①和③都属于一次电池 D.⑤的电解液可为水溶液
3.如图为发光二极管连接柠檬电池装置,下列说法正确的是
A.该装置实现了电能转化为化学能 B.电子由铜经发光二极管流向铁环
C.可将柠檬替换成盛装酒精溶液的装置 D.负极的电极反应为:
4.下列有关电池的说法中,不正确的是
A.燃料电池是一种高效且对环境友好的新型电池,燃料储存在电池内部
B.铅蓄电池是可充电电池,电极的正极材料为PbO2
C.手机上用的锂离子电池收于二次电池
D.锌铜原电池在工作时,电子沿外电路从锌电极流向铜电极
5.原电池是直接把化学能转化为电能的装置。
(1)如图所示:按照构成原电池的基本要素来看,Zn的作用是(填字母,下同)____;稀硫酸的作用是________。
a.负极反应物 b.负极材料 c.正极反应物
d.正极材料 e.离子导体 f.电子导体
(2) ①在Cu-Zn原电池中,Zn片上发生________反应(填“氧化”或“还原”)。Cu片上发生的电极反应为________。
②外电路中电子流向_____极;内电路溶液中SO移向___极。
③能证明化学能转化为电能的实验现象为________。
(3)某原电池的总反应为Zn+Cu2+=Cu+Zn2+,该原电池正确的组成是__。
(4)从化学的角度分析,原电池装置产生电流的原因是:原电池可将________,并通过能导电的物质形成闭合回路,产生电流。
参考答案:
题号 1 2 3 4
答案 D C D A
5.
ab 、 ce
①氧化 2H+ + 2e- = H2↑ ②正、负 ③Cu片上有气泡或电流计指针发生偏转
AC
将氧化反应和还原反应分开在不同区域进行
1
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
