8.3 酸和碱的反应 教学预案(表格式) 九年级化学科粤版下册
文档属性
| 名称 | 8.3 酸和碱的反应 教学预案(表格式) 九年级化学科粤版下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 99.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-01 00:00:00 | ||
图片预览

文档简介
课时教学预案
课题 常见的酸碱盐(科粤版) 8.3酸和碱的反应
学 习 目 标 1.通过教师引导和分组实验,学会借助指示剂判断中和反应发生的实验方法; 2.通过分析盐酸与氢氧化钠的反应初步感受从个别到一般的思维方法,结合微粒的观点初步认识中和反应的实质; 3.通过阅读课本、查阅资料等途径了解中和反应在实际中的应用。
评 价 任 务 通过完成评价任务1、思考1,检测学习目标1; 通过完成学生实验、思考2和评价任务2,检测学习目标2; 通过课堂资料分享,检测学习目标3; 4.通过完成课堂检测,检测学习目标1、2、3。
学习 重难点 重点:中和反应及其应用 难点:结合微粒的观点初步认识中和反应的实质
学 情 分 析 九年级学生把化学实验当作一件非常有趣的事情,有强烈的好奇心;但不喜欢化学基本理论学习,看完实验不能对现象进行深入思考;多数学生只对化学实验现象感兴趣,对过程、结论缺乏认真思考,甚至对分析问题厌倦;学生习惯于被动接受式的传统教学,缺乏合作意识、独立发现和自主学习与探究的能力;对化学实验仪器的使用、实验设计能力、实事求是的科学态度都有待于培养。
教学 策略 演示实验、分组实验、示范讲解法 对比分析法、归纳总结法
课前 准备 教学PPT 药品:稀盐酸、氢氧化钠溶液(稀)、无色酚酞溶液 仪器:试管、量筒、胶头滴管、(玻璃棒、酒精灯选用)
【教学过程】
教学环节 教师活动 学生活动 设计意图
活动一: 创设情境 引导探究 (4分钟) 1.多媒体出示打油诗: 夏恼 夏晚最烦恼,处处蚊子咬; 嗡嗡叮上身,红点知多少。 【设问】夏天是蚊子肆虐的季节,如果你被蚊子叮了,皮肤就会红肿发痒。有经验的老人都会说:“涂点肥皂水就好了”。这是什么原因呢? 为了弄清这个问题,这节课我们一起来学习第八章第三节——酸和碱的反应。 阅读打油诗,描述获取的信息、回答问题。 1.多媒体创设情境,让学生感受生活中处处有化学; 2.为课题的引入作铺垫。
2.明确学习目标 学生自读 初步认识本节课内容,勾画重难点
活 动 二 学 习 新 知 22分钟 指导 阅读 酸、碱各自有相似的化学性质,这是什么原因造成的呢 酸和碱有什么组成上的特点 教师讲解。 学生思考,阅读课本P237-P238回答。观看课件。 1.为分析酸碱组成做准备; 2.指导阅读教材,师生互动。
过渡 酸和碱之间是否会发生化学反应 如果发生化学反应,又会有什么特点 我们通过实验来探究。 思考 激发兴趣
实验探究 设计探究方案 引:“从老师提供的药品中选择适当的物质,设计探究方案 提供药品是:NaOH溶液、盐酸、无色酚酞溶液 问:“怎么设计实验步骤?” 小组讨论,形成初步设计思路 自主选择两组或者两组以上药品,设计探究方案。 交流 1.学会问题的解决方法。 2.培养学生交流与合作的能力。 3.培养学生的发散思维能力。
实施探究过程 1.组织学生进行探究活动; 2.要求学生同步填写表格。 1.实施探究活动; 2.认真观察实验,如实填写表格。 1.培养相互合作能力,动手操作能力,观察能力。 2.形成再一次认知冲突,为进一步探究作铺垫。
交流与发现 交流与发现 组织小组代表交流各自在探究过程中观察到的现象及对应结论; 有明显现象(例将稀盐酸滴入盛有氢氧化钠溶液和无色酚酞溶液混合物的试管内); (2)无明显现象。(将稀盐酸滴入盛有氢氧化钠的试管内) 交流各自体验,形成初步认知,感受成功 1.培养学生学习交流的能力; 2.增强学生的成就感、愉悦感和自信心。
再设计 再探究 引:HCl+NaOH无明显现象,怎么来判断是否发生了反应?组织学生具体针对“HCl+NaOH”这一组再设计,再探究。 学生思考讨论,完成探究 形成对中和反应的初步认识
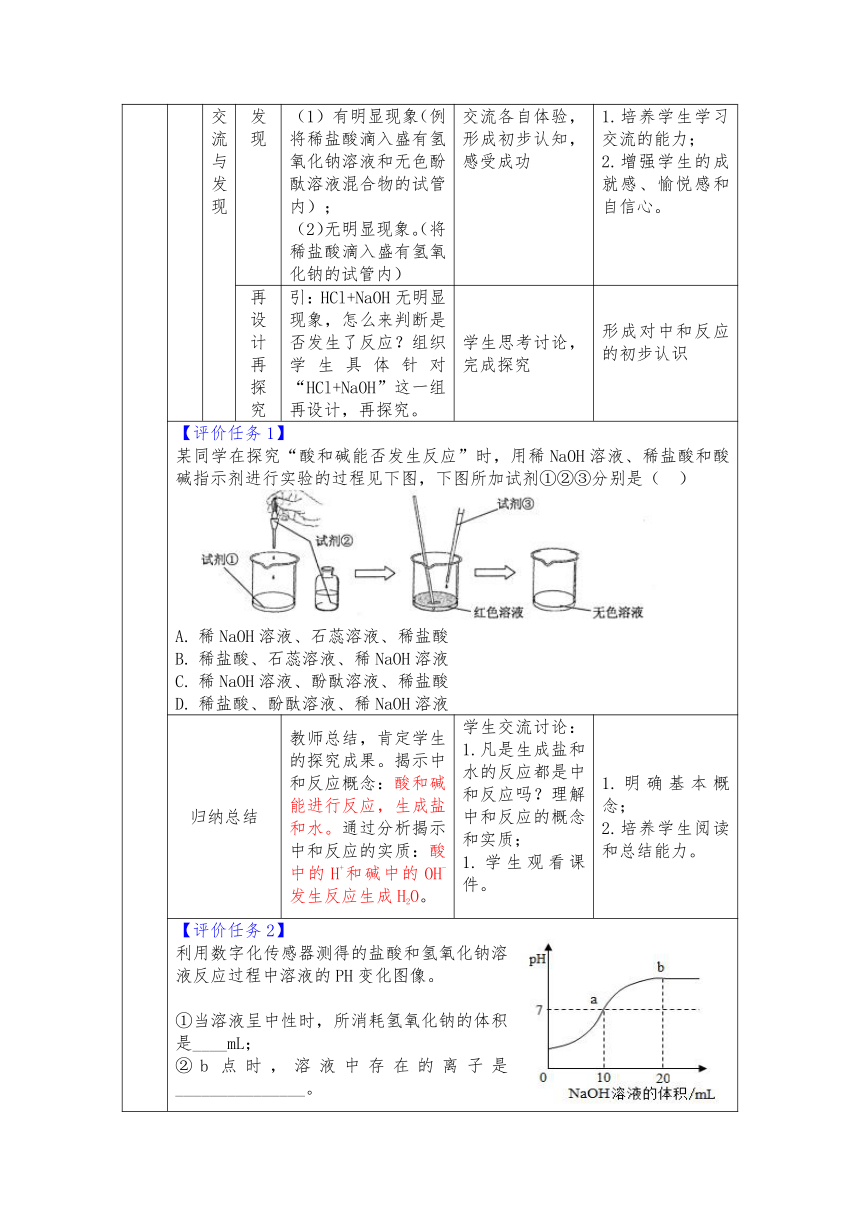
【评价任务1】 某同学在探究“酸和碱能否发生反应”时,用稀NaOH溶液、稀盐酸和酸碱指示剂进行实验的过程见下图,下图所加试剂①②③分别是( ) 稀NaOH溶液、石蕊溶液、稀盐酸 稀盐酸、石蕊溶液、稀NaOH溶液 稀NaOH溶液、酚酞溶液、稀盐酸 稀盐酸、酚酞溶液、稀NaOH溶液
归纳总结 教师总结,肯定学生的探究成果。揭示中和反应概念:酸和碱能进行反应,生成盐和水。通过分析揭示中和反应的实质:酸中的H+和碱中的OH-发生反应生成H2O。 学生交流讨论:1.凡是生成盐和水的反应都是中和反应吗?理解中和反应的概念和实质; 学生观看课件。 1.明确基本概念; 2.培养学生阅读和总结能力。
【评价任务2】 利用数字化传感器测得的盐酸和氢氧化钠溶液反应过程中溶液的PH变化图像。 ①当溶液呈中性时,所消耗氢氧化钠的体积是____mL; ②b点时,溶液中存在的离子是_______________。
活动三 知识延伸 化学与生活 (5分钟) 课件展示:改良土壤的酸碱性。 ②处理工厂的废水。 ③ 组织小组讨论:“胃舒平”为什么能治疗胃酸过多的病人 (主要成分氢氧化铝) 阅读课本P239—P240 1.感受生活中处处有化学,生活离不开化学。 2.进一步理解中和反应。 3.书写有关化学方程式。 巩固所学知识 应用所学知识解决现实生活中的问题。
活动四 课堂小结 (3分钟) 1.反思本节课学到的知识 2.应用本节知识解决有关中考真题。 教师点评:课堂效果,做出积极评价和总体评价。 学生畅所欲言本节课收获,学到了什么?提高了什么认识? 学生:分享 学生梳理知识点,形成知识体系框架,使学生能对自己这一节课的收获、不足进行总结,发现问题,及时解决,养成良好的学习习惯。
活动五 评价任务3 达标检测 (10分钟) 【课堂检测】 下列对酸碱盐性质的归纳不正确的是( ) 酸能和碱反应生成盐和水 碱能和某些非金属氧化物反应生成盐和水 酸能和某些金属氧化物反应生成盐和水 有盐和水生成的反应一定是中和反应 2.胃酸过多的病人,其胃液的PH 较正常人的要__(填“大”或“小”),服用含有氢氧化铝的药物后可使病人恢复正常,原因是___________(用化学方程式表示)。 【提升任务】 3.某学生按如图操作进行中和反应实验,回答问题。 5mL氢氧化钠溶液 滴加稀盐酸至恰好完全反应,发生反应的化学方程式为________________; 下列对于反应前后烧杯中溶液的分析错误的是______(填字母) 颜色改变 温度升高 碱性增强 质量减少 【链接中考—通辽市中考题节选】 某实验小组的同学用氢氧化钙溶液和稀盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液中滴加稀盐酸一会后,发现忘记了加指示剂,因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究.
(1)探究烧杯内溶液中溶质的成分:
【提出问题】烧杯内溶液中的溶质是什么?
【进行猜想】
猜想一:CaCl2和Ca(OH)2和HCl
猜想二:CaCl2、Ca(OH)2
猜想三:CaCl2、HCl 猜想四:________
【查阅资料】氯化钙溶液呈中性 小明认为猜想一不合理,理由是_______________。 反思交流:为验证猜想三正确,下列几种实验方案还可行的是________。 取反应后的溶液于试管中,加入镁粉冒气泡; B.取反应后的溶液于试管中,加入硝酸银溶液,生成白色沉淀。 限时 独立完成检测 通过达标测评,反馈矫正,巩固所学,达成教学目标。
活动六 布置作业 (1分钟) 基础作业:练习册P64【知识点一】—【知识点四】2、3、4、8 课后能力提升:1 真题演练1、2 选作:练习册P66【知识点二】5 课后能力提升:3
板书设计 8.3 酸和碱的反应 一、酸和碱的组成 二、中和反应 1.定义:酸 + 碱 → 盐 + 水 2.实质 三、中和反应的应用
课题 常见的酸碱盐(科粤版) 8.3酸和碱的反应
学 习 目 标 1.通过教师引导和分组实验,学会借助指示剂判断中和反应发生的实验方法; 2.通过分析盐酸与氢氧化钠的反应初步感受从个别到一般的思维方法,结合微粒的观点初步认识中和反应的实质; 3.通过阅读课本、查阅资料等途径了解中和反应在实际中的应用。
评 价 任 务 通过完成评价任务1、思考1,检测学习目标1; 通过完成学生实验、思考2和评价任务2,检测学习目标2; 通过课堂资料分享,检测学习目标3; 4.通过完成课堂检测,检测学习目标1、2、3。
学习 重难点 重点:中和反应及其应用 难点:结合微粒的观点初步认识中和反应的实质
学 情 分 析 九年级学生把化学实验当作一件非常有趣的事情,有强烈的好奇心;但不喜欢化学基本理论学习,看完实验不能对现象进行深入思考;多数学生只对化学实验现象感兴趣,对过程、结论缺乏认真思考,甚至对分析问题厌倦;学生习惯于被动接受式的传统教学,缺乏合作意识、独立发现和自主学习与探究的能力;对化学实验仪器的使用、实验设计能力、实事求是的科学态度都有待于培养。
教学 策略 演示实验、分组实验、示范讲解法 对比分析法、归纳总结法
课前 准备 教学PPT 药品:稀盐酸、氢氧化钠溶液(稀)、无色酚酞溶液 仪器:试管、量筒、胶头滴管、(玻璃棒、酒精灯选用)
【教学过程】
教学环节 教师活动 学生活动 设计意图
活动一: 创设情境 引导探究 (4分钟) 1.多媒体出示打油诗: 夏恼 夏晚最烦恼,处处蚊子咬; 嗡嗡叮上身,红点知多少。 【设问】夏天是蚊子肆虐的季节,如果你被蚊子叮了,皮肤就会红肿发痒。有经验的老人都会说:“涂点肥皂水就好了”。这是什么原因呢? 为了弄清这个问题,这节课我们一起来学习第八章第三节——酸和碱的反应。 阅读打油诗,描述获取的信息、回答问题。 1.多媒体创设情境,让学生感受生活中处处有化学; 2.为课题的引入作铺垫。
2.明确学习目标 学生自读 初步认识本节课内容,勾画重难点
活 动 二 学 习 新 知 22分钟 指导 阅读 酸、碱各自有相似的化学性质,这是什么原因造成的呢 酸和碱有什么组成上的特点 教师讲解。 学生思考,阅读课本P237-P238回答。观看课件。 1.为分析酸碱组成做准备; 2.指导阅读教材,师生互动。
过渡 酸和碱之间是否会发生化学反应 如果发生化学反应,又会有什么特点 我们通过实验来探究。 思考 激发兴趣
实验探究 设计探究方案 引:“从老师提供的药品中选择适当的物质,设计探究方案 提供药品是:NaOH溶液、盐酸、无色酚酞溶液 问:“怎么设计实验步骤?” 小组讨论,形成初步设计思路 自主选择两组或者两组以上药品,设计探究方案。 交流 1.学会问题的解决方法。 2.培养学生交流与合作的能力。 3.培养学生的发散思维能力。
实施探究过程 1.组织学生进行探究活动; 2.要求学生同步填写表格。 1.实施探究活动; 2.认真观察实验,如实填写表格。 1.培养相互合作能力,动手操作能力,观察能力。 2.形成再一次认知冲突,为进一步探究作铺垫。
交流与发现 交流与发现 组织小组代表交流各自在探究过程中观察到的现象及对应结论; 有明显现象(例将稀盐酸滴入盛有氢氧化钠溶液和无色酚酞溶液混合物的试管内); (2)无明显现象。(将稀盐酸滴入盛有氢氧化钠的试管内) 交流各自体验,形成初步认知,感受成功 1.培养学生学习交流的能力; 2.增强学生的成就感、愉悦感和自信心。
再设计 再探究 引:HCl+NaOH无明显现象,怎么来判断是否发生了反应?组织学生具体针对“HCl+NaOH”这一组再设计,再探究。 学生思考讨论,完成探究 形成对中和反应的初步认识
【评价任务1】 某同学在探究“酸和碱能否发生反应”时,用稀NaOH溶液、稀盐酸和酸碱指示剂进行实验的过程见下图,下图所加试剂①②③分别是( ) 稀NaOH溶液、石蕊溶液、稀盐酸 稀盐酸、石蕊溶液、稀NaOH溶液 稀NaOH溶液、酚酞溶液、稀盐酸 稀盐酸、酚酞溶液、稀NaOH溶液
归纳总结 教师总结,肯定学生的探究成果。揭示中和反应概念:酸和碱能进行反应,生成盐和水。通过分析揭示中和反应的实质:酸中的H+和碱中的OH-发生反应生成H2O。 学生交流讨论:1.凡是生成盐和水的反应都是中和反应吗?理解中和反应的概念和实质; 学生观看课件。 1.明确基本概念; 2.培养学生阅读和总结能力。
【评价任务2】 利用数字化传感器测得的盐酸和氢氧化钠溶液反应过程中溶液的PH变化图像。 ①当溶液呈中性时,所消耗氢氧化钠的体积是____mL; ②b点时,溶液中存在的离子是_______________。
活动三 知识延伸 化学与生活 (5分钟) 课件展示:改良土壤的酸碱性。 ②处理工厂的废水。 ③ 组织小组讨论:“胃舒平”为什么能治疗胃酸过多的病人 (主要成分氢氧化铝) 阅读课本P239—P240 1.感受生活中处处有化学,生活离不开化学。 2.进一步理解中和反应。 3.书写有关化学方程式。 巩固所学知识 应用所学知识解决现实生活中的问题。
活动四 课堂小结 (3分钟) 1.反思本节课学到的知识 2.应用本节知识解决有关中考真题。 教师点评:课堂效果,做出积极评价和总体评价。 学生畅所欲言本节课收获,学到了什么?提高了什么认识? 学生:分享 学生梳理知识点,形成知识体系框架,使学生能对自己这一节课的收获、不足进行总结,发现问题,及时解决,养成良好的学习习惯。
活动五 评价任务3 达标检测 (10分钟) 【课堂检测】 下列对酸碱盐性质的归纳不正确的是( ) 酸能和碱反应生成盐和水 碱能和某些非金属氧化物反应生成盐和水 酸能和某些金属氧化物反应生成盐和水 有盐和水生成的反应一定是中和反应 2.胃酸过多的病人,其胃液的PH 较正常人的要__(填“大”或“小”),服用含有氢氧化铝的药物后可使病人恢复正常,原因是___________(用化学方程式表示)。 【提升任务】 3.某学生按如图操作进行中和反应实验,回答问题。 5mL氢氧化钠溶液 滴加稀盐酸至恰好完全反应,发生反应的化学方程式为________________; 下列对于反应前后烧杯中溶液的分析错误的是______(填字母) 颜色改变 温度升高 碱性增强 质量减少 【链接中考—通辽市中考题节选】 某实验小组的同学用氢氧化钙溶液和稀盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液中滴加稀盐酸一会后,发现忘记了加指示剂,因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究.
(1)探究烧杯内溶液中溶质的成分:
【提出问题】烧杯内溶液中的溶质是什么?
【进行猜想】
猜想一:CaCl2和Ca(OH)2和HCl
猜想二:CaCl2、Ca(OH)2
猜想三:CaCl2、HCl 猜想四:________
【查阅资料】氯化钙溶液呈中性 小明认为猜想一不合理,理由是_______________。 反思交流:为验证猜想三正确,下列几种实验方案还可行的是________。 取反应后的溶液于试管中,加入镁粉冒气泡; B.取反应后的溶液于试管中,加入硝酸银溶液,生成白色沉淀。 限时 独立完成检测 通过达标测评,反馈矫正,巩固所学,达成教学目标。
活动六 布置作业 (1分钟) 基础作业:练习册P64【知识点一】—【知识点四】2、3、4、8 课后能力提升:1 真题演练1、2 选作:练习册P66【知识点二】5 课后能力提升:3
板书设计 8.3 酸和碱的反应 一、酸和碱的组成 二、中和反应 1.定义:酸 + 碱 → 盐 + 水 2.实质 三、中和反应的应用
