浙江省2022年中考科学模拟题汇编-42物质的推断(含解析)
文档属性
| 名称 | 浙江省2022年中考科学模拟题汇编-42物质的推断(含解析) |

|
|
| 格式 | doc | ||
| 文件大小 | 164.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-04-03 00:00:00 | ||
图片预览


文档简介
浙江省2022年中考科学模拟题汇编-42物质的推断
学校:___________姓名:___________班级:___________考号:___________
一、选择题
1.(2022·浙江杭州·统考二模)2022年第24届冬季奥运会将由北京市和张家口市联合举行。如图所示,“五环”中相交两环中的物质间能够发生化学反应,其中A、B、C、D分别是HCl、Fe2O3、H2、CuSO4中的一种。下列说法中正确的是( )
A.A物质与B物质间发生的反应是工业炼铁的主要反应原理
B.B物质与C物质间发生反应的化学方程式为:4HCl+Fe2O3═2H2O+2FeCl2
C.C物质与NaOH溶液发生反应时无明显现象
D.D物质的溶液与NaOH溶液发生反应时产生红褐色沉淀
二、填空题
2.(2022·浙江绍兴·统考一模)如图表示NaCl、Na2CO3、AgNO3、BaCl2、HCl五种溶液之间的部分反应关系,线条相连的溶液之间可以发生化学反应。请问:
(1)E是___________溶液。
(2)A和B反应有气体生成,则C是___________溶液。
(3)图中还缺少一条连线,此线应连在___________两溶液之间。(填字母)
3.(2022·浙江宁波·统考二模)硝酸钾是一种重要的工业原料,我国年产量达到6万多吨。小科和小宁在实验室用不同的方案制取硝酸钾。
[实验步骤]
I. 小科将A、B盐加到装有少量水的试管中,充分振荡制取硝酸钾,如图甲。
II.小宁向试管中依次加入浓度为10%的酸溶液15g,浓度为15%的碱溶液8g,充分振荡制取硝酸钾,如图乙。
[实验分析]
(1)小宁想分析小科所用的A、B盐成分,分别取A、B盐配成溶液后进行以下实验。
I.取少量A、B盐溶液分别滴加稀盐酸,A盐溶液有气泡生成,B盐溶液无明显现象。
II.另取少量A、B盐溶液,分别滴加氢氧化钠溶液,A、B盐溶液均无明显现象。
则B盐可能是___________(写出一种即可) 。
(2)工业生产中,目的产物的实际生成量占目的产物的理论生成量的百分率称为收率。已知小宁最终制得硝酸钾1.8g,则反应的收率为___________( 计算结果保留到0.1%) 。
(3)请你从安全的角度,对小宁制取硝酸钾的方案进行评价:___________。
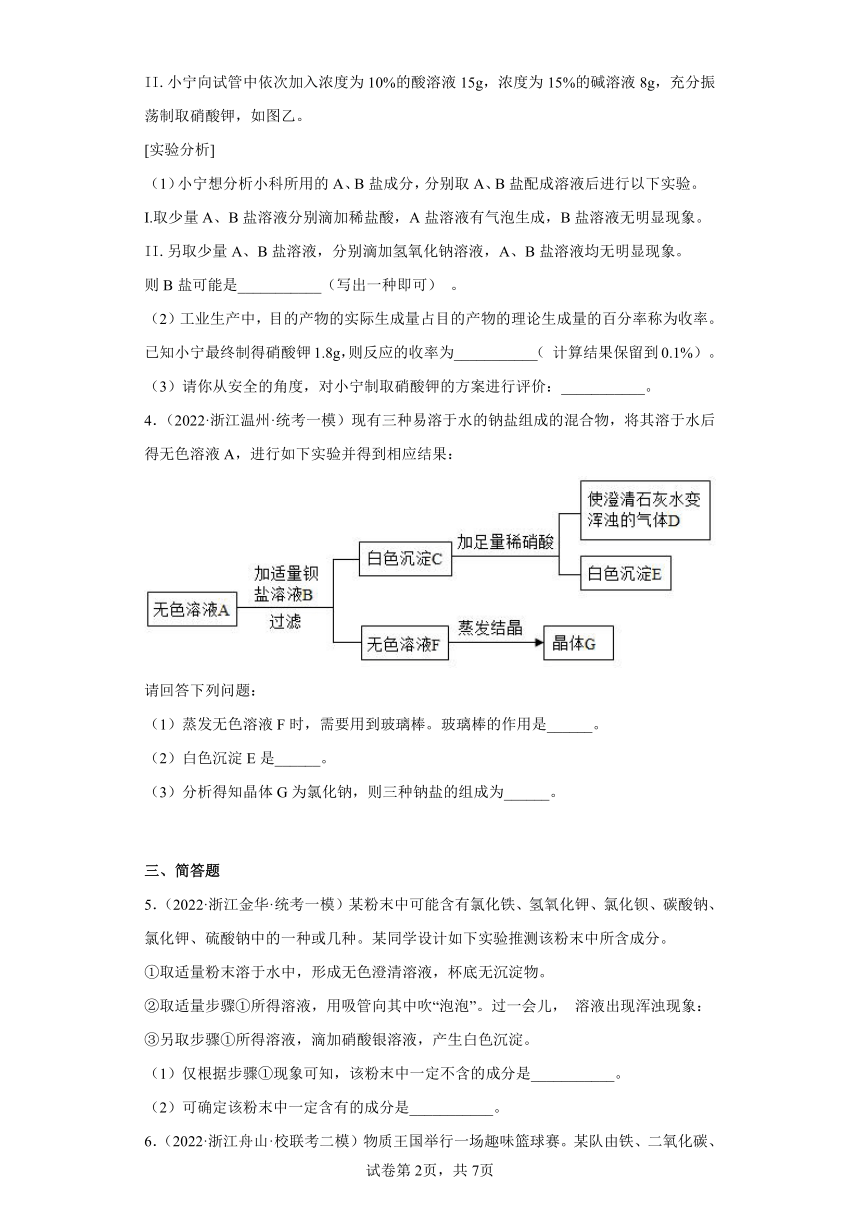
4.(2022·浙江温州·统考一模)现有三种易溶于水的钠盐组成的混合物,将其溶于水后得无色溶液A,进行如下实验并得到相应结果:
请回答下列问题:
(1)蒸发无色溶液F时,需要用到玻璃棒。玻璃棒的作用是______。
(2)白色沉淀E是______。
(3)分析得知晶体G为氯化钠,则三种钠盐的组成为______。
三、简答题
5.(2022·浙江金华·统考一模)某粉末中可能含有氯化铁、氢氧化钾、氯化钡、碳酸钠、氯化钾、硫酸钠中的一种或几种。某同学设计如下实验推测该粉末中所含成分。
①取适量粉末溶于水中,形成无色澄清溶液,杯底无沉淀物。
②取适量步骤①所得溶液,用吸管向其中吹“泡泡”。过一会儿, 溶液出现浑浊现象:
③另取步骤①所得溶液,滴加硝酸银溶液,产生白色沉淀。
(1)仅根据步骤①现象可知,该粉末中一定不含的成分是___________。
(2)可确定该粉末中一定含有的成分是___________。
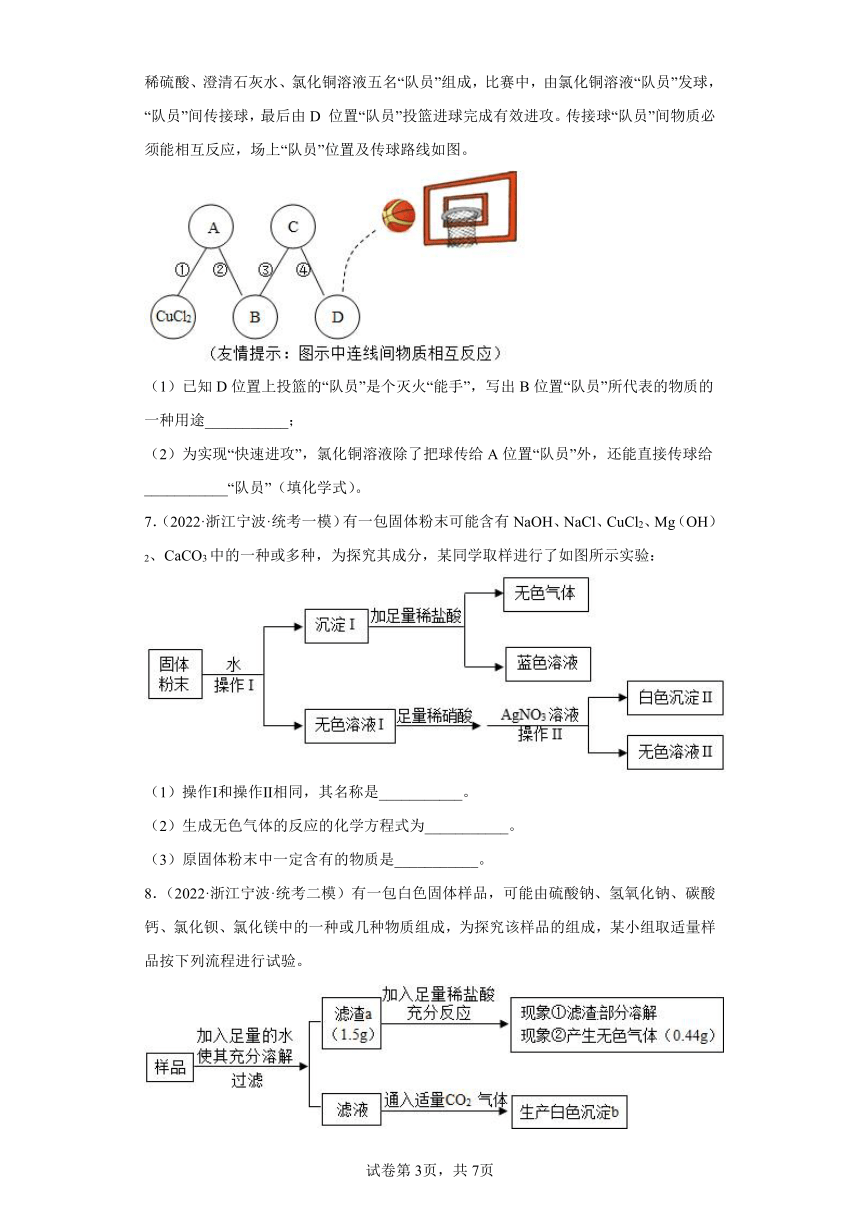
6.(2022·浙江舟山·校联考二模)物质王国举行一场趣味篮球赛。某队由铁、二氧化碳、稀硫酸、澄清石灰水、氯化铜溶液五名“队员”组成,比赛中,由氯化铜溶液“队员”发球,“队员”间传接球,最后由D 位置“队员”投篮进球完成有效进攻。传接球“队员”间物质必须能相互反应,场上“队员”位置及传球路线如图。
(1)已知D位置上投篮的“队员”是个灭火“能手”,写出B位置“队员”所代表的物质的一种用途___________;
(2)为实现“快速进攻”,氯化铜溶液除了把球传给A位置“队员”外,还能直接传球给___________“队员”(填化学式)。
7.(2022·浙江宁波·统考一模)有一包固体粉末可能含有NaOH、NaCl、CuCl2、Mg(OH)2、CaCO3中的一种或多种,为探究其成分,某同学取样进行了如图所示实验:
(1)操作Ⅰ和操作Ⅱ相同,其名称是___________。
(2)生成无色气体的反应的化学方程式为___________。
(3)原固体粉末中一定含有的物质是___________。
8.(2022·浙江宁波·统考二模)有一包白色固体样品,可能由硫酸钠、氢氧化钠、碳酸钙、氯化钡、氯化镁中的一种或几种物质组成,为探究该样品的组成,某小组取适量样品按下列流程进行试验。
请回答:
(1)滤渣a的成分是___________,可能含有___________。
(2)溶液中溶质的成分有___________。
(3)若现象①“滤渣部分溶解”变为“滤渣全部溶解”,其他现象不变,则原样品不存在的物质是___________。
9.(2022·浙江宁波·统考二模)A、 B、C、D、E五种物质均为初中科学中所涉及的常见物质,它们存在如图的转化关系,“一”表示可以向箭头所指方向一步转化,弧线表示两种物质间可以发生反应,C是常见气体,D是常见单质,图中反应条件与其他物质均已略去。诸回答下列问题:
(1) A可能的化学式为___________。
(2)写出A→E的两个化学方程式:___________、___________。
四、探究题
10.(2022·浙江舟山·校联考二模)茶垢清洁剂能快速消除茶具上附着的茶垢,某小组同学对茶垢清洁剂进行了探究。
【查阅资料】下图是某品牌茶垢清洁剂说明书中的部分内容。
主要成分:过碳酸钠(化学式为2Na2CO3·3H2O2)去渍原理:过碳酸钠溶于水时生成碳酸钠(俗称纯碱)和过氧化氢······
【提出问题Ⅰ】茶垢清洁剂溶于水时生成过氧化氢,是否生成氧气?
【实验1】在盛有茶垢清洁剂固体的小烧杯中,加适量常温水,完全溶解后得到无色溶液,观察到有小气泡缓慢冒出,伸入带火星的木条,木条不复燃。
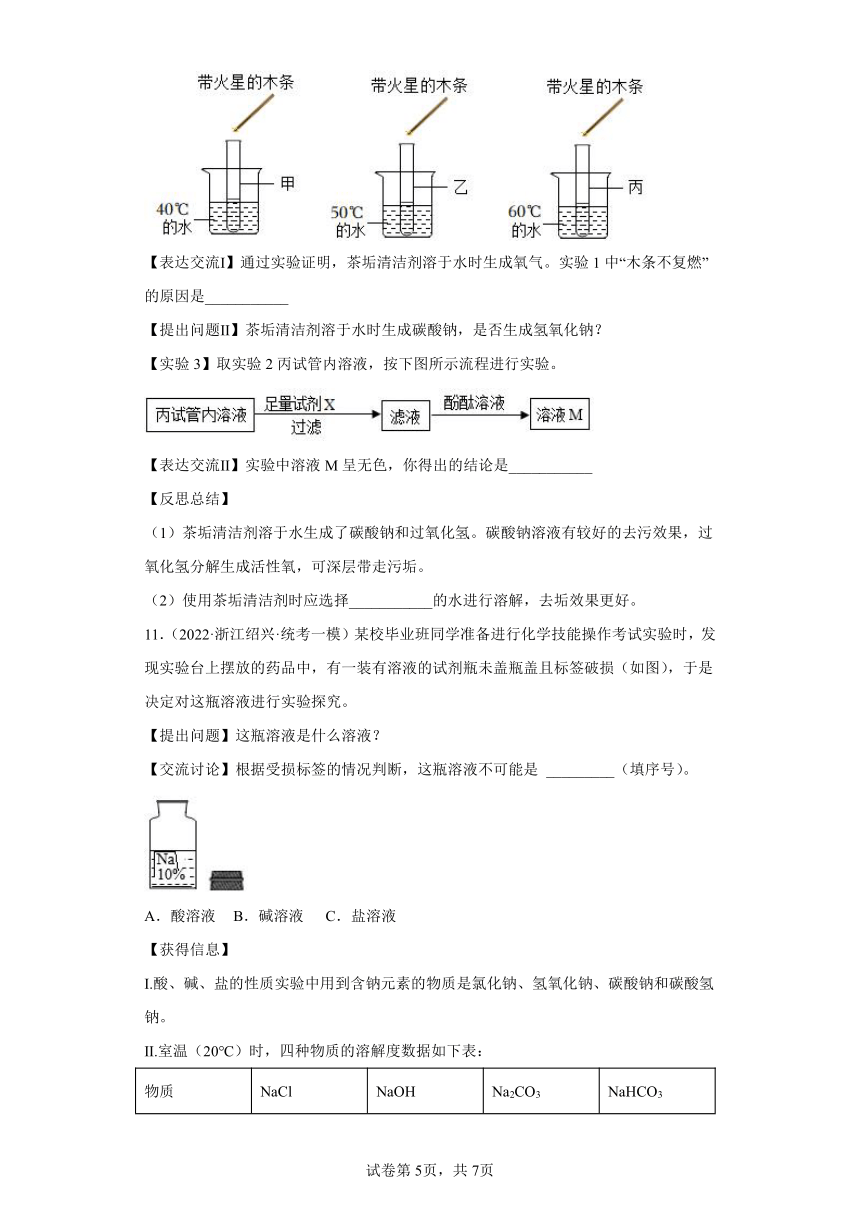
【实验2】取三份等量的实验1中的溶液,分别加入甲、乙、丙三支试管中,按下图所示进行实验。观察到都较快产生气泡,且温度越高产生气泡越快;伸入带火星的木条,木条都复燃。
【表达交流Ⅰ】通过实验证明,茶垢清洁剂溶于水时生成氧气。实验1中“木条不复燃”的原因是___________
【提出问题Ⅱ】茶垢清洁剂溶于水时生成碳酸钠,是否生成氢氧化钠?
【实验3】取实验2丙试管内溶液,按下图所示流程进行实验。
【表达交流Ⅱ】实验中溶液M呈无色,你得出的结论是___________
【反思总结】
(1)茶垢清洁剂溶于水生成了碳酸钠和过氧化氢。碳酸钠溶液有较好的去污效果,过氧化氢分解生成活性氧,可深层带走污垢。
(2)使用茶垢清洁剂时应选择___________的水进行溶解,去垢效果更好。
11.(2022·浙江绍兴·统考一模)某校毕业班同学准备进行化学技能操作考试实验时,发现实验台上摆放的药品中,有一装有溶液的试剂瓶未盖瓶盖且标签破损(如图),于是决定对这瓶溶液进行实验探究。
【提出问题】这瓶溶液是什么溶液?
【交流讨论】根据受损标签的情况判断,这瓶溶液不可能是 _________(填序号)。
A.酸溶液 B.碱溶液 C.盐溶液
【获得信息】
Ⅰ.酸、碱、盐的性质实验中用到含钠元素的物质是氯化钠、氢氧化钠、碳酸钠和碳酸氢钠。
Ⅱ.室温(20℃)时,四种物质的溶解度数据如下表:
物质 NaCl NaOH Na2CO3 NaHCO3
溶解度/g 36 109 215 9.6
Ⅲ.已知NaCl、BaCl2的水溶液呈中性。
【提出猜想】这瓶溶液可能是:
猜想一:氯化钠溶液 猜想二:碳酸钠溶液
猜想三:氢氧化钠溶液 猜想四:碳酸氢钠溶液
经过讨论,大家认为猜想四不合理,理由是___________。
【实验推断】
(1)小丽用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>7,则这瓶溶液不可能是___________。
(2)小明取样滴加过量的BaCl2溶液并不断振荡,观察到有沉淀产生,静置后,取少许上层清液,滴入酚酞溶液,振荡后无明显现象。则这瓶溶液的原溶液可能是___________。
【实验反思】实验室中,存取液体药品应注意使用后应立即盖上瓶塞并放回原处。
12.(2022·浙江丽水·统考一模)无土栽培是利用营养液栽培作物的一种方法。现有一种无色营养液,可能含有硝酸钙 、碳酸钾、氯化钾、硝酸钾中的一种或几种。为探究其成分,某同学设计并完成了下图所示的实验。
(1)绿叶类蔬菜可以适当多施含 ________的营养液(选填“N”或“P”或“K”);
(2)白色沉淀a 的化学式___________;
(3)分析上述实验可知营养液中一定含有的成分是 ___________。
13.(2022·浙江金华·统考一模)有一包固体样品,可能由氢氧化钠、硫酸钠、碳酸钠、硝酸镁、碳酸钙中的一种或几种物质组成。为确定该样品的组成,科学兴趣小组同学取适量样品进行探究,过程如图(微溶视为不溶):
根据以上信息回答下列问题:
(1)白色沉淀B中可能存在的物质有______;
(2)该样品中一定存在的物质是______。
参考答案:
1.C
【分析】所给的四中物质中,氢气只能与氧化铁反应,故A为氢气,B为氧化铁,氧化铁能与盐酸反应,故C为盐酸,D为硫酸铜。
【详解】A、A物质与B物质间发生是氢气与氧化铁反应,工业炼铁是一氧化碳与氧化铁反应,故错误;
B、B物质与C物质是氧化铁与盐酸反应,化学方程式为,故错误;
C、C物质与NaOH溶液反应是盐酸和氢氧化钠反应生成氯化钠和水,此反应无明显现象,故正确;
D、D物质的溶液与NaOH溶液发生反应时产生蓝色沉淀氢氧化铜,故错误。
故选C。
2. NaCl ##氯化钠 BaCl2##氯化钡 BD##DB
【分析】NaCl、Na2CO3、AgNO3、BaCl2、HCl五种溶液之间的部分反应关系,线条相连的溶液之间可以发生化学反应,氯化钠只会与硝酸银反应,所以E是氯化钠,D是硝酸银,A、C会与硝酸银反应,所以A、C是盐酸、氯化钡中的一种,B是碳酸钠,经过验证,推导正确。
【详解】(1)由分析可知,E是NaCl溶液;
(2)A和B反应有气体生成,所以A、B是碳酸钠和稀盐酸,C是BaCl2溶液;
(3)图中还缺少一条连线,硝酸银和碳酸钠反应生成碳酸银沉淀和硝酸钠,此线应连在BD两溶液之间。
3. 硝酸钙(或硝酸钡) 83.2%
解:依题意可得HNO3的质量为:10%×15g=1.5g,KOH的质量为:15%×8g=1.2g,假设KOH完全反应,消耗HNO3的质量为x,生成KNO3的质量为y。
,x=1.35g<1.5g,即HNO3过量,KOH全部反应转化为KNO3,有,y=g,则反应的收率为:≈83.2%。 硝酸是强酸,具有强腐蚀性(或“氢氧化钾具有强腐蚀性”)
【详解】(1)因为小科将A、B盐加到装有少量水的试管中,充分振荡制取硝酸钾。I.取少量A、B盐溶液分别滴加稀盐酸,A盐溶液有气泡生成,说明A盐溶液含有碳酸根离子,则A是碳酸钾,B盐溶液无明显现象,B含有硝酸根离子。II.另取少量A、B盐溶液,分别滴加氢氧化钠溶液,A、B盐溶液均无明显现象。根据以上实验现象,则B盐可能是硝酸钙(或硝酸钡)。
(2)见答案
(3)从安全的角度,对小宁制取硝酸钾的方案进行评价:硝酸是强酸,具有强腐蚀性(或“氢氧化钾具有强腐蚀性”)。
4. 使溶液受热均匀,防止局部过热 硫酸钡##BaSO4 硫酸钠、碳酸钠、氯化钠
【分析】无色溶液A和钡盐生成的白色沉淀部分溶于硝酸,且生成气体,说明溶液A中含有碳酸根离子和硫酸根离子,且A是三种钠盐,因此A中含有碳酸钠和硫酸钠;滤液蒸发结晶有氯化钠析出,说明F溶液中含有氯化钠。
【详解】(1)蒸发时玻璃棒的作用是:使溶液受热均匀,防止局部过热。
(2)碳酸钠和氯化钡产生的碳酸钡沉淀,碳酸钡和硝酸反应产生的二氧化碳;白色沉淀E是硫酸钠和氯化钡反应产生的硫酸钡沉淀。
(3)原混合物中含有的三种易溶于水的钠盐分别是碳酸钠、硫酸钠和氯化钠。
5. 氯化铁 氢氧化钾、氯化钡
【分析】氯化铁在溶液中显黄色,碳酸根离子、硫酸根离子和钡离子会生成白色沉淀,氢氧化钾和二氧化碳反应生成碳酸钾和水,碳酸钾和氯化钡反应生成碳酸钡沉淀,氯离子和银离子反应生成氯化银沉淀:①取适量粉末溶于水中,形成无色澄清溶液,杯底无沉淀物,所以样品中一定不含氯化铁,氯化钡和碳酸钠、硫酸钠不能同时含有;
②取适量步骤①所得溶液,用吸管向其中吹“泡泡”。过一会儿,溶液出现浑浊现象,所以样品中一定含有氢氧化钾和氯化钡,一定不含硫酸钠、碳酸钠;
③另取步骤①所得溶液,滴加硝酸银溶液,产生白色沉淀,氯化钡可以提供氯离子,所以样品中可能含有氯化钾。
【详解】由分析可知(1)仅根据步骤①现象可知,该粉末中一定不含的成分是氯化铁;
(2)可确定该粉末中一定含有的成分是氢氧化钾、氯化钡。
6. 除铁锈(合理即可) Ca(OH)2
【分析】可以选择特殊位置,例如已知D位置上投篮的“队员”是个灭火“能手”,说明D是二氧化碳,二氧化碳能和氢氧化钙反应,氢氧化钙能和稀硫酸、氯化铜反应,稀硫酸能和铁反应,铁能和氯化铜反应,由此可知:C是氢氧化钙,B是稀硫酸,A是铁。
【详解】分析可知(1)B应该为稀硫酸,它与氧化铁反应生成硫酸铁和水,因此它可以除去铁锈,制取化肥、农药;
(2)氯化铜除能和铁反应外,还能够和氢氧化钙反应,氯化铜除传球给A位置“队员”外,还能直接传球给氢氧化钙“队员”,化学式为Ca(OH)2。
7. 过滤 CaCO3+2HCl=CaCl2+H2O+CO2 ↑ NaOH、CuCl2、 CaCO3
【分析】结合图框,固体粉末加入足量的水过滤,得到沉淀Ⅰ,往沉淀Ⅰ中加入盐酸有无色气体生成和蓝色溶液,CaCO3和稀盐酸反应会生成气体,说明固体粉末中含有碳酸钙。氢氧化铜沉淀与盐酸反应生成氯化铜和水,氯化铜溶液呈蓝色,说明固体粉末中含有NaOH、CuCl2.因为存在氢氧化钠和氯化铜,氢氧化钠与氯化铜反应生成氢氧化铜沉淀和氯化钠,所以溶液Ⅰ一定含有钠离子和氯离子,进而后面实验对氯离子的检验没有意义,因为无法确定原固体中含有氯化钠,因此无法确定是否含有NaCl、Mg(OH)2。
【详解】(1)由图可知,操作Ⅰ和操作Ⅱ相同,都是用于固体和液体的分离,其名称是过滤,故填过滤。
(2)由分析可知,无色气体是碳酸钙和稀盐酸反应生成的二氧化碳,即碳酸钙与稀盐酸反应,生成氯化钙、水和二氧化碳,故反应的化学方程式写为:CaCO3+2HCl=CaCl2+H2O+CO2↑。
(3)由上述分析可知,原固体粉末中一定含有NaOH、CuCl2、CaCO3,故填NaOH、CuCl2、 CaCO3。
8. 碳酸钙、硫酸钡 氢氧化镁 氯化钡、 氢氧化钠和氯化钠 硫酸钠
【详解】根据硫酸钠与氯化钡反应产生不溶于酸的硫酸钡沉淀,碳酸钙与盐酸反应产生二氧化碳,氢氧化钠与二氧化碳反应生成碳酸钠,碳酸钠与化钡反应产生碳酸钡沉淀分析。
样品中加入足量的水得滤渣a和滤液,滤渣a加足量稀盐酸,部分溶解且有无色气体产生,则说明a中含有能与盐酸反应的碳酸钙,又有不与盐酸反应的硫酸钡,由气体质量0.44g,即二氧化碳质量为0.44g,设碳酸钙质量为x
而滤渣a为1.5克,因a中含有硫酸钡,所以不能证明是否含有氢氧化镁,滤液中通入适量二氧化碳,产生白色沉淀b,说明滤液中含有氢氧化钠和氯化钡,氢氧化钠与二氧化碳反应生成碳酸钠,碳酸钠与氯化钡反应生成碳酸钡沉淀。
(1)滤渣a为碳酸钙、硫酸钡,可能含氢氧化镁,故①填碳酸钙、硫酸钡,②填氢氧化镁。
(2)溶液中溶质的成分为氯化钡、氢氧化钠,硫酸钠与氯化钡反应生成的氯化钠,故③填氯化钡、氢氧化钠和氯化钠。
(3) 若现象①“滤渣部分溶解”变为“滤渣全部溶解”,其他现象不变,说明滤渣中不含有硫酸钡,则原样品不存在的物质是硫酸钠,故④填硫酸钠。
9. CO2##H2O 2Mg+CO22MgO+C或6CO2+6H2O=C6H12O6+6O2 H2O+SO2= H2SO3或H2O+N2O3= 2HNO2.
【分析】由题文和图可知,C是常见气体,D是常见单质,都能够与A相互转化,且D和E、D和C能够相互转化,则A为二氧化碳,C是一氧化碳,D是氧气,B是碳酸,E是碳或葡萄糖,或者A为水,C是氢气,D为氧气,B是碳酸,E是能够与氧气反应的亚硫酸或亚硝酸。
【详解】(1)由分析可知,A为二氧化碳或水,其化学式分别为CO2、H2O,故填CO2或H2O。
(2)由分析可知,A可以为二氧化碳,E如为碳,则A→E的反应是镁与二氧化碳在点燃的条件下反应生成氧化镁和碳,反应的化学方程式为:2Mg+CO22MgO+C,A为二氧化碳,E如为葡萄糖,则A→E的反应是二氧化碳与水反应生成葡萄糖和氧气,反应的化学方程式为:6CO2+6H2O=C6H12O6+6O2,故填2Mg+CO22MgO+C或6CO2+6H2O=C6H12O6+6O2;
由分析可知,A还可以是水,E是能够与氧气反应的亚硫酸或亚硝酸,则A→E的反应是水与二氧化硫反应生成亚硫酸,反应的化学方程式为:H2O+SO2=H2SO3,或者是水与三氧化二氮反应生成亚硝酸,反应的化学方程式为H2O+N2O3= 2HNO2,故填H2O+SO2= H2SO3或H2O+N2O3= 2HNO2.。
10. 产生氧气速率较慢,氧气浓度较低,不能使带火星的木条复燃 茶垢清洁剂溶于水时没有生成氢氧化钠 温度较高
【详解】[表达交流Ⅰ]
实验1中产生氧气速率较慢,氧气浓度过低,不能使带火星的木条复燃;
[表达交流Ⅱ]
(1)加入试剂X的目的是除去溶液中碳酸钠,所以加入足量的氯化钙或氯化钡,氢氧化钠能使酚酞试液变红色,所以溶液M呈无色,说明没有氢氧化钠;
[反思总结]
根据题目中实验信息可知,在较高温度下,产生氧气速率快,另外碳酸钠在较高温度下,溶解度较大,利用碳酸钠的溶解,所以利用温度较高的水溶解茶垢剂可以取得良好的去垢的效果。
11. A 20℃时,碳酸氢钠的溶解度为9.6g,饱和溶液的溶质质量分数<10% 氯化钠溶液 碳酸钠溶液(或完全变质的氢氧化钠溶液)
【详解】[交流讨论]酸是由氢离子和酸根离子构成,碱是由金属离子和氢氧根离子构成,盐是由金属离子和酸根离子构成,酸中没有钠离子;
[提出猜想]20℃时,碳酸氢钠的溶解度为9.6g,该温度下,碳酸氢钠饱和溶液的溶质质量分数=×100%≈8.8%,不可能得到10%的碳酸氢钠溶液,故猜想四错误;
[实验推断](1)由于溶液pH>7,显碱性,而氯化钠溶液显中性,pH=7,故不可能是氯化钠溶液;
(2)氯化钡与碳酸钠反应生成碳酸钡和氯化钠,滴加过量的氯化钡产生白色沉淀,说明含碳酸钠,过量的氯化钡能将碳酸钠除尽,静置后,取少许上层清液,滴入酚酞溶液,振荡后无明显现象,说明不含氢氧化钠,说明这瓶溶液的原溶液可能是碳酸钠溶液(也可能是完全变质的氢氧化钠溶液)。
12. N CaCO3 硝酸钙、氯化钾
【分析】向营养液中加入碳酸钠溶液,生成白色沉淀a,说明营养液中一定有硝酸钙,一定没有碳酸钾,向营养液中加入硝酸银溶液,生成白色沉淀b,说明营养液中有氯化钾中,硝酸钾可能有,也可能没有。
【详解】(1)氮肥可以使作物枝叶繁茂,叶色浓绿;绿叶类蔬菜可以适当多施含氮元素的营养液;
(2)碳酸钠和硝酸钙反应生成碳酸钙白色沉淀,故白色沉淀a 的化学式为:CaCO3;
(3)由分析可知,营养液中一定含有硝酸钙、氯化钾。
13. BaCO3、Mg(OH)2 Na2SO4
【分析】有一包固体样品,可能由氢氧化钠、硫酸钠、硝酸镁、碳酸钠、碳酸钙中的一种或几种物质组成。加入足量的水充分溶解后,得到白色沉淀A,加入过量稀硝酸,充分反应后沉淀全部溶解,生成气体,说明沉淀中含有碳酸盐,应为碳酸钙,沉淀中还可能含有氢氧化镁,说明原混合物中可能含有氢氧化钠、硫酸镁;得到的无色滤液,说明原混合物中不含硝酸铜;无色滤液中加入过量的氢氧化钡溶液,得到白色沉淀B,加入过量稀硝酸,只有部分沉淀溶解,说明沉淀中含有硫酸钡,则原混合物中一定含有硫酸钠;还含有能与稀硝酸反应的沉淀,同时还应生成了溶于酸的氢氧化镁沉淀或碳酸钡沉淀。
【详解】由分析可知:(1)白色沉淀B中可能存在的物质有:BaCO3、Mg(OH)2;
(2)该样品中一定存在的物质是Na2SO4。
试卷第1页,共3页
试卷第1页,共3页
学校:___________姓名:___________班级:___________考号:___________
一、选择题
1.(2022·浙江杭州·统考二模)2022年第24届冬季奥运会将由北京市和张家口市联合举行。如图所示,“五环”中相交两环中的物质间能够发生化学反应,其中A、B、C、D分别是HCl、Fe2O3、H2、CuSO4中的一种。下列说法中正确的是( )
A.A物质与B物质间发生的反应是工业炼铁的主要反应原理
B.B物质与C物质间发生反应的化学方程式为:4HCl+Fe2O3═2H2O+2FeCl2
C.C物质与NaOH溶液发生反应时无明显现象
D.D物质的溶液与NaOH溶液发生反应时产生红褐色沉淀
二、填空题
2.(2022·浙江绍兴·统考一模)如图表示NaCl、Na2CO3、AgNO3、BaCl2、HCl五种溶液之间的部分反应关系,线条相连的溶液之间可以发生化学反应。请问:
(1)E是___________溶液。
(2)A和B反应有气体生成,则C是___________溶液。
(3)图中还缺少一条连线,此线应连在___________两溶液之间。(填字母)
3.(2022·浙江宁波·统考二模)硝酸钾是一种重要的工业原料,我国年产量达到6万多吨。小科和小宁在实验室用不同的方案制取硝酸钾。
[实验步骤]
I. 小科将A、B盐加到装有少量水的试管中,充分振荡制取硝酸钾,如图甲。
II.小宁向试管中依次加入浓度为10%的酸溶液15g,浓度为15%的碱溶液8g,充分振荡制取硝酸钾,如图乙。
[实验分析]
(1)小宁想分析小科所用的A、B盐成分,分别取A、B盐配成溶液后进行以下实验。
I.取少量A、B盐溶液分别滴加稀盐酸,A盐溶液有气泡生成,B盐溶液无明显现象。
II.另取少量A、B盐溶液,分别滴加氢氧化钠溶液,A、B盐溶液均无明显现象。
则B盐可能是___________(写出一种即可) 。
(2)工业生产中,目的产物的实际生成量占目的产物的理论生成量的百分率称为收率。已知小宁最终制得硝酸钾1.8g,则反应的收率为___________( 计算结果保留到0.1%) 。
(3)请你从安全的角度,对小宁制取硝酸钾的方案进行评价:___________。
4.(2022·浙江温州·统考一模)现有三种易溶于水的钠盐组成的混合物,将其溶于水后得无色溶液A,进行如下实验并得到相应结果:
请回答下列问题:
(1)蒸发无色溶液F时,需要用到玻璃棒。玻璃棒的作用是______。
(2)白色沉淀E是______。
(3)分析得知晶体G为氯化钠,则三种钠盐的组成为______。
三、简答题
5.(2022·浙江金华·统考一模)某粉末中可能含有氯化铁、氢氧化钾、氯化钡、碳酸钠、氯化钾、硫酸钠中的一种或几种。某同学设计如下实验推测该粉末中所含成分。
①取适量粉末溶于水中,形成无色澄清溶液,杯底无沉淀物。
②取适量步骤①所得溶液,用吸管向其中吹“泡泡”。过一会儿, 溶液出现浑浊现象:
③另取步骤①所得溶液,滴加硝酸银溶液,产生白色沉淀。
(1)仅根据步骤①现象可知,该粉末中一定不含的成分是___________。
(2)可确定该粉末中一定含有的成分是___________。
6.(2022·浙江舟山·校联考二模)物质王国举行一场趣味篮球赛。某队由铁、二氧化碳、稀硫酸、澄清石灰水、氯化铜溶液五名“队员”组成,比赛中,由氯化铜溶液“队员”发球,“队员”间传接球,最后由D 位置“队员”投篮进球完成有效进攻。传接球“队员”间物质必须能相互反应,场上“队员”位置及传球路线如图。
(1)已知D位置上投篮的“队员”是个灭火“能手”,写出B位置“队员”所代表的物质的一种用途___________;
(2)为实现“快速进攻”,氯化铜溶液除了把球传给A位置“队员”外,还能直接传球给___________“队员”(填化学式)。
7.(2022·浙江宁波·统考一模)有一包固体粉末可能含有NaOH、NaCl、CuCl2、Mg(OH)2、CaCO3中的一种或多种,为探究其成分,某同学取样进行了如图所示实验:
(1)操作Ⅰ和操作Ⅱ相同,其名称是___________。
(2)生成无色气体的反应的化学方程式为___________。
(3)原固体粉末中一定含有的物质是___________。
8.(2022·浙江宁波·统考二模)有一包白色固体样品,可能由硫酸钠、氢氧化钠、碳酸钙、氯化钡、氯化镁中的一种或几种物质组成,为探究该样品的组成,某小组取适量样品按下列流程进行试验。
请回答:
(1)滤渣a的成分是___________,可能含有___________。
(2)溶液中溶质的成分有___________。
(3)若现象①“滤渣部分溶解”变为“滤渣全部溶解”,其他现象不变,则原样品不存在的物质是___________。
9.(2022·浙江宁波·统考二模)A、 B、C、D、E五种物质均为初中科学中所涉及的常见物质,它们存在如图的转化关系,“一”表示可以向箭头所指方向一步转化,弧线表示两种物质间可以发生反应,C是常见气体,D是常见单质,图中反应条件与其他物质均已略去。诸回答下列问题:
(1) A可能的化学式为___________。
(2)写出A→E的两个化学方程式:___________、___________。
四、探究题
10.(2022·浙江舟山·校联考二模)茶垢清洁剂能快速消除茶具上附着的茶垢,某小组同学对茶垢清洁剂进行了探究。
【查阅资料】下图是某品牌茶垢清洁剂说明书中的部分内容。
主要成分:过碳酸钠(化学式为2Na2CO3·3H2O2)去渍原理:过碳酸钠溶于水时生成碳酸钠(俗称纯碱)和过氧化氢······
【提出问题Ⅰ】茶垢清洁剂溶于水时生成过氧化氢,是否生成氧气?
【实验1】在盛有茶垢清洁剂固体的小烧杯中,加适量常温水,完全溶解后得到无色溶液,观察到有小气泡缓慢冒出,伸入带火星的木条,木条不复燃。
【实验2】取三份等量的实验1中的溶液,分别加入甲、乙、丙三支试管中,按下图所示进行实验。观察到都较快产生气泡,且温度越高产生气泡越快;伸入带火星的木条,木条都复燃。
【表达交流Ⅰ】通过实验证明,茶垢清洁剂溶于水时生成氧气。实验1中“木条不复燃”的原因是___________
【提出问题Ⅱ】茶垢清洁剂溶于水时生成碳酸钠,是否生成氢氧化钠?
【实验3】取实验2丙试管内溶液,按下图所示流程进行实验。
【表达交流Ⅱ】实验中溶液M呈无色,你得出的结论是___________
【反思总结】
(1)茶垢清洁剂溶于水生成了碳酸钠和过氧化氢。碳酸钠溶液有较好的去污效果,过氧化氢分解生成活性氧,可深层带走污垢。
(2)使用茶垢清洁剂时应选择___________的水进行溶解,去垢效果更好。
11.(2022·浙江绍兴·统考一模)某校毕业班同学准备进行化学技能操作考试实验时,发现实验台上摆放的药品中,有一装有溶液的试剂瓶未盖瓶盖且标签破损(如图),于是决定对这瓶溶液进行实验探究。
【提出问题】这瓶溶液是什么溶液?
【交流讨论】根据受损标签的情况判断,这瓶溶液不可能是 _________(填序号)。
A.酸溶液 B.碱溶液 C.盐溶液
【获得信息】
Ⅰ.酸、碱、盐的性质实验中用到含钠元素的物质是氯化钠、氢氧化钠、碳酸钠和碳酸氢钠。
Ⅱ.室温(20℃)时,四种物质的溶解度数据如下表:
物质 NaCl NaOH Na2CO3 NaHCO3
溶解度/g 36 109 215 9.6
Ⅲ.已知NaCl、BaCl2的水溶液呈中性。
【提出猜想】这瓶溶液可能是:
猜想一:氯化钠溶液 猜想二:碳酸钠溶液
猜想三:氢氧化钠溶液 猜想四:碳酸氢钠溶液
经过讨论,大家认为猜想四不合理,理由是___________。
【实验推断】
(1)小丽用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>7,则这瓶溶液不可能是___________。
(2)小明取样滴加过量的BaCl2溶液并不断振荡,观察到有沉淀产生,静置后,取少许上层清液,滴入酚酞溶液,振荡后无明显现象。则这瓶溶液的原溶液可能是___________。
【实验反思】实验室中,存取液体药品应注意使用后应立即盖上瓶塞并放回原处。
12.(2022·浙江丽水·统考一模)无土栽培是利用营养液栽培作物的一种方法。现有一种无色营养液,可能含有硝酸钙 、碳酸钾、氯化钾、硝酸钾中的一种或几种。为探究其成分,某同学设计并完成了下图所示的实验。
(1)绿叶类蔬菜可以适当多施含 ________的营养液(选填“N”或“P”或“K”);
(2)白色沉淀a 的化学式___________;
(3)分析上述实验可知营养液中一定含有的成分是 ___________。
13.(2022·浙江金华·统考一模)有一包固体样品,可能由氢氧化钠、硫酸钠、碳酸钠、硝酸镁、碳酸钙中的一种或几种物质组成。为确定该样品的组成,科学兴趣小组同学取适量样品进行探究,过程如图(微溶视为不溶):
根据以上信息回答下列问题:
(1)白色沉淀B中可能存在的物质有______;
(2)该样品中一定存在的物质是______。
参考答案:
1.C
【分析】所给的四中物质中,氢气只能与氧化铁反应,故A为氢气,B为氧化铁,氧化铁能与盐酸反应,故C为盐酸,D为硫酸铜。
【详解】A、A物质与B物质间发生是氢气与氧化铁反应,工业炼铁是一氧化碳与氧化铁反应,故错误;
B、B物质与C物质是氧化铁与盐酸反应,化学方程式为,故错误;
C、C物质与NaOH溶液反应是盐酸和氢氧化钠反应生成氯化钠和水,此反应无明显现象,故正确;
D、D物质的溶液与NaOH溶液发生反应时产生蓝色沉淀氢氧化铜,故错误。
故选C。
2. NaCl ##氯化钠 BaCl2##氯化钡 BD##DB
【分析】NaCl、Na2CO3、AgNO3、BaCl2、HCl五种溶液之间的部分反应关系,线条相连的溶液之间可以发生化学反应,氯化钠只会与硝酸银反应,所以E是氯化钠,D是硝酸银,A、C会与硝酸银反应,所以A、C是盐酸、氯化钡中的一种,B是碳酸钠,经过验证,推导正确。
【详解】(1)由分析可知,E是NaCl溶液;
(2)A和B反应有气体生成,所以A、B是碳酸钠和稀盐酸,C是BaCl2溶液;
(3)图中还缺少一条连线,硝酸银和碳酸钠反应生成碳酸银沉淀和硝酸钠,此线应连在BD两溶液之间。
3. 硝酸钙(或硝酸钡) 83.2%
解:依题意可得HNO3的质量为:10%×15g=1.5g,KOH的质量为:15%×8g=1.2g,假设KOH完全反应,消耗HNO3的质量为x,生成KNO3的质量为y。
,x=1.35g<1.5g,即HNO3过量,KOH全部反应转化为KNO3,有,y=g,则反应的收率为:≈83.2%。 硝酸是强酸,具有强腐蚀性(或“氢氧化钾具有强腐蚀性”)
【详解】(1)因为小科将A、B盐加到装有少量水的试管中,充分振荡制取硝酸钾。I.取少量A、B盐溶液分别滴加稀盐酸,A盐溶液有气泡生成,说明A盐溶液含有碳酸根离子,则A是碳酸钾,B盐溶液无明显现象,B含有硝酸根离子。II.另取少量A、B盐溶液,分别滴加氢氧化钠溶液,A、B盐溶液均无明显现象。根据以上实验现象,则B盐可能是硝酸钙(或硝酸钡)。
(2)见答案
(3)从安全的角度,对小宁制取硝酸钾的方案进行评价:硝酸是强酸,具有强腐蚀性(或“氢氧化钾具有强腐蚀性”)。
4. 使溶液受热均匀,防止局部过热 硫酸钡##BaSO4 硫酸钠、碳酸钠、氯化钠
【分析】无色溶液A和钡盐生成的白色沉淀部分溶于硝酸,且生成气体,说明溶液A中含有碳酸根离子和硫酸根离子,且A是三种钠盐,因此A中含有碳酸钠和硫酸钠;滤液蒸发结晶有氯化钠析出,说明F溶液中含有氯化钠。
【详解】(1)蒸发时玻璃棒的作用是:使溶液受热均匀,防止局部过热。
(2)碳酸钠和氯化钡产生的碳酸钡沉淀,碳酸钡和硝酸反应产生的二氧化碳;白色沉淀E是硫酸钠和氯化钡反应产生的硫酸钡沉淀。
(3)原混合物中含有的三种易溶于水的钠盐分别是碳酸钠、硫酸钠和氯化钠。
5. 氯化铁 氢氧化钾、氯化钡
【分析】氯化铁在溶液中显黄色,碳酸根离子、硫酸根离子和钡离子会生成白色沉淀,氢氧化钾和二氧化碳反应生成碳酸钾和水,碳酸钾和氯化钡反应生成碳酸钡沉淀,氯离子和银离子反应生成氯化银沉淀:①取适量粉末溶于水中,形成无色澄清溶液,杯底无沉淀物,所以样品中一定不含氯化铁,氯化钡和碳酸钠、硫酸钠不能同时含有;
②取适量步骤①所得溶液,用吸管向其中吹“泡泡”。过一会儿,溶液出现浑浊现象,所以样品中一定含有氢氧化钾和氯化钡,一定不含硫酸钠、碳酸钠;
③另取步骤①所得溶液,滴加硝酸银溶液,产生白色沉淀,氯化钡可以提供氯离子,所以样品中可能含有氯化钾。
【详解】由分析可知(1)仅根据步骤①现象可知,该粉末中一定不含的成分是氯化铁;
(2)可确定该粉末中一定含有的成分是氢氧化钾、氯化钡。
6. 除铁锈(合理即可) Ca(OH)2
【分析】可以选择特殊位置,例如已知D位置上投篮的“队员”是个灭火“能手”,说明D是二氧化碳,二氧化碳能和氢氧化钙反应,氢氧化钙能和稀硫酸、氯化铜反应,稀硫酸能和铁反应,铁能和氯化铜反应,由此可知:C是氢氧化钙,B是稀硫酸,A是铁。
【详解】分析可知(1)B应该为稀硫酸,它与氧化铁反应生成硫酸铁和水,因此它可以除去铁锈,制取化肥、农药;
(2)氯化铜除能和铁反应外,还能够和氢氧化钙反应,氯化铜除传球给A位置“队员”外,还能直接传球给氢氧化钙“队员”,化学式为Ca(OH)2。
7. 过滤 CaCO3+2HCl=CaCl2+H2O+CO2 ↑ NaOH、CuCl2、 CaCO3
【分析】结合图框,固体粉末加入足量的水过滤,得到沉淀Ⅰ,往沉淀Ⅰ中加入盐酸有无色气体生成和蓝色溶液,CaCO3和稀盐酸反应会生成气体,说明固体粉末中含有碳酸钙。氢氧化铜沉淀与盐酸反应生成氯化铜和水,氯化铜溶液呈蓝色,说明固体粉末中含有NaOH、CuCl2.因为存在氢氧化钠和氯化铜,氢氧化钠与氯化铜反应生成氢氧化铜沉淀和氯化钠,所以溶液Ⅰ一定含有钠离子和氯离子,进而后面实验对氯离子的检验没有意义,因为无法确定原固体中含有氯化钠,因此无法确定是否含有NaCl、Mg(OH)2。
【详解】(1)由图可知,操作Ⅰ和操作Ⅱ相同,都是用于固体和液体的分离,其名称是过滤,故填过滤。
(2)由分析可知,无色气体是碳酸钙和稀盐酸反应生成的二氧化碳,即碳酸钙与稀盐酸反应,生成氯化钙、水和二氧化碳,故反应的化学方程式写为:CaCO3+2HCl=CaCl2+H2O+CO2↑。
(3)由上述分析可知,原固体粉末中一定含有NaOH、CuCl2、CaCO3,故填NaOH、CuCl2、 CaCO3。
8. 碳酸钙、硫酸钡 氢氧化镁 氯化钡、 氢氧化钠和氯化钠 硫酸钠
【详解】根据硫酸钠与氯化钡反应产生不溶于酸的硫酸钡沉淀,碳酸钙与盐酸反应产生二氧化碳,氢氧化钠与二氧化碳反应生成碳酸钠,碳酸钠与化钡反应产生碳酸钡沉淀分析。
样品中加入足量的水得滤渣a和滤液,滤渣a加足量稀盐酸,部分溶解且有无色气体产生,则说明a中含有能与盐酸反应的碳酸钙,又有不与盐酸反应的硫酸钡,由气体质量0.44g,即二氧化碳质量为0.44g,设碳酸钙质量为x
而滤渣a为1.5克,因a中含有硫酸钡,所以不能证明是否含有氢氧化镁,滤液中通入适量二氧化碳,产生白色沉淀b,说明滤液中含有氢氧化钠和氯化钡,氢氧化钠与二氧化碳反应生成碳酸钠,碳酸钠与氯化钡反应生成碳酸钡沉淀。
(1)滤渣a为碳酸钙、硫酸钡,可能含氢氧化镁,故①填碳酸钙、硫酸钡,②填氢氧化镁。
(2)溶液中溶质的成分为氯化钡、氢氧化钠,硫酸钠与氯化钡反应生成的氯化钠,故③填氯化钡、氢氧化钠和氯化钠。
(3) 若现象①“滤渣部分溶解”变为“滤渣全部溶解”,其他现象不变,说明滤渣中不含有硫酸钡,则原样品不存在的物质是硫酸钠,故④填硫酸钠。
9. CO2##H2O 2Mg+CO22MgO+C或6CO2+6H2O=C6H12O6+6O2 H2O+SO2= H2SO3或H2O+N2O3= 2HNO2.
【分析】由题文和图可知,C是常见气体,D是常见单质,都能够与A相互转化,且D和E、D和C能够相互转化,则A为二氧化碳,C是一氧化碳,D是氧气,B是碳酸,E是碳或葡萄糖,或者A为水,C是氢气,D为氧气,B是碳酸,E是能够与氧气反应的亚硫酸或亚硝酸。
【详解】(1)由分析可知,A为二氧化碳或水,其化学式分别为CO2、H2O,故填CO2或H2O。
(2)由分析可知,A可以为二氧化碳,E如为碳,则A→E的反应是镁与二氧化碳在点燃的条件下反应生成氧化镁和碳,反应的化学方程式为:2Mg+CO22MgO+C,A为二氧化碳,E如为葡萄糖,则A→E的反应是二氧化碳与水反应生成葡萄糖和氧气,反应的化学方程式为:6CO2+6H2O=C6H12O6+6O2,故填2Mg+CO22MgO+C或6CO2+6H2O=C6H12O6+6O2;
由分析可知,A还可以是水,E是能够与氧气反应的亚硫酸或亚硝酸,则A→E的反应是水与二氧化硫反应生成亚硫酸,反应的化学方程式为:H2O+SO2=H2SO3,或者是水与三氧化二氮反应生成亚硝酸,反应的化学方程式为H2O+N2O3= 2HNO2,故填H2O+SO2= H2SO3或H2O+N2O3= 2HNO2.。
10. 产生氧气速率较慢,氧气浓度较低,不能使带火星的木条复燃 茶垢清洁剂溶于水时没有生成氢氧化钠 温度较高
【详解】[表达交流Ⅰ]
实验1中产生氧气速率较慢,氧气浓度过低,不能使带火星的木条复燃;
[表达交流Ⅱ]
(1)加入试剂X的目的是除去溶液中碳酸钠,所以加入足量的氯化钙或氯化钡,氢氧化钠能使酚酞试液变红色,所以溶液M呈无色,说明没有氢氧化钠;
[反思总结]
根据题目中实验信息可知,在较高温度下,产生氧气速率快,另外碳酸钠在较高温度下,溶解度较大,利用碳酸钠的溶解,所以利用温度较高的水溶解茶垢剂可以取得良好的去垢的效果。
11. A 20℃时,碳酸氢钠的溶解度为9.6g,饱和溶液的溶质质量分数<10% 氯化钠溶液 碳酸钠溶液(或完全变质的氢氧化钠溶液)
【详解】[交流讨论]酸是由氢离子和酸根离子构成,碱是由金属离子和氢氧根离子构成,盐是由金属离子和酸根离子构成,酸中没有钠离子;
[提出猜想]20℃时,碳酸氢钠的溶解度为9.6g,该温度下,碳酸氢钠饱和溶液的溶质质量分数=×100%≈8.8%,不可能得到10%的碳酸氢钠溶液,故猜想四错误;
[实验推断](1)由于溶液pH>7,显碱性,而氯化钠溶液显中性,pH=7,故不可能是氯化钠溶液;
(2)氯化钡与碳酸钠反应生成碳酸钡和氯化钠,滴加过量的氯化钡产生白色沉淀,说明含碳酸钠,过量的氯化钡能将碳酸钠除尽,静置后,取少许上层清液,滴入酚酞溶液,振荡后无明显现象,说明不含氢氧化钠,说明这瓶溶液的原溶液可能是碳酸钠溶液(也可能是完全变质的氢氧化钠溶液)。
12. N CaCO3 硝酸钙、氯化钾
【分析】向营养液中加入碳酸钠溶液,生成白色沉淀a,说明营养液中一定有硝酸钙,一定没有碳酸钾,向营养液中加入硝酸银溶液,生成白色沉淀b,说明营养液中有氯化钾中,硝酸钾可能有,也可能没有。
【详解】(1)氮肥可以使作物枝叶繁茂,叶色浓绿;绿叶类蔬菜可以适当多施含氮元素的营养液;
(2)碳酸钠和硝酸钙反应生成碳酸钙白色沉淀,故白色沉淀a 的化学式为:CaCO3;
(3)由分析可知,营养液中一定含有硝酸钙、氯化钾。
13. BaCO3、Mg(OH)2 Na2SO4
【分析】有一包固体样品,可能由氢氧化钠、硫酸钠、硝酸镁、碳酸钠、碳酸钙中的一种或几种物质组成。加入足量的水充分溶解后,得到白色沉淀A,加入过量稀硝酸,充分反应后沉淀全部溶解,生成气体,说明沉淀中含有碳酸盐,应为碳酸钙,沉淀中还可能含有氢氧化镁,说明原混合物中可能含有氢氧化钠、硫酸镁;得到的无色滤液,说明原混合物中不含硝酸铜;无色滤液中加入过量的氢氧化钡溶液,得到白色沉淀B,加入过量稀硝酸,只有部分沉淀溶解,说明沉淀中含有硫酸钡,则原混合物中一定含有硫酸钠;还含有能与稀硝酸反应的沉淀,同时还应生成了溶于酸的氢氧化镁沉淀或碳酸钡沉淀。
【详解】由分析可知:(1)白色沉淀B中可能存在的物质有:BaCO3、Mg(OH)2;
(2)该样品中一定存在的物质是Na2SO4。
试卷第1页,共3页
试卷第1页,共3页
