6.1化学反应与能量变化 基础练习(含答案) 2022-2023学年高一下学期化学人教版(2019)必修第二册
文档属性
| 名称 | 6.1化学反应与能量变化 基础练习(含答案) 2022-2023学年高一下学期化学人教版(2019)必修第二册 |
|
|
| 格式 | zip | ||
| 文件大小 | 346.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-03 00:00:00 | ||
图片预览


文档简介
6.1化学反应与能量变化
一、单选题(本大题共14小题)
1. 电池是人类生产和生活中的重要能量来源,各式各样电池的发展是化学对人类的一大贡献。下列有关电池的叙述正确的是( )
A. 原电池反应均是自发的氧化还原反应
B. 氢氧燃料电池工作时氢气在正极被氧化
C. 氢氧燃料电池是将热能转化为电能的装置
D. 铅蓄电池在放电过程中,负极质量减少,正极质量增加
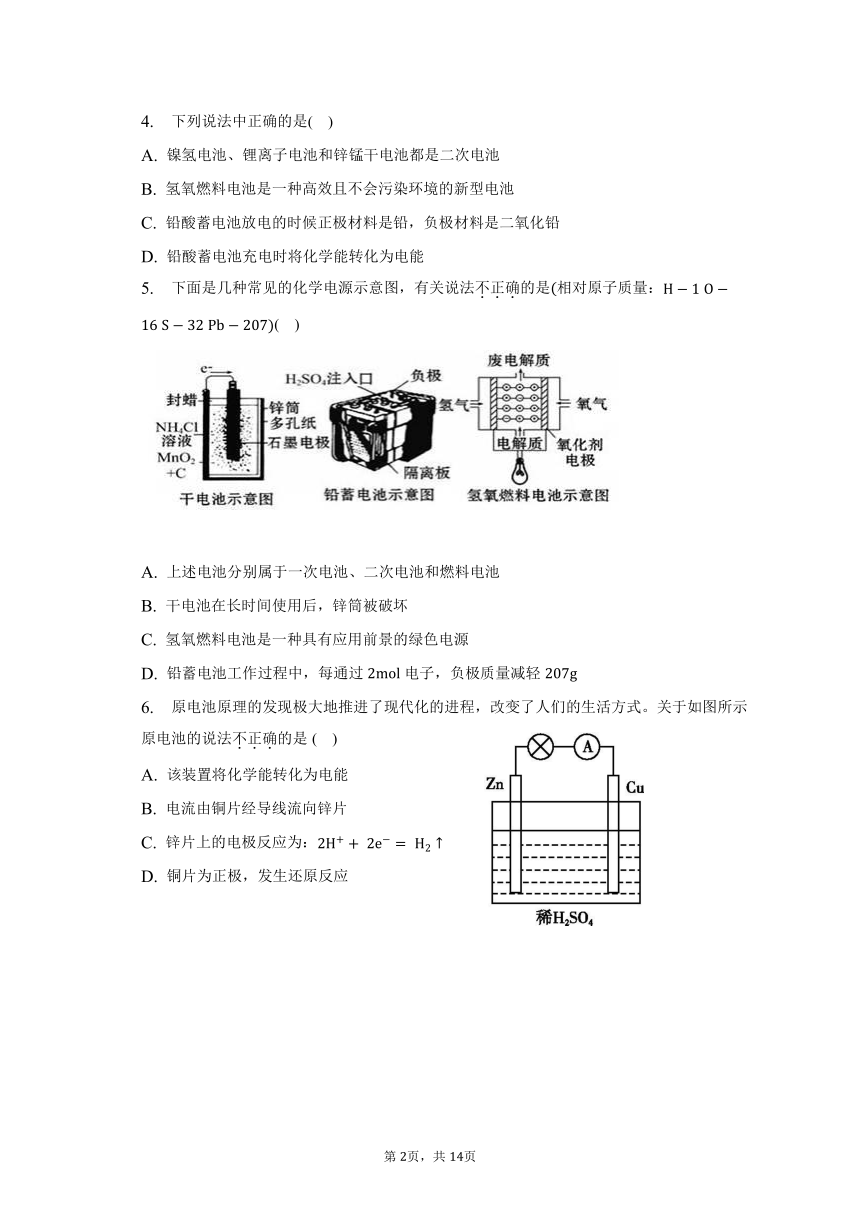
2. 如图所示是几种常见的化学电源示意图,有关说法正确的是( )
A. 上述电池分别属于一次电池、二次电池和燃料电池
B. 干电池工作时,向锌筒移动
C. 铅蓄电池工作过程中,每通过电子,负极质量减轻
D. 氢氧燃料电池的正极反应一定是
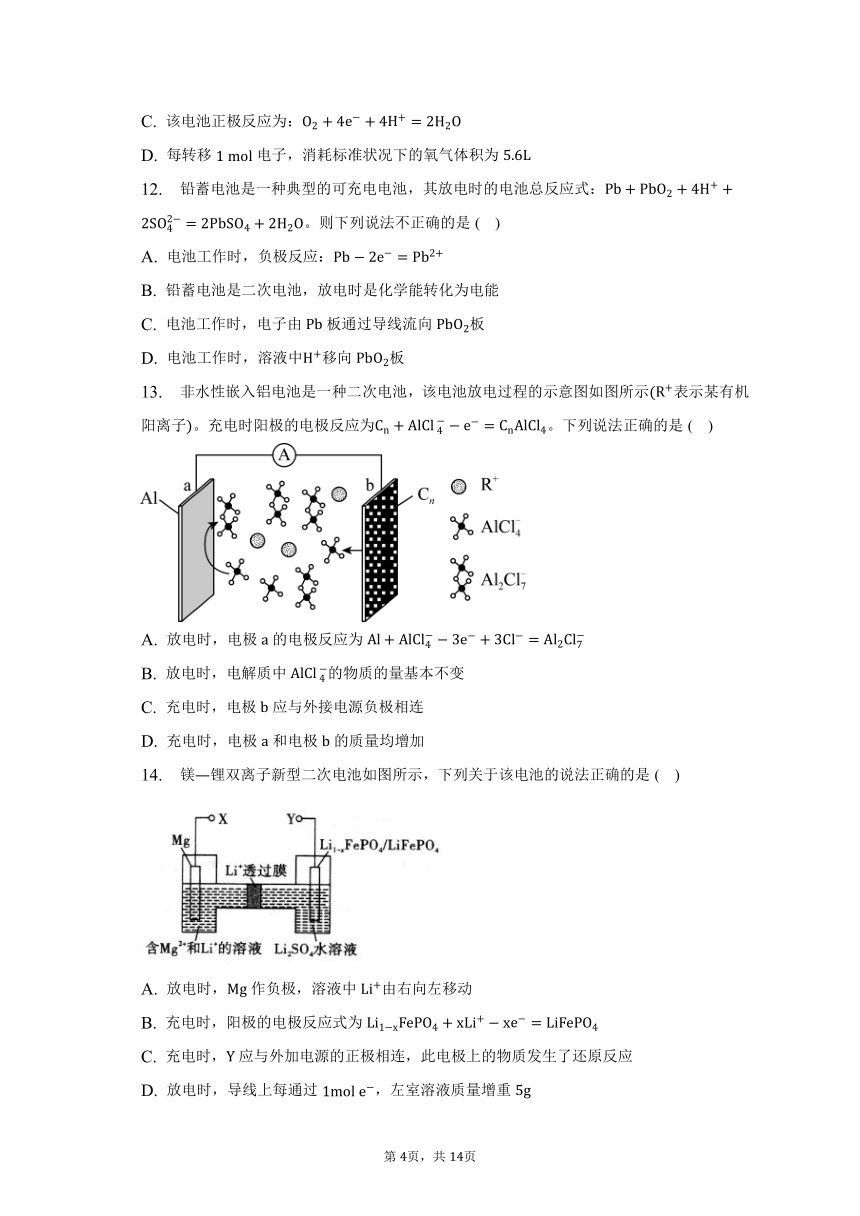
3. 下列电池工作时,在正极放电的是 ( )
A. B.
C. D.
4. 下列说法中正确的是( )
A. 镍氢电池、锂离子电池和锌锰干电池都是二次电池
B. 氢氧燃料电池是一种高效且不会污染环境的新型电池
C. 铅酸蓄电池放电的时候正极材料是铅,负极材料是二氧化铅
D. 铅酸蓄电池充电时将化学能转化为电能
5. 下面是几种常见的化学电源示意图,有关说法不正确的是相对原子质量:( )
A. 上述电池分别属于一次电池、二次电池和燃料电池
B. 干电池在长时间使用后,锌筒被破坏
C. 氢氧燃料电池是一种具有应用前景的绿色电源
D. 铅蓄电池工作过程中,每通过电子,负极质量减轻
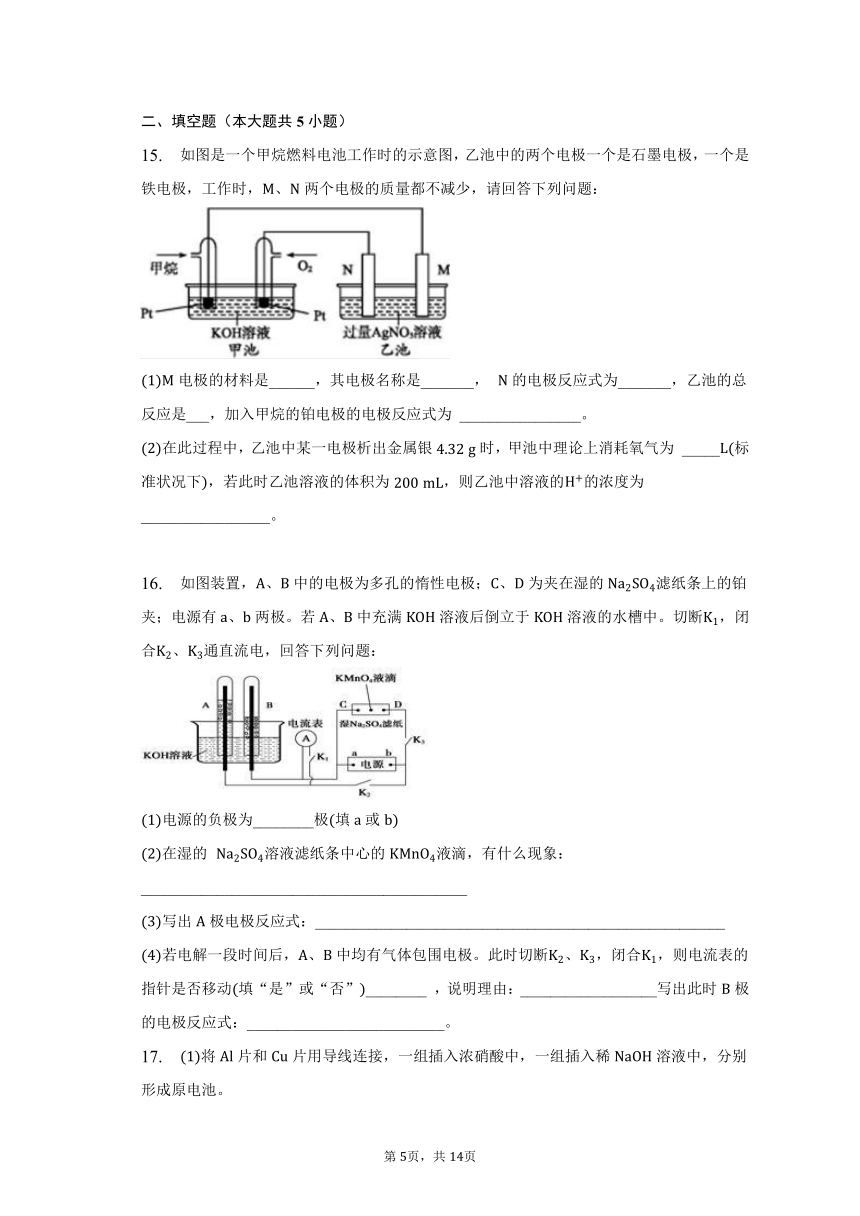
6. 原电池原理的发现极大地推进了现代化的进程,改变了人们的生活方式。关于如图所示原电池的说法不正确的是( )
A. 该装置将化学能转化为电能
B. 电流由铜片经导线流向锌片
C. 锌片上的电极反应为:
D. 铜片为正极,发生还原反应
7. 下列设备工作时,将化学能转化为热能的是( )
A. B.
C. D.
8. 把锌片和铜片用导线连接后,浸入的盐酸溶液中,可能产生的结果是 ( )
A. 铜片上放出氯气 B. 铜片上放出氧气 C. 铜片上放出氢气 D. 铜片上放出氮气
9. 下列有关化学电源叙述正确的是( )
A. 水果电池是高效环保的家用电池
B. 锌锰干电池是一种常用的二次电池
C. 锌锰干电池工作一段时间后锌外壳逐渐变薄
D. 锌锰干电池碳棒是负极
10. 某化学兴趣小组学习原电池知识后,决定用其原理,尝试利用铁粉、活性炭、无机盐等物质开发产品。小组提出的设想或对原理的理解不正确的是( )
A. 打算制成小包装用于糕点的脱氧剂
B. 利用反应放出热量的原理制成暖宝宝
C. 调整电池结构,可降低温度,可用于延长糕点保质期
D. 正极的电极反应为:
11. 氨氧燃料电池具有很大的发展潜力。下图为某氨氧燃料电池示意图,下列说法错误的是 ( )
A. 电极为该电池的负极
B. 电子流向为电极经外电路流向电极,溶液中离子趋向电极
C. 该电池正极反应为:
D. 每转移电子,消耗标准状况下的氧气体积为
12. 铅蓄电池是一种典型的可充电电池,其放电时的电池总反应式:。则下列说法不正确的是( )
A. 电池工作时,负极反应:
B. 铅蓄电池是二次电池,放电时是化学能转化为电能
C. 电池工作时,电子由板通过导线流向板
D. 电池工作时,溶液中移向板
13. 非水性嵌入铝电池是一种二次电池,该电池放电过程的示意图如图所示表示某有机阳离子。充电时阳极的电极反应为。下列说法正确的是( )
A. 放电时,电极的电极反应为
B. 放电时,电解质中的物质的量基本不变
C. 充电时,电极应与外接电源负极相连
D. 充电时,电极和电极的质量均增加
14. 镁锂双离子新型二次电池如图所示,下列关于该电池的说法正确的是( )
A. 放电时,作负极,溶液中由右向左移动
B. 充电时,阳极的电极反应式为
C. 充电时,应与外加电源的正极相连,此电极上的物质发生了还原反应
D. 放电时,导线上每通过,左室溶液质量增重
二、填空题(本大题共5小题)
15. 如图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时,、两个电极的质量都不减少,请回答下列问题:
电极的材料是______,其电极名称是_______, 的电极反应式为_______,乙池的总反应是___,加入甲烷的铂电极的电极反应式为 ________________。
在此过程中,乙池中某一电极析出金属银时,甲池中理论上消耗氧气为 _____标准状况下,若此时乙池溶液的体积为,则乙池中溶液的的浓度为 _________________。
16. 如图装置,、中的电极为多孔的惰性电极;、为夹在湿的滤纸条上的铂夹;电源有、两极。若、中充满溶液后倒立于溶液的水槽中。切断,闭合、通直流电,回答下列问题:
电源的负极为________极填或
在湿的 溶液滤纸条中心的液滴,有什么现象:___________________________________________
写出极电极反应式:______________________________________________________
若电解一段时间后,、中均有气体包围电极。此时切断、,闭合,则电流表的指针是否移动填“是”或“否”________ ,说明理由:__________________写出此时极的电极反应式:__________________________。
17. 将片和片用导线连接,一组插入浓硝酸中,一组插入稀溶液中,分别形成原电池。
写出插入稀溶液中形成原电池的负极反应____________________________________。
写出插入浓硝酸中形成原电池的正极反应__________________________________________。
铅蓄电池是最常见的二次电池,工作时的总反应为。由于其电压稳定、使用方便、安全可靠、价格低廉,所以在生产、生活中使用广泛,写出铅蓄电池放电时的正极反应________________________________________________________;充电时的阴极反应________________________________________________________。该电池在工作时,电极的质量将________填“增加”“减小”或“不变”,若该电池反应消耗了,则转移电子的数目为________________。
18. 镁、铝是重要的金属,回答下列问题:
镁的原子结构示意图为________________。
是一种重要的储氢材料,其与水反应放出氢气,将反应生成的氢气与氧气设计成氢氧燃料电池如下图。
写出与水反应的化学方程式:________________________________。
负极电极反应式为________________________________。
若中反应生成,且能量转化率为,则导线中通过电子的物质的量为________。
某同学在实验室设计了如图所示的原电池:
池中负极为:________填化学式,下同,池中负极为:________。
写出池中负极电极反应式:________________________________。
19. 写出的电子式:_________,
写出的电子式和结构式:_________,_________,
写出甲烷燃料电池在碱性条件下的电极反应式.
负极:_______________________
正极:_______________________
写出铅蓄电池充电时的电极反应式.
阴极:______________________
阳极:______________________
答案和解析
1.【答案】
【解答】
A.构成原电池的条件之一是:能自发的进行氧化还原反应,所以原电池反应均是自发的氧化还原反应,故A正确;
B.氢氧燃料电池工作时氢气在负极上失电子被氧化,故B错误;
C.氢氧燃料电池也是原电池,所以氢氧燃料电池是将化学能转变为电能的装置,故C错误;
D.根据铅蓄电池放电时,负极电极反应式为:;正极电极反应式为:,所以正负极质量都增加,故D错误。
故选A。
2.【答案】
【解答】
A.干电池是一次性电池,铅蓄电池是可充电电池属于二次电池,氢氧燃料电池属于燃料电池,故A正确;
B.在干电池中,作负极,向正极碳棒移动,故B错误;
C.铅蓄电池工作过程中,硫酸铅在负极上析出,该极质量应该增加而非减小,故C错误;
D.氢氧燃料电池的正极反应受溶液的酸碱性影响,则电极反应式不一定是 ,故D错误。
故选A。
3.【答案】
【解答】
A.锌锰干电池中电极反应式:负极:,正极:,不符合题意,故A错误;
B.酸性氢氧燃料电池电极反应式为、;碱性氢氧燃料电池电极反应式为、,符合题意,故B正确;
C.铅蓄电池放电时负极电极反应为,正极电极反应为,不符合题意,故C错误;
D.镍镉电池放电正极反应为,负极反应为,不符合题意,故D错误。
故选B。
4.【答案】
【解答】
A.镍氢电池、锂电池为二次电池,锌锰干电池为一次电池,故A错误;
B.氢氧燃料电池产物为,不污染环境,故B正确;
C.铅蓄电池放电的时候,被氧化,为原电池的负极,被还原,为原电池的正极,故C错误;
D.铅蓄电池充电时是将电能转化为化学能,故D错误;
故选B。
5.【答案】
【解答】
A.干电池是一次性电池,铅蓄电池是可充电电池属于二次电池,氢氧燃料电池属于燃料电池,故A正确;
B.在干电池中,作负极,被氧化,生成锌离子而被腐蚀,故B正确;
C.氢氧燃料电池不需要将还原剂和氧化剂全部储藏在电池内,且工作的最终产物是水,故氢氧燃料电池是一种具有应用前景的绿色电源,故C正确;
D.铅蓄电池工作过程中,硫酸铅在负极上析出,该极质量应该增加而非减小,故D错误。
6.【答案】
【解答】
A.原电池是化学能转化为电能,故A正确;
B.为正极,则电流由铜片通过导线流向锌片,故B正确;
C.发生与硫酸的电池反应,则为负极,为正极,锌片上发生的反应为,故C错误;
D.为正极,得到电子,发生还原反应,故D正确。
故选C。
7~9.【答案】D 、C 、C
10.【答案】
【解答】
铁粉、活性炭、无机盐等形成原电池反应,
A.铁为负极,被氧化生成,具有还原性,可制成小包装用于糕点的脱氧剂,故A正确;
B.铁与氧气、水形成原电池,之后发生系列反应,其中铁生锈的过程是放热反应,故B正确;
C.反应放热,不能降低温度,故C错误;
D.正极上氧气得电子被还原,电极方程式为,故D正确。
故选:。
11.【答案】
【解答】
A.在电极上失去电子发生氧化反应,为原电池的负极,故A正确;
B.电子流向为负极经外电路流向正极,即由经外电路流向,溶液中离子趋向负极,即电极,故B正确;
C.正极反应方程式为,故C错误;
D.消耗氧气转移电子,所以每转移电子,消耗氧气,标准状况下的体积为,故D正确。
故选C。
12.【答案】
【解答】
铅蓄电池中,总反应式,依据元素化合价变化可知:为负极,发生失去电子的氧化反应,电极反应式,为正极,发生得到电子的还原反应,电极反应式为,电池工作时,电子从负极沿导线流向正极,内电路中阳离子移向正极,阴离子移向负极,据此作答。
A.电池工作时,负极失去电子与结合生成,所以电极反应式为,故A错误;
B.铅蓄电池是可充电电池、是二次电池,放电时是化学能转化为电能,故B正确;
C.电池工作时,电子从负极沿导线流向正极,故C正确;
D.电池工作时,内电路中阳离子移向正极,阴离子移向负极,故D正确。
13.【答案】
【解答】
A.放电时,电极为,为负极,电极反应为,并且非水性体系中不存在氯离子,所以电极反应错误,故A项错误;
B.放电时,负极反应为,正极反应为,所以总反应为,电解质溶液中的物质的量减小,故B项错误;
C.充电时,电极为阳极,应与外接电源的正极相连,故C项错误;
D.充电时,电极为阳极,电极反应为,为阴极,电极反应为,电极和电极的质量均增加,故D项正确;
答案选D。
14.【答案】
【解答】
放电时,电极失电子,为负极,为正极。
A.放电时,阳离子移向正极,所以由左向右移动,故A错误;
B.充电时是电解池原理,阳极失去电子,电极反应式为,故B错误;
C.充电时,为阳极,应与外加电源的正极相连,但此电极上的物质失去电子,发生的是氧化反应,故C错误;
D.放电时,导线上每通过,左室中将溶解成为进入溶液,但同时将有从左室移入右室,减轻,故溶液质量只增重,故D正确。
故选D。
15.【答案】;阴极;;;
;
【解答】
碱性甲烷燃料电池中通入甲烷的一极为原电池的负极,负极上甲烷失电子发生氧化反应,电极反应式为,通入氧气的一极为原电池的正极,乙池为电解池,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时、两个电极的质量都不减少,连接原电池的正极,应为电解池的阳极,则应为石墨材料,电极反应式是,为阴极,电极材料是,电极反应式为,则乙池的总反应式为,
故答案为:;阴极;;;;
,根据可知转移电子为,甲池中通入氧气的一极为正极,反应式为,则消耗,;乙池中某一电极析出金属银时,由乙池的总反应式可知,产生氢离子的物质的量是,则其浓度是,
故答案为:;。
16.【答案】
紫色向方向移动
是;形成氢氧燃料电池;
【解答】
切断,闭合、通直流电,电极、及氢氧化钾溶液构成电解池,根据离子的放电顺序,溶液中氢离子、氢氧根离子放电,分别生成氢气和氧气,氢气和氧气的体积比为:,通过图象知,极上气体体积是极上气体体积的倍,所以极上得到氢气,极上得到氧气,所以极是阴极,极是阳极,故是负极,是正极;
故答案为:;
浸有硫酸钠的滤纸和电极、与电源也构成了电解池,因为是负极,是正极,所以是阴极,是阳极,电解质溶液中的阳离子钾离子向阴极移动,阴离子高锰酸根离子向阳极移动,所以极呈紫色;故答案为:紫色向方向移动;
通过图象知,极上气体体积是极上气体体积的倍,所以极上得到氢气,极上得到氧气,所以极是阴极,极是阳极,水溶液中氢氧根离子失电子生成氧气,电极反应为:;
故答案为:;
若电解一段时间,、中均有气体包围电极,切断、,闭合,此装置构成氢氧燃料原电池,所以有电流通过,电流表的指针移动,此时中的电极反应式为,中电极反应 ;
故答案为:是;形成氢氧燃料电池;。
17.【答案】 ;
; ;增加; ;增加; ;
【解答】
铝片和铜片插入稀溶液中,金属铜不反应,金属铝能和氢氧化钠失去电子的氧化还原反应,则金属为负极,电极反应为;
铝片和铜片插入浓溶液中,金属铝会钝化,金属铜和浓硝酸之间会发生氧化还原反应,则金属为负极,金属作正极,正极反应为;
铅蓄电池放电时,正极上二氧化铅得电子发生还原反应,正极电极反应式为,负极发生失去电子的氧化反应生成,电极反应式为,充电时,外加电源的负极与原电池的负极相接,原电池的负极作阴极,电极反应与原电池的负极相反,即充电时的阴极反应,该电池在工作时,电极为负极发生电极反应为:,生成的硫酸铅附着在电极上,电极的质量将增大,电池的总反应为,消耗硫酸转移电子,若该电池反应消耗了,则转移电子,数目为。
18.【答案】;
;
;
;
;;
。
【解答】
镁的原子结构示意图为,
故答案为:;
写出与水反应的化学方程式:,
故答案为:;
氢气是负极放电物质,电极反应式为,
故答案为:;
若能量转化率为,当参与电极反应时,转移电子数为,
故答案为:;
池中较活泼的金属是负极,则负极为;由于不与氢氧化钠溶液反应,则池中负极为:;
故答案为:;;
写出池中负极电极反应式:。
故答案为:。
19.【答案】
;
;
;
【解答】
为离子化合物,电子式为。
的结构式为,电子式为。
甲烷燃料电池中,负极为甲烷放电,碱性条件下转化为,电极反应为:;正极为放电,电极反应为:。
铅蓄电池充电时阴极发生还原反应,电极反应为:;
阳极发生氧化反应,电极反应为:。
第1页,共1页
一、单选题(本大题共14小题)
1. 电池是人类生产和生活中的重要能量来源,各式各样电池的发展是化学对人类的一大贡献。下列有关电池的叙述正确的是( )
A. 原电池反应均是自发的氧化还原反应
B. 氢氧燃料电池工作时氢气在正极被氧化
C. 氢氧燃料电池是将热能转化为电能的装置
D. 铅蓄电池在放电过程中,负极质量减少,正极质量增加
2. 如图所示是几种常见的化学电源示意图,有关说法正确的是( )
A. 上述电池分别属于一次电池、二次电池和燃料电池
B. 干电池工作时,向锌筒移动
C. 铅蓄电池工作过程中,每通过电子,负极质量减轻
D. 氢氧燃料电池的正极反应一定是
3. 下列电池工作时,在正极放电的是 ( )
A. B.
C. D.
4. 下列说法中正确的是( )
A. 镍氢电池、锂离子电池和锌锰干电池都是二次电池
B. 氢氧燃料电池是一种高效且不会污染环境的新型电池
C. 铅酸蓄电池放电的时候正极材料是铅,负极材料是二氧化铅
D. 铅酸蓄电池充电时将化学能转化为电能
5. 下面是几种常见的化学电源示意图,有关说法不正确的是相对原子质量:( )
A. 上述电池分别属于一次电池、二次电池和燃料电池
B. 干电池在长时间使用后,锌筒被破坏
C. 氢氧燃料电池是一种具有应用前景的绿色电源
D. 铅蓄电池工作过程中,每通过电子,负极质量减轻
6. 原电池原理的发现极大地推进了现代化的进程,改变了人们的生活方式。关于如图所示原电池的说法不正确的是( )
A. 该装置将化学能转化为电能
B. 电流由铜片经导线流向锌片
C. 锌片上的电极反应为:
D. 铜片为正极,发生还原反应
7. 下列设备工作时,将化学能转化为热能的是( )
A. B.
C. D.
8. 把锌片和铜片用导线连接后,浸入的盐酸溶液中,可能产生的结果是 ( )
A. 铜片上放出氯气 B. 铜片上放出氧气 C. 铜片上放出氢气 D. 铜片上放出氮气
9. 下列有关化学电源叙述正确的是( )
A. 水果电池是高效环保的家用电池
B. 锌锰干电池是一种常用的二次电池
C. 锌锰干电池工作一段时间后锌外壳逐渐变薄
D. 锌锰干电池碳棒是负极
10. 某化学兴趣小组学习原电池知识后,决定用其原理,尝试利用铁粉、活性炭、无机盐等物质开发产品。小组提出的设想或对原理的理解不正确的是( )
A. 打算制成小包装用于糕点的脱氧剂
B. 利用反应放出热量的原理制成暖宝宝
C. 调整电池结构,可降低温度,可用于延长糕点保质期
D. 正极的电极反应为:
11. 氨氧燃料电池具有很大的发展潜力。下图为某氨氧燃料电池示意图,下列说法错误的是 ( )
A. 电极为该电池的负极
B. 电子流向为电极经外电路流向电极,溶液中离子趋向电极
C. 该电池正极反应为:
D. 每转移电子,消耗标准状况下的氧气体积为
12. 铅蓄电池是一种典型的可充电电池,其放电时的电池总反应式:。则下列说法不正确的是( )
A. 电池工作时,负极反应:
B. 铅蓄电池是二次电池,放电时是化学能转化为电能
C. 电池工作时,电子由板通过导线流向板
D. 电池工作时,溶液中移向板
13. 非水性嵌入铝电池是一种二次电池,该电池放电过程的示意图如图所示表示某有机阳离子。充电时阳极的电极反应为。下列说法正确的是( )
A. 放电时,电极的电极反应为
B. 放电时,电解质中的物质的量基本不变
C. 充电时,电极应与外接电源负极相连
D. 充电时,电极和电极的质量均增加
14. 镁锂双离子新型二次电池如图所示,下列关于该电池的说法正确的是( )
A. 放电时,作负极,溶液中由右向左移动
B. 充电时,阳极的电极反应式为
C. 充电时,应与外加电源的正极相连,此电极上的物质发生了还原反应
D. 放电时,导线上每通过,左室溶液质量增重
二、填空题(本大题共5小题)
15. 如图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时,、两个电极的质量都不减少,请回答下列问题:
电极的材料是______,其电极名称是_______, 的电极反应式为_______,乙池的总反应是___,加入甲烷的铂电极的电极反应式为 ________________。
在此过程中,乙池中某一电极析出金属银时,甲池中理论上消耗氧气为 _____标准状况下,若此时乙池溶液的体积为,则乙池中溶液的的浓度为 _________________。
16. 如图装置,、中的电极为多孔的惰性电极;、为夹在湿的滤纸条上的铂夹;电源有、两极。若、中充满溶液后倒立于溶液的水槽中。切断,闭合、通直流电,回答下列问题:
电源的负极为________极填或
在湿的 溶液滤纸条中心的液滴,有什么现象:___________________________________________
写出极电极反应式:______________________________________________________
若电解一段时间后,、中均有气体包围电极。此时切断、,闭合,则电流表的指针是否移动填“是”或“否”________ ,说明理由:__________________写出此时极的电极反应式:__________________________。
17. 将片和片用导线连接,一组插入浓硝酸中,一组插入稀溶液中,分别形成原电池。
写出插入稀溶液中形成原电池的负极反应____________________________________。
写出插入浓硝酸中形成原电池的正极反应__________________________________________。
铅蓄电池是最常见的二次电池,工作时的总反应为。由于其电压稳定、使用方便、安全可靠、价格低廉,所以在生产、生活中使用广泛,写出铅蓄电池放电时的正极反应________________________________________________________;充电时的阴极反应________________________________________________________。该电池在工作时,电极的质量将________填“增加”“减小”或“不变”,若该电池反应消耗了,则转移电子的数目为________________。
18. 镁、铝是重要的金属,回答下列问题:
镁的原子结构示意图为________________。
是一种重要的储氢材料,其与水反应放出氢气,将反应生成的氢气与氧气设计成氢氧燃料电池如下图。
写出与水反应的化学方程式:________________________________。
负极电极反应式为________________________________。
若中反应生成,且能量转化率为,则导线中通过电子的物质的量为________。
某同学在实验室设计了如图所示的原电池:
池中负极为:________填化学式,下同,池中负极为:________。
写出池中负极电极反应式:________________________________。
19. 写出的电子式:_________,
写出的电子式和结构式:_________,_________,
写出甲烷燃料电池在碱性条件下的电极反应式.
负极:_______________________
正极:_______________________
写出铅蓄电池充电时的电极反应式.
阴极:______________________
阳极:______________________
答案和解析
1.【答案】
【解答】
A.构成原电池的条件之一是:能自发的进行氧化还原反应,所以原电池反应均是自发的氧化还原反应,故A正确;
B.氢氧燃料电池工作时氢气在负极上失电子被氧化,故B错误;
C.氢氧燃料电池也是原电池,所以氢氧燃料电池是将化学能转变为电能的装置,故C错误;
D.根据铅蓄电池放电时,负极电极反应式为:;正极电极反应式为:,所以正负极质量都增加,故D错误。
故选A。
2.【答案】
【解答】
A.干电池是一次性电池,铅蓄电池是可充电电池属于二次电池,氢氧燃料电池属于燃料电池,故A正确;
B.在干电池中,作负极,向正极碳棒移动,故B错误;
C.铅蓄电池工作过程中,硫酸铅在负极上析出,该极质量应该增加而非减小,故C错误;
D.氢氧燃料电池的正极反应受溶液的酸碱性影响,则电极反应式不一定是 ,故D错误。
故选A。
3.【答案】
【解答】
A.锌锰干电池中电极反应式:负极:,正极:,不符合题意,故A错误;
B.酸性氢氧燃料电池电极反应式为、;碱性氢氧燃料电池电极反应式为、,符合题意,故B正确;
C.铅蓄电池放电时负极电极反应为,正极电极反应为,不符合题意,故C错误;
D.镍镉电池放电正极反应为,负极反应为,不符合题意,故D错误。
故选B。
4.【答案】
【解答】
A.镍氢电池、锂电池为二次电池,锌锰干电池为一次电池,故A错误;
B.氢氧燃料电池产物为,不污染环境,故B正确;
C.铅蓄电池放电的时候,被氧化,为原电池的负极,被还原,为原电池的正极,故C错误;
D.铅蓄电池充电时是将电能转化为化学能,故D错误;
故选B。
5.【答案】
【解答】
A.干电池是一次性电池,铅蓄电池是可充电电池属于二次电池,氢氧燃料电池属于燃料电池,故A正确;
B.在干电池中,作负极,被氧化,生成锌离子而被腐蚀,故B正确;
C.氢氧燃料电池不需要将还原剂和氧化剂全部储藏在电池内,且工作的最终产物是水,故氢氧燃料电池是一种具有应用前景的绿色电源,故C正确;
D.铅蓄电池工作过程中,硫酸铅在负极上析出,该极质量应该增加而非减小,故D错误。
6.【答案】
【解答】
A.原电池是化学能转化为电能,故A正确;
B.为正极,则电流由铜片通过导线流向锌片,故B正确;
C.发生与硫酸的电池反应,则为负极,为正极,锌片上发生的反应为,故C错误;
D.为正极,得到电子,发生还原反应,故D正确。
故选C。
7~9.【答案】D 、C 、C
10.【答案】
【解答】
铁粉、活性炭、无机盐等形成原电池反应,
A.铁为负极,被氧化生成,具有还原性,可制成小包装用于糕点的脱氧剂,故A正确;
B.铁与氧气、水形成原电池,之后发生系列反应,其中铁生锈的过程是放热反应,故B正确;
C.反应放热,不能降低温度,故C错误;
D.正极上氧气得电子被还原,电极方程式为,故D正确。
故选:。
11.【答案】
【解答】
A.在电极上失去电子发生氧化反应,为原电池的负极,故A正确;
B.电子流向为负极经外电路流向正极,即由经外电路流向,溶液中离子趋向负极,即电极,故B正确;
C.正极反应方程式为,故C错误;
D.消耗氧气转移电子,所以每转移电子,消耗氧气,标准状况下的体积为,故D正确。
故选C。
12.【答案】
【解答】
铅蓄电池中,总反应式,依据元素化合价变化可知:为负极,发生失去电子的氧化反应,电极反应式,为正极,发生得到电子的还原反应,电极反应式为,电池工作时,电子从负极沿导线流向正极,内电路中阳离子移向正极,阴离子移向负极,据此作答。
A.电池工作时,负极失去电子与结合生成,所以电极反应式为,故A错误;
B.铅蓄电池是可充电电池、是二次电池,放电时是化学能转化为电能,故B正确;
C.电池工作时,电子从负极沿导线流向正极,故C正确;
D.电池工作时,内电路中阳离子移向正极,阴离子移向负极,故D正确。
13.【答案】
【解答】
A.放电时,电极为,为负极,电极反应为,并且非水性体系中不存在氯离子,所以电极反应错误,故A项错误;
B.放电时,负极反应为,正极反应为,所以总反应为,电解质溶液中的物质的量减小,故B项错误;
C.充电时,电极为阳极,应与外接电源的正极相连,故C项错误;
D.充电时,电极为阳极,电极反应为,为阴极,电极反应为,电极和电极的质量均增加,故D项正确;
答案选D。
14.【答案】
【解答】
放电时,电极失电子,为负极,为正极。
A.放电时,阳离子移向正极,所以由左向右移动,故A错误;
B.充电时是电解池原理,阳极失去电子,电极反应式为,故B错误;
C.充电时,为阳极,应与外加电源的正极相连,但此电极上的物质失去电子,发生的是氧化反应,故C错误;
D.放电时,导线上每通过,左室中将溶解成为进入溶液,但同时将有从左室移入右室,减轻,故溶液质量只增重,故D正确。
故选D。
15.【答案】;阴极;;;
;
【解答】
碱性甲烷燃料电池中通入甲烷的一极为原电池的负极,负极上甲烷失电子发生氧化反应,电极反应式为,通入氧气的一极为原电池的正极,乙池为电解池,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时、两个电极的质量都不减少,连接原电池的正极,应为电解池的阳极,则应为石墨材料,电极反应式是,为阴极,电极材料是,电极反应式为,则乙池的总反应式为,
故答案为:;阴极;;;;
,根据可知转移电子为,甲池中通入氧气的一极为正极,反应式为,则消耗,;乙池中某一电极析出金属银时,由乙池的总反应式可知,产生氢离子的物质的量是,则其浓度是,
故答案为:;。
16.【答案】
紫色向方向移动
是;形成氢氧燃料电池;
【解答】
切断,闭合、通直流电,电极、及氢氧化钾溶液构成电解池,根据离子的放电顺序,溶液中氢离子、氢氧根离子放电,分别生成氢气和氧气,氢气和氧气的体积比为:,通过图象知,极上气体体积是极上气体体积的倍,所以极上得到氢气,极上得到氧气,所以极是阴极,极是阳极,故是负极,是正极;
故答案为:;
浸有硫酸钠的滤纸和电极、与电源也构成了电解池,因为是负极,是正极,所以是阴极,是阳极,电解质溶液中的阳离子钾离子向阴极移动,阴离子高锰酸根离子向阳极移动,所以极呈紫色;故答案为:紫色向方向移动;
通过图象知,极上气体体积是极上气体体积的倍,所以极上得到氢气,极上得到氧气,所以极是阴极,极是阳极,水溶液中氢氧根离子失电子生成氧气,电极反应为:;
故答案为:;
若电解一段时间,、中均有气体包围电极,切断、,闭合,此装置构成氢氧燃料原电池,所以有电流通过,电流表的指针移动,此时中的电极反应式为,中电极反应 ;
故答案为:是;形成氢氧燃料电池;。
17.【答案】 ;
; ;增加; ;增加; ;
【解答】
铝片和铜片插入稀溶液中,金属铜不反应,金属铝能和氢氧化钠失去电子的氧化还原反应,则金属为负极,电极反应为;
铝片和铜片插入浓溶液中,金属铝会钝化,金属铜和浓硝酸之间会发生氧化还原反应,则金属为负极,金属作正极,正极反应为;
铅蓄电池放电时,正极上二氧化铅得电子发生还原反应,正极电极反应式为,负极发生失去电子的氧化反应生成,电极反应式为,充电时,外加电源的负极与原电池的负极相接,原电池的负极作阴极,电极反应与原电池的负极相反,即充电时的阴极反应,该电池在工作时,电极为负极发生电极反应为:,生成的硫酸铅附着在电极上,电极的质量将增大,电池的总反应为,消耗硫酸转移电子,若该电池反应消耗了,则转移电子,数目为。
18.【答案】;
;
;
;
;;
。
【解答】
镁的原子结构示意图为,
故答案为:;
写出与水反应的化学方程式:,
故答案为:;
氢气是负极放电物质,电极反应式为,
故答案为:;
若能量转化率为,当参与电极反应时,转移电子数为,
故答案为:;
池中较活泼的金属是负极,则负极为;由于不与氢氧化钠溶液反应,则池中负极为:;
故答案为:;;
写出池中负极电极反应式:。
故答案为:。
19.【答案】
;
;
;
【解答】
为离子化合物,电子式为。
的结构式为,电子式为。
甲烷燃料电池中,负极为甲烷放电,碱性条件下转化为,电极反应为:;正极为放电,电极反应为:。
铅蓄电池充电时阴极发生还原反应,电极反应为:;
阳极发生氧化反应,电极反应为:。
第1页,共1页
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
