浙江省温州市鹿城区2023年初中毕业生升学适应性测试科学试卷(word版,含答案)
文档属性
| 名称 | 浙江省温州市鹿城区2023年初中毕业生升学适应性测试科学试卷(word版,含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-04-03 00:00:00 | ||
图片预览



文档简介
鹿城区2023年初中毕业生升学适应性测试
科学试题卷
欢迎参加考试!请你认真审题,积极思考,细心答题,发挥最佳水平。答题时,请注意以几点:
1.全卷共8页,有四大题,32小题。全卷满分180分。考试时间120分钟。
2.答案必须写在答题卷相应的位置上,写在试题卷、草稿纸上均无效。
3.答题前,认真阅读答题卷上的《注意事项》,按规定答题。
4.本卷可能用到的相对原子质量: H-1 C-12 N-14 O-16 Na-23 Cl- -35.5
5.g取10牛/千克。祝你成功!
试题卷I
一、选择题(本题有15小题,每小题4分,共60分。每小题只有一个选项是正确的,不选、多选、错选均不给分)
1.温州城区坐落于温瑞平原,被瓯江、楠溪江等分割成几块(如图所示),向内纵深地区湖荡连绵。形成这种地形的外力作用主要是()
A.冰川 B.流水 C.风力 D.生物
2. 2022年秋,为了缓解旱情温州曾发射碘化银(AgI)炮弹生成凝结核实施人工降雨,其反应化学方程式为: 2AgI=2Ag+I, 该反应属于()
A.分解反应 B.化合反应 C.复分解反应 D. 置换反应
3. 如图,农场工人在分离谷粒与空壳时,使用铁锹将混合物以相同角度同时抛酒出去,落地时谷粒远而空壳近,实现二者分离。此过程中()
A.谷粒有惯性、空壳无惯性 B.谷粒和空壳均有惯性
C.谷粒无惯性、空壳有惯性 D.谷粒和空壳均无惯性
温州“屏纸”被称为中国古代造纸术的“活化石”。下图是生产。“屏纸”过程中的几个重要工序。根据信息回答第4至第6小题。
4.温州“屏纸”常以竹子作为原材料,下列不是选择竹子作为“屏纸”原料的理由是()
A.竹子的生长周期短种植成材快 B.竹子中富含纸张的主要成分纤维素
C.温州的气候特征适合竹子生长 D.用竹子造纸可以传承古代竹简文化
5. “捞纸”工序是利用竹帘将纸浆中的竹纤维与水分离,其原理类似于物质分离中的()
A.结晶 B.过滤 C.蒸馏 D.沉淀
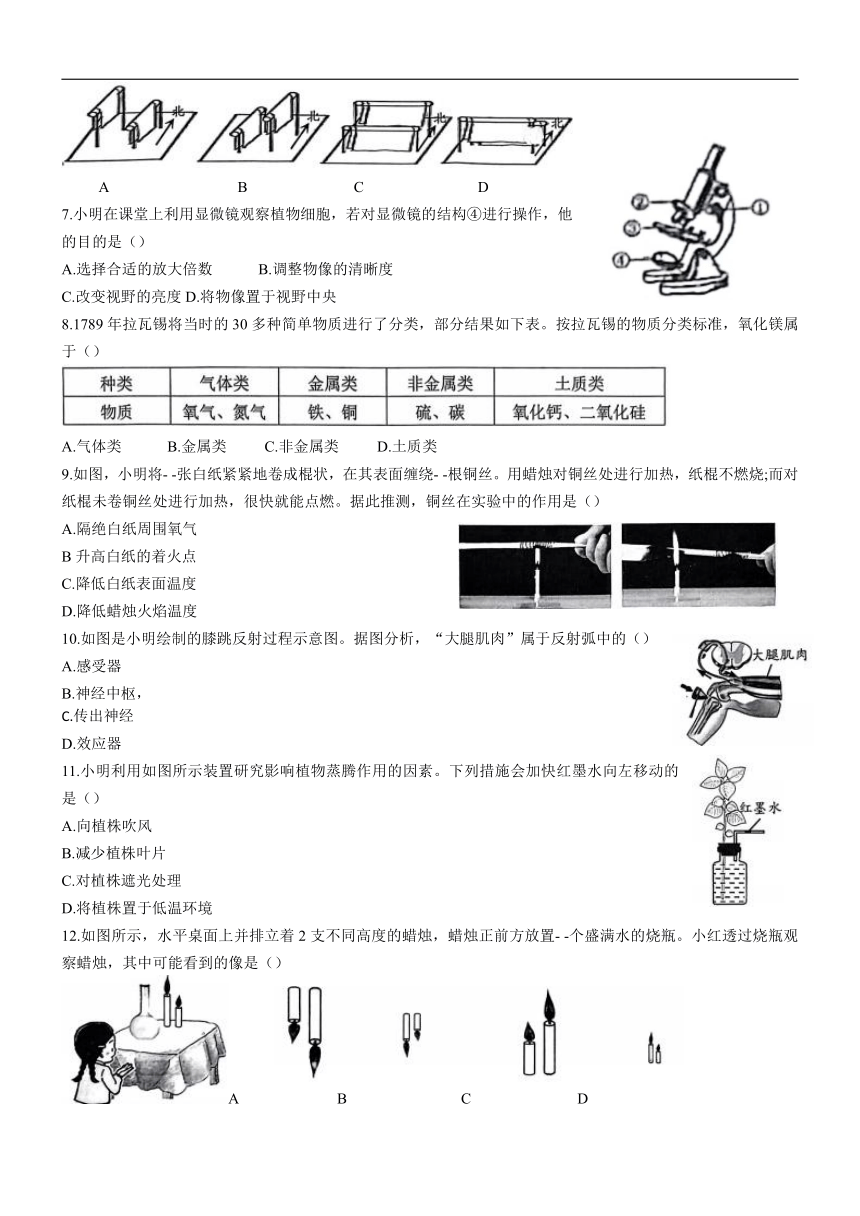
6.“晒纸”是将刚生产的湿纸,通过自然蒸发使纸张变千。若无风情况下在同一地点为了更快完成晒纸工序,下列晾晒方式最合理的是()
A B C D
7.小明在课堂上利用显微镜观察植物细胞,若对显微镜的结构④进行操作,他的目的是()
A.选择合适的放大倍数 B.调整物像的清晰度
C.改变视野的亮度D.将物像置于视野中央
8.1789年拉瓦锡将当时的30多种简单物质进行了分类,部分结果如下表。按拉瓦锡的物质分类标准,氧化镁属于()
A.气体类 B.金属类 C.非金属类 D.土质类
9.如图,小明将- -张白纸紧紧地卷成棍状,在其表面缠绕- -根铜丝。用蜡烛对铜丝处进行加热,纸棍不燃烧;而对纸棍未卷铜丝处进行加热,很快就能点燃。据此推测,铜丝在实验中的作用是()
A.隔绝白纸周围氧气
B升高白纸的着火点
C.降低白纸表面温度
D.降低蜡烛火焰温度
10.如图是小明绘制的膝跳反射过程示意图。据图分析,“大腿肌肉”属于反射弧中的()
A.感受器
B.神经中枢,
C.传出神经
D.效应器
11.小明利用如图所示装置研究影响植物蒸腾作用的因素。下列措施会加快红墨水向左移动的是()
A.向植株吹风
B.减少植株叶片
C.对植株遮光处理
D.将植株置于低温环境
12.如图所示,水平桌面上并排立着2支不同高度的蜡烛,蜡烛正前方放置- -个盛满水的烧瓶。小红透过烧瓶观察蜡烛,其中可能看到的像是()
A B C D
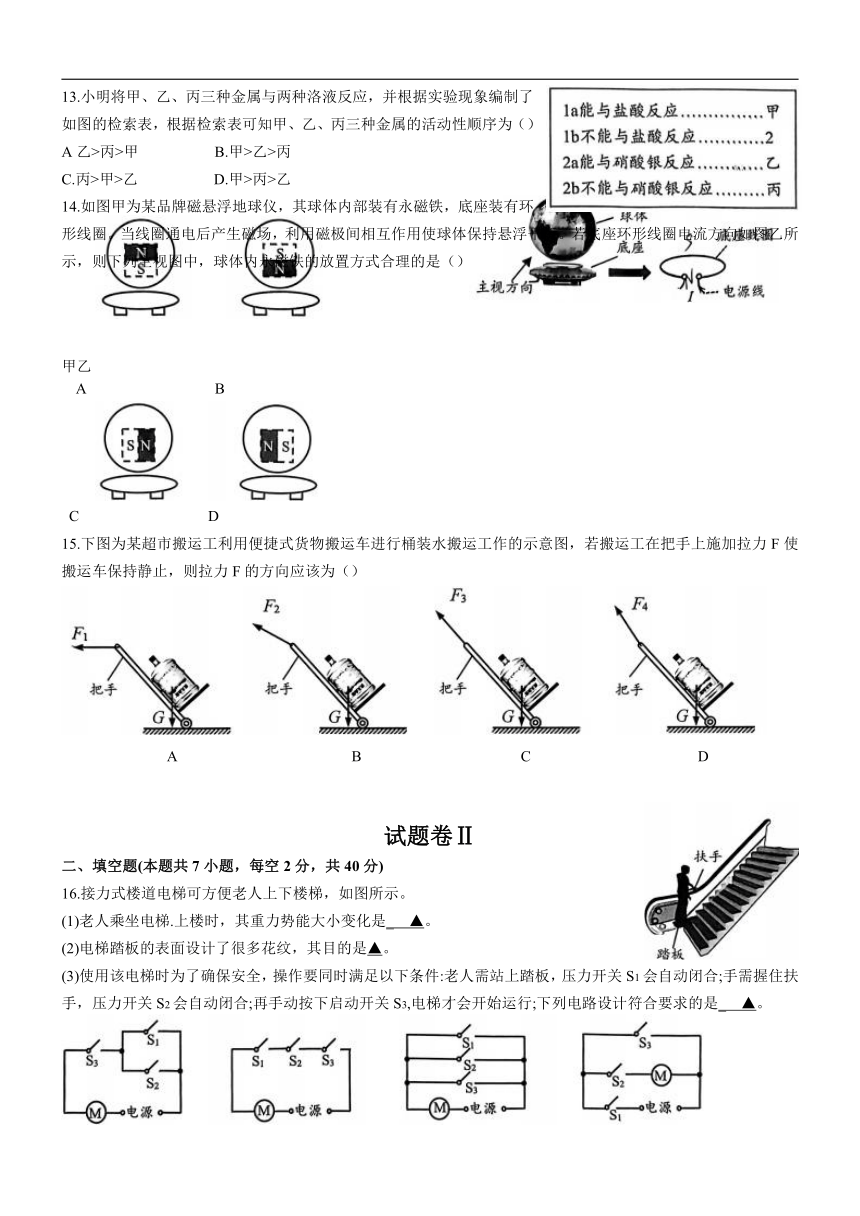
13.小明将甲、乙、丙三种金属与两种洛液反应,并根据实验现象编制了如图的检索表,根据检索表可知甲、乙、丙三种金属的活动性顺序为()
A乙>丙>甲 B.甲>乙>丙
C.丙>甲>乙 D.甲>丙>乙
14.如图甲为某品牌磁悬浮地球仪,其球体内部装有永磁铁,底座装有环形线圈。当线圈通电后产生磁场,利用磁极间相互作用使球体保持悬浮平衡。若底座环形线圈电流方向如图乙所示,则下列主视图中,球体内永磁铁的放置方式合理的是()
甲乙
A B
C D
15.下图为某超市搬运工利用便捷式货物搬运车进行桶装水搬运工作的示意图,若搬运工在把手上施加拉力F使搬运车保持静止,则拉力F的方向应该为()
A B C D
试题卷Ⅱ
二、填空题(本题共7小题,每空2分,共40分)
16.接力式楼道电梯可方便老人上下楼梯,如图所示。
(1)老人乘坐电梯.上楼时,其重力势能大小变化是_ ▲。
(2)电梯踏板的表面设计了很多花纹,其目的是▲。
(3)使用该电梯时为了确保安全,操作要同时满足以下条件:老人需站上踏板,压力开关S1会自动闭合;手需握住扶手,压力开关S2会自动闭合;再手动按下启动开关S3,电梯才会开始运行;下列电路设计符合要求的是_ ▲。
A B C D
17.小明同学在实验室利用粗盐提纯所制取的精盐,配制50克溶质质量分数为5%的氯化钠溶液。
(1)粗盐提纯的主要步骤为溶解、过滤、蒸发。为加快粗盐溶解,可采取的措施为▲。(列举一点)
(2)为完成氯化钠溶液配制,需称量食盐▲。
(3)配制所得的氯化钠溶液中,各元素质量分数如图所示,图中①所代表的元素是
▲。
18.鱼菜共生是一种新型的复合耕作体系,它能实现养鱼不换水、种菜不施肥的生态共生效应。装置原理如右图所示,由养殖区、种植区、转化槽组成,转化槽中细菌能将有机物转化为无机盐。整个装置通过水泵实现系统内的水循环。
(1)从生态系统的成分看,转化槽中的细菌属于▲。
(2)该系统利用水泵将养殖区中的水送入种植区中,水泵每小时做功36000J,则水泵的功率至少为▲瓦。
(3)减少草鱼的投放量有利于黑鱼的生长,请利用生态系统的知识解释其原因▲。
19.建立模型能帮助我们认识自然现象。如图是学生利用模型讨论温州地区冬寒夏热的问题。
甲乙丙
(1)图甲是太阳内部释放能量过程的模型图,该变化属于▲。(选填“核聚变”或“核裂变”)
(2)小明认为温州冬寒夏热是地球在夏季距离太阳较近。请从图乙中找出否定他观点的证据:▲。
(3,小红用图丙模型解释冬寒夏热,认为夏季正午时地面单位面积接受到的太阳能比冬季多,这是因为地球以一个倾斜的角度绕太阳公转,造成夏季和冬季的▲不同而导致的。
20.甲流是由甲型流感病毒引起的,多在春秋季节爆发的病毒性流行感冒。
(1)甲流爆发时其病毒会产生不同的类型,这是由于病毒会发生▲。
(2)医生建议人们每年要接种最新甲流疫苗,从传染病的预防措施来看,其属于▲。
(3)新鲜大蒜中含有蒜氨酸,当大蒜被切开后,蒜氨酸会生成大蒜素。大蒜素具有较强的抗病毒作用,能溶于酸性溶液,遇热很快失效。大蒜作为调味品,主要有以下几种食用方法:
①鹏大蒜与食物-起煮熟后食用②将生蒜切碎泡醋,食用大蒜醋③将大蒜切片生吃
若人们想食用大蒜预防甲流,请选择-一个你支持的食用方法并说明理由:▲。
21.我国研发出了一种新型水陆两栖飞行器一“同济飞鱼”(如图甲所示),它既能在空中飞行,也能在水中畅游。
(1)两栖飞行器在水中通过螺旋桨转动向后划水即可实现向前航行,其原理是▲。
(2)两栖飞行器装有深度计,图乙是其工作电路,压力传感器的电阻随压力的增大而减小。闭合开关,飞行器在深海下潜过程中显示器示数大小变化是▲。
(3)两栖飞行器还自带声波测距仪,某次飞行器悬停空中向障碍物发射声波,从发出声波至接收到反射回来的声波共用时2秒,若声波的速度为340米/秒,则飞行器离障碍物的距离是▲米。
22.科学家对元素的相对原子质量的认识经历了漫长的时间。
材料一: 19世纪初,有化学家认为:氢是母体,其他元素原子的相对原子质量理论上都是氢的整数倍,少数元素如Cl是35.5倍,则是由于实验误差造成的。
材料二: 1886年, 英国科学家克鲁克斯大胆假设:同一元素的原子,可以有不同的相对原子质量。化学家测定出的元素相对原子质量是其不同原子相对原子质量的平均值。
材料三: 1961年8月,国际上采用"C的1/12作为相对原子质量的标准,确定各个同位素原子的相对原子质量。某元素的相对原子质量是其各种同位素原子的相对原子质量乘以各自在该元素中所占的百分比之和。
(1)在克鲁克斯假设中,同种元素的原子,相对原子质最却不同,是因为原子结构中的某种微粒数不同,该微粒的名称是▲。
(2)结合已学知识和上述材料分析,下列说法正确的▲。(可多选 )
A.实验结果与预测有偏差时,可以忽略当作实验误差处理。
B.某元素的相对原子质量一定大于它所有的同位素原子的相对原子质量
C.自然界中大部分元素都有同位素原子,由此推测大部分元素的相对原子质量不是整数。
D. CI 的相对原子质量是35.5,其自然界仅有的两种同位素原子中,35Cl 所占的百分比大于37C1。
E.在化学变化中某金属原子失去电子与其他原子化合,计算该化合物相对分子质量时仍能使用该金属元素原来的相对原子质量。
三、实验探究题(本题有4小题,第26 (1)题6分,其余每空3分,共36分)题,每空3分,共36分)
23.开封后的牛奶放置- - 段时间后还能喝吗 小红查阅资料发现牛奶中的乳酸含量在0.12%-0.18%时为正常,超过0.18%为变质。为探究开封后牛奶变质的影响因素,小红进行如下实验:
①取甲、乙两瓶牛奶,打开。
②将甲瓶牛奶放置在20℃的恒温箱中,将乙瓶牛奶放置在4℃的恒温箱中。
③每隔8小时同时从甲乙两瓶牛奶中取样,并测量取样样品中的乳酸含量。
部分数据如表所示:
(1)写出步骤①中需要控制相同的- -种因素:▲。
(2)本实验中除了测量乳酸含量的仪器外,还需要用到的测量工具有▲。(写出两种)
(3)开封后放置一段时间的牛奶到底能不能喝 请结合探究结果,提出建议并说明理由。▲。
24.为了探究氯酸钾制取氧气时,生成氧气的速度与加入二氧化锰的质量有怎样的关系 小明用图甲装置开展实验。步骤如下:
①检查装置气密性,在500毫升集气瓶中装满水;
②取20克氯酸钾平均分成10份,分别装入10支试管中,分别记为①- D组,往10支试管中分别装入0.1克、0.2克、0.3克、0.4克、0.5克、0.65克、 1克、1.3克、2克、3克二氧化锰,并混合均匀;
③将10支试管分别加热,记录生成300毫升氧气所需时间,计算生成氧气的速度如图乙。
甲乙
(1)和向下排空气法相比,本实验中用排水法收集氧气的优点是▲。
(2)分析实验数据,得出的初步结论是▲。
(3) 4克氯酸钾和1. 3克二氧化锰混合均匀加热,据图推测,收集300亳升氧气所需要的时间约为▲秒。
25.为了探究影响导体电阻大小的因素,小明将长度均为6厘米且横截面积相同、粗细均匀的两种金属丝AB和金属丝BC对接相连,并按图甲连接电路,电源电压为12伏。他进行了如下实验。
甲乙丙
①将导线a一端与电压表正接线柱相连,另--端滑片P与金属丝接触良好并能沿金属丝左右滑动。
②闭合开关,将导线a的滑片P从金属丝AB的左端A点缓慢向右移动,一直移到金属丝BC的右端C点,记录并绘制电压表示数随AP长度l的变化关系如图乙。
(1)步骤②中某次电压表示数如图丙所示,此时金属丝AP两端电压为▲伏。
(2)实验完成后,小明得出结论:粗细均匀的同种导体,其电阻与长度成正比;长度和粗细相同的不同导体电阻不同。请利用电学相关知识并结合图乙说明小明得出结论的理由:▲。
(3)小明利用图甲装置进行另- -次实验,将滑片P固定在B处,将导线b的上端从C点缓慢向A点方向移动距离I'为10厘米,请画出在移动过程中电压表示数U随I'的变化关系图像。▲
26.小明想在家中测量食盐的密度,现有电子秤、玻璃杯2个、勺子、滴管、记号笔、足量的清水和食盐。
(1)请你帮助小明写出实验步骤完成测量(测量的各量用字母表示,清水的密度为ρ0)。▲
(2)转换法是实验中常用的方法,请在教材的实验里举- -例并写出转换法中相对应的量。▲
四、解答题(本题有6小题,第27题6分,第28题6分,第29题7分,第30题6分,第31题9分,第32题10分,共44分)
27.香蕉外皮易变黑变质,储存时间较短。资料显示:香蕉皮易变黑与其细胞内酚类物质和多酚氧化酶有关,其分布如图所示;若香蕉外皮细胞破裂,酚类物质与多酚氧化酶混合,会发生反应:酚类+氧气多酚氧化酶,黑色物质,导致外皮变黑。
(1)人食用香蕉后,其消化吸收的主要器官为▲。
(2)图中的液泡膜能控制液泡内酚类物质不进入细胞中的其他部位,与此具有类似功能的细胞结构是▲。
(3)为防止香蕉皮变黑腐烂,可以利用保鲜膜包裹香蕉或悬挂香蕉这些小妙招来延长保鲜时间。请你结合材料与知识,分析其中一种保鲜方法的科学原理。▲。
28.小明实验时发现:向盛有碳酸钠溶液的试管中滴加几滴稀盐酸时,并没有预想的气泡生成。是原溶液中没有碳酸根离子还是另有奧秘 于是他利用图甲装置进行如下实验。
实验一:在空的广口瓶中加入10克稀盐酸溶液,用注射器向瓶中缓慢注入足量碳酸钠溶液,测得产生二氧化碳气体情况如图乙所示。
实验二:试剂和装置都不变,在空的广口瓶中加入10.6 克碳酸钠溶液,用注射器向瓶中缓慢注入足量的稀盐酸溶液,测得产生二氧化碳气体情况如图丙所示。
甲乙丙
(1)请用化学方程式表示实验-一中广口瓶内发生的化学反应:▲。
(2)实验中能否定“原溶液内没有碳酸钙离子”的证据是▲。
(3)在实验一-和实验二中,最终产生的二氧化碳的质量相同的原因是▲。
29.科学课上,同学们开展“制作呼吸模型”项目化学习,下表为模型的评价量表。
某小组利用吸管、木板、气球和铁丝等材料制作模型,用保鲜膜将整个装置包住形成一一个密闭环境,如图甲所示。
(1)图甲模型中气球模拟的人体器官是▲。
(2)若要用该模型演示吸气过程,则同学对铁丝的操作为▲。
(3)根据评价量表,该模型的指标一-被评为优秀,指标二为合格,为使该模型能更好的体现人体结构特征,结合图乙请选择合适的材料对该模型进行改进:▲。(写出两点)
30.在生活中可以利用一碗水来鉴别鸡蛋的新鲜程度。
资料一:鸡蛋放置时间越久,越不新鲜,不同新鲜程度的鸡蛋在水中的浮沉情况如图甲。
甲乙
资料二:用放大镜观察鸡蛋外壳,发现鸡蛋壳表面布满一一个个气孔,如图乙所示。
资料三:鸡蛋在放置过程中,体积不会发生变化。
请结合.上述资料并综合运用所学知识,对“不同新鲜程度鸡蛋在水中的浮沉情况”进行解释。
31.吸氢能作为治疗一些疾病的辅助手段。如图甲是一款家用氢气发生器,裝置可以稳定提供纯净氢气,其工作原理如图乙所示。在水箱中加入蒸馏水,电解槽内的水电解(2H2O=通电=2H2↑+O2↑), 产生的氧气和.氢气分别从氧气出口和氢气出口排出。
(1)限压阀可以控制内部气压大小,当气压达到设定值时,限压阀打开,让气体排出。若要实现电解速度过大时两个限压阀同时排气,图乙中两限压阀的设定值PA和Pp的大小关系应为▲。
(2)氢气发生器要定时补充水,水箱水位最高时体积为1800毫升,水位最低时体积为900毫升。若产生氢气的速度为25克时,请计算一次充满水,能供应氢气多少小时
(3)根据装置原理图,推测装置C的作用是▲。
32.校本课程《陶艺》课上,烧制不同的陶、瓷作品需要不同的温度。为了能满足上述要求小明设计了一个电热式烧制炉的电路模型(如图甲所示)。工作电路: S1 为电源开关; S2为衔铁的同步开关( 电磁继电器吸下衔铁时S2同时断开) ;烧制炉的加热元件由阻值为48.4欧的R1和阻值为193.6欧的R2两个发热电阻组成。闭合S1和S2,烧制炉开始工作,先高功率升温,后保温期间能自动实现高功率、低功率两档切换。控制电路:烧制炉利用温差电源控制炉内温度达成恒温烧制。温差电源的热点(T1 点)放在炉中,冷点(T2点)放在低温恒温箱中,其提供的电压与T1、T2两点间的温度差关系如图乙所示。当温差电源使电磁继电器的电流达到0.015A时,电磁铁恰好能将弹性衔铁吸下,同时S2断开;一段时间后,温度降到预设值以下,释放弹性衔铁,同时S2闭合;如此反复,直至恒温烧制结束。
甲乙丙
(1)当S1和S2刚闭合时,工作电路中的两电阻的工作状态是▲。
A.仅R1工作 B.R1与R2串联工作
C.仅R2工作 D.R1与R2并联工作
(2)烧制炉烧制某陶瓷作品时,工作电路的高功率和低功率随时间变化如图丙所示,则烧制炉完成本次工作消耗的电能共为多少
(3)控制电路通过改变R0接入电路的阻值,实现改变烧制炉内的烧制温度。若控制电路中电磁继电器的线圈阻值为0.5欧,温差电源的冷点温度恒为20℃,现要烧制骨瓷作品需将炉内温度控制为1220℃,则需移动R0上的滑片使其接入电路的阻值为▲欧。
科学试题卷
欢迎参加考试!请你认真审题,积极思考,细心答题,发挥最佳水平。答题时,请注意以几点:
1.全卷共8页,有四大题,32小题。全卷满分180分。考试时间120分钟。
2.答案必须写在答题卷相应的位置上,写在试题卷、草稿纸上均无效。
3.答题前,认真阅读答题卷上的《注意事项》,按规定答题。
4.本卷可能用到的相对原子质量: H-1 C-12 N-14 O-16 Na-23 Cl- -35.5
5.g取10牛/千克。祝你成功!
试题卷I
一、选择题(本题有15小题,每小题4分,共60分。每小题只有一个选项是正确的,不选、多选、错选均不给分)
1.温州城区坐落于温瑞平原,被瓯江、楠溪江等分割成几块(如图所示),向内纵深地区湖荡连绵。形成这种地形的外力作用主要是()
A.冰川 B.流水 C.风力 D.生物
2. 2022年秋,为了缓解旱情温州曾发射碘化银(AgI)炮弹生成凝结核实施人工降雨,其反应化学方程式为: 2AgI=2Ag+I, 该反应属于()
A.分解反应 B.化合反应 C.复分解反应 D. 置换反应
3. 如图,农场工人在分离谷粒与空壳时,使用铁锹将混合物以相同角度同时抛酒出去,落地时谷粒远而空壳近,实现二者分离。此过程中()
A.谷粒有惯性、空壳无惯性 B.谷粒和空壳均有惯性
C.谷粒无惯性、空壳有惯性 D.谷粒和空壳均无惯性
温州“屏纸”被称为中国古代造纸术的“活化石”。下图是生产。“屏纸”过程中的几个重要工序。根据信息回答第4至第6小题。
4.温州“屏纸”常以竹子作为原材料,下列不是选择竹子作为“屏纸”原料的理由是()
A.竹子的生长周期短种植成材快 B.竹子中富含纸张的主要成分纤维素
C.温州的气候特征适合竹子生长 D.用竹子造纸可以传承古代竹简文化
5. “捞纸”工序是利用竹帘将纸浆中的竹纤维与水分离,其原理类似于物质分离中的()
A.结晶 B.过滤 C.蒸馏 D.沉淀
6.“晒纸”是将刚生产的湿纸,通过自然蒸发使纸张变千。若无风情况下在同一地点为了更快完成晒纸工序,下列晾晒方式最合理的是()
A B C D
7.小明在课堂上利用显微镜观察植物细胞,若对显微镜的结构④进行操作,他的目的是()
A.选择合适的放大倍数 B.调整物像的清晰度
C.改变视野的亮度D.将物像置于视野中央
8.1789年拉瓦锡将当时的30多种简单物质进行了分类,部分结果如下表。按拉瓦锡的物质分类标准,氧化镁属于()
A.气体类 B.金属类 C.非金属类 D.土质类
9.如图,小明将- -张白纸紧紧地卷成棍状,在其表面缠绕- -根铜丝。用蜡烛对铜丝处进行加热,纸棍不燃烧;而对纸棍未卷铜丝处进行加热,很快就能点燃。据此推测,铜丝在实验中的作用是()
A.隔绝白纸周围氧气
B升高白纸的着火点
C.降低白纸表面温度
D.降低蜡烛火焰温度
10.如图是小明绘制的膝跳反射过程示意图。据图分析,“大腿肌肉”属于反射弧中的()
A.感受器
B.神经中枢,
C.传出神经
D.效应器
11.小明利用如图所示装置研究影响植物蒸腾作用的因素。下列措施会加快红墨水向左移动的是()
A.向植株吹风
B.减少植株叶片
C.对植株遮光处理
D.将植株置于低温环境
12.如图所示,水平桌面上并排立着2支不同高度的蜡烛,蜡烛正前方放置- -个盛满水的烧瓶。小红透过烧瓶观察蜡烛,其中可能看到的像是()
A B C D
13.小明将甲、乙、丙三种金属与两种洛液反应,并根据实验现象编制了如图的检索表,根据检索表可知甲、乙、丙三种金属的活动性顺序为()
A乙>丙>甲 B.甲>乙>丙
C.丙>甲>乙 D.甲>丙>乙
14.如图甲为某品牌磁悬浮地球仪,其球体内部装有永磁铁,底座装有环形线圈。当线圈通电后产生磁场,利用磁极间相互作用使球体保持悬浮平衡。若底座环形线圈电流方向如图乙所示,则下列主视图中,球体内永磁铁的放置方式合理的是()
甲乙
A B
C D
15.下图为某超市搬运工利用便捷式货物搬运车进行桶装水搬运工作的示意图,若搬运工在把手上施加拉力F使搬运车保持静止,则拉力F的方向应该为()
A B C D
试题卷Ⅱ
二、填空题(本题共7小题,每空2分,共40分)
16.接力式楼道电梯可方便老人上下楼梯,如图所示。
(1)老人乘坐电梯.上楼时,其重力势能大小变化是_ ▲。
(2)电梯踏板的表面设计了很多花纹,其目的是▲。
(3)使用该电梯时为了确保安全,操作要同时满足以下条件:老人需站上踏板,压力开关S1会自动闭合;手需握住扶手,压力开关S2会自动闭合;再手动按下启动开关S3,电梯才会开始运行;下列电路设计符合要求的是_ ▲。
A B C D
17.小明同学在实验室利用粗盐提纯所制取的精盐,配制50克溶质质量分数为5%的氯化钠溶液。
(1)粗盐提纯的主要步骤为溶解、过滤、蒸发。为加快粗盐溶解,可采取的措施为▲。(列举一点)
(2)为完成氯化钠溶液配制,需称量食盐▲。
(3)配制所得的氯化钠溶液中,各元素质量分数如图所示,图中①所代表的元素是
▲。
18.鱼菜共生是一种新型的复合耕作体系,它能实现养鱼不换水、种菜不施肥的生态共生效应。装置原理如右图所示,由养殖区、种植区、转化槽组成,转化槽中细菌能将有机物转化为无机盐。整个装置通过水泵实现系统内的水循环。
(1)从生态系统的成分看,转化槽中的细菌属于▲。
(2)该系统利用水泵将养殖区中的水送入种植区中,水泵每小时做功36000J,则水泵的功率至少为▲瓦。
(3)减少草鱼的投放量有利于黑鱼的生长,请利用生态系统的知识解释其原因▲。
19.建立模型能帮助我们认识自然现象。如图是学生利用模型讨论温州地区冬寒夏热的问题。
甲乙丙
(1)图甲是太阳内部释放能量过程的模型图,该变化属于▲。(选填“核聚变”或“核裂变”)
(2)小明认为温州冬寒夏热是地球在夏季距离太阳较近。请从图乙中找出否定他观点的证据:▲。
(3,小红用图丙模型解释冬寒夏热,认为夏季正午时地面单位面积接受到的太阳能比冬季多,这是因为地球以一个倾斜的角度绕太阳公转,造成夏季和冬季的▲不同而导致的。
20.甲流是由甲型流感病毒引起的,多在春秋季节爆发的病毒性流行感冒。
(1)甲流爆发时其病毒会产生不同的类型,这是由于病毒会发生▲。
(2)医生建议人们每年要接种最新甲流疫苗,从传染病的预防措施来看,其属于▲。
(3)新鲜大蒜中含有蒜氨酸,当大蒜被切开后,蒜氨酸会生成大蒜素。大蒜素具有较强的抗病毒作用,能溶于酸性溶液,遇热很快失效。大蒜作为调味品,主要有以下几种食用方法:
①鹏大蒜与食物-起煮熟后食用②将生蒜切碎泡醋,食用大蒜醋③将大蒜切片生吃
若人们想食用大蒜预防甲流,请选择-一个你支持的食用方法并说明理由:▲。
21.我国研发出了一种新型水陆两栖飞行器一“同济飞鱼”(如图甲所示),它既能在空中飞行,也能在水中畅游。
(1)两栖飞行器在水中通过螺旋桨转动向后划水即可实现向前航行,其原理是▲。
(2)两栖飞行器装有深度计,图乙是其工作电路,压力传感器的电阻随压力的增大而减小。闭合开关,飞行器在深海下潜过程中显示器示数大小变化是▲。
(3)两栖飞行器还自带声波测距仪,某次飞行器悬停空中向障碍物发射声波,从发出声波至接收到反射回来的声波共用时2秒,若声波的速度为340米/秒,则飞行器离障碍物的距离是▲米。
22.科学家对元素的相对原子质量的认识经历了漫长的时间。
材料一: 19世纪初,有化学家认为:氢是母体,其他元素原子的相对原子质量理论上都是氢的整数倍,少数元素如Cl是35.5倍,则是由于实验误差造成的。
材料二: 1886年, 英国科学家克鲁克斯大胆假设:同一元素的原子,可以有不同的相对原子质量。化学家测定出的元素相对原子质量是其不同原子相对原子质量的平均值。
材料三: 1961年8月,国际上采用"C的1/12作为相对原子质量的标准,确定各个同位素原子的相对原子质量。某元素的相对原子质量是其各种同位素原子的相对原子质量乘以各自在该元素中所占的百分比之和。
(1)在克鲁克斯假设中,同种元素的原子,相对原子质最却不同,是因为原子结构中的某种微粒数不同,该微粒的名称是▲。
(2)结合已学知识和上述材料分析,下列说法正确的▲。(可多选 )
A.实验结果与预测有偏差时,可以忽略当作实验误差处理。
B.某元素的相对原子质量一定大于它所有的同位素原子的相对原子质量
C.自然界中大部分元素都有同位素原子,由此推测大部分元素的相对原子质量不是整数。
D. CI 的相对原子质量是35.5,其自然界仅有的两种同位素原子中,35Cl 所占的百分比大于37C1。
E.在化学变化中某金属原子失去电子与其他原子化合,计算该化合物相对分子质量时仍能使用该金属元素原来的相对原子质量。
三、实验探究题(本题有4小题,第26 (1)题6分,其余每空3分,共36分)题,每空3分,共36分)
23.开封后的牛奶放置- - 段时间后还能喝吗 小红查阅资料发现牛奶中的乳酸含量在0.12%-0.18%时为正常,超过0.18%为变质。为探究开封后牛奶变质的影响因素,小红进行如下实验:
①取甲、乙两瓶牛奶,打开。
②将甲瓶牛奶放置在20℃的恒温箱中,将乙瓶牛奶放置在4℃的恒温箱中。
③每隔8小时同时从甲乙两瓶牛奶中取样,并测量取样样品中的乳酸含量。
部分数据如表所示:
(1)写出步骤①中需要控制相同的- -种因素:▲。
(2)本实验中除了测量乳酸含量的仪器外,还需要用到的测量工具有▲。(写出两种)
(3)开封后放置一段时间的牛奶到底能不能喝 请结合探究结果,提出建议并说明理由。▲。
24.为了探究氯酸钾制取氧气时,生成氧气的速度与加入二氧化锰的质量有怎样的关系 小明用图甲装置开展实验。步骤如下:
①检查装置气密性,在500毫升集气瓶中装满水;
②取20克氯酸钾平均分成10份,分别装入10支试管中,分别记为①- D组,往10支试管中分别装入0.1克、0.2克、0.3克、0.4克、0.5克、0.65克、 1克、1.3克、2克、3克二氧化锰,并混合均匀;
③将10支试管分别加热,记录生成300毫升氧气所需时间,计算生成氧气的速度如图乙。
甲乙
(1)和向下排空气法相比,本实验中用排水法收集氧气的优点是▲。
(2)分析实验数据,得出的初步结论是▲。
(3) 4克氯酸钾和1. 3克二氧化锰混合均匀加热,据图推测,收集300亳升氧气所需要的时间约为▲秒。
25.为了探究影响导体电阻大小的因素,小明将长度均为6厘米且横截面积相同、粗细均匀的两种金属丝AB和金属丝BC对接相连,并按图甲连接电路,电源电压为12伏。他进行了如下实验。
甲乙丙
①将导线a一端与电压表正接线柱相连,另--端滑片P与金属丝接触良好并能沿金属丝左右滑动。
②闭合开关,将导线a的滑片P从金属丝AB的左端A点缓慢向右移动,一直移到金属丝BC的右端C点,记录并绘制电压表示数随AP长度l的变化关系如图乙。
(1)步骤②中某次电压表示数如图丙所示,此时金属丝AP两端电压为▲伏。
(2)实验完成后,小明得出结论:粗细均匀的同种导体,其电阻与长度成正比;长度和粗细相同的不同导体电阻不同。请利用电学相关知识并结合图乙说明小明得出结论的理由:▲。
(3)小明利用图甲装置进行另- -次实验,将滑片P固定在B处,将导线b的上端从C点缓慢向A点方向移动距离I'为10厘米,请画出在移动过程中电压表示数U随I'的变化关系图像。▲
26.小明想在家中测量食盐的密度,现有电子秤、玻璃杯2个、勺子、滴管、记号笔、足量的清水和食盐。
(1)请你帮助小明写出实验步骤完成测量(测量的各量用字母表示,清水的密度为ρ0)。▲
(2)转换法是实验中常用的方法,请在教材的实验里举- -例并写出转换法中相对应的量。▲
四、解答题(本题有6小题,第27题6分,第28题6分,第29题7分,第30题6分,第31题9分,第32题10分,共44分)
27.香蕉外皮易变黑变质,储存时间较短。资料显示:香蕉皮易变黑与其细胞内酚类物质和多酚氧化酶有关,其分布如图所示;若香蕉外皮细胞破裂,酚类物质与多酚氧化酶混合,会发生反应:酚类+氧气多酚氧化酶,黑色物质,导致外皮变黑。
(1)人食用香蕉后,其消化吸收的主要器官为▲。
(2)图中的液泡膜能控制液泡内酚类物质不进入细胞中的其他部位,与此具有类似功能的细胞结构是▲。
(3)为防止香蕉皮变黑腐烂,可以利用保鲜膜包裹香蕉或悬挂香蕉这些小妙招来延长保鲜时间。请你结合材料与知识,分析其中一种保鲜方法的科学原理。▲。
28.小明实验时发现:向盛有碳酸钠溶液的试管中滴加几滴稀盐酸时,并没有预想的气泡生成。是原溶液中没有碳酸根离子还是另有奧秘 于是他利用图甲装置进行如下实验。
实验一:在空的广口瓶中加入10克稀盐酸溶液,用注射器向瓶中缓慢注入足量碳酸钠溶液,测得产生二氧化碳气体情况如图乙所示。
实验二:试剂和装置都不变,在空的广口瓶中加入10.6 克碳酸钠溶液,用注射器向瓶中缓慢注入足量的稀盐酸溶液,测得产生二氧化碳气体情况如图丙所示。
甲乙丙
(1)请用化学方程式表示实验-一中广口瓶内发生的化学反应:▲。
(2)实验中能否定“原溶液内没有碳酸钙离子”的证据是▲。
(3)在实验一-和实验二中,最终产生的二氧化碳的质量相同的原因是▲。
29.科学课上,同学们开展“制作呼吸模型”项目化学习,下表为模型的评价量表。
某小组利用吸管、木板、气球和铁丝等材料制作模型,用保鲜膜将整个装置包住形成一一个密闭环境,如图甲所示。
(1)图甲模型中气球模拟的人体器官是▲。
(2)若要用该模型演示吸气过程,则同学对铁丝的操作为▲。
(3)根据评价量表,该模型的指标一-被评为优秀,指标二为合格,为使该模型能更好的体现人体结构特征,结合图乙请选择合适的材料对该模型进行改进:▲。(写出两点)
30.在生活中可以利用一碗水来鉴别鸡蛋的新鲜程度。
资料一:鸡蛋放置时间越久,越不新鲜,不同新鲜程度的鸡蛋在水中的浮沉情况如图甲。
甲乙
资料二:用放大镜观察鸡蛋外壳,发现鸡蛋壳表面布满一一个个气孔,如图乙所示。
资料三:鸡蛋在放置过程中,体积不会发生变化。
请结合.上述资料并综合运用所学知识,对“不同新鲜程度鸡蛋在水中的浮沉情况”进行解释。
31.吸氢能作为治疗一些疾病的辅助手段。如图甲是一款家用氢气发生器,裝置可以稳定提供纯净氢气,其工作原理如图乙所示。在水箱中加入蒸馏水,电解槽内的水电解(2H2O=通电=2H2↑+O2↑), 产生的氧气和.氢气分别从氧气出口和氢气出口排出。
(1)限压阀可以控制内部气压大小,当气压达到设定值时,限压阀打开,让气体排出。若要实现电解速度过大时两个限压阀同时排气,图乙中两限压阀的设定值PA和Pp的大小关系应为▲。
(2)氢气发生器要定时补充水,水箱水位最高时体积为1800毫升,水位最低时体积为900毫升。若产生氢气的速度为25克时,请计算一次充满水,能供应氢气多少小时
(3)根据装置原理图,推测装置C的作用是▲。
32.校本课程《陶艺》课上,烧制不同的陶、瓷作品需要不同的温度。为了能满足上述要求小明设计了一个电热式烧制炉的电路模型(如图甲所示)。工作电路: S1 为电源开关; S2为衔铁的同步开关( 电磁继电器吸下衔铁时S2同时断开) ;烧制炉的加热元件由阻值为48.4欧的R1和阻值为193.6欧的R2两个发热电阻组成。闭合S1和S2,烧制炉开始工作,先高功率升温,后保温期间能自动实现高功率、低功率两档切换。控制电路:烧制炉利用温差电源控制炉内温度达成恒温烧制。温差电源的热点(T1 点)放在炉中,冷点(T2点)放在低温恒温箱中,其提供的电压与T1、T2两点间的温度差关系如图乙所示。当温差电源使电磁继电器的电流达到0.015A时,电磁铁恰好能将弹性衔铁吸下,同时S2断开;一段时间后,温度降到预设值以下,释放弹性衔铁,同时S2闭合;如此反复,直至恒温烧制结束。
甲乙丙
(1)当S1和S2刚闭合时,工作电路中的两电阻的工作状态是▲。
A.仅R1工作 B.R1与R2串联工作
C.仅R2工作 D.R1与R2并联工作
(2)烧制炉烧制某陶瓷作品时,工作电路的高功率和低功率随时间变化如图丙所示,则烧制炉完成本次工作消耗的电能共为多少
(3)控制电路通过改变R0接入电路的阻值,实现改变烧制炉内的烧制温度。若控制电路中电磁继电器的线圈阻值为0.5欧,温差电源的冷点温度恒为20℃,现要烧制骨瓷作品需将炉内温度控制为1220℃,则需移动R0上的滑片使其接入电路的阻值为▲欧。
同课章节目录
