化学人教版(2019)选择性必修3 2.3.1苯及苯的同系物(共29张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 2.3.1苯及苯的同系物(共29张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-04 00:00:00 | ||
图片预览








文档简介
(共29张PPT)
第三节 芳香烃
第二章 烃
物理性质
颜色
气味
毒性
水溶性
挥发性
熔点
沸点
密度
无色
有特殊气味
有毒
不溶于水
易挥发
80.1℃
5.5℃
0.88g/cm3
苯是一种重要的化工原料和有机溶剂。
一:苯——最简单的芳香烃
1、苯的物理性质
2、苯的分子结构
1825年,英国科学家法拉第在煤气灯中首先发现苯,并测得其含碳量,确定其最简式为CH;
1834年,德国科学家米希尔里希制得苯,并将其命名为苯;
之后,法国化学家日拉尔等确定其分子量为78,苯分子式为C6H6。
C6H14 C6H6
—8H
高度不饱和的结构
德国有机化学家凯库勒给出的苯的结构
苯分子中是否有不饱和键?如何验证?
【实验2-1】
实验操作
实验现象
结 论
液体分层,上层 色,
下层_____色
液体分层,上层 色,
下层___色
无
紫红
橙黄
无
苯不能被酸性KMnO4溶液氧化,也不能与溴水反应。苯不溶于水,溴在苯中的溶解度比在水中的大
萃取
苯分子中具有不同于烯烃和炔烃的特殊结构
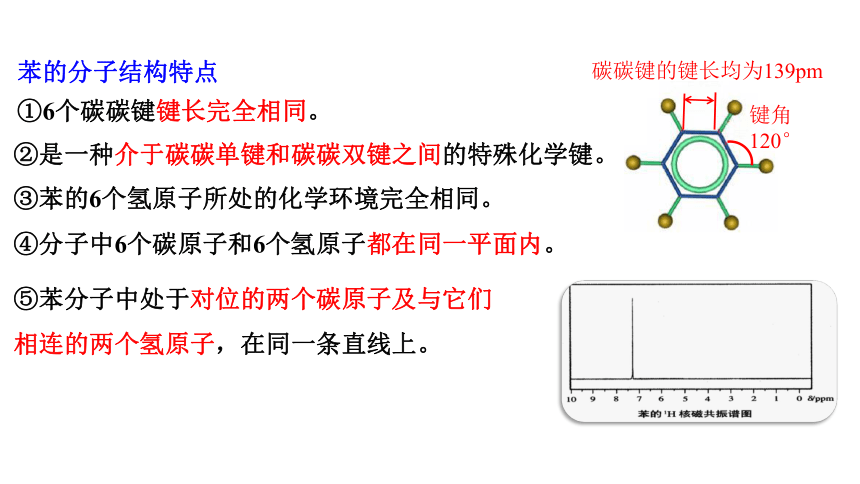
④分子中6个碳原子和6个氢原子都在同一平面内。
①6个碳碳键键长完全相同。
②是一种介于碳碳单键和碳碳双键之间的特殊化学键。
⑤苯分子中处于对位的两个碳原子及与它们相连的两个氢原子,在同一条直线上。
③苯的6个氢原子所处的化学环境完全相同。
苯的分子结构特点
键角120°
碳碳键的键长均为139pm
每个碳原子还剩余一个未参与杂化的p轨道,分别垂直于苯分子平面,六个p轨道相互平行重叠形成大π键,均匀地对称分布在苯环平面的上下两侧。
苯分子6个碳原子均采取sp2杂化,分别与氢原子及相邻碳原子以σ键结合,键间夹角均为120o,连接成六元环状。
σ键
大π键
p轨道
苯的成键特点
结构式
键线式
结构简式
球棍模型
填充模型
C6H6
分子式
苯的分子结构
3、苯的化学性质
在通常情况下不易发生烯烃和炔烃所容易发生的加成反应,在一定条件下可发生氧化、加成和取代反应。
(1) 氧化反应:
现象:
火焰明亮,伴有浓重的黑烟 (与乙炔相同)
方程式:
2C6H6 + 15O2 12CO2 + 6H2O
点燃
①苯不能使酸性高锰酸钾溶液褪色。
②可燃性:
(2)取代反应:
①溴代反应:
溴苯,无色液体,有特殊气味,不溶于水,密度比水大。
溴苯
I) 实验中需使用液溴,不能使用溴水。试剂的加入顺序为:先加苯,再加溴,最后加铁粉
II) 反应中加入的是铁粉,实际起催化作用的是FeBr3
III) 苯与Br2只发生一元取代反应
IV) 长导管的作用:导气兼起冷凝回流作用
V) 导管末端不能伸入到液面中(防止倒吸)
制取溴苯的实验设计如图
注意事项:
实验现象:I) 导管口有白雾产生
II) 锥形瓶中出现浅黄色沉淀
III) 反应结束后烧瓶中液体倒入盛有水的烧杯中,烧杯底部有油状的褐色液体
生成的HBr遇水蒸气
产生AgBr沉淀
溴苯中混有溴
思考:如何获得纯净的溴苯?
产物中可能含有溴苯、苯、
HBr和Br2
试剂:
操作:
目的:
水
分液
除HBr
HBr水溶液
溴苯
苯、溴
试剂:
操作:
目的:
NaOH
分液
除Br2
NaBr溶液
NaBrO溶液
溴苯
苯
溴苯
苯
蒸馏
除苯
操作:
目的:
②硝化反应:
硝基苯,带有苦杏仁气味的无色液体,不溶于水,密度比水大。
硝基苯
制取硝基苯的实验设计如图
Ⅰ)试剂的加入顺序:先加浓硝酸,再加浓硫酸,等混合液冷却到50-60℃后,再加苯
Ⅱ)用水浴加热,控制温度在50-60℃,温度计放在水浴中。温度过高,苯挥发,硝酸分解。 水浴加热的优点:容易控制温度,受热均匀
Ⅳ)浓硫酸的作用:催化剂、吸水剂
Ⅲ)试管上方的长导管的作用是冷凝流、减少反应物的挥发。
注意事项:
实验现象:将反应后的液体倒入一个盛有水的烧杯中,可以观察到烧杯底部有黄色油状物质生成 (硝基苯因溶有少量NO2而显黄色)。
思考:如何获得纯净的硝基苯?
产物中可能含有硝基苯、苯、硫酸、硝酸、NO2
试剂:
操作:
目的:
水
分液
除酸
酸液
硝基苯
苯
残余酸
试剂:
操作:
目的:
NaOH
分液
除酸
盐溶液
硝基苯
苯
硝基苯
苯
蒸馏
除苯
操作:
目的:
③磺化反应:
70~80℃
磺酸基:-SO3H
苯磺酸
苯磺酸易溶于水,是一种强酸,可以看作是硫酸分子里的一个羟基被苯环取代的产物。磺化反应可用于制备合成洗涤剂。
(3) 加成反应
+ H2
催化剂(Ni)
△
环己烷
3
①苯与H2加成:
②苯与Cl2在紫外线作用下加成
六氯环己烷
或
(农药六六六)
苯的大π键比较稳定,通常状态下不易发生加成反应
(Pt或Ni作为催化剂并且加热)
+ 3Cl2
紫外线
苯的同系物 名称 熔点/℃ 沸点/℃ 密度/(g·cm-3)
甲苯 -95 111 0.867
乙苯 -95 136 0.867
邻二甲苯 (1,2-二甲苯) -25 144 0.880
间二甲苯 (1,3-二甲苯) -48 139 0.864
对二甲苯 (1,4-二甲苯) 13 138 0.861
CH3
C2H5
CH3
CH3
CH3
CH3
CH3
CH3
分析课本P46表2-2,总结苯的同系物结构特点及物理性质规律
二:苯的同系物
1、组成和结构特点
苯的同系物是指苯环上的氢原子被烷基取代所得到的一系列产物
结构特点:其分子中有一个苯环,侧链都是烷基。
通式:CnH2n-6(n≥7)。
概念:
课堂练习1:下列有机物属于芳香族化合物的有 ,属于芳香烃的有 ,属于苯的同系物的有 。
①②③④⑥⑦⑧⑨
②③④⑧⑨
①
—OH
②
—CH3
③
—CH3
—CH3
④
CH = CH2
⑤
⑥
—NO2
⑦
C
O
OH
⑧
⑨
芳香族化合物
芳香烃
苯及苯的同系物
②③⑧
2、物理性质
①气味类似苯,无色液体,密度比水小,不溶于水,易溶于有机溶剂,本身也常作为有机溶剂 。
三种二甲苯的熔、沸点与密度
①熔点:对二甲苯>邻二甲苯>间二甲苯。
②沸点:邻二甲苯>间二甲苯>对二甲苯。
③密度:邻二甲苯>间二甲苯>对二甲苯。
②随碳原子数增多,熔沸点依次升高,密度依次增大;苯环上的支链越多,溶沸点越低
③同分异构体中,苯环上的侧链越短,侧链在苯环上分布越散,熔沸点越低
都含有苯环,性质相似
例如: 可燃烧;易取代(卤代、硝化);能加成等。
比较苯和甲苯结构的异同点, 推测甲苯的化学性质。
甲苯含有甲基,由于苯环和甲基相互影响,在化学性质上与苯也有不同之处。
3、化学性质
—CH3
【实验2-2】
实验内容 实验现象 解释
(1)向两支分别盛有2mL苯和甲苯的试管中各入几滴溴水,静置
(2)将上述试管用力振荡,静置
(3)向两支分别盛有2mL苯和甲苯的试管中各加入几滴酸性高锰酸钾溶液,静置
(4)将上述试管用力振荡,静置
都分层,溴水沉到液体底部
苯、甲苯的密度均小于溴水
液体分层,上层呈橙黄色
溴与苯、甲苯不反应,但易溶于苯、甲苯被萃取
液体分层,上层呈无色,下层呈紫红色
苯、甲苯的密度均小于酸性高锰酸钾溶液
苯无现象、甲苯使酸性高锰酸钾溶液褪色
甲苯能被酸性高锰酸钾氧化,苯不能
【思考与讨论】
结合苯和甲苯的分子结构特点及上述实验结果,分析苯和甲苯的物理性质、化学性质有哪些相似点和不同点。
芳香烃 苯 甲苯
分子式 结构简式
结构相似性
结构不同点
分子间的关系
物理性质相似点
化学性质 不同点
相同点
CH3
C6H6
C7H8
都含有苯环
苯环上没有取代基
苯环上有甲基取代基
结构相似,分子组成相差CH2,互为同系物
无色液体,比水轻,不溶于水
与酸性高锰酸钾溶液不反应
与溴水不反应,萃取,能燃烧,易取代,难加成
能被酸性高锰酸钾氧化,溶液褪色
①燃烧反应:
现象:火焰明亮并带有浓烟
②可使酸性高锰酸钾溶液褪色。这是由于甲苯上的甲基被酸性KMnO4氧化的结果(侧链氧化)。
结论:苯环对侧链影响:苯环活化侧链, 使侧链易于氧化。
(1)氧化反应
酸性高锰酸钾溶液
─
CH3
─
COOH
甲烷和苯都不能使酸性高锰酸钾溶液褪色
(2)取代反应
2,4,6-三硝基甲苯
CH3
|
|
NO2
CH3
|
NO2
O2N
+ 3HNO3
+ 3H2O
浓硫酸
△
①硝化反应
2,4,6-三硝基甲苯,又叫梯恩梯(TNT),淡黄色针状晶体,不溶于水。 在引爆剂作用下发生猛烈爆炸,是一种烈性炸药。
结论:苯环的侧链影响了苯环:甲基活化了苯环的邻位和对位。硝基取代更易发生,且取代的位置均以甲基的邻、对位为主。
CH3
+Cl2
光照
Fe
CH2Cl
+HCl
CH3
Cl
+HCl
CH3
Cl
+HCl
或
②卤代反应
特点:有机产物不唯一、产物以一氯甲苯为主
CH3
Cl
Cl
CH3
Cl
Cl
Cl
CH3
Cl
Cl
有可能还生成
在一定条件下甲苯与H2发生加成反应,生成甲基环己烷,化学反应方程式为
(3)加成反应
环己烷
+ 3H2
很困难
催化剂
△
CH3
|
CH3
|
+ 3H2
很困难
甲基环己烷
催化剂
△
【思考与讨论】
(1) 在光照条件下,甲苯与氯气能发生类似甲烷与氯气的取代反应,请写出可能的有机产物的结构简式。分离提纯这些有机化合物的方法是什么?
(2) 在FeBr3催化下,甲苯与溴发生取代反应可以生成一溴代甲苯,请写出该反应的主要有机产物的结构简式,并从化学键和官能团的角度分析反应中有机化合物变化。
CHCl2
CCl3
用蒸馏法
CH2Cl
Br
CH3
Br
CH3
甲基与苯环相互作用,苯环甲基邻、对位氢原子变得比较活泼。
(3) 在Pt作催化剂和加热的条件下,甲苯与氢气能发生类似苯与氢气的加成反应,请写出该反应的化学方程式。
(4) 对比苯与甲苯的结构,以及二者发生硝化反应的产物,你能得出什么结论?
甲苯可生成甲基邻、对位的一硝基、二硝基、三硝基取代产物,苯一般只生一硝基取代产物。结论:甲基与苯环相互作用,使甲基邻、对位氢原子变得比较活泼。
课堂小结
苯 苯的同系物
相 同 点 结构组成 ①分子中都含有一个苯环 ②都符合通式CnH(2n-6)
化学性质 ①燃烧时现象相同,火焰明亮,伴有浓烟 ②都易发生苯环上的取代反应 ③都能发生加成反应,都比较困难
不 同 点 取代反应 易发生取代反应,主要得到一元取代产物 更容易发生取代反应,得到多元取代产物
氧化反应 难被氧化,不能使酸性高锰酸钾溶液褪色 易被氧化,能使酸性高锰酸钾溶液褪色
差异原因 苯的同系物分子中,苯环与侧链相互影响,苯环影响侧链,使侧链烃基性质变得活泼,而易被氧化。侧链烃基影响苯环,使苯环邻对位氢原子变得活泼,而易被取代
第三节 芳香烃
第二章 烃
物理性质
颜色
气味
毒性
水溶性
挥发性
熔点
沸点
密度
无色
有特殊气味
有毒
不溶于水
易挥发
80.1℃
5.5℃
0.88g/cm3
苯是一种重要的化工原料和有机溶剂。
一:苯——最简单的芳香烃
1、苯的物理性质
2、苯的分子结构
1825年,英国科学家法拉第在煤气灯中首先发现苯,并测得其含碳量,确定其最简式为CH;
1834年,德国科学家米希尔里希制得苯,并将其命名为苯;
之后,法国化学家日拉尔等确定其分子量为78,苯分子式为C6H6。
C6H14 C6H6
—8H
高度不饱和的结构
德国有机化学家凯库勒给出的苯的结构
苯分子中是否有不饱和键?如何验证?
【实验2-1】
实验操作
实验现象
结 论
液体分层,上层 色,
下层_____色
液体分层,上层 色,
下层___色
无
紫红
橙黄
无
苯不能被酸性KMnO4溶液氧化,也不能与溴水反应。苯不溶于水,溴在苯中的溶解度比在水中的大
萃取
苯分子中具有不同于烯烃和炔烃的特殊结构
④分子中6个碳原子和6个氢原子都在同一平面内。
①6个碳碳键键长完全相同。
②是一种介于碳碳单键和碳碳双键之间的特殊化学键。
⑤苯分子中处于对位的两个碳原子及与它们相连的两个氢原子,在同一条直线上。
③苯的6个氢原子所处的化学环境完全相同。
苯的分子结构特点
键角120°
碳碳键的键长均为139pm
每个碳原子还剩余一个未参与杂化的p轨道,分别垂直于苯分子平面,六个p轨道相互平行重叠形成大π键,均匀地对称分布在苯环平面的上下两侧。
苯分子6个碳原子均采取sp2杂化,分别与氢原子及相邻碳原子以σ键结合,键间夹角均为120o,连接成六元环状。
σ键
大π键
p轨道
苯的成键特点
结构式
键线式
结构简式
球棍模型
填充模型
C6H6
分子式
苯的分子结构
3、苯的化学性质
在通常情况下不易发生烯烃和炔烃所容易发生的加成反应,在一定条件下可发生氧化、加成和取代反应。
(1) 氧化反应:
现象:
火焰明亮,伴有浓重的黑烟 (与乙炔相同)
方程式:
2C6H6 + 15O2 12CO2 + 6H2O
点燃
①苯不能使酸性高锰酸钾溶液褪色。
②可燃性:
(2)取代反应:
①溴代反应:
溴苯,无色液体,有特殊气味,不溶于水,密度比水大。
溴苯
I) 实验中需使用液溴,不能使用溴水。试剂的加入顺序为:先加苯,再加溴,最后加铁粉
II) 反应中加入的是铁粉,实际起催化作用的是FeBr3
III) 苯与Br2只发生一元取代反应
IV) 长导管的作用:导气兼起冷凝回流作用
V) 导管末端不能伸入到液面中(防止倒吸)
制取溴苯的实验设计如图
注意事项:
实验现象:I) 导管口有白雾产生
II) 锥形瓶中出现浅黄色沉淀
III) 反应结束后烧瓶中液体倒入盛有水的烧杯中,烧杯底部有油状的褐色液体
生成的HBr遇水蒸气
产生AgBr沉淀
溴苯中混有溴
思考:如何获得纯净的溴苯?
产物中可能含有溴苯、苯、
HBr和Br2
试剂:
操作:
目的:
水
分液
除HBr
HBr水溶液
溴苯
苯、溴
试剂:
操作:
目的:
NaOH
分液
除Br2
NaBr溶液
NaBrO溶液
溴苯
苯
溴苯
苯
蒸馏
除苯
操作:
目的:
②硝化反应:
硝基苯,带有苦杏仁气味的无色液体,不溶于水,密度比水大。
硝基苯
制取硝基苯的实验设计如图
Ⅰ)试剂的加入顺序:先加浓硝酸,再加浓硫酸,等混合液冷却到50-60℃后,再加苯
Ⅱ)用水浴加热,控制温度在50-60℃,温度计放在水浴中。温度过高,苯挥发,硝酸分解。 水浴加热的优点:容易控制温度,受热均匀
Ⅳ)浓硫酸的作用:催化剂、吸水剂
Ⅲ)试管上方的长导管的作用是冷凝流、减少反应物的挥发。
注意事项:
实验现象:将反应后的液体倒入一个盛有水的烧杯中,可以观察到烧杯底部有黄色油状物质生成 (硝基苯因溶有少量NO2而显黄色)。
思考:如何获得纯净的硝基苯?
产物中可能含有硝基苯、苯、硫酸、硝酸、NO2
试剂:
操作:
目的:
水
分液
除酸
酸液
硝基苯
苯
残余酸
试剂:
操作:
目的:
NaOH
分液
除酸
盐溶液
硝基苯
苯
硝基苯
苯
蒸馏
除苯
操作:
目的:
③磺化反应:
70~80℃
磺酸基:-SO3H
苯磺酸
苯磺酸易溶于水,是一种强酸,可以看作是硫酸分子里的一个羟基被苯环取代的产物。磺化反应可用于制备合成洗涤剂。
(3) 加成反应
+ H2
催化剂(Ni)
△
环己烷
3
①苯与H2加成:
②苯与Cl2在紫外线作用下加成
六氯环己烷
或
(农药六六六)
苯的大π键比较稳定,通常状态下不易发生加成反应
(Pt或Ni作为催化剂并且加热)
+ 3Cl2
紫外线
苯的同系物 名称 熔点/℃ 沸点/℃ 密度/(g·cm-3)
甲苯 -95 111 0.867
乙苯 -95 136 0.867
邻二甲苯 (1,2-二甲苯) -25 144 0.880
间二甲苯 (1,3-二甲苯) -48 139 0.864
对二甲苯 (1,4-二甲苯) 13 138 0.861
CH3
C2H5
CH3
CH3
CH3
CH3
CH3
CH3
分析课本P46表2-2,总结苯的同系物结构特点及物理性质规律
二:苯的同系物
1、组成和结构特点
苯的同系物是指苯环上的氢原子被烷基取代所得到的一系列产物
结构特点:其分子中有一个苯环,侧链都是烷基。
通式:CnH2n-6(n≥7)。
概念:
课堂练习1:下列有机物属于芳香族化合物的有 ,属于芳香烃的有 ,属于苯的同系物的有 。
①②③④⑥⑦⑧⑨
②③④⑧⑨
①
—OH
②
—CH3
③
—CH3
—CH3
④
CH = CH2
⑤
⑥
—NO2
⑦
C
O
OH
⑧
⑨
芳香族化合物
芳香烃
苯及苯的同系物
②③⑧
2、物理性质
①气味类似苯,无色液体,密度比水小,不溶于水,易溶于有机溶剂,本身也常作为有机溶剂 。
三种二甲苯的熔、沸点与密度
①熔点:对二甲苯>邻二甲苯>间二甲苯。
②沸点:邻二甲苯>间二甲苯>对二甲苯。
③密度:邻二甲苯>间二甲苯>对二甲苯。
②随碳原子数增多,熔沸点依次升高,密度依次增大;苯环上的支链越多,溶沸点越低
③同分异构体中,苯环上的侧链越短,侧链在苯环上分布越散,熔沸点越低
都含有苯环,性质相似
例如: 可燃烧;易取代(卤代、硝化);能加成等。
比较苯和甲苯结构的异同点, 推测甲苯的化学性质。
甲苯含有甲基,由于苯环和甲基相互影响,在化学性质上与苯也有不同之处。
3、化学性质
—CH3
【实验2-2】
实验内容 实验现象 解释
(1)向两支分别盛有2mL苯和甲苯的试管中各入几滴溴水,静置
(2)将上述试管用力振荡,静置
(3)向两支分别盛有2mL苯和甲苯的试管中各加入几滴酸性高锰酸钾溶液,静置
(4)将上述试管用力振荡,静置
都分层,溴水沉到液体底部
苯、甲苯的密度均小于溴水
液体分层,上层呈橙黄色
溴与苯、甲苯不反应,但易溶于苯、甲苯被萃取
液体分层,上层呈无色,下层呈紫红色
苯、甲苯的密度均小于酸性高锰酸钾溶液
苯无现象、甲苯使酸性高锰酸钾溶液褪色
甲苯能被酸性高锰酸钾氧化,苯不能
【思考与讨论】
结合苯和甲苯的分子结构特点及上述实验结果,分析苯和甲苯的物理性质、化学性质有哪些相似点和不同点。
芳香烃 苯 甲苯
分子式 结构简式
结构相似性
结构不同点
分子间的关系
物理性质相似点
化学性质 不同点
相同点
CH3
C6H6
C7H8
都含有苯环
苯环上没有取代基
苯环上有甲基取代基
结构相似,分子组成相差CH2,互为同系物
无色液体,比水轻,不溶于水
与酸性高锰酸钾溶液不反应
与溴水不反应,萃取,能燃烧,易取代,难加成
能被酸性高锰酸钾氧化,溶液褪色
①燃烧反应:
现象:火焰明亮并带有浓烟
②可使酸性高锰酸钾溶液褪色。这是由于甲苯上的甲基被酸性KMnO4氧化的结果(侧链氧化)。
结论:苯环对侧链影响:苯环活化侧链, 使侧链易于氧化。
(1)氧化反应
酸性高锰酸钾溶液
─
CH3
─
COOH
甲烷和苯都不能使酸性高锰酸钾溶液褪色
(2)取代反应
2,4,6-三硝基甲苯
CH3
|
|
NO2
CH3
|
NO2
O2N
+ 3HNO3
+ 3H2O
浓硫酸
△
①硝化反应
2,4,6-三硝基甲苯,又叫梯恩梯(TNT),淡黄色针状晶体,不溶于水。 在引爆剂作用下发生猛烈爆炸,是一种烈性炸药。
结论:苯环的侧链影响了苯环:甲基活化了苯环的邻位和对位。硝基取代更易发生,且取代的位置均以甲基的邻、对位为主。
CH3
+Cl2
光照
Fe
CH2Cl
+HCl
CH3
Cl
+HCl
CH3
Cl
+HCl
或
②卤代反应
特点:有机产物不唯一、产物以一氯甲苯为主
CH3
Cl
Cl
CH3
Cl
Cl
Cl
CH3
Cl
Cl
有可能还生成
在一定条件下甲苯与H2发生加成反应,生成甲基环己烷,化学反应方程式为
(3)加成反应
环己烷
+ 3H2
很困难
催化剂
△
CH3
|
CH3
|
+ 3H2
很困难
甲基环己烷
催化剂
△
【思考与讨论】
(1) 在光照条件下,甲苯与氯气能发生类似甲烷与氯气的取代反应,请写出可能的有机产物的结构简式。分离提纯这些有机化合物的方法是什么?
(2) 在FeBr3催化下,甲苯与溴发生取代反应可以生成一溴代甲苯,请写出该反应的主要有机产物的结构简式,并从化学键和官能团的角度分析反应中有机化合物变化。
CHCl2
CCl3
用蒸馏法
CH2Cl
Br
CH3
Br
CH3
甲基与苯环相互作用,苯环甲基邻、对位氢原子变得比较活泼。
(3) 在Pt作催化剂和加热的条件下,甲苯与氢气能发生类似苯与氢气的加成反应,请写出该反应的化学方程式。
(4) 对比苯与甲苯的结构,以及二者发生硝化反应的产物,你能得出什么结论?
甲苯可生成甲基邻、对位的一硝基、二硝基、三硝基取代产物,苯一般只生一硝基取代产物。结论:甲基与苯环相互作用,使甲基邻、对位氢原子变得比较活泼。
课堂小结
苯 苯的同系物
相 同 点 结构组成 ①分子中都含有一个苯环 ②都符合通式CnH(2n-6)
化学性质 ①燃烧时现象相同,火焰明亮,伴有浓烟 ②都易发生苯环上的取代反应 ③都能发生加成反应,都比较困难
不 同 点 取代反应 易发生取代反应,主要得到一元取代产物 更容易发生取代反应,得到多元取代产物
氧化反应 难被氧化,不能使酸性高锰酸钾溶液褪色 易被氧化,能使酸性高锰酸钾溶液褪色
差异原因 苯的同系物分子中,苯环与侧链相互影响,苯环影响侧链,使侧链烃基性质变得活泼,而易被氧化。侧链烃基影响苯环,使苯环邻对位氢原子变得活泼,而易被取代
