10.1常见的酸和碱同步练习(含答案)人教版化学九年级下册
文档属性
| 名称 | 10.1常见的酸和碱同步练习(含答案)人教版化学九年级下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 237.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-04 00:00:00 | ||
图片预览



文档简介
10.1常见的酸和碱同步练习人教版化学九年级下册
学校:___________姓名:___________班级:___________考号:___________
一、单选题(共30分)
1.(本题3分)逻辑推理是一种重要的化学思维方法。下列推理合理的是( )
A.因为碱溶液呈碱性,所以显碱性的溶液一定都是碱的溶液
B.因为H2O和H2O2的组成元素相同,所以它们的化学性质相同
C.单质中只含有一种元素,只含有一种元素的纯净物质一定是单质
D.置换反应中一定有单质生成,则有单质生成的化学反应一定是置换反应
2.(本题3分)下列有关盐酸和硫酸的说法正确的是
A.打开浓盐酸的瓶塞,观察到有白烟
B.浓硫酸可以做干燥剂是因为有脱水性
C.实验室可以用石灰石和稀硫酸制取二氧化碳
D.浓盐酸和浓硫酸敞口放置一段时间后,溶质质量分数都会变小
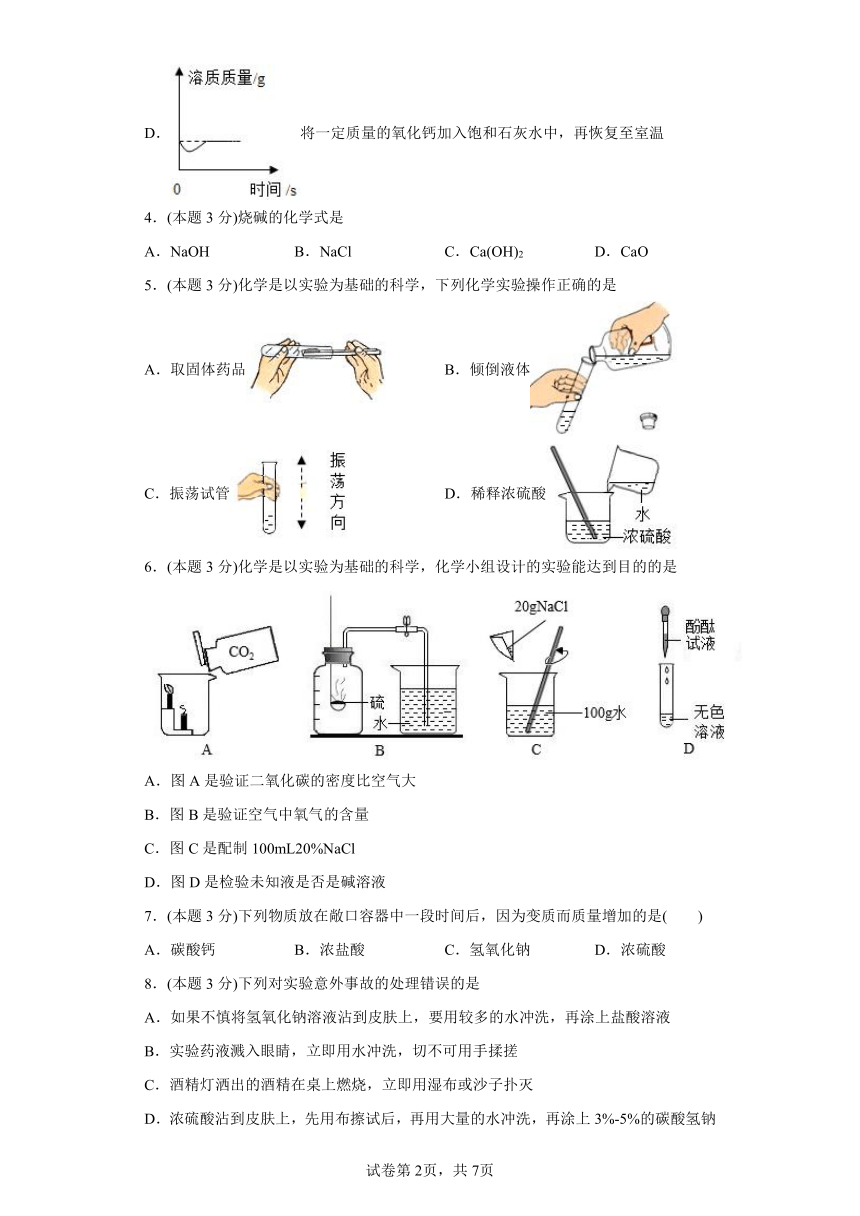
3.(本题3分)下列图像分别与选项中的操作相对应,其中合理的是
A.在密闭容器内加热汞得到氧化汞
B.在密闭装置内点燃过量红磷测定空气中氧气的含量
C.久置于空气中未经打磨的铝片与盐酸反应
D.将一定质量的氧化钙加入饱和石灰水中,再恢复至室温
4.(本题3分)烧碱的化学式是
A.NaOH B.NaCl C.Ca(OH)2 D.CaO
5.(本题3分)化学是以实验为基础的科学,下列化学实验操作正确的是
A.取固体药品 B.倾倒液体
C.振荡试管 D.稀释浓硫酸
6.(本题3分)化学是以实验为基础的科学,化学小组设计的实验能达到目的的是
A.图A是验证二氧化碳的密度比空气大
B.图B是验证空气中氧气的含量
C.图C是配制100mL20%NaCl
D.图D是检验未知液是否是碱溶液
7.(本题3分)下列物质放在敞口容器中一段时间后,因为变质而质量增加的是( )
A.碳酸钙 B.浓盐酸 C.氢氧化钠 D.浓硫酸
8.(本题3分)下列对实验意外事故的处理错误的是
A.如果不慎将氢氧化钠溶液沾到皮肤上,要用较多的水冲洗,再涂上盐酸溶液
B.实验药液溅入眼睛,立即用水冲洗,切不可用手揉搓
C.酒精灯洒出的酒精在桌上燃烧,立即用湿布或沙子扑灭
D.浓硫酸沾到皮肤上,先用布擦试后,再用大量的水冲洗,再涂上3%-5%的碳酸氢钠溶液
9.(本题3分)使用酸、碱等腐蚀性药品时,必须按照操作规程进行。下列处理方法错误的是( )
A.有腐蚀性的药液溅入眼睛内,要立即用水冲洗,切不可用手揉搓
B.稀酸飞溅到皮肤上,立即用大量的水冲洗,再涂上3%~5%的碳酸氢钠溶液
C.不小心打翻了燃着的酒精灯,应立即浇水来熄灭桌子上燃着的酒精
D.氢氧化钠溶液溅在皮肤上,先用水冲洗后,再涂上硼酸溶液
10.(本题3分)下列四种物质久置空气中,质量增加且没有新物质生成的是( )
A.氨水 B.烧碱 C.浓硫酸 D.浓盐酸
二、判断题(共15分)
11.(本题3分)酸溶液能使紫色石蕊溶液变红色,则稀盐酸能使紫色石蕊溶液变成红色( )
12.(本题3分)用氢氧化钠溶液除去二氧化碳中的氯化氢气体( )
13.(本题3分)酸溶液具有相似化学性质的原因是都含有氢元素( )
14.(本题3分)稀硫酸稀释将水沿器壁慢慢注入浓硫酸中。( )
15.(本题3分)浓盐酸稀释后可以用来给金属除锈( )
三、填空题(共15分)
16.(本题3分)盐酸是重要的化工原料,也是实验室中最常用的化学试剂之一、
(1)用质量分数为37%的浓盐酸配制1000g质量分数为0.37%(pH约为1)的稀盐酸。
①所配稀盐酸中溶质的质量为_______g,所需浓盐酸的质量为_______g。
②已知浓盐酸密度为1.19g/cm3,量取上述所需浓盐酸用到的仪器是_______(填标号)。
A.10mL量筒 B.50mL量筒 C.试管 D.胶头滴管
(2)取少量氢氧化钙粉末于试管中,加入2mL水,振荡,得到白色浑浊液,滴加1滴酚酞溶液,再滴加稀盐酸至反应完全,可观察到的现象是_______。
(3)取等质量的铁片和铁粉放入两支试管中,分别加入相同体积相同浓度的稀盐酸。
①铁与稀盐酸反应的化学方程式为_______。
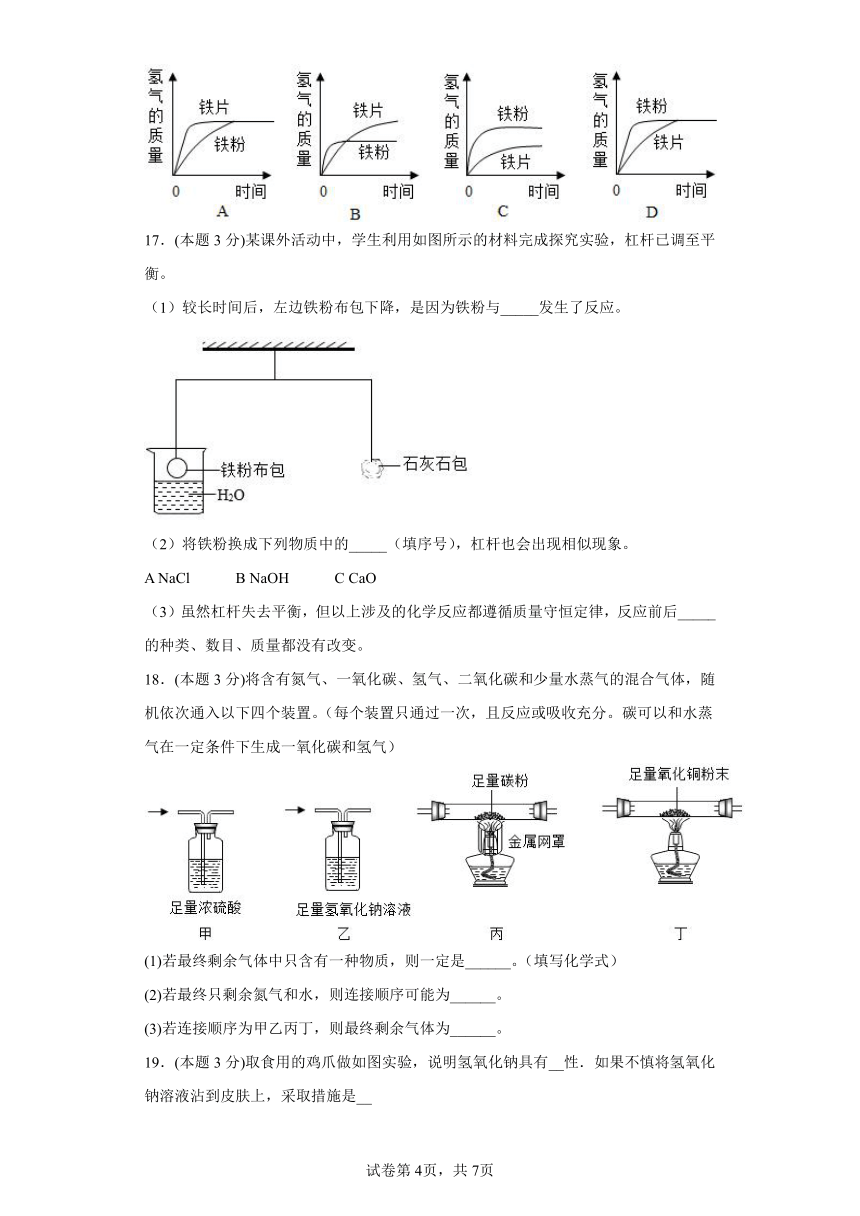
②如图示意图中,与实验结果相符的是_______(填标号)。
17.(本题3分)某课外活动中,学生利用如图所示的材料完成探究实验,杠杆已调至平衡。
(1)较长时间后,左边铁粉布包下降,是因为铁粉与_____发生了反应。
(2)将铁粉换成下列物质中的_____(填序号),杠杆也会出现相似现象。
A NaCl B NaOH C CaO
(3)虽然杠杆失去平衡,但以上涉及的化学反应都遵循质量守恒定律,反应前后_____的种类、数目、质量都没有改变。
18.(本题3分)将含有氮气、一氧化碳、氢气、二氧化碳和少量水蒸气的混合气体,随机依次通入以下四个装置。(每个装置只通过一次,且反应或吸收充分。碳可以和水蒸气在一定条件下生成一氧化碳和氢气)
(1)若最终剩余气体中只含有一种物质,则一定是______。(填写化学式)
(2)若最终只剩余氮气和水,则连接顺序可能为______。
(3)若连接顺序为甲乙丙丁,则最终剩余气体为______。
19.(本题3分)取食用的鸡爪做如图实验,说明氢氧化钠具有__性.如果不慎将氢氧化钠溶液沾到皮肤上,采取措施是__
20.(本题3分)水是一种重要的资源,根据你所学的知识回答下列问题。
(1)在日常生活中,人们常用________来区分硬软水。
(2)自来水厂常用活性炭来净水,活性炭净水是利用活性炭的_________ 作用。
(3)水电解过程中发生变化的微粒是_________ 。
(4)实验室稀释浓硫酸时,应将_________沿烧杯壁缓缓地注入盛有________的烧杯中。
(5)用湿抹布扑盖实验桌上燃烧的酒精,其主要灭火原理是_________。
四、综合应用题(共40分)
21.(本题10分)经脱硫、脱氮净化后的水煤气中含有CO、CO2、H2和水蒸气中的一种或多种。为了检验该气体的成分,并测定某氧化铜样品(含少量铜)中氧化铜的质量分数,同学们设计了如图一所示实验,实线框内仪器待组装,如图二所示(部分夹持仪器已略去)。
已知:无水硫酸铜遇水由白色变为蓝色,碱石灰由氢氧化钠和氧化钙组成。
回答问题:
(1)实验前连接装置并检查____________依次称量氧化铜样品和装置G(含试剂)的质量,分别记为W1和W2。
(2)图一实线框内装置的正确连接顺序是a-_________(填导管口序号)。
(3)加热前,当通入水煤气时,A、B两装置中均有明显的现象,装置B中发生反应的化学方程式为_________。
(4)加热过程中,同学们观察到__________由此判断原气体中含有CO。
(5)待氧化铜样品完全反应后,冷却,再依次称量硬质玻璃管中剩余固体和装置G(含试剂)的质量,分别记为W3和W4,样品中氧化铜的质量分数为___________。
22.(本题15分)取久置敞口放置的氢氧化钠溶液于烧杯中,倒入一定量的稀硫酸充分反应。为探究反应后所得溶液X的成分,兴趣小组进行了如图实验(所加试剂均足量)。
(1)产生的无色气体是_______。
(2)溶液X的溶质是_______。(填写化学式)
(3)计算溶液X中硫酸钠的质量。
(4)设计实验将滤液A变成纯净的氯化钠晶体,请简述你的实验操作步骤_______。
23.(本题15分)下图是实验室常用气体制备装置,据图回答问题:
(1)用A装置制取氧气的化学方程式是_________________。选择D装置收集氧气是因为_________。将带火星的木炭伸入盛有氧气的集气瓶中,木炭剧烈燃烧,发出白光,说明氧气能________,该反应的化学方程式为_____________。
(2)实验室制取氨气:Ca(OH)2(固)+2NH4Cl(固)CaCl2(固)+2H2O+2NH3↑,要制取并收集干燥的氨气,所选装置正确的连接顺序是( )→( )→( )(填字母代号)。
为探究氨气的性质,按下图装置进行实验。观察到黑色粉末变红,白色无水硫酸铜变蓝,同时反应中还有一种气体单质生成。
【查阅资料】Cu2O是红色,易与稀硫酸反应:Cu2O+H2SO4==CuSO4+Cu+H2O。
【提出问题】得到的红色物质是什么?
(3)【猜想】①是Cu;②是Cu2O;③是______。
若猜想①成立,玻璃管中发生反应的化学方程式为__________________,说明NH3具有______性。
(4)【设计实验】请你设计一个简单的实验来验证红色物质中是否存在Cu2O______________。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.D
3.A
4.A
5.A
6.A
7.C
8.A
9.C
10.C
11.正确
12.错误
13.错误
14.错误
15.正确
16.(1) 3.7 10 AD
(2)溶液由红色变为无色
(3)
D
17. 水和氧气 BC 原子
18.(1)N2
(2)甲丙丁乙
(3)N2、CO2、H2O
19. 腐蚀 要立即用大量水冲洗,然后涂上硼酸溶液
20. 肥皂水 吸附 水分子 液硫酸 水 隔绝氧气
21.(1)装置气密性
(2)e-f-c-d-b
(3)
(4)装置F中澄清石灰水变浑浊
(5)
22.(1)CO2
(2)NaOH、Na2CO3、Na2SO4
(3)设溶液X中硫酸钠的质量为x。
答:溶液X中硫酸钠的质量为2.84g。
(4)加入足量的稀盐酸,再加热浓缩、蒸发结晶
23.(1) 密度比空气大 支持燃烧(或助燃) C+O2CO2
(2) A G E
(3) Cu和Cu2O 2NH3+3CuO3Cu+3H2O+N2 还原
(4)取少量红色物质放于试管,向试管中倒入稀硫酸,若溶液逐渐变为蓝色则有Cu2O,若溶液不变色,则无Cu2O
答案第1页,共2页
答案第1页,共2页
学校:___________姓名:___________班级:___________考号:___________
一、单选题(共30分)
1.(本题3分)逻辑推理是一种重要的化学思维方法。下列推理合理的是( )
A.因为碱溶液呈碱性,所以显碱性的溶液一定都是碱的溶液
B.因为H2O和H2O2的组成元素相同,所以它们的化学性质相同
C.单质中只含有一种元素,只含有一种元素的纯净物质一定是单质
D.置换反应中一定有单质生成,则有单质生成的化学反应一定是置换反应
2.(本题3分)下列有关盐酸和硫酸的说法正确的是
A.打开浓盐酸的瓶塞,观察到有白烟
B.浓硫酸可以做干燥剂是因为有脱水性
C.实验室可以用石灰石和稀硫酸制取二氧化碳
D.浓盐酸和浓硫酸敞口放置一段时间后,溶质质量分数都会变小
3.(本题3分)下列图像分别与选项中的操作相对应,其中合理的是
A.在密闭容器内加热汞得到氧化汞
B.在密闭装置内点燃过量红磷测定空气中氧气的含量
C.久置于空气中未经打磨的铝片与盐酸反应
D.将一定质量的氧化钙加入饱和石灰水中,再恢复至室温
4.(本题3分)烧碱的化学式是
A.NaOH B.NaCl C.Ca(OH)2 D.CaO
5.(本题3分)化学是以实验为基础的科学,下列化学实验操作正确的是
A.取固体药品 B.倾倒液体
C.振荡试管 D.稀释浓硫酸
6.(本题3分)化学是以实验为基础的科学,化学小组设计的实验能达到目的的是
A.图A是验证二氧化碳的密度比空气大
B.图B是验证空气中氧气的含量
C.图C是配制100mL20%NaCl
D.图D是检验未知液是否是碱溶液
7.(本题3分)下列物质放在敞口容器中一段时间后,因为变质而质量增加的是( )
A.碳酸钙 B.浓盐酸 C.氢氧化钠 D.浓硫酸
8.(本题3分)下列对实验意外事故的处理错误的是
A.如果不慎将氢氧化钠溶液沾到皮肤上,要用较多的水冲洗,再涂上盐酸溶液
B.实验药液溅入眼睛,立即用水冲洗,切不可用手揉搓
C.酒精灯洒出的酒精在桌上燃烧,立即用湿布或沙子扑灭
D.浓硫酸沾到皮肤上,先用布擦试后,再用大量的水冲洗,再涂上3%-5%的碳酸氢钠溶液
9.(本题3分)使用酸、碱等腐蚀性药品时,必须按照操作规程进行。下列处理方法错误的是( )
A.有腐蚀性的药液溅入眼睛内,要立即用水冲洗,切不可用手揉搓
B.稀酸飞溅到皮肤上,立即用大量的水冲洗,再涂上3%~5%的碳酸氢钠溶液
C.不小心打翻了燃着的酒精灯,应立即浇水来熄灭桌子上燃着的酒精
D.氢氧化钠溶液溅在皮肤上,先用水冲洗后,再涂上硼酸溶液
10.(本题3分)下列四种物质久置空气中,质量增加且没有新物质生成的是( )
A.氨水 B.烧碱 C.浓硫酸 D.浓盐酸
二、判断题(共15分)
11.(本题3分)酸溶液能使紫色石蕊溶液变红色,则稀盐酸能使紫色石蕊溶液变成红色( )
12.(本题3分)用氢氧化钠溶液除去二氧化碳中的氯化氢气体( )
13.(本题3分)酸溶液具有相似化学性质的原因是都含有氢元素( )
14.(本题3分)稀硫酸稀释将水沿器壁慢慢注入浓硫酸中。( )
15.(本题3分)浓盐酸稀释后可以用来给金属除锈( )
三、填空题(共15分)
16.(本题3分)盐酸是重要的化工原料,也是实验室中最常用的化学试剂之一、
(1)用质量分数为37%的浓盐酸配制1000g质量分数为0.37%(pH约为1)的稀盐酸。
①所配稀盐酸中溶质的质量为_______g,所需浓盐酸的质量为_______g。
②已知浓盐酸密度为1.19g/cm3,量取上述所需浓盐酸用到的仪器是_______(填标号)。
A.10mL量筒 B.50mL量筒 C.试管 D.胶头滴管
(2)取少量氢氧化钙粉末于试管中,加入2mL水,振荡,得到白色浑浊液,滴加1滴酚酞溶液,再滴加稀盐酸至反应完全,可观察到的现象是_______。
(3)取等质量的铁片和铁粉放入两支试管中,分别加入相同体积相同浓度的稀盐酸。
①铁与稀盐酸反应的化学方程式为_______。
②如图示意图中,与实验结果相符的是_______(填标号)。
17.(本题3分)某课外活动中,学生利用如图所示的材料完成探究实验,杠杆已调至平衡。
(1)较长时间后,左边铁粉布包下降,是因为铁粉与_____发生了反应。
(2)将铁粉换成下列物质中的_____(填序号),杠杆也会出现相似现象。
A NaCl B NaOH C CaO
(3)虽然杠杆失去平衡,但以上涉及的化学反应都遵循质量守恒定律,反应前后_____的种类、数目、质量都没有改变。
18.(本题3分)将含有氮气、一氧化碳、氢气、二氧化碳和少量水蒸气的混合气体,随机依次通入以下四个装置。(每个装置只通过一次,且反应或吸收充分。碳可以和水蒸气在一定条件下生成一氧化碳和氢气)
(1)若最终剩余气体中只含有一种物质,则一定是______。(填写化学式)
(2)若最终只剩余氮气和水,则连接顺序可能为______。
(3)若连接顺序为甲乙丙丁,则最终剩余气体为______。
19.(本题3分)取食用的鸡爪做如图实验,说明氢氧化钠具有__性.如果不慎将氢氧化钠溶液沾到皮肤上,采取措施是__
20.(本题3分)水是一种重要的资源,根据你所学的知识回答下列问题。
(1)在日常生活中,人们常用________来区分硬软水。
(2)自来水厂常用活性炭来净水,活性炭净水是利用活性炭的_________ 作用。
(3)水电解过程中发生变化的微粒是_________ 。
(4)实验室稀释浓硫酸时,应将_________沿烧杯壁缓缓地注入盛有________的烧杯中。
(5)用湿抹布扑盖实验桌上燃烧的酒精,其主要灭火原理是_________。
四、综合应用题(共40分)
21.(本题10分)经脱硫、脱氮净化后的水煤气中含有CO、CO2、H2和水蒸气中的一种或多种。为了检验该气体的成分,并测定某氧化铜样品(含少量铜)中氧化铜的质量分数,同学们设计了如图一所示实验,实线框内仪器待组装,如图二所示(部分夹持仪器已略去)。
已知:无水硫酸铜遇水由白色变为蓝色,碱石灰由氢氧化钠和氧化钙组成。
回答问题:
(1)实验前连接装置并检查____________依次称量氧化铜样品和装置G(含试剂)的质量,分别记为W1和W2。
(2)图一实线框内装置的正确连接顺序是a-_________(填导管口序号)。
(3)加热前,当通入水煤气时,A、B两装置中均有明显的现象,装置B中发生反应的化学方程式为_________。
(4)加热过程中,同学们观察到__________由此判断原气体中含有CO。
(5)待氧化铜样品完全反应后,冷却,再依次称量硬质玻璃管中剩余固体和装置G(含试剂)的质量,分别记为W3和W4,样品中氧化铜的质量分数为___________。
22.(本题15分)取久置敞口放置的氢氧化钠溶液于烧杯中,倒入一定量的稀硫酸充分反应。为探究反应后所得溶液X的成分,兴趣小组进行了如图实验(所加试剂均足量)。
(1)产生的无色气体是_______。
(2)溶液X的溶质是_______。(填写化学式)
(3)计算溶液X中硫酸钠的质量。
(4)设计实验将滤液A变成纯净的氯化钠晶体,请简述你的实验操作步骤_______。
23.(本题15分)下图是实验室常用气体制备装置,据图回答问题:
(1)用A装置制取氧气的化学方程式是_________________。选择D装置收集氧气是因为_________。将带火星的木炭伸入盛有氧气的集气瓶中,木炭剧烈燃烧,发出白光,说明氧气能________,该反应的化学方程式为_____________。
(2)实验室制取氨气:Ca(OH)2(固)+2NH4Cl(固)CaCl2(固)+2H2O+2NH3↑,要制取并收集干燥的氨气,所选装置正确的连接顺序是( )→( )→( )(填字母代号)。
为探究氨气的性质,按下图装置进行实验。观察到黑色粉末变红,白色无水硫酸铜变蓝,同时反应中还有一种气体单质生成。
【查阅资料】Cu2O是红色,易与稀硫酸反应:Cu2O+H2SO4==CuSO4+Cu+H2O。
【提出问题】得到的红色物质是什么?
(3)【猜想】①是Cu;②是Cu2O;③是______。
若猜想①成立,玻璃管中发生反应的化学方程式为__________________,说明NH3具有______性。
(4)【设计实验】请你设计一个简单的实验来验证红色物质中是否存在Cu2O______________。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.D
3.A
4.A
5.A
6.A
7.C
8.A
9.C
10.C
11.正确
12.错误
13.错误
14.错误
15.正确
16.(1) 3.7 10 AD
(2)溶液由红色变为无色
(3)
D
17. 水和氧气 BC 原子
18.(1)N2
(2)甲丙丁乙
(3)N2、CO2、H2O
19. 腐蚀 要立即用大量水冲洗,然后涂上硼酸溶液
20. 肥皂水 吸附 水分子 液硫酸 水 隔绝氧气
21.(1)装置气密性
(2)e-f-c-d-b
(3)
(4)装置F中澄清石灰水变浑浊
(5)
22.(1)CO2
(2)NaOH、Na2CO3、Na2SO4
(3)设溶液X中硫酸钠的质量为x。
答:溶液X中硫酸钠的质量为2.84g。
(4)加入足量的稀盐酸,再加热浓缩、蒸发结晶
23.(1) 密度比空气大 支持燃烧(或助燃) C+O2CO2
(2) A G E
(3) Cu和Cu2O 2NH3+3CuO3Cu+3H2O+N2 还原
(4)取少量红色物质放于试管,向试管中倒入稀硫酸,若溶液逐渐变为蓝色则有Cu2O,若溶液不变色,则无Cu2O
答案第1页,共2页
答案第1页,共2页
同课章节目录
