第一章 第一节 第2课时 有机化合物中的共价键及同分异构现象课件(共36张PPT)2022-2023学年下学期高二化学人教版(2019)选择性必修3
文档属性
| 名称 | 第一章 第一节 第2课时 有机化合物中的共价键及同分异构现象课件(共36张PPT)2022-2023学年下学期高二化学人教版(2019)选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 7.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-04 00:00:00 | ||
图片预览




文档简介
(共36张PPT)
第一章 有机化合物的结构特点与研究方法
第一节 有机化合物的结构特点
第2课时 有机物中的共价键和同分异构现象
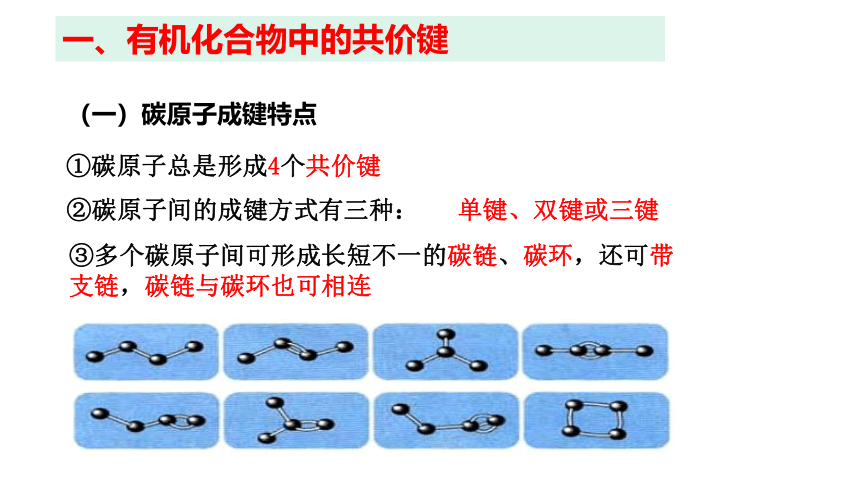
(一)碳原子成键特点
①碳原子总是形成4个共价键
②碳原子间的成键方式有三种:
单键、双键或三键
③多个碳原子间可形成长短不一的碳链、碳环,还可带支链,碳链与碳环也可相连
一、有机化合物中的共价键
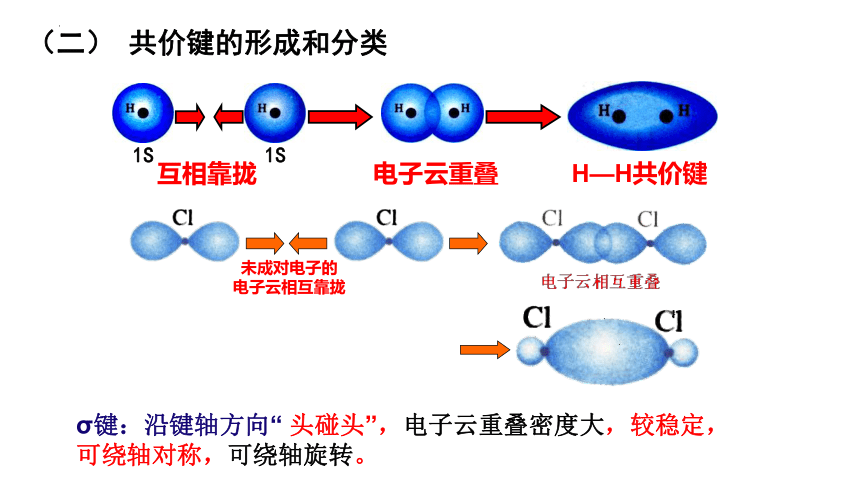
(二) 共价键的形成和分类
1S
1S
互相靠拢
电子云重叠
H—H共价键
未成对电子的
电子云相互靠拢
σ键:沿键轴方向“ 头碰头”,电子云重叠密度大,较稳定,
可绕轴对称,可绕轴旋转。
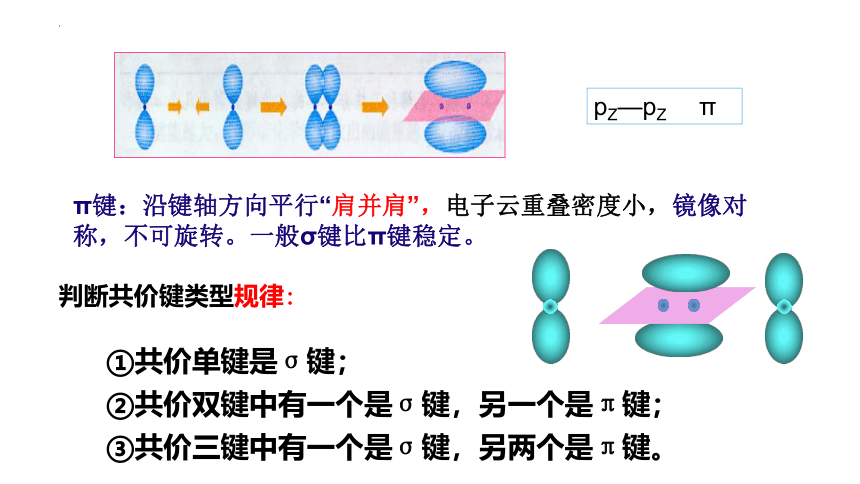
pZ—pZ π
π键:沿键轴方向平行“肩并肩”,电子云重叠密度小,镜像对称,不可旋转。一般σ键比π键稳定。
判断共价键类型规律:
①共价单键是σ键;
②共价双键中有一个是σ键,另一个是π键;
③共价三键中有一个是σ键,另两个是π键。
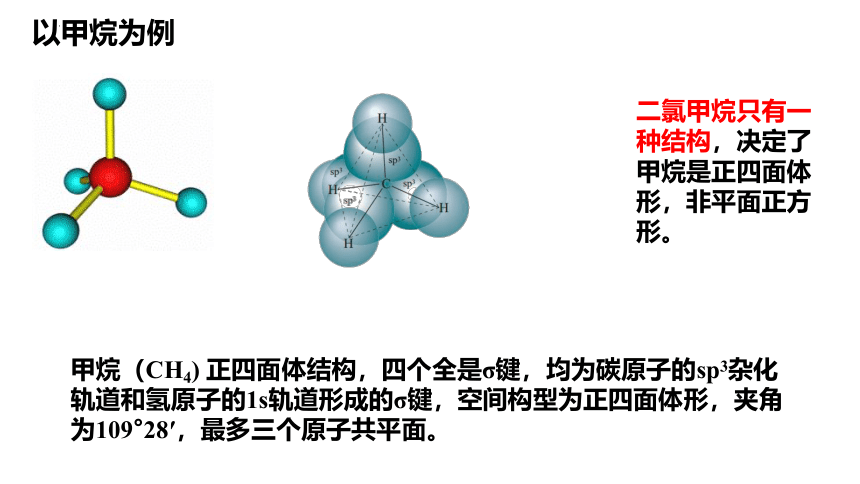
以甲烷为例
甲烷(CH4) 正四面体结构,四个全是σ键,均为碳原子的sp3杂化轨道和氢原子的1s轨道形成的σ键,空间构型为正四面体形,夹角为109°28′,最多三个原子共平面。
二氯甲烷只有一种结构,决定了甲烷是正四面体形,非平面正方形。
乙烯分子中的所有原子都在同一平面内,键角约为120°。
以乙烯为例
乙烯中,两个碳原子均以sp2杂化轨道和氢原子的1s轨道及另一个碳原子的sp2杂化轨道进行重叠,形成4个C-H σ键与一个C-C σ键,两个碳原子为杂化的p轨道以“肩并肩”的形式形成π键。
乙烯中,σ键与π键数目之比为5:1。
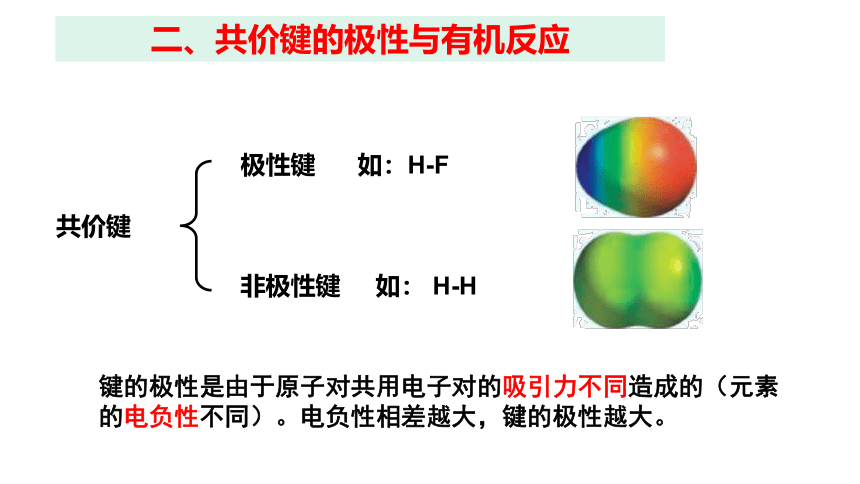
二、共价键的极性与有机反应
共价键
极性键 如:H-F
非极性键 如: H-H
键的极性是由于原子对共用电子对的吸引力不同造成的(元素的电负性不同)。电负性相差越大,键的极性越大。
结论:原子间电负性的差异越大→共用电子对偏移的程度越大→共价键极性越强,在反应中越容易发生断裂→官能团及其邻近的化学键往往是发生化学反应的活性部位
向两只分别盛有蒸馏水和无水乙醇的烧杯中各加入同样大小的钠(约绿豆大),观察现象。
实验1-1 乙醇与钠的反应
水和钠 无水乙醇和钠
实验原理
实验现象
剧烈程度 剧烈程度:H2O>CH3CH2OH
受乙基的影响,乙醇分子中氢氧键的极性比水分子氢氧键的极性弱,
乙醇比水更难电离出氢离子
2Na+2H2O=2NaOH+H2↑
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
浮、熔、游、响、红
钠沉入底部,有气体产生,最终钠粒消失,液体仍为无色透明。
如果钠快放入乙酸中,反应现象会如何?为什么?
钠与乙酸反应更剧烈,甚至会有火焰产生。
乙酸中羰基的吸电子效应,其分子中的H-O的极性比水中的H-O强,更易与钠发生反应。乙酸具有弱酸性。
2.试从键的极性强弱角度比较甲酸、乙酸、丙酸的酸性强弱?
甲酸>乙酸>丙酸
【解释】烃基为推电子基团,烃基越长推电子效应越大,使羧基中的羟基极性越小,羧酸的酸性越弱。
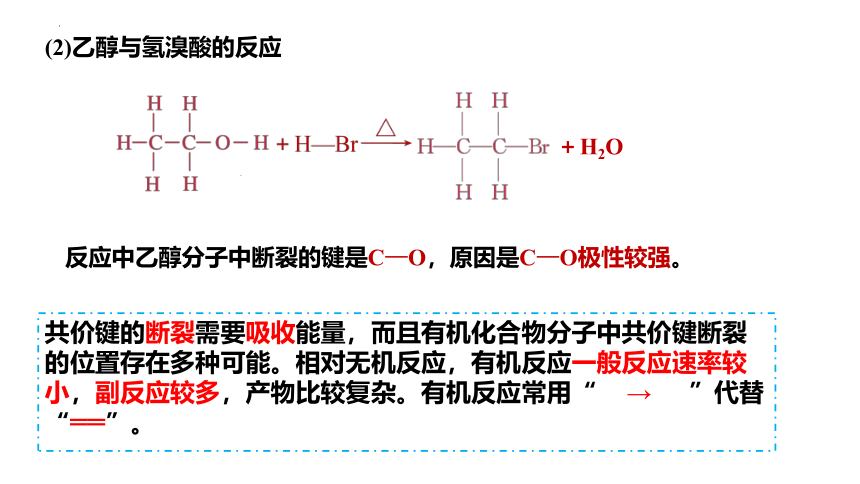
共价键的断裂需要吸收能量,而且有机化合物分子中共价键断裂的位置存在多种可能。相对无机反应,有机反应一般反应速率较小,副反应较多,产物比较复杂。有机反应常用“ → ”代替“══”。
(2)乙醇与氢溴酸的反应
+H2O
反应中乙醇分子中断裂的键是C—O,原因是C—O极性较强。
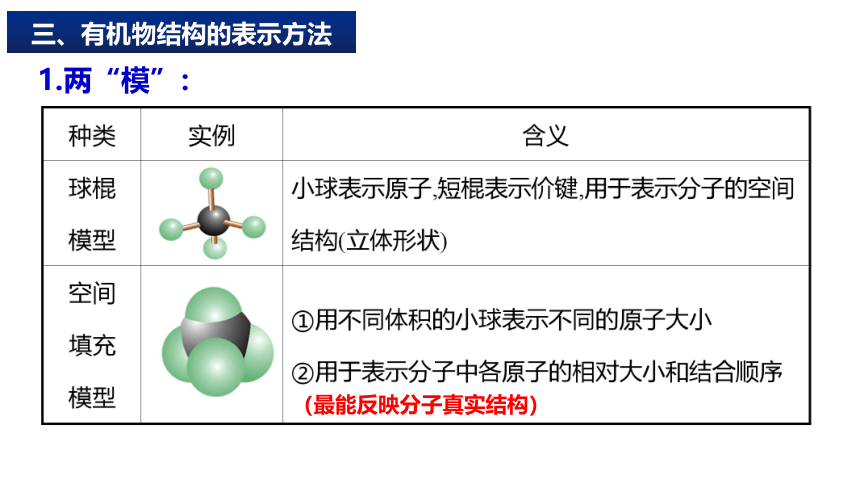
1.两“模”:
(最能反映分子真实结构)
三、有机物结构的表示方法
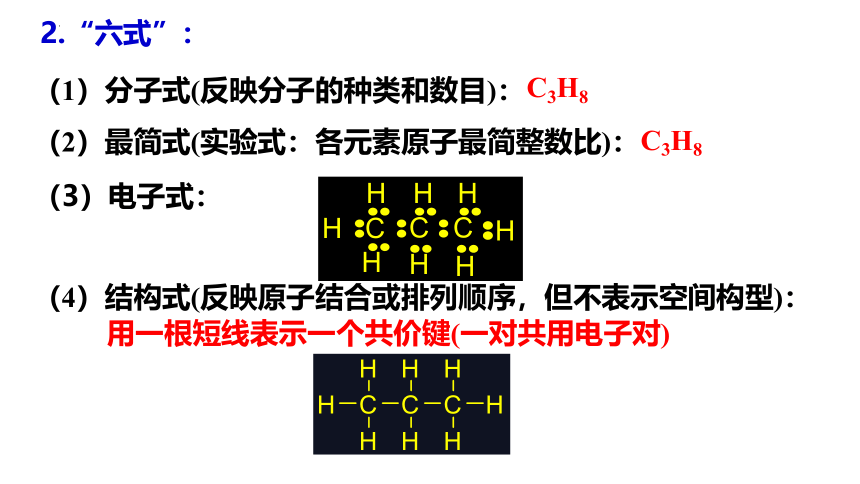
用一根短线表示一个共价键(一对共用电子对)
2.“六式”:
(1)分子式(反映分子的种类和数目):
(2)最简式(实验式:各元素原子最简整数比):
C3H8
C3H8
(3)电子式:
(4)结构式(反映原子结合或排列顺序,但不表示空间构型):
(5)结构简式:
(省略与合并)
省略C H键,把同一碳原子上的H合并
CH3 CH2 CH2 CH CH3
CH3
省略横线上C C键
CH3CH2CH2CHCH3
CH3
或:CH3(CH2)2CH(CH3)2
书写结构简式注意:
①表示原子间形成单键的“—”可以省略
②碳碳双键( C=C)和碳碳三键(C≡C)不能省略,
③约定俗成的可省略的碳氧双键:-CHO、-COOH、-COO-(酯基)、-CONH-(肽键)等。
(结构简式)
CH3CH=CH2
C-C=C
(碳架结构)
(键线式)
键线式的书写
由碳架式省略C后即成。
(6)键线式:
CH3CH=CHCH3
CH3CHClCH2CH3
Cl
注意:
①用键线表示碳架,端点、拐点、交叉点是C。
只要求表示出碳碳键(单键、双键、三键)
及与碳原子相连的基团。
②两根单键或单键和双键之间夹角120°,
单键和三键之间夹角180°。
③—OH、—CHO、—COOH、—X等官能团中的C、H保留,
杂原子及杂原子上的氢原子保留。
例1:写出下列有机物的键线式:
教材P9 资料卡片
有机物分子组成和结构的表示方法
分子式
最简式
电子式
结构式
结构简式
键线式
碳骨架式
球棍模型
空间填充模型
只表示分子的组成,不能反映物质的结构.
只表示分子的部分组成,不能反映物质的结构.
既能表示分子的组成,
又能反映物质的结构.
但书写麻烦!
既能表示分子的组成,又能反映物质的结构.
只能表示碳原子的连接方式,不能表示分子组成!
既能表示分子的组成,又能反映物质的结构.
一般只用于题目分析,正规的书写表达时不用!
常用
归纳总结
C4H10为什么有两种不同的结构呢?
三、有机化合物中的同分异构现象
二、有机化合物的同分异构现象
(一)同分异构现象与同分异构体
同分异构体现象:化合物具有相同的分子式,但具有不同的结构现象
具有同分异构体现象的化合物互称为同分异构体。
注意
五个相同:
相同分子式、相同相对分子质量、相同最简式、相同分子式、相同质量分数、
两个不同:
结构不同、性质不同
构造
碳架
位置
官能团
立体
顺反
对映
手性异构
(二)、同分异构体的类型
课本P9 表1-2 有机化合物的构造异构现象
【例2】下列哪些属于同分异构体,是同分异构体的属于何种异构?
① CH3COOH和 HCOOCH3
② CH3CH2CHO和 CH3COCH3
③ CH3CH2CH2OH和CH3CHOHCH3
④ CH3—CH—CH3和 CH3 CH2CH2 CH3
⑤ CH3CH=CHCH2CH3和 CH3CH2CH = CHCH3
官能团异构
官能团异构
碳链异构
CH3
位置异构
同种物质
⑥
二、碳架异构的书写方法
减碳法
减碳对称法:先确定碳链结构,再补氢原子。
【例3】写出己烷(C6H14)的同分异构体的结构简式。
(2)主链减少1个碳:主链为5个碳原子,支链有1个碳原子
(1)一条直链: 主链为6个碳原子,没有支链
主链由长到短;位置由心到边;
(3)主链减少2个碳: 主链为4个碳原子,支链有2个碳原子
支链由整到散;
注意:
①.找中心对称线,对称C支链不重复
②.减C数目不超过C原子数的1/2
③.补H(C 4个价键)
④.甲基不连主链两端乙基不连主链两端的第二位
丙基不连主链两端的第三位…………
⑤. 支链由整到散,苯环中先从邻、间到对位。
【练习】1. 分子式为C6H14的烷烃在结构式中含有3个甲基的同分异构体有( )个
(A)2个 (B)3个 (C)4个 (D)5个
2. 写出庚烷C7H16同分异构体的碳链骨架。
√
共9种
【练习2】写出庚烷(C7H16)同分异构体的碳链骨架。
C—C—C—C—C—C —C
C—C—C—C—C —C
C
C—C—C—C—C —C
C
C— C—C—C—C
C
C
C—C—C—C—C
C
C
C—C—C—C
C
C
C
C— C—C—C—C
C
C
C— C—C—C—C
C
C
C— C—C—C—C
C
C
碳原子数目越多,同分异构体越多
碳原子数 1 2 3 4 5 6 7 8 9 10
烷烃同分异构体数 1 1 1 2 3 5 9 18 35 75
碳原子数 11 12 … 15 20 同分异构体数 159 355 … 4347 366319
三、位置异构的书写方法
异构类型 实例 书写方法
位置异构 C4H8:
C6H4Cl2: 官能团的位置不同
表3-位置异构现象
1-丁烯
2-丁烯
CH2=CH—CH2—CH3
1
2
3
4
CH3—CH=CH—CH3
1
2
3
4
邻二氯苯
间二氯苯
对二氯苯
取代法
插入法
定一移一法
定二移一法
三、位置异构的书写方法
等效氢法
1.等效氢法:有几种氢原子,就有多少种一取代物。
①
②
碳架异构
位置异构
①
②
③ ④
【例2】写出一氯丁烷(C4H9Cl)的同分异构体的结构简式。
三、位置异构的书写方法
等效氢法
必备知识:等效氢
同一碳原子上的氢
乙烷
同一碳原子上所连甲基上的氢
位于对称位置的氢
苯环上的氢
等效氢
新戊烷
【例3】下列物质的一溴代物有几种?
3
CH3 — CH — CH2 — CH — CH3
CH3
CH3
4
CH3 — C — CH2 — CH — CH3
CH3
CH3
CH3
2
CH3
CH3
3
(2)应用:
判断一卤代物的同分异构体的数目。若某烃中有几种氢原子,则其一卤代物就有几种。
烃基 甲基 (—CH3) 乙基 (—C2H5) 丙基 (—C3H7) 丁基 (—C4H9) 戊基
(—C5H11)
种类
1
1
2
4
8
【例4】已知C4H9Cl的同分异构体数目为4种,则分子式为C4H10O的醇的异构体有_____种
【练习3】已知C5H11OH有8种同分异构体,则分子式为C5H10O的醛有 种,分子式为C6H12O2的羧酸有 种。
插入法
三、位置异构的书写方法
2.插入法:先写碳骨架异构,再插入官能团。
【例5】写出丁烯(C4H8,含有4个碳原子和一个 )的同分异构体的结构简式。
位置异构
碳架异构
①
②
【练习4】分子式为C5H10的烯烃有( )
A.3种 B.4种 C.5种 D.6种
适用于烯烃、炔烃、醚、酮、酯等的异构
三、位置异构的书写方法
定一移一法
对于二元取代物,一般选择定一移一法即固定一个取代基的位置,再移动另一个取代基,以确定同分异构体的数目。
【例5】分子式为C3H6Cl2的同分异构体共有( )
A、3种 B、4种 C、5种 D、6种
第一步:写出一取代物的结构。
第二步:在一取代物的结构中,逐步加入另一个取代基。
(注意:重复的要去掉)
B
一氯代物 二氯代物
⑦ ⑧ ⑨
【练习4】写出二氯丁烷(C4H8Cl2)的同分异构体的结构简式。
⑤
⑥
⑦
⑧
⑨
①
②
③
④
① ② ③ ④
⑤ ⑥
与②号重复
与③号重复
与⑧号重复
↓
↓
↓
共9种
1
3
3
3
1
1
C6H5Cl
C6H4Cl2
C6H3Cl3
C6H2Cl4
C6HCl5
C6Cl6
【例6】下列苯的衍生物物质有几种同分异构体?
换元法:烃的n元取代物与(m-n)元取代物种类数相等,m代表烃中H原子数目
1.同分异构体的书写顺序
(1)首先考虑官能团异构,符合同一分子式可能有哪几类不同的有机物,确定先写哪一类有机物。
(2)在确定另一类具有相同官能团有机物的同分异构体时,应先考虑碳链异构。
(3)在同一官能团的基础上,再考虑官能团的位置异构。
特别提醒
官能团异构——碳链异构——位置异构
【小结】常见的官能团异构现象
序 号 类 别 通 式
1 烯烃 CnH2n
环烷烃 2 炔烃 CnH2n-2
二烯烃 3 饱和一元脂肪醇 CnH2n+2O
饱和醚 4 饱和一元脂肪醛 CnH2nO
酮 5 饱和羧酸 CnH2nO2
饱和羧酸酯 【练习1】进行一氯取代反应后,只能生成三种沸点不同的产物的烷烃是 ( )
A (CH3) 2 CH CH2CH2CH3
B (CH3 CH2) 2 CHCH3
C (CH3) 2 CH CH (CH3) 2
D (CH3) 3 C CH2CH3
D
【练习2】C3H8的分子中有六个氢原子被氯原子取代,可能的同分异构体有 ( )
A.3种 B.4种
C.5种 D.6种
B
【练习3】某烃的一种同分异构体只能生成一种一氯代物,该烃的分子式可以是( )
A.C3H8 B. C4H10 C. C5H12 D. CH4
C
【课后练习】
第一章 有机化合物的结构特点与研究方法
第一节 有机化合物的结构特点
第2课时 有机物中的共价键和同分异构现象
(一)碳原子成键特点
①碳原子总是形成4个共价键
②碳原子间的成键方式有三种:
单键、双键或三键
③多个碳原子间可形成长短不一的碳链、碳环,还可带支链,碳链与碳环也可相连
一、有机化合物中的共价键
(二) 共价键的形成和分类
1S
1S
互相靠拢
电子云重叠
H—H共价键
未成对电子的
电子云相互靠拢
σ键:沿键轴方向“ 头碰头”,电子云重叠密度大,较稳定,
可绕轴对称,可绕轴旋转。
pZ—pZ π
π键:沿键轴方向平行“肩并肩”,电子云重叠密度小,镜像对称,不可旋转。一般σ键比π键稳定。
判断共价键类型规律:
①共价单键是σ键;
②共价双键中有一个是σ键,另一个是π键;
③共价三键中有一个是σ键,另两个是π键。
以甲烷为例
甲烷(CH4) 正四面体结构,四个全是σ键,均为碳原子的sp3杂化轨道和氢原子的1s轨道形成的σ键,空间构型为正四面体形,夹角为109°28′,最多三个原子共平面。
二氯甲烷只有一种结构,决定了甲烷是正四面体形,非平面正方形。
乙烯分子中的所有原子都在同一平面内,键角约为120°。
以乙烯为例
乙烯中,两个碳原子均以sp2杂化轨道和氢原子的1s轨道及另一个碳原子的sp2杂化轨道进行重叠,形成4个C-H σ键与一个C-C σ键,两个碳原子为杂化的p轨道以“肩并肩”的形式形成π键。
乙烯中,σ键与π键数目之比为5:1。
二、共价键的极性与有机反应
共价键
极性键 如:H-F
非极性键 如: H-H
键的极性是由于原子对共用电子对的吸引力不同造成的(元素的电负性不同)。电负性相差越大,键的极性越大。
结论:原子间电负性的差异越大→共用电子对偏移的程度越大→共价键极性越强,在反应中越容易发生断裂→官能团及其邻近的化学键往往是发生化学反应的活性部位
向两只分别盛有蒸馏水和无水乙醇的烧杯中各加入同样大小的钠(约绿豆大),观察现象。
实验1-1 乙醇与钠的反应
水和钠 无水乙醇和钠
实验原理
实验现象
剧烈程度 剧烈程度:H2O>CH3CH2OH
受乙基的影响,乙醇分子中氢氧键的极性比水分子氢氧键的极性弱,
乙醇比水更难电离出氢离子
2Na+2H2O=2NaOH+H2↑
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
浮、熔、游、响、红
钠沉入底部,有气体产生,最终钠粒消失,液体仍为无色透明。
如果钠快放入乙酸中,反应现象会如何?为什么?
钠与乙酸反应更剧烈,甚至会有火焰产生。
乙酸中羰基的吸电子效应,其分子中的H-O的极性比水中的H-O强,更易与钠发生反应。乙酸具有弱酸性。
2.试从键的极性强弱角度比较甲酸、乙酸、丙酸的酸性强弱?
甲酸>乙酸>丙酸
【解释】烃基为推电子基团,烃基越长推电子效应越大,使羧基中的羟基极性越小,羧酸的酸性越弱。
共价键的断裂需要吸收能量,而且有机化合物分子中共价键断裂的位置存在多种可能。相对无机反应,有机反应一般反应速率较小,副反应较多,产物比较复杂。有机反应常用“ → ”代替“══”。
(2)乙醇与氢溴酸的反应
+H2O
反应中乙醇分子中断裂的键是C—O,原因是C—O极性较强。
1.两“模”:
(最能反映分子真实结构)
三、有机物结构的表示方法
用一根短线表示一个共价键(一对共用电子对)
2.“六式”:
(1)分子式(反映分子的种类和数目):
(2)最简式(实验式:各元素原子最简整数比):
C3H8
C3H8
(3)电子式:
(4)结构式(反映原子结合或排列顺序,但不表示空间构型):
(5)结构简式:
(省略与合并)
省略C H键,把同一碳原子上的H合并
CH3 CH2 CH2 CH CH3
CH3
省略横线上C C键
CH3CH2CH2CHCH3
CH3
或:CH3(CH2)2CH(CH3)2
书写结构简式注意:
①表示原子间形成单键的“—”可以省略
②碳碳双键( C=C)和碳碳三键(C≡C)不能省略,
③约定俗成的可省略的碳氧双键:-CHO、-COOH、-COO-(酯基)、-CONH-(肽键)等。
(结构简式)
CH3CH=CH2
C-C=C
(碳架结构)
(键线式)
键线式的书写
由碳架式省略C后即成。
(6)键线式:
CH3CH=CHCH3
CH3CHClCH2CH3
Cl
注意:
①用键线表示碳架,端点、拐点、交叉点是C。
只要求表示出碳碳键(单键、双键、三键)
及与碳原子相连的基团。
②两根单键或单键和双键之间夹角120°,
单键和三键之间夹角180°。
③—OH、—CHO、—COOH、—X等官能团中的C、H保留,
杂原子及杂原子上的氢原子保留。
例1:写出下列有机物的键线式:
教材P9 资料卡片
有机物分子组成和结构的表示方法
分子式
最简式
电子式
结构式
结构简式
键线式
碳骨架式
球棍模型
空间填充模型
只表示分子的组成,不能反映物质的结构.
只表示分子的部分组成,不能反映物质的结构.
既能表示分子的组成,
又能反映物质的结构.
但书写麻烦!
既能表示分子的组成,又能反映物质的结构.
只能表示碳原子的连接方式,不能表示分子组成!
既能表示分子的组成,又能反映物质的结构.
一般只用于题目分析,正规的书写表达时不用!
常用
归纳总结
C4H10为什么有两种不同的结构呢?
三、有机化合物中的同分异构现象
二、有机化合物的同分异构现象
(一)同分异构现象与同分异构体
同分异构体现象:化合物具有相同的分子式,但具有不同的结构现象
具有同分异构体现象的化合物互称为同分异构体。
注意
五个相同:
相同分子式、相同相对分子质量、相同最简式、相同分子式、相同质量分数、
两个不同:
结构不同、性质不同
构造
碳架
位置
官能团
立体
顺反
对映
手性异构
(二)、同分异构体的类型
课本P9 表1-2 有机化合物的构造异构现象
【例2】下列哪些属于同分异构体,是同分异构体的属于何种异构?
① CH3COOH和 HCOOCH3
② CH3CH2CHO和 CH3COCH3
③ CH3CH2CH2OH和CH3CHOHCH3
④ CH3—CH—CH3和 CH3 CH2CH2 CH3
⑤ CH3CH=CHCH2CH3和 CH3CH2CH = CHCH3
官能团异构
官能团异构
碳链异构
CH3
位置异构
同种物质
⑥
二、碳架异构的书写方法
减碳法
减碳对称法:先确定碳链结构,再补氢原子。
【例3】写出己烷(C6H14)的同分异构体的结构简式。
(2)主链减少1个碳:主链为5个碳原子,支链有1个碳原子
(1)一条直链: 主链为6个碳原子,没有支链
主链由长到短;位置由心到边;
(3)主链减少2个碳: 主链为4个碳原子,支链有2个碳原子
支链由整到散;
注意:
①.找中心对称线,对称C支链不重复
②.减C数目不超过C原子数的1/2
③.补H(C 4个价键)
④.甲基不连主链两端乙基不连主链两端的第二位
丙基不连主链两端的第三位…………
⑤. 支链由整到散,苯环中先从邻、间到对位。
【练习】1. 分子式为C6H14的烷烃在结构式中含有3个甲基的同分异构体有( )个
(A)2个 (B)3个 (C)4个 (D)5个
2. 写出庚烷C7H16同分异构体的碳链骨架。
√
共9种
【练习2】写出庚烷(C7H16)同分异构体的碳链骨架。
C—C—C—C—C—C —C
C—C—C—C—C —C
C
C—C—C—C—C —C
C
C— C—C—C—C
C
C
C—C—C—C—C
C
C
C—C—C—C
C
C
C
C— C—C—C—C
C
C
C— C—C—C—C
C
C
C— C—C—C—C
C
C
碳原子数目越多,同分异构体越多
碳原子数 1 2 3 4 5 6 7 8 9 10
烷烃同分异构体数 1 1 1 2 3 5 9 18 35 75
碳原子数 11 12 … 15 20 同分异构体数 159 355 … 4347 366319
三、位置异构的书写方法
异构类型 实例 书写方法
位置异构 C4H8:
C6H4Cl2: 官能团的位置不同
表3-位置异构现象
1-丁烯
2-丁烯
CH2=CH—CH2—CH3
1
2
3
4
CH3—CH=CH—CH3
1
2
3
4
邻二氯苯
间二氯苯
对二氯苯
取代法
插入法
定一移一法
定二移一法
三、位置异构的书写方法
等效氢法
1.等效氢法:有几种氢原子,就有多少种一取代物。
①
②
碳架异构
位置异构
①
②
③ ④
【例2】写出一氯丁烷(C4H9Cl)的同分异构体的结构简式。
三、位置异构的书写方法
等效氢法
必备知识:等效氢
同一碳原子上的氢
乙烷
同一碳原子上所连甲基上的氢
位于对称位置的氢
苯环上的氢
等效氢
新戊烷
【例3】下列物质的一溴代物有几种?
3
CH3 — CH — CH2 — CH — CH3
CH3
CH3
4
CH3 — C — CH2 — CH — CH3
CH3
CH3
CH3
2
CH3
CH3
3
(2)应用:
判断一卤代物的同分异构体的数目。若某烃中有几种氢原子,则其一卤代物就有几种。
烃基 甲基 (—CH3) 乙基 (—C2H5) 丙基 (—C3H7) 丁基 (—C4H9) 戊基
(—C5H11)
种类
1
1
2
4
8
【例4】已知C4H9Cl的同分异构体数目为4种,则分子式为C4H10O的醇的异构体有_____种
【练习3】已知C5H11OH有8种同分异构体,则分子式为C5H10O的醛有 种,分子式为C6H12O2的羧酸有 种。
插入法
三、位置异构的书写方法
2.插入法:先写碳骨架异构,再插入官能团。
【例5】写出丁烯(C4H8,含有4个碳原子和一个 )的同分异构体的结构简式。
位置异构
碳架异构
①
②
【练习4】分子式为C5H10的烯烃有( )
A.3种 B.4种 C.5种 D.6种
适用于烯烃、炔烃、醚、酮、酯等的异构
三、位置异构的书写方法
定一移一法
对于二元取代物,一般选择定一移一法即固定一个取代基的位置,再移动另一个取代基,以确定同分异构体的数目。
【例5】分子式为C3H6Cl2的同分异构体共有( )
A、3种 B、4种 C、5种 D、6种
第一步:写出一取代物的结构。
第二步:在一取代物的结构中,逐步加入另一个取代基。
(注意:重复的要去掉)
B
一氯代物 二氯代物
⑦ ⑧ ⑨
【练习4】写出二氯丁烷(C4H8Cl2)的同分异构体的结构简式。
⑤
⑥
⑦
⑧
⑨
①
②
③
④
① ② ③ ④
⑤ ⑥
与②号重复
与③号重复
与⑧号重复
↓
↓
↓
共9种
1
3
3
3
1
1
C6H5Cl
C6H4Cl2
C6H3Cl3
C6H2Cl4
C6HCl5
C6Cl6
【例6】下列苯的衍生物物质有几种同分异构体?
换元法:烃的n元取代物与(m-n)元取代物种类数相等,m代表烃中H原子数目
1.同分异构体的书写顺序
(1)首先考虑官能团异构,符合同一分子式可能有哪几类不同的有机物,确定先写哪一类有机物。
(2)在确定另一类具有相同官能团有机物的同分异构体时,应先考虑碳链异构。
(3)在同一官能团的基础上,再考虑官能团的位置异构。
特别提醒
官能团异构——碳链异构——位置异构
【小结】常见的官能团异构现象
序 号 类 别 通 式
1 烯烃 CnH2n
环烷烃 2 炔烃 CnH2n-2
二烯烃 3 饱和一元脂肪醇 CnH2n+2O
饱和醚 4 饱和一元脂肪醛 CnH2nO
酮 5 饱和羧酸 CnH2nO2
饱和羧酸酯 【练习1】进行一氯取代反应后,只能生成三种沸点不同的产物的烷烃是 ( )
A (CH3) 2 CH CH2CH2CH3
B (CH3 CH2) 2 CHCH3
C (CH3) 2 CH CH (CH3) 2
D (CH3) 3 C CH2CH3
D
【练习2】C3H8的分子中有六个氢原子被氯原子取代,可能的同分异构体有 ( )
A.3种 B.4种
C.5种 D.6种
B
【练习3】某烃的一种同分异构体只能生成一种一氯代物,该烃的分子式可以是( )
A.C3H8 B. C4H10 C. C5H12 D. CH4
C
【课后练习】
