备战2023河南中考考点过关-第十单元 酸和碱 课件(共78张PPT)
文档属性
| 名称 | 备战2023河南中考考点过关-第十单元 酸和碱 课件(共78张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-06 00:00:00 | ||
图片预览










文档简介
(共78张PPT)
第十单元 酸和碱
&1& 溶液的酸碱性与
1.酸碱指示剂
酸碱指示剂的变色规律:
紫色石蕊溶液:在酸中显______色,在碱中显______色;
[紫色石蕊溶液显色口诀:酸里红(谐音:山里红),碱里蓝]
无色酚酞溶液:在酸中显______色,在碱中显______色。
(无色酚酞溶液显色口诀:遇酸色不变,遇碱红艳艳)
红
蓝
无
红
【特别提醒】 (1)指示剂的变色过程属于化学变化,是酸或碱使指示
剂变色,不是指示剂使酸或碱变色。
(2)指示剂颜色的变化,只能说明溶液显酸性或碱性,不能说明某溶液
就是酸或碱的溶液,因为有些盐溶液也显酸性或碱性。
2.溶液酸碱度的表示方法——
(1) 溶液的酸碱度常用______来表示,
(2) 溶液酸碱性与
酸性溶液的
碱性溶液的
中性溶液的
小
>
大
=
(3) 溶液
定时,用__________蘸取待测溶液滴到___________上,然后再与________
______比较,读出该溶液的
玻璃棒
标准比色卡
(4)
①了解空气污染情况:
的原因:_ _____________________(用化学方程式表示)];
②测定人体内或排出液体的
③化工生产中,许多反应要在一定
④农业生产中,农作物一般适宜在
<
【温馨提示】 酸性溶液或碱性溶液稀释过程中溶液
见题型三。
辨析易错易混·正误判断
1.酸溶液能使紫色石蕊溶液变红,则能使紫色石蕊溶液变红的一定是酸
溶液。( )
×
[解析] 能使紫色石蕊溶液变红的溶液显酸性,但不一定是酸溶液,如硝酸
铵溶液显酸性,但它是盐溶液。
2.氢氧化钠溶液和碳酸钠溶液均显碱性,都能使无色酚酞溶液变红。
( )
√
3.所有的碱都能使无色酚酞溶液变红。( )
×
[解析] 不溶于水的碱[如
自由移动的
4.只有无色酚酞溶液和紫色石蕊溶液遇酸、碱性溶液能变色。( )
×
考点过关练
1.&2& 酸碱指示剂在不同的酸碱性溶液里能显示不同的颜色,因此,酸碱指示剂可以检验溶液的酸碱性。测定溶液的
(1) [2022天津中考] 生活中一些常见物质的
中碱性最强的是( )
A.厕所清洁剂 B.食盐水 C.肥皂水 D.炉具清洁剂
D
(2) 某同学想用
的是( )
A.用干燥的
B.用干燥的
C.用干燥的
D.用湿润的
A
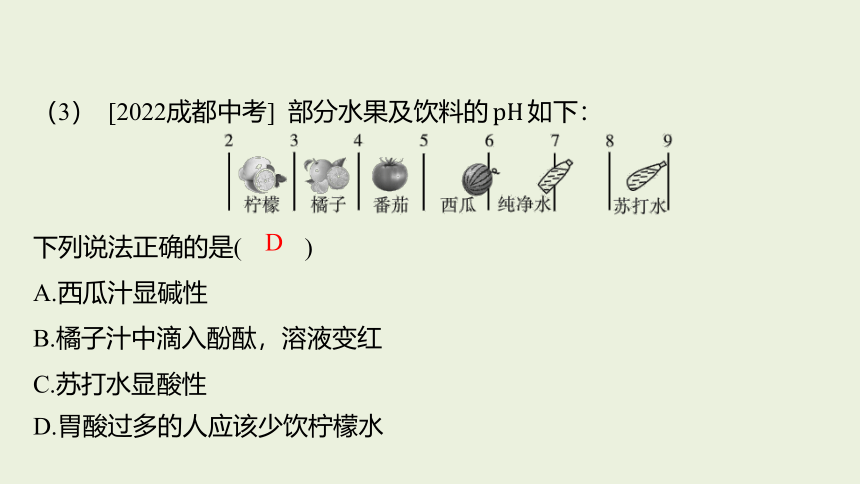
(3) [2022成都中考] 部分水果及饮料的
下列说法正确的是( )
A.西瓜汁显碱性
B.橘子汁中滴入酚酞,溶液变红
C.苏打水显酸性
D.胃酸过多的人应该少饮柠檬水
D
&3& 常见酸的性质和用途
1.概念:解离时产生的阳离子全部是______的化合物。
2.浓盐酸和浓硫酸的物理性质和用途
浓盐酸 浓硫酸
溶质(化学式) ①_______ ②_________
物理 性质 颜色状 态 无色液体 无色黏稠状液体
浓盐酸 浓硫酸
物理 性质 气味 有③__________气味 无
挥发性 有④________性(打开瓶 塞,瓶口产生大量⑤______) 不易挥发
用途
药、染料以及冶炼金属、精
炼石油和金属除锈等;
刺激性
挥发
白雾
除锈
续表
3.浓硫酸的特性
吸水性(物 理性质) 浓硫酸具有吸水性,在实验室中常用作①__________
腐蚀性(化 学性质) 浓硫酸能夺取纸张、木材等物质中的水分,生成黑色的碳,
具有强脱水作用,有强烈的②__________,如不慎将浓硫
酸沾在衣服上或皮肤上,应立即用③______________,然
后再涂上
干燥剂
腐蚀性
大量水冲洗
浓硫酸稀释:稀释浓硫酸时,一定要把④
__________沿容器内壁慢慢注入⑤______中,并
用玻璃棒不断⑥________,切不可把水倒入浓硫
酸中
. .
浓硫酸
水
搅拌
续表
4.其他常见的酸:碳酸、醋酸(常用于除水垢)、硝酸等。
5.酸溶液的通性
盐酸 硫酸
与指示剂 作用 能使石蕊溶液变红,不能使酚酞溶液变色
盐酸 硫酸
酸+活泼 金属
__________________________
铁与硫酸反应:④
_ _________________________
现象:⑤__________________
___________________
有气泡产生,溶液由无色变成浅绿色
续表
盐酸 硫酸
酸+金属 氧化物→ 盐+水 用盐酸除铁锈:⑥__________ _______________________ 现象:⑦__________________ _____________________ 氧化铜与硫酸反应:⑧_____
_________________________
_
现象:⑨_________________
____________________
红棕色固体溶解,溶液由无色变成黄色
黑色固体溶解,溶液由无色变成蓝色
续表
盐酸 硫酸
酸+碱
_________________________
____________________
现象: ________________
_____________________
蓝色固体溶解,溶液由无色变成蓝色
续表
盐酸 硫酸
酸+盐→ 新酸+新 盐 碳酸钙与稀盐酸反应: ___ __________________________ ____________________ 现象: _________________ ___________ 碳酸钠与稀硫酸反应:
_________________________
_________________________
现象: ______________
总结 稀硫酸和稀盐酸具有相似化学性质的原因是 __________________
固体逐渐溶解,有气泡产生
有气泡产生
溶液中都含有
续表
6.稀盐酸和稀硫酸的特性
(1) 稀盐酸与硝酸银反应
化学方程式:_______________________________;
现象:__________________;
应用:检验______(填离子符号)。
有白色沉淀生成
(2) 稀硫酸与硝酸钡反应
化学方程式:______________________________________;
现象:__________________;
应用:检验________(填离子符号)。
总结:酸的化学性质不完全相同的原因是________________。
有白色沉淀生成
酸根离子不同
辨析易错易混·正误判断
1.某固体中加入稀盐酸产生气体,该气体一定是
×
[解析] 活泼金属与稀盐酸反应会产生氢气。
2.酸中含有氢元素,所以含有氢元素的化合物一定是酸。( )
×
考点过关练
1.&4& 学习了酸的化学性质,某同学以稀硫酸为主题,绘制了“多
彩酸世界”思维导图。
(1) 若用
蓝
(2) 若想实现③,得到浅绿色溶液,可选用的单质是______。
铁
(3) 若选用
_ ________________________________。
(4) 根据上图,请你总结酸的通性:_____________________________
___________________________________________________________。
能使酸碱指示剂变色、能与活泼金属反应、能与金属氧化物反应、能与碱反应、能与某些盐反应
(5) (拓展)常见的酸(用化学式填空):硝酸________,食醋中含
有的酸____________,铅酸蓄电池中含有的酸_________,人体胃液中含
有的酸_______,汽水中含有的酸_________。
【归纳总结】
酸的共性
稀硫酸能够与氯化钡溶液发生复分解反应,微观实质是:
件,二者不反应。
&5& 常见碱的性质和用途
1.概念:解离时产生的阴离子全部是_______的化合物。
2.氢氧化钠、氢氧化钙的性质和用途
氢氧化钠 氢氧化钙
俗名 ______________________ __________________
颜色、状态 白色固体 白色粉末状固体
溶解性 ______溶于水,并放出大量的热 微溶于水,溶解度随温
度升高而________
火碱、烧碱、苛性钠
熟石灰、消石灰
易
减小
氢氧化钠 氢氧化钙
吸水性 易吸水潮解
腐蚀性 有强烈腐蚀性 有腐蚀性
用途 (1)实验室可作干燥剂;(2)是 化工原料,广泛用于制取肥皂,以 及石油、造纸、纺织和印染等工业; (3)作炉具清洁剂 (1)作建筑材料;
(2)改良酸性土壤;
(3)配制波尔多液
续表
【特别提醒】 (1)氢氧化钠固体易吸水,可作干燥剂(不能用于干燥
酸性气体,如
的盐和水);
(2)氢氧化钠溶液不能作干燥剂。
(3)氢氧化钠具有强烈的腐蚀性,若不慎沾到皮肤上,应立即用大量的
水冲洗,再涂上硼酸溶液。
3.其他常见的碱
氨水(溶质的化学式为____________)——无色液体,易挥发出有刺激
性气味的气体,常用作氮肥,是一种不含金属元素的碱;氢氧化钾(化
学式为_______)等。
4.碱溶液的通性
氢氧化钠 氢氧化钙
与指示剂作 用 能使石蕊溶液变①________,能使酚酞溶液变②________
碱+非金属氧 化物
________________
蓝色
红色
氢氧化钠 氢氧化钙
碱+酸
_______________
碱+盐
____________________(配制波
尔多液)
现象:⑨__________________
总结 氢氧化钠和氢氧化钙具有相似化学性质的原因是⑩ ____________________
有蓝色沉淀生成
溶液中都含有
续表
5.氢氧化钙的特性
与碳酸钠反应,化学方程式为
_______________________________________;
现象:__________________________________;
应用:_________(写化学式)的工业制备。
总结:碱的化学性质不完全相同的原因是______________。
溶液变浑浊(或有白色沉淀生成)
阳离子不同
辨析易错易混·正误判断
1.碱中一定含有氢元素、氧元素和金属元素。( )
×
[解析] 氨水
2.氢氧化钠易吸水潮解,可用于干燥氯化氢和二氧化碳气体。( )
×
[解析] 氢氧化钠会与氯化氢或二氧化碳反应,不能用于干燥这两者。
考点过关练
1.&6& 物质的结构决定性质,物质的性质决定用途,反应本质决定变化现象。
(1) 如图是某同学构建的氢氧化钙部分知识网络,其中
“—”表示相连物质能发生化学反应,
别不同。请回答:
① 酚酞溶液在
_______。
② 列举熟石灰
一种用途____________________________。
改良酸性土壤(合理即可)
③
现象的一个化学方程式:
_ _________________________________________________。
(2) 氢氧化钠和氢氧化钙是两种常见的碱,下列说法错误的是_____
(填字母)。
A.溶解性:氢氧化钠易溶于水,氢氧化钙微溶于水
B.保存:在空气中易变质,都需密封保存
C.鉴别:对两者的溶液取样后分别滴入酚酞溶液
D.用途:氢氧化钠可用于制炉具清洁剂,氢氧化钙可用于配制农药波尔
多液
C
&7& 中和反应
1.定义:______和______作用生成盐和水的反应,叫做中和反应。
酸
碱
2.实质:_ __________________。
3.中和反应的实验探究(详见实验帮)
4.中和反应在实际中的应用
(1)用________________________改良酸性土壤(氢氧化钠有强烈的腐
蚀性,故不能用氢氧化钠)。
(2)用熟石灰处理酸性废水。
(3)服用含氢氧化铝或氢氧化镁的药物治疗胃酸过多症。
(4)被蚊虫叮咬(含蚁酸)后涂抹牙膏、肥皂水等碱性物质可缓解痛痒。
氢氧化钙(或熟石灰)
辨析易错易混·正误判断
1.中和反应一定生成盐和水,则生成盐和水的反应一定是中和反应。
( )
×
2.中和反应一定是复分解反应,复分解反应一定是中和反应。( )
×
[解析] 中和反应一定是复分解反应,但复分解反应不一定是中和反应,
如硫酸铜和氢氧化钠反应生成氢氧化铜和硫酸钠,属于复分解反应,但
不属于中和反应。
考点过关练
1.&8& 反应物的量不同,反应程度不同,所得溶液中所含溶质(组成)不同。
(1) [2022河北中考] 向含有酚酞的氢氧化钠溶液中慢慢滴入稀硫酸,该
过程中溶液
B
A.
B.
C.
D.
(2) 如图是利用数字化传感器测得的盐酸与氢氧化钠溶液反应过程中
溶液
① 该反应的化学方程式为_ __________________________。
② 当溶液呈中性时,所消耗氢氧化钠溶液的体积是______
10
③ 请在虚线框内将
[答案] &9&
1.以
写出图中涉及的化学方程式:
① ___________________________、_____________________________、
____________________________、
___________________________________;
② ___________________________、
_________________________________、
__________________________________、
___________________________________、
___________________________________、
___________________________________;
③ _______________________________________、
____________________________________、
_________________________________________、
_ ____________________________________________;
④ ________________________________、
____________________________、
_____________________________________、
_ _____________________________;
⑤ _ ________________________________;
⑥ _ ______________________________。
2.以
写出图中涉及的化学方程式:
① ___________________________、
___________________________________、
_________________________________、
_ __________________________________;
② _____________________________________、
______________________________________、
______________________________________、
_ ______________________________________;
③ ________________________________、
_ ________________________________;
④ _ ______________________________________(工业制烧碱的原理)。
实验 常见酸碱与指示剂的作用
(1) 紫色石蕊溶液遇稀盐酸、稀硫酸变______色,遇氢氧化钙、氢氧化
钠溶液变______色。
红
蓝
(2) 无色酚酞溶液遇稀酸不变色,遇氢氧化钙、氢氧化钠溶液变______色。
红
创新考法
(3) 某同学自制酸碱指示剂,将牵牛花捣烂后加入
再用纱布过滤,制得紫色的牵牛花汁液,并将其分别滴入白醋、石灰水
和水中,结果如下:
白醋 石灰水 水
牵牛花汁液颜色变化 由紫色变红色 由紫色变绿色 不变色
①
作溶剂(或溶解色素)
② 牵牛花汁液能做酸碱指示剂的依据是____________________________
________________;
其在酸性、碱性、中性溶液中显示不同的颜色
③ 将牵牛花汁液滴入碳酸钠溶液中,观察到的现象是________________。
溶液由紫色变绿色
(4) 如下图所示,在白色点滴板1~6孔穴中分别滴加2滴无色酚酞溶液。
① 孔穴3的作用是__________;
作对照
② 孔穴6中溶液变为红色,说明碳酸钾溶液显________(填“酸性”“碱性”
或“中性”);
碱性
③ 向孔穴4中滴加稀硫酸至过量,观察到的现象是______________________,
用化学方程式解释其原因:
___________________________________;
溶液由红色变为无色
④ 若将图中的酚酞溶液用紫色石蕊溶液替换,则溶液变为红色的孔穴有
________。
实验 酸碱中和反应
1.实验装置
2.反应原理:_ __________________________(用化学方程式表示)。
3.实验现象及结论
(1) 在碱溶液中加入无色酚酞溶液时,出现的现象为_______________
_______。
溶液由无色变为红色
(2) 向含有酚酞的碱溶液中滴加酸,当__________________________
时,证明酸碱恰好完全中和。
溶液由红色恰好变为无色
4.酸碱中和反应的微观实质
(1) 如图是氢氧化钠与盐酸反应的示意图。用实际参加
反应的离子符号来表示反应的式子叫做离子方程式。请写
出氢氧化钠与盐酸反应的离子方程式。
[答案]
(2) 酸和碱能发生化学反应,试写出氯酸
[答案]
拓展探究
5.中和反应后溶液中溶质成分的探究
以
(1) 恰好完全反应时,溶液的
对应图中_____点。
B
(2) 碱过量时,溶液的
色,对应图中_____点。
A
(3) 酸过量时,溶液的
对应图中_____点。
C
【反思设问】 溶液呈无色时,检验溶质的成分可选用的试剂有哪些?
[答案] 石蕊溶液、
6.酸碱中和反应的数字化实验
酸碱中和反应的过程中,除了有新物质生成外,还
伴随有能量变化和溶液酸碱度的变化。某同学用传
感器探究稀氢氧化钠溶液与稀盐酸反应过程中溶液
温度和
(1) 氢氧化钠和稀盐酸的反应属于________(填“吸热”或“放热”)反应。
放热
(2)
&10& 同学们用如图1所示的装置
完成酸碱中和反应实验。
图1
(1) 步骤Ⅰ中观察到的现象是______________________;步骤Ⅱ中加入一
定量的稀盐酸,用玻璃棒搅拌后发现溶液变为无色,此时________(填“能”或
“不能”)得出稀盐酸与氢氧化钠恰好中和的结论,发生反应的化学方程式为_ _
_________________________。
溶液由无色变为红色
不能
(2) 图2是利用数字化传感器测得的稀盐酸与氢氧化钠溶液反应过程中
溶液
图2
① (综合探究)为确认
实验步骤 实验现象 实验结论
取少量
向另一份滴加
方程式为
_ _______________________________
溶质中不含
② 由上述实验现象能否说明
[答案] 不能。若稀盐酸过量,也能出现与题中相同的现象。
(3) (创新考法)将稀盐酸分别滴入
均无明显现象。混合后相关变化的微观示意图如图3所示,下列说法正确的是
_____(填字母)。
图3
A.物质间均未发生化学反应 B.变化中都有新物质产生
C.混合后溶液酸碱性都不变 D.甲可表示酸碱反应的实质
D
【思路分析】由题图3甲可知,稀盐酸与氢氧化钠发生了化学反应,反应
的实质是氢离子与氢氧根离子结合生成了水分子,混合后溶液酸碱性发
生了改变,A、C错误,D正确。题图3乙所示溶液中的离子混合前后没
有发生变化,没有新物质生成,B错误。
命题点1 常见酸和碱的性质及用途(必考)
1.[2017河南9] 下列溶液在空气中敞口放置后,溶液质量因发生化学反应
而减小的是( )
A.石灰水 B.浓硫酸 C.浓盐酸 D.烧碱溶液
A
2.[2020河南25(1)] 酸具有相似的性质,因为不同的酸在水溶液中都能
解离出____(填字母)。
3.[2022河南25(1)(2)]
(1)在实验室常用浓硫酸做干燥剂,这是因为浓硫酸具有_____(填字
母)。
a.酸性
c.氧化性
(2) 请简述氢氧化钙(俗称熟石灰)在生产或生活中的一种用途。
[答案] 熟石灰可用来改良酸性土壤。(或用石灰浆粉刷墙壁、用石灰乳
与硫酸铜溶液配制农药波尔多液等,合理即可)
4.[2018河南17] 铁锈(主要成分是
成物为
5.[2017河南16第二空] 在医疗上可以用小苏打治疗胃酸
其原理是_____________________________________(用化学方程式表
示)。
6.[2016河南23(3)] 浓硫酸和浓盐酸敞口放置均会变稀,这是为什么?
[答案] 因为浓硫酸有吸水性,溶剂会增多;浓盐酸有挥发性,溶质会减少。
7.[2019河南22] 某化学兴趣小组的同学利用压强传感器、
数据采集器和计算机等数字化实验设备,测定铝片与足
量稀硫酸反应时气体压强的变化,实验结果如图所示。
(1) 开始一段时间气体压强几乎不变,其原因是什么?
[答案] 铝片表面有一层致密的氧化铝薄膜,稀硫酸与氧化铝反应时不生成
气体。
(2) 写出
[答案]
8.[2015河南22(2)③] 氨气与酸反应生成铵盐。将蘸有浓盐酸的玻璃棒靠近集满氨气的瓶口时,有大量白烟产生,而改用浓硫酸时无此现象。请解释白烟产生的原因。
[答案] 浓盐酸挥发出的氯化氢气体与氨气反应,在空气中生成了白色固体
颗粒。
9.[2013河南18(3)] 如图,用滤纸做成的小花喷洒某溶液后放在烧
杯上方,片刻后变成红色。请推测喷洒液和烧杯中的溶液可能是什
么?(写出一组即可)
[答案] 石蕊溶液和浓盐酸(或酚酞溶液和浓氨水等)。
【考向拓展】 实验小组用下图装置进行微型实验。
按下列表中选项加入试剂,实验时滴入甲,浸有丙
的棉花不变红 的是( )
B
选项 甲 乙 丙
A 浓氨水 — 无色酚酞溶液
B 石灰水 碳酸钠 无色酚酞溶液
C 稀盐酸 石灰石 紫色石蕊溶液
D 浓盐酸 锌粒 紫色石蕊溶液
10.[2021河南22(2)②] 氨气极易溶于水,氨水显碱性。则如图实验可
观察到什么现象?
[答案] 试管内液面上升,试管中的溶液变成红色。
命题点2 中和反应及
11.[2016河南23(2)] 盐酸与氢氧化钠溶液反应时溶液
示。下列说法正确的是____(填字母)。
d.该图所对应操作是将盐酸滴入氢氧化钠溶液中
【考向拓展】 用熟石灰中和一定量的盐酸时,溶液的
学方程式为_________________________________,该反应
的基本反应类型是______________;当加入熟石灰
溶液中的溶质为______________。若改用
相同量盐酸反应,所得溶液的
“=”)。
复分解反应
<
12.如图是氢氧化钠溶液与硫酸反应时溶液
(1) [2018河南25(2)①] 根据图示判断,该实验是将
______(填“氢氧化钠溶液”或“硫酸”)滴加到另一种溶液中。
硫酸
(2) [2020河南25(3)第一空;2018河南25(2)②] 滴入溶液体积为
(3) [2020河南25(3)第二空] 当滴入溶液为
色石蕊溶液变成______色。
红
13.[2017河南21] 向盛有氢氧化钠溶液(滴有酚酞溶液)的烧杯中滴加盐酸时,观察到烧杯中的溶液由红色变为无色。
(1) 请写出有关反应的化学方程式。
[答案]
(2) 烧杯中无色溶液的溶质可能只有
[答案] 紫色石蕊溶液(或
14.下图是氢氧化钠与盐酸反应的示意图。
(1) 反应前后没有发生变化的离子有____________。 [2021河南17]
(2) ① 用实际参加反应的离子符号来表示该反应:
_ __________________。
② 向滴有酚酞的稀氢氧化钠溶液中滴入稀盐酸至过量,
观察到溶液颜色的变化是__________________。[2022河南25(3)]
由红色变成无色
15.[2013河南21(2)] 某化学小组进行“酸和碱的中和反应”实验:将盐
酸滴入一定量的澄清石灰水中,无明显现象。取反应后的部分溶液加热、
蒸干,得到白色固体。
以下是探究白色固体成分的实验,已知
实验操作 测定结果 白色固体成分
用
________
用玻璃棒蘸取溶液滴到
实验反思:无明显现象的中和反应可借助酸碱指示剂判断反应终点。
第十单元 酸和碱
&1& 溶液的酸碱性与
1.酸碱指示剂
酸碱指示剂的变色规律:
紫色石蕊溶液:在酸中显______色,在碱中显______色;
[紫色石蕊溶液显色口诀:酸里红(谐音:山里红),碱里蓝]
无色酚酞溶液:在酸中显______色,在碱中显______色。
(无色酚酞溶液显色口诀:遇酸色不变,遇碱红艳艳)
红
蓝
无
红
【特别提醒】 (1)指示剂的变色过程属于化学变化,是酸或碱使指示
剂变色,不是指示剂使酸或碱变色。
(2)指示剂颜色的变化,只能说明溶液显酸性或碱性,不能说明某溶液
就是酸或碱的溶液,因为有些盐溶液也显酸性或碱性。
2.溶液酸碱度的表示方法——
(1) 溶液的酸碱度常用______来表示,
(2) 溶液酸碱性与
酸性溶液的
碱性溶液的
中性溶液的
小
>
大
=
(3) 溶液
定时,用__________蘸取待测溶液滴到___________上,然后再与________
______比较,读出该溶液的
玻璃棒
标准比色卡
(4)
①了解空气污染情况:
的原因:_ _____________________(用化学方程式表示)];
②测定人体内或排出液体的
③化工生产中,许多反应要在一定
④农业生产中,农作物一般适宜在
<
【温馨提示】 酸性溶液或碱性溶液稀释过程中溶液
见题型三。
辨析易错易混·正误判断
1.酸溶液能使紫色石蕊溶液变红,则能使紫色石蕊溶液变红的一定是酸
溶液。( )
×
[解析] 能使紫色石蕊溶液变红的溶液显酸性,但不一定是酸溶液,如硝酸
铵溶液显酸性,但它是盐溶液。
2.氢氧化钠溶液和碳酸钠溶液均显碱性,都能使无色酚酞溶液变红。
( )
√
3.所有的碱都能使无色酚酞溶液变红。( )
×
[解析] 不溶于水的碱[如
自由移动的
4.只有无色酚酞溶液和紫色石蕊溶液遇酸、碱性溶液能变色。( )
×
考点过关练
1.&2& 酸碱指示剂在不同的酸碱性溶液里能显示不同的颜色,因此,酸碱指示剂可以检验溶液的酸碱性。测定溶液的
(1) [2022天津中考] 生活中一些常见物质的
中碱性最强的是( )
A.厕所清洁剂 B.食盐水 C.肥皂水 D.炉具清洁剂
D
(2) 某同学想用
的是( )
A.用干燥的
B.用干燥的
C.用干燥的
D.用湿润的
A
(3) [2022成都中考] 部分水果及饮料的
下列说法正确的是( )
A.西瓜汁显碱性
B.橘子汁中滴入酚酞,溶液变红
C.苏打水显酸性
D.胃酸过多的人应该少饮柠檬水
D
&3& 常见酸的性质和用途
1.概念:解离时产生的阳离子全部是______的化合物。
2.浓盐酸和浓硫酸的物理性质和用途
浓盐酸 浓硫酸
溶质(化学式) ①_______ ②_________
物理 性质 颜色状 态 无色液体 无色黏稠状液体
浓盐酸 浓硫酸
物理 性质 气味 有③__________气味 无
挥发性 有④________性(打开瓶 塞,瓶口产生大量⑤______) 不易挥发
用途
药、染料以及冶炼金属、精
炼石油和金属除锈等;
刺激性
挥发
白雾
除锈
续表
3.浓硫酸的特性
吸水性(物 理性质) 浓硫酸具有吸水性,在实验室中常用作①__________
腐蚀性(化 学性质) 浓硫酸能夺取纸张、木材等物质中的水分,生成黑色的碳,
具有强脱水作用,有强烈的②__________,如不慎将浓硫
酸沾在衣服上或皮肤上,应立即用③______________,然
后再涂上
干燥剂
腐蚀性
大量水冲洗
浓硫酸稀释:稀释浓硫酸时,一定要把④
__________沿容器内壁慢慢注入⑤______中,并
用玻璃棒不断⑥________,切不可把水倒入浓硫
酸中
. .
浓硫酸
水
搅拌
续表
4.其他常见的酸:碳酸、醋酸(常用于除水垢)、硝酸等。
5.酸溶液的通性
盐酸 硫酸
与指示剂 作用 能使石蕊溶液变红,不能使酚酞溶液变色
盐酸 硫酸
酸+活泼 金属
__________________________
铁与硫酸反应:④
_ _________________________
现象:⑤__________________
___________________
有气泡产生,溶液由无色变成浅绿色
续表
盐酸 硫酸
酸+金属 氧化物→ 盐+水 用盐酸除铁锈:⑥__________ _______________________ 现象:⑦__________________ _____________________ 氧化铜与硫酸反应:⑧_____
_________________________
_
现象:⑨_________________
____________________
红棕色固体溶解,溶液由无色变成黄色
黑色固体溶解,溶液由无色变成蓝色
续表
盐酸 硫酸
酸+碱
_________________________
____________________
现象: ________________
_____________________
蓝色固体溶解,溶液由无色变成蓝色
续表
盐酸 硫酸
酸+盐→ 新酸+新 盐 碳酸钙与稀盐酸反应: ___ __________________________ ____________________ 现象: _________________ ___________ 碳酸钠与稀硫酸反应:
_________________________
_________________________
现象: ______________
总结 稀硫酸和稀盐酸具有相似化学性质的原因是 __________________
固体逐渐溶解,有气泡产生
有气泡产生
溶液中都含有
续表
6.稀盐酸和稀硫酸的特性
(1) 稀盐酸与硝酸银反应
化学方程式:_______________________________;
现象:__________________;
应用:检验______(填离子符号)。
有白色沉淀生成
(2) 稀硫酸与硝酸钡反应
化学方程式:______________________________________;
现象:__________________;
应用:检验________(填离子符号)。
总结:酸的化学性质不完全相同的原因是________________。
有白色沉淀生成
酸根离子不同
辨析易错易混·正误判断
1.某固体中加入稀盐酸产生气体,该气体一定是
×
[解析] 活泼金属与稀盐酸反应会产生氢气。
2.酸中含有氢元素,所以含有氢元素的化合物一定是酸。( )
×
考点过关练
1.&4& 学习了酸的化学性质,某同学以稀硫酸为主题,绘制了“多
彩酸世界”思维导图。
(1) 若用
蓝
(2) 若想实现③,得到浅绿色溶液,可选用的单质是______。
铁
(3) 若选用
_ ________________________________。
(4) 根据上图,请你总结酸的通性:_____________________________
___________________________________________________________。
能使酸碱指示剂变色、能与活泼金属反应、能与金属氧化物反应、能与碱反应、能与某些盐反应
(5) (拓展)常见的酸(用化学式填空):硝酸________,食醋中含
有的酸____________,铅酸蓄电池中含有的酸_________,人体胃液中含
有的酸_______,汽水中含有的酸_________。
【归纳总结】
酸的共性
稀硫酸能够与氯化钡溶液发生复分解反应,微观实质是:
件,二者不反应。
&5& 常见碱的性质和用途
1.概念:解离时产生的阴离子全部是_______的化合物。
2.氢氧化钠、氢氧化钙的性质和用途
氢氧化钠 氢氧化钙
俗名 ______________________ __________________
颜色、状态 白色固体 白色粉末状固体
溶解性 ______溶于水,并放出大量的热 微溶于水,溶解度随温
度升高而________
火碱、烧碱、苛性钠
熟石灰、消石灰
易
减小
氢氧化钠 氢氧化钙
吸水性 易吸水潮解
腐蚀性 有强烈腐蚀性 有腐蚀性
用途 (1)实验室可作干燥剂;(2)是 化工原料,广泛用于制取肥皂,以 及石油、造纸、纺织和印染等工业; (3)作炉具清洁剂 (1)作建筑材料;
(2)改良酸性土壤;
(3)配制波尔多液
续表
【特别提醒】 (1)氢氧化钠固体易吸水,可作干燥剂(不能用于干燥
酸性气体,如
的盐和水);
(2)氢氧化钠溶液不能作干燥剂。
(3)氢氧化钠具有强烈的腐蚀性,若不慎沾到皮肤上,应立即用大量的
水冲洗,再涂上硼酸溶液。
3.其他常见的碱
氨水(溶质的化学式为____________)——无色液体,易挥发出有刺激
性气味的气体,常用作氮肥,是一种不含金属元素的碱;氢氧化钾(化
学式为_______)等。
4.碱溶液的通性
氢氧化钠 氢氧化钙
与指示剂作 用 能使石蕊溶液变①________,能使酚酞溶液变②________
碱+非金属氧 化物
________________
蓝色
红色
氢氧化钠 氢氧化钙
碱+酸
_______________
碱+盐
____________________(配制波
尔多液)
现象:⑨__________________
总结 氢氧化钠和氢氧化钙具有相似化学性质的原因是⑩ ____________________
有蓝色沉淀生成
溶液中都含有
续表
5.氢氧化钙的特性
与碳酸钠反应,化学方程式为
_______________________________________;
现象:__________________________________;
应用:_________(写化学式)的工业制备。
总结:碱的化学性质不完全相同的原因是______________。
溶液变浑浊(或有白色沉淀生成)
阳离子不同
辨析易错易混·正误判断
1.碱中一定含有氢元素、氧元素和金属元素。( )
×
[解析] 氨水
2.氢氧化钠易吸水潮解,可用于干燥氯化氢和二氧化碳气体。( )
×
[解析] 氢氧化钠会与氯化氢或二氧化碳反应,不能用于干燥这两者。
考点过关练
1.&6& 物质的结构决定性质,物质的性质决定用途,反应本质决定变化现象。
(1) 如图是某同学构建的氢氧化钙部分知识网络,其中
“—”表示相连物质能发生化学反应,
别不同。请回答:
① 酚酞溶液在
_______。
② 列举熟石灰
一种用途____________________________。
改良酸性土壤(合理即可)
③
现象的一个化学方程式:
_ _________________________________________________。
(2) 氢氧化钠和氢氧化钙是两种常见的碱,下列说法错误的是_____
(填字母)。
A.溶解性:氢氧化钠易溶于水,氢氧化钙微溶于水
B.保存:在空气中易变质,都需密封保存
C.鉴别:对两者的溶液取样后分别滴入酚酞溶液
D.用途:氢氧化钠可用于制炉具清洁剂,氢氧化钙可用于配制农药波尔
多液
C
&7& 中和反应
1.定义:______和______作用生成盐和水的反应,叫做中和反应。
酸
碱
2.实质:_ __________________。
3.中和反应的实验探究(详见实验帮)
4.中和反应在实际中的应用
(1)用________________________改良酸性土壤(氢氧化钠有强烈的腐
蚀性,故不能用氢氧化钠)。
(2)用熟石灰处理酸性废水。
(3)服用含氢氧化铝或氢氧化镁的药物治疗胃酸过多症。
(4)被蚊虫叮咬(含蚁酸)后涂抹牙膏、肥皂水等碱性物质可缓解痛痒。
氢氧化钙(或熟石灰)
辨析易错易混·正误判断
1.中和反应一定生成盐和水,则生成盐和水的反应一定是中和反应。
( )
×
2.中和反应一定是复分解反应,复分解反应一定是中和反应。( )
×
[解析] 中和反应一定是复分解反应,但复分解反应不一定是中和反应,
如硫酸铜和氢氧化钠反应生成氢氧化铜和硫酸钠,属于复分解反应,但
不属于中和反应。
考点过关练
1.&8& 反应物的量不同,反应程度不同,所得溶液中所含溶质(组成)不同。
(1) [2022河北中考] 向含有酚酞的氢氧化钠溶液中慢慢滴入稀硫酸,该
过程中溶液
B
A.
B.
C.
D.
(2) 如图是利用数字化传感器测得的盐酸与氢氧化钠溶液反应过程中
溶液
① 该反应的化学方程式为_ __________________________。
② 当溶液呈中性时,所消耗氢氧化钠溶液的体积是______
10
③ 请在虚线框内将
[答案] &9&
1.以
写出图中涉及的化学方程式:
① ___________________________、_____________________________、
____________________________、
___________________________________;
② ___________________________、
_________________________________、
__________________________________、
___________________________________、
___________________________________、
___________________________________;
③ _______________________________________、
____________________________________、
_________________________________________、
_ ____________________________________________;
④ ________________________________、
____________________________、
_____________________________________、
_ _____________________________;
⑤ _ ________________________________;
⑥ _ ______________________________。
2.以
写出图中涉及的化学方程式:
① ___________________________、
___________________________________、
_________________________________、
_ __________________________________;
② _____________________________________、
______________________________________、
______________________________________、
_ ______________________________________;
③ ________________________________、
_ ________________________________;
④ _ ______________________________________(工业制烧碱的原理)。
实验 常见酸碱与指示剂的作用
(1) 紫色石蕊溶液遇稀盐酸、稀硫酸变______色,遇氢氧化钙、氢氧化
钠溶液变______色。
红
蓝
(2) 无色酚酞溶液遇稀酸不变色,遇氢氧化钙、氢氧化钠溶液变______色。
红
创新考法
(3) 某同学自制酸碱指示剂,将牵牛花捣烂后加入
再用纱布过滤,制得紫色的牵牛花汁液,并将其分别滴入白醋、石灰水
和水中,结果如下:
白醋 石灰水 水
牵牛花汁液颜色变化 由紫色变红色 由紫色变绿色 不变色
①
作溶剂(或溶解色素)
② 牵牛花汁液能做酸碱指示剂的依据是____________________________
________________;
其在酸性、碱性、中性溶液中显示不同的颜色
③ 将牵牛花汁液滴入碳酸钠溶液中,观察到的现象是________________。
溶液由紫色变绿色
(4) 如下图所示,在白色点滴板1~6孔穴中分别滴加2滴无色酚酞溶液。
① 孔穴3的作用是__________;
作对照
② 孔穴6中溶液变为红色,说明碳酸钾溶液显________(填“酸性”“碱性”
或“中性”);
碱性
③ 向孔穴4中滴加稀硫酸至过量,观察到的现象是______________________,
用化学方程式解释其原因:
___________________________________;
溶液由红色变为无色
④ 若将图中的酚酞溶液用紫色石蕊溶液替换,则溶液变为红色的孔穴有
________。
实验 酸碱中和反应
1.实验装置
2.反应原理:_ __________________________(用化学方程式表示)。
3.实验现象及结论
(1) 在碱溶液中加入无色酚酞溶液时,出现的现象为_______________
_______。
溶液由无色变为红色
(2) 向含有酚酞的碱溶液中滴加酸,当__________________________
时,证明酸碱恰好完全中和。
溶液由红色恰好变为无色
4.酸碱中和反应的微观实质
(1) 如图是氢氧化钠与盐酸反应的示意图。用实际参加
反应的离子符号来表示反应的式子叫做离子方程式。请写
出氢氧化钠与盐酸反应的离子方程式。
[答案]
(2) 酸和碱能发生化学反应,试写出氯酸
[答案]
拓展探究
5.中和反应后溶液中溶质成分的探究
以
(1) 恰好完全反应时,溶液的
对应图中_____点。
B
(2) 碱过量时,溶液的
色,对应图中_____点。
A
(3) 酸过量时,溶液的
对应图中_____点。
C
【反思设问】 溶液呈无色时,检验溶质的成分可选用的试剂有哪些?
[答案] 石蕊溶液、
6.酸碱中和反应的数字化实验
酸碱中和反应的过程中,除了有新物质生成外,还
伴随有能量变化和溶液酸碱度的变化。某同学用传
感器探究稀氢氧化钠溶液与稀盐酸反应过程中溶液
温度和
(1) 氢氧化钠和稀盐酸的反应属于________(填“吸热”或“放热”)反应。
放热
(2)
&10& 同学们用如图1所示的装置
完成酸碱中和反应实验。
图1
(1) 步骤Ⅰ中观察到的现象是______________________;步骤Ⅱ中加入一
定量的稀盐酸,用玻璃棒搅拌后发现溶液变为无色,此时________(填“能”或
“不能”)得出稀盐酸与氢氧化钠恰好中和的结论,发生反应的化学方程式为_ _
_________________________。
溶液由无色变为红色
不能
(2) 图2是利用数字化传感器测得的稀盐酸与氢氧化钠溶液反应过程中
溶液
图2
① (综合探究)为确认
实验步骤 实验现象 实验结论
取少量
向另一份滴加
方程式为
_ _______________________________
溶质中不含
② 由上述实验现象能否说明
[答案] 不能。若稀盐酸过量,也能出现与题中相同的现象。
(3) (创新考法)将稀盐酸分别滴入
均无明显现象。混合后相关变化的微观示意图如图3所示,下列说法正确的是
_____(填字母)。
图3
A.物质间均未发生化学反应 B.变化中都有新物质产生
C.混合后溶液酸碱性都不变 D.甲可表示酸碱反应的实质
D
【思路分析】由题图3甲可知,稀盐酸与氢氧化钠发生了化学反应,反应
的实质是氢离子与氢氧根离子结合生成了水分子,混合后溶液酸碱性发
生了改变,A、C错误,D正确。题图3乙所示溶液中的离子混合前后没
有发生变化,没有新物质生成,B错误。
命题点1 常见酸和碱的性质及用途(必考)
1.[2017河南9] 下列溶液在空气中敞口放置后,溶液质量因发生化学反应
而减小的是( )
A.石灰水 B.浓硫酸 C.浓盐酸 D.烧碱溶液
A
2.[2020河南25(1)] 酸具有相似的性质,因为不同的酸在水溶液中都能
解离出____(填字母)。
3.[2022河南25(1)(2)]
(1)在实验室常用浓硫酸做干燥剂,这是因为浓硫酸具有_____(填字
母)。
a.酸性
c.氧化性
(2) 请简述氢氧化钙(俗称熟石灰)在生产或生活中的一种用途。
[答案] 熟石灰可用来改良酸性土壤。(或用石灰浆粉刷墙壁、用石灰乳
与硫酸铜溶液配制农药波尔多液等,合理即可)
4.[2018河南17] 铁锈(主要成分是
成物为
5.[2017河南16第二空] 在医疗上可以用小苏打治疗胃酸
其原理是_____________________________________(用化学方程式表
示)。
6.[2016河南23(3)] 浓硫酸和浓盐酸敞口放置均会变稀,这是为什么?
[答案] 因为浓硫酸有吸水性,溶剂会增多;浓盐酸有挥发性,溶质会减少。
7.[2019河南22] 某化学兴趣小组的同学利用压强传感器、
数据采集器和计算机等数字化实验设备,测定铝片与足
量稀硫酸反应时气体压强的变化,实验结果如图所示。
(1) 开始一段时间气体压强几乎不变,其原因是什么?
[答案] 铝片表面有一层致密的氧化铝薄膜,稀硫酸与氧化铝反应时不生成
气体。
(2) 写出
[答案]
8.[2015河南22(2)③] 氨气与酸反应生成铵盐。将蘸有浓盐酸的玻璃棒靠近集满氨气的瓶口时,有大量白烟产生,而改用浓硫酸时无此现象。请解释白烟产生的原因。
[答案] 浓盐酸挥发出的氯化氢气体与氨气反应,在空气中生成了白色固体
颗粒。
9.[2013河南18(3)] 如图,用滤纸做成的小花喷洒某溶液后放在烧
杯上方,片刻后变成红色。请推测喷洒液和烧杯中的溶液可能是什
么?(写出一组即可)
[答案] 石蕊溶液和浓盐酸(或酚酞溶液和浓氨水等)。
【考向拓展】 实验小组用下图装置进行微型实验。
按下列表中选项加入试剂,实验时滴入甲,浸有丙
的棉花
B
选项 甲 乙 丙
A 浓氨水 — 无色酚酞溶液
B 石灰水 碳酸钠 无色酚酞溶液
C 稀盐酸 石灰石 紫色石蕊溶液
D 浓盐酸 锌粒 紫色石蕊溶液
10.[2021河南22(2)②] 氨气极易溶于水,氨水显碱性。则如图实验可
观察到什么现象?
[答案] 试管内液面上升,试管中的溶液变成红色。
命题点2 中和反应及
11.[2016河南23(2)] 盐酸与氢氧化钠溶液反应时溶液
示。下列说法正确的是____(填字母)。
d.该图所对应操作是将盐酸滴入氢氧化钠溶液中
【考向拓展】 用熟石灰中和一定量的盐酸时,溶液的
学方程式为_________________________________,该反应
的基本反应类型是______________;当加入熟石灰
溶液中的溶质为______________。若改用
相同量盐酸反应,所得溶液的
“=”)。
复分解反应
<
12.如图是氢氧化钠溶液与硫酸反应时溶液
(1) [2018河南25(2)①] 根据图示判断,该实验是将
______(填“氢氧化钠溶液”或“硫酸”)滴加到另一种溶液中。
硫酸
(2) [2020河南25(3)第一空;2018河南25(2)②] 滴入溶液体积为
(3) [2020河南25(3)第二空] 当滴入溶液为
色石蕊溶液变成______色。
红
13.[2017河南21] 向盛有氢氧化钠溶液(滴有酚酞溶液)的烧杯中滴加盐酸时,观察到烧杯中的溶液由红色变为无色。
(1) 请写出有关反应的化学方程式。
[答案]
(2) 烧杯中无色溶液的溶质可能只有
[答案] 紫色石蕊溶液(或
14.下图是氢氧化钠与盐酸反应的示意图。
(1) 反应前后没有发生变化的离子有____________。 [2021河南17]
(2) ① 用实际参加反应的离子符号来表示该反应:
_ __________________。
② 向滴有酚酞的稀氢氧化钠溶液中滴入稀盐酸至过量,
观察到溶液颜色的变化是__________________。[2022河南25(3)]
由红色变成无色
15.[2013河南21(2)] 某化学小组进行“酸和碱的中和反应”实验:将盐
酸滴入一定量的澄清石灰水中,无明显现象。取反应后的部分溶液加热、
蒸干,得到白色固体。
以下是探究白色固体成分的实验,已知
实验操作 测定结果 白色固体成分
用
________
用玻璃棒蘸取溶液滴到
实验反思:无明显现象的中和反应可借助酸碱指示剂判断反应终点。
同课章节目录
