江苏省无锡市洛社高级中学2013-2014学年高一下学期期中考试化学试题
文档属性
| 名称 | 江苏省无锡市洛社高级中学2013-2014学年高一下学期期中考试化学试题 |  | |
| 格式 | zip | ||
| 文件大小 | 188.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2014-05-16 12:37:59 | ||
图片预览


文档简介
洛社高级中学2013-2014学年高一下学期期中考试
化学试题
时间:100分钟 总分:100分
本试卷可能用到的原子量:H-1 N-14 O-16 S-32 Cu-64
第Ⅰ卷 选择题(共50分)
选择题(本题包括25小题,每小题2分,共50分。每小题只有一个选项符合题意。)
1、引起1998年广东珠江口附近海域发生的赤潮主要是由于
A.环境污染导致有毒藻类大量繁殖 B.温室效应导致水温升高
C.人类大量捕捞鱼类 D.人类活动导致鱼的食物不足
2、下列叙述正确的是
A. O2的结构式为 O-O B.硫离子的结构示意图为:
C.CCl4分子的比例模型: D.H2O的电子式:
3、下列物质中,不含有共价键的是
A.MgCl2 B.MgCO3 C.HCl D.NaOH
4、下列物质互为同分异构体的一组是
A. 氧气与臭氧 B. 乙醇(CH3CH2OH)和二甲醚(CH3OCH3)
C. 35Cl和37Cl D. 火碱与烧碱
5、已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是原子半径最小的元素,Y的最高正价与最低负价的代数和为0,Z的二价阳离子与氖原子具有相同的核外电子排布,W原子最外层电子数是最内层电子数的3倍。下列说法正确的是
A.R的原子半径比Z的大 B.R的氢化物的热稳定性比W的强
C.X与Y形成的化合物只有一种 D. Y的最高价氧化物的水化物的酸性比W的强
6、2SO2+O2 2SO3 ,是工业上制造氮肥的重要反应。下列关于该反应的说法正确的是
A.增加N2的浓度加快反应速率 B.降低体系温度能加快反应速率
C.使用催化剂不影响反应速率
D.若反应在密闭容器中进行,SO2和O2能100%转化为SO3
7、下列变化过程与能量的说法中正确的是
A.中和反应是吸热反应 B.燃烧属于放热反应
C.化学键断裂放出能量 D.反应物总能量与生成物总能量一定相等
下列试剂:①浓HNO3 ②AgNO3 ③NaCl溶液④氯水⑤氨水⑥NaHCO3应避光保存的是 A.①②③ B. ④⑤⑥ C . ①②④ D . ②③⑥
9、下列变化中,属于物理变化的是
①红磷加热升华变成白磷 ②氯化铵晶体受热后由试管底部移到试管上部 ③固体碘受热变成碘蒸气 ④干冰汽化 ⑤浓硝酸从无色液体变成黄色液体
A. ①② B. ③④ C. ④⑤ D. ③④⑤
10、下列除去杂质的操作方法正确的是
A.食盐中有少量的NH4Cl:加过量的烧碱溶液后加热蒸干
B. NO2中有少量的NO:通入过量的氧气
C. CO2中混有少量的HCl:通过饱和的NaHCO3溶液后再干燥
D. 红磷中有少量的白磷:加热到40℃,使白磷自燃
11、下列有关比较,正确的是
A.稳定性:SiH4>PH3>H2S B.非金属性:Si< S < P
C.酸性:H4SiO4通过一次反应不能直接完成的是 ⑴N2→NO2 ⑵NO2→NO ⑶NH3→NO ⑷NH3→NO2 ⑸Cu→Cu(NO3)2 ⑹HNO3→NO2 A.⑴⑹ B.⑵⑸ C.⑷⑸ D. ⑴⑷
13、常温下能用铝制容器盛放的是 A.浓盐酸 B.浓硝酸 C.稀硝酸 D.稀硫酸
14、通常状况下能共存,且能用浓硫酸干燥的一组气体是 A.H2、O2、N2、 B.O2、NO、NO2 C.H2、N2、NH3 D. NH3、HCl、NO2 15、下列反应的离子方程式正确的是 A.铜与稀硝酸反应:3Cu+2NO3-+4H+=3Cu2++2NO2↑+2H2O B.NO2气体与水反应:3NO2+H2O=2H++2NO3-+NO C.铁与稀盐酸反应:2Fe + 6H+ = 2Fe3+ + 3H2↑
D.AlCl3溶液中加入氨水:Al3++3OH-=Al(OH)3↓
16、下列性质可以证明化合物内一定存在离子键的是
A.可溶于水 B.具有较高的熔点 C.水溶液能导电 D.熔融状态能导电
17、下列各组物质发生状态变化所克服的微粒间的相互作用属于同种类型的是
A.食盐和蔗糖溶于水 B.氯化钠和硫熔化
C.碘和干冰升华 D.二氧化硅和氧化钠熔化
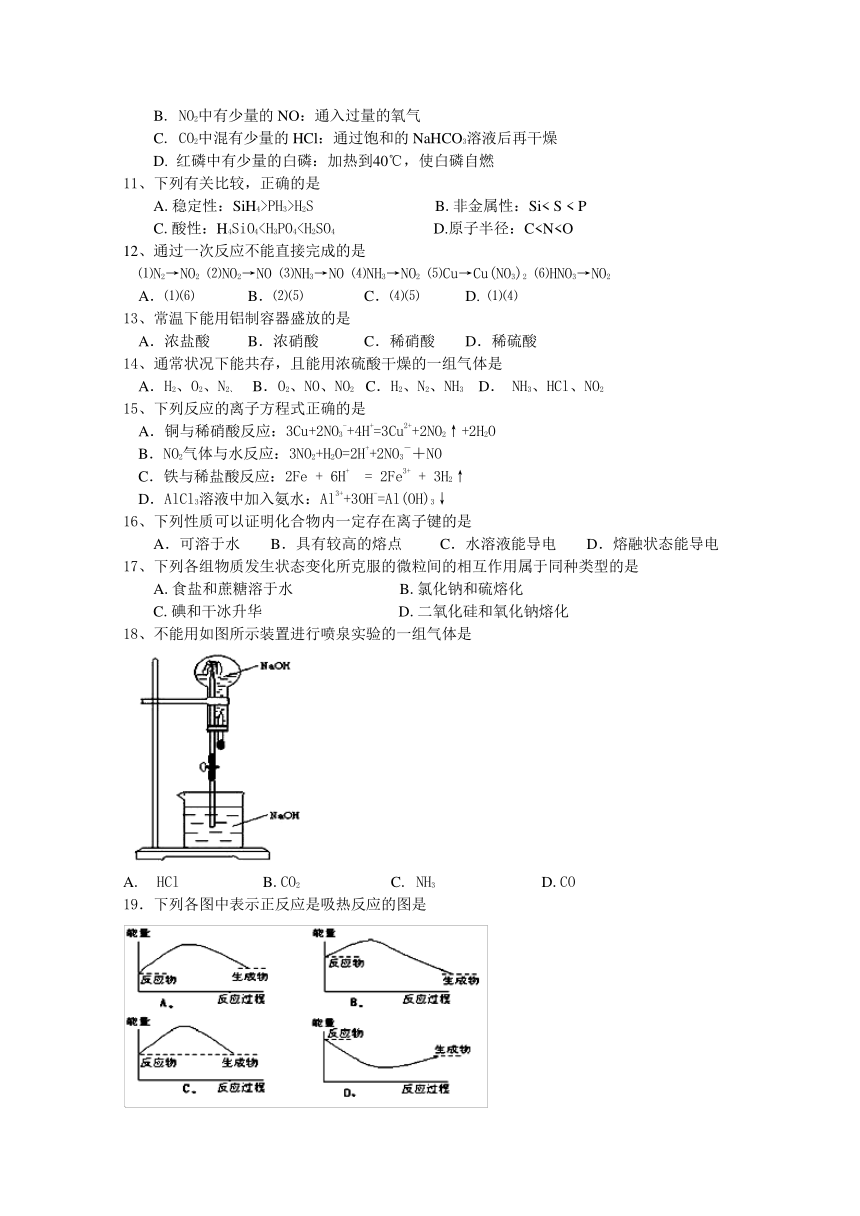
18、不能用如图所示装置进行喷泉实验的一组气体是
A. HCl B.CO2 C. NH3 D.CO
19.下列各图中表示正反应是吸热反应的图是
20、在2A+B 3C+5D反应中,表示该反应速率最快的是
A.v(A)= 0.5 mol/(L·s) B.v(B)= 0.3 mol/(L·s)
C.v(C)= 0.8 mol/(L·s) D.v(D)= 1 mol/(L·s)
21、在一定温度下,可逆A(g) + 3B(g) 2C(g)达到平衡的标志是:
A.C的生成速率与B的生成速率相等 B.单位时间生成n molA,同时生成3n molB C.A、B、C的体积分数不再变化 D.A、B、C的分子数比为1:3:2
22、从经济效益和环境保护考虑,大量制取硝酸铜最适宜采用的方法是: A.Cu+HNO3(浓)→Cu(NO3)2+NO2↑ B.Cu+HNO3 (稀) →Cu(NO3)2+NO↑+H2O C.Cu+O2→CuO,CuO+HNO3 (稀) →Cu(NO3)+H2O D.Cu +AgNO3 →Cu(NO3)2+Ag
23、在酸性溶液中能大量共存的离子组是
A.K+、OH-、Na+ B.Fe2+、NO3-、Na+
C.Ba2+、SO42-、Na+ D.Ca2+、 Cl-、Na+
24、下图是实验室制取氨气的装置和选用的试剂,其中错误的是
A.①④ B.①③ C.②④ D.②③
25、将3. 84克铜粉与一定质量浓硝酸反应,当铜完全作用时,收集到气体4.48L(标况下),则所消耗硝酸的物质的量是
A. 0.26mol B. 0.32mol C. 0.16mol D. 0.2mol
第II卷 非选择题(共50分)
二、填空题
26、(10分,每空1分)下表标出的是元素周期表的一部分元素,回答下列问题:
(1)表中用字母标出的14种元素中,化学性质最不活泼的是 (用元素符号表示,下同),金属性最强的是 ,非金属性最强的是 ,常温下单质为液态的非金属元素是 ,属于过渡元素的是 (该空用字母表示)。
(2)B、F、C气态氢化物的化学式分别为 、 、 ,其中以 最不稳定。
(3)第二周期中原子半径最小的是 。
27、(9分,每空1分)现有①BaCl2、②金刚石、③KNO3、④Na2SO4、⑤干冰、⑥碘片六种
物质,按下列要求回答:
(1)(填序号)熔化时不需要破坏化学键的是 ,熔化时需要破坏共价键的是 , 熔点最高的是 ,熔点最低的是 。
(2)(填序号)属于离子化合物的是 ,只有离子键的物质是 ,晶体以分子间作用力结合的是 。
(3)①的电子式是 ,⑤的电子式是 。
28、(6分,除离子方程式2分外,其余每空1分)X、Y、Z、W四种元素在元素周期表中序数逐渐增大。X为非金属元素,且X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。试推断:
(1)X、Y、Z的元素符号分别是: 、 、
(2)有X、Y、Z所形成的离子化合物是 ,它与W的最高价氧化物对应水化物的溶液加热时反应的离子方程式是
29、(11分,每空2分)实验室合成氨装置如图:
试回答:
(1)装置甲的作用是:①_____________________,②_____________________________,
(2)从丙导出的气体是_______________,
(3)乙中发生的反应方程式为________________________________________,
(4)检验产物的简单化学方法是______________________________________________。
30、(8分,每空2分)某温度时,在2L容器中x、y、z三种物质随时间的变化关系曲线如图所示。
(1)由图中的数据分析,该反应的化学方程式为 ;
(2)反应开始至2min、5min z的平均反应速率为 、 ;
(3)5min后z的生成速率比5min末z的生成速率 (大、小、相等)。
31、(6分)标准状况下,将560LNH3溶于水最终形成1L溶液,求氨水的物质的量浓度和质量分数。
(9分,每空1分)(1)⑤⑥ 、②、 ② 、⑤ (2)①③④ 、① 、⑤⑥
28、(6分,除离子方程式2分外,其余每空1分)1)H N O
(2)NH4NO3 NH4++OH-NH3↑+H2O
30、(8分,每空2分)(1)3x+y 2z
(2)0.05mol·(l·min)-1;0.04mol·(l·min)-1
相等
31、(6分,每问3分)25mol/L、29.8%
化学试题
时间:100分钟 总分:100分
本试卷可能用到的原子量:H-1 N-14 O-16 S-32 Cu-64
第Ⅰ卷 选择题(共50分)
选择题(本题包括25小题,每小题2分,共50分。每小题只有一个选项符合题意。)
1、引起1998年广东珠江口附近海域发生的赤潮主要是由于
A.环境污染导致有毒藻类大量繁殖 B.温室效应导致水温升高
C.人类大量捕捞鱼类 D.人类活动导致鱼的食物不足
2、下列叙述正确的是
A. O2的结构式为 O-O B.硫离子的结构示意图为:
C.CCl4分子的比例模型: D.H2O的电子式:
3、下列物质中,不含有共价键的是
A.MgCl2 B.MgCO3 C.HCl D.NaOH
4、下列物质互为同分异构体的一组是
A. 氧气与臭氧 B. 乙醇(CH3CH2OH)和二甲醚(CH3OCH3)
C. 35Cl和37Cl D. 火碱与烧碱
5、已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是原子半径最小的元素,Y的最高正价与最低负价的代数和为0,Z的二价阳离子与氖原子具有相同的核外电子排布,W原子最外层电子数是最内层电子数的3倍。下列说法正确的是
A.R的原子半径比Z的大 B.R的氢化物的热稳定性比W的强
C.X与Y形成的化合物只有一种 D. Y的最高价氧化物的水化物的酸性比W的强
6、2SO2+O2 2SO3 ,是工业上制造氮肥的重要反应。下列关于该反应的说法正确的是
A.增加N2的浓度加快反应速率 B.降低体系温度能加快反应速率
C.使用催化剂不影响反应速率
D.若反应在密闭容器中进行,SO2和O2能100%转化为SO3
7、下列变化过程与能量的说法中正确的是
A.中和反应是吸热反应 B.燃烧属于放热反应
C.化学键断裂放出能量 D.反应物总能量与生成物总能量一定相等
下列试剂:①浓HNO3 ②AgNO3 ③NaCl溶液④氯水⑤氨水⑥NaHCO3应避光保存的是 A.①②③ B. ④⑤⑥ C . ①②④ D . ②③⑥
9、下列变化中,属于物理变化的是
①红磷加热升华变成白磷 ②氯化铵晶体受热后由试管底部移到试管上部 ③固体碘受热变成碘蒸气 ④干冰汽化 ⑤浓硝酸从无色液体变成黄色液体
A. ①② B. ③④ C. ④⑤ D. ③④⑤
10、下列除去杂质的操作方法正确的是
A.食盐中有少量的NH4Cl:加过量的烧碱溶液后加热蒸干
B. NO2中有少量的NO:通入过量的氧气
C. CO2中混有少量的HCl:通过饱和的NaHCO3溶液后再干燥
D. 红磷中有少量的白磷:加热到40℃,使白磷自燃
11、下列有关比较,正确的是
A.稳定性:SiH4>PH3>H2S B.非金属性:Si< S < P
C.酸性:H4SiO4
D.AlCl3溶液中加入氨水:Al3++3OH-=Al(OH)3↓
16、下列性质可以证明化合物内一定存在离子键的是
A.可溶于水 B.具有较高的熔点 C.水溶液能导电 D.熔融状态能导电
17、下列各组物质发生状态变化所克服的微粒间的相互作用属于同种类型的是
A.食盐和蔗糖溶于水 B.氯化钠和硫熔化
C.碘和干冰升华 D.二氧化硅和氧化钠熔化
18、不能用如图所示装置进行喷泉实验的一组气体是
A. HCl B.CO2 C. NH3 D.CO
19.下列各图中表示正反应是吸热反应的图是
20、在2A+B 3C+5D反应中,表示该反应速率最快的是
A.v(A)= 0.5 mol/(L·s) B.v(B)= 0.3 mol/(L·s)
C.v(C)= 0.8 mol/(L·s) D.v(D)= 1 mol/(L·s)
21、在一定温度下,可逆A(g) + 3B(g) 2C(g)达到平衡的标志是:
A.C的生成速率与B的生成速率相等 B.单位时间生成n molA,同时生成3n molB C.A、B、C的体积分数不再变化 D.A、B、C的分子数比为1:3:2
22、从经济效益和环境保护考虑,大量制取硝酸铜最适宜采用的方法是: A.Cu+HNO3(浓)→Cu(NO3)2+NO2↑ B.Cu+HNO3 (稀) →Cu(NO3)2+NO↑+H2O C.Cu+O2→CuO,CuO+HNO3 (稀) →Cu(NO3)+H2O D.Cu +AgNO3 →Cu(NO3)2+Ag
23、在酸性溶液中能大量共存的离子组是
A.K+、OH-、Na+ B.Fe2+、NO3-、Na+
C.Ba2+、SO42-、Na+ D.Ca2+、 Cl-、Na+
24、下图是实验室制取氨气的装置和选用的试剂,其中错误的是
A.①④ B.①③ C.②④ D.②③
25、将3. 84克铜粉与一定质量浓硝酸反应,当铜完全作用时,收集到气体4.48L(标况下),则所消耗硝酸的物质的量是
A. 0.26mol B. 0.32mol C. 0.16mol D. 0.2mol
第II卷 非选择题(共50分)
二、填空题
26、(10分,每空1分)下表标出的是元素周期表的一部分元素,回答下列问题:
(1)表中用字母标出的14种元素中,化学性质最不活泼的是 (用元素符号表示,下同),金属性最强的是 ,非金属性最强的是 ,常温下单质为液态的非金属元素是 ,属于过渡元素的是 (该空用字母表示)。
(2)B、F、C气态氢化物的化学式分别为 、 、 ,其中以 最不稳定。
(3)第二周期中原子半径最小的是 。
27、(9分,每空1分)现有①BaCl2、②金刚石、③KNO3、④Na2SO4、⑤干冰、⑥碘片六种
物质,按下列要求回答:
(1)(填序号)熔化时不需要破坏化学键的是 ,熔化时需要破坏共价键的是 , 熔点最高的是 ,熔点最低的是 。
(2)(填序号)属于离子化合物的是 ,只有离子键的物质是 ,晶体以分子间作用力结合的是 。
(3)①的电子式是 ,⑤的电子式是 。
28、(6分,除离子方程式2分外,其余每空1分)X、Y、Z、W四种元素在元素周期表中序数逐渐增大。X为非金属元素,且X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。试推断:
(1)X、Y、Z的元素符号分别是: 、 、
(2)有X、Y、Z所形成的离子化合物是 ,它与W的最高价氧化物对应水化物的溶液加热时反应的离子方程式是
29、(11分,每空2分)实验室合成氨装置如图:
试回答:
(1)装置甲的作用是:①_____________________,②_____________________________,
(2)从丙导出的气体是_______________,
(3)乙中发生的反应方程式为________________________________________,
(4)检验产物的简单化学方法是______________________________________________。
30、(8分,每空2分)某温度时,在2L容器中x、y、z三种物质随时间的变化关系曲线如图所示。
(1)由图中的数据分析,该反应的化学方程式为 ;
(2)反应开始至2min、5min z的平均反应速率为 、 ;
(3)5min后z的生成速率比5min末z的生成速率 (大、小、相等)。
31、(6分)标准状况下,将560LNH3溶于水最终形成1L溶液,求氨水的物质的量浓度和质量分数。
(9分,每空1分)(1)⑤⑥ 、②、 ② 、⑤ (2)①③④ 、① 、⑤⑥
28、(6分,除离子方程式2分外,其余每空1分)1)H N O
(2)NH4NO3 NH4++OH-NH3↑+H2O
30、(8分,每空2分)(1)3x+y 2z
(2)0.05mol·(l·min)-1;0.04mol·(l·min)-1
相等
31、(6分,每问3分)25mol/L、29.8%
同课章节目录
