【备考2023】浙教版科学中考“临阵磨枪”专题训练(二十一):物质鉴别、检验、推断【word,含解析】
文档属性
| 名称 | 【备考2023】浙教版科学中考“临阵磨枪”专题训练(二十一):物质鉴别、检验、推断【word,含解析】 |

|
|
| 格式 | doc | ||
| 文件大小 | 133.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-04-07 00:00:00 | ||
图片预览


文档简介
1.某固体由 Ba2+、Cu2+、Na+、Cl﹣、CO32﹣、SO42﹣中的几种离子构成,取一定质量的该固体样品,进行如下实验:
①将固体溶于水得无色透明溶液,加入足量BaCl2溶液过滤,得到白色沉淀和无色滤液。
②在白色沉淀中加入过量稀硝酸,白色沉淀部分溶解并产生气泡。
③在无色滤液中滴加AgNO3溶液产生白色沉淀。
由此推断该固体中一定含有的离子是( )
A.Na+、CO32﹣、SO42﹣
B.Na+、CO32﹣、SO42﹣、Cl﹣
C.Ba2+、CO32﹣、SO42﹣、Cl﹣
D.Cu2+、Ba2+、CO32﹣、SO42﹣
2.有一包白色固体样品,可能含氢氧化钠、硝酸钠、碳酸钠、硫酸钠、氯化钡中的一种或几种。小金同学为探究其成分,完成了以下实验:①取少量白色固体溶于水,得到无色溶液,等分为两份:②往一份无色溶液中加入稀硫酸,产生沉淀质量与所加稀硫酸质量关系如图所示;③往另一份无色溶液中通入适量的CO2,产生白色沉淀。下列说法正确的是( )
A.样品中一定存在NaOH、NaNO3、BaCl2,一定不存在Na2SO4
B.加入硫酸后产生的沉淀一定有BaSO4,可能有BaCO3
C.样品中一定含BaCl2,可能含NaOH
D.通入二氧化碳后产生的沉淀一定只有BaCO3
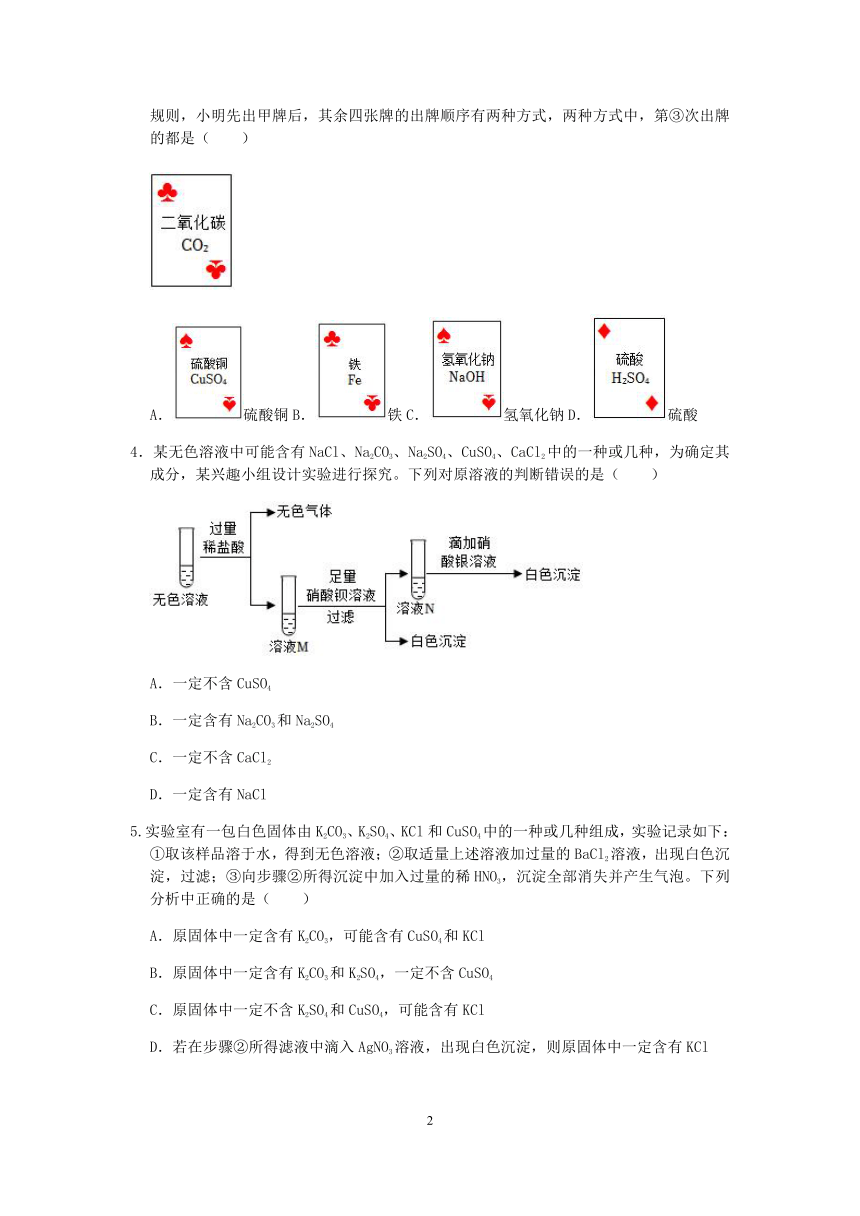
3.“停课不停学”期间小明在家里玩“纸牌接龙”游戏,规则是:出一张牌后,下一张牌上所提示的物质要与先出的那张牌上所提示的物质发生化学反应。小明先出甲牌后,手上还有A,B,C,D四张牌。出牌顺序:甲____________________;为符合游戏规则,小明先出甲牌后,其余四张牌的出牌顺序有两种方式,两种方式中,第③次出牌的都是( )
A.硫酸铜B.铁C.氢氧化钠D.硫酸
4.某无色溶液中可能含有NaCl、Na2CO3、Na2SO4、CuSO4、CaCl2中的一种或几种,为确定其成分,某兴趣小组设计实验进行探究。下列对原溶液的判断错误的是( )
A.一定不含CuSO4
B.一定含有Na2CO3和Na2SO4
C.一定不含CaCl2
D.一定含有NaCl
5.实验室有一包白色固体由K2CO3、K2SO4、KCl和CuSO4中的一种或几种组成,实验记录如下:①取该样品溶于水,得到无色溶液;②取适量上述溶液加过量的BaCl2溶液,出现白色沉淀,过滤;③向步骤②所得沉淀中加入过量的稀HNO3,沉淀全部消失并产生气泡。下列分析中正确的是( )
A.原固体中一定含有K2CO3,可能含有CuSO4和KCl
B.原固体中一定含有K2CO3和K2SO4,一定不含CuSO4
C.原固体中一定不含K2SO4和CuSO4,可能含有KCl
D.若在步骤②所得滤液中滴入AgNO3溶液,出现白色沉淀,则原固体中一定含有KCl
6.甲、乙、丙、丁为初中化学常见物质,其转化关系为初中化学常见反应。根据图示(反应条件已省略),下列说法正确的是( )
A.若甲为单质、乙为化合物,该反应一定是置换反应
B.若丙、丁分别是盐和水,则甲和乙分别是酸和碱
C.若甲为BaCl2溶液,该过程为复分解反应,则丙、丁中一定有一种物质是BaCO3或BaSO4
D.若甲、乙、丙、丁均为化合物,该反应前后各元素的化合价不一定改变
7.甲、乙、丙三种物质存在如下转化关系(均为一步反应,部分反应物、生成物或反应条件均已略去),则下列对于甲物质的判断,错误的是( )
A.若乙是最常用的溶剂,丙是单质,则甲可能是H2O2
B.若甲是一种常见的黑色固体,乙和丙是组成元素相同的两种气体,则甲应该是C
C.若乙是常见的一种温室气体,丙是大理石的主要成分,则甲只能是K2CO3
D.若甲是黑色固体,乙是紫红色金属,丙的溶液显蓝色,则甲一定是CuO
8.甲、乙、丙、丁四种溶液中,分别含有Ba2+、Mg2+、Na+、H+、Cl﹣、OH﹣、CO32﹣、SO42﹣中的一种阳离子和一种阴离子。为确定四种溶液中分别含有哪种阳离子或阴离子,进行了如下实验:
①将甲溶液分别与其他三种溶液混合,都观察到白色沉淀生成
②将乙、丁溶液混合,有气泡产生
③向丙溶液中滴入AgNO3溶液,可明显观察到白色沉淀,加稀硝酸后,沉淀不消失
分析实验得到的以下结论中错误的是( )
A.甲溶液中一定含有Ba2+ B.乙溶液中可能含有SO42﹣
C.丙溶液中一定含有Cl﹣ D.丁溶液中一定含有Na+
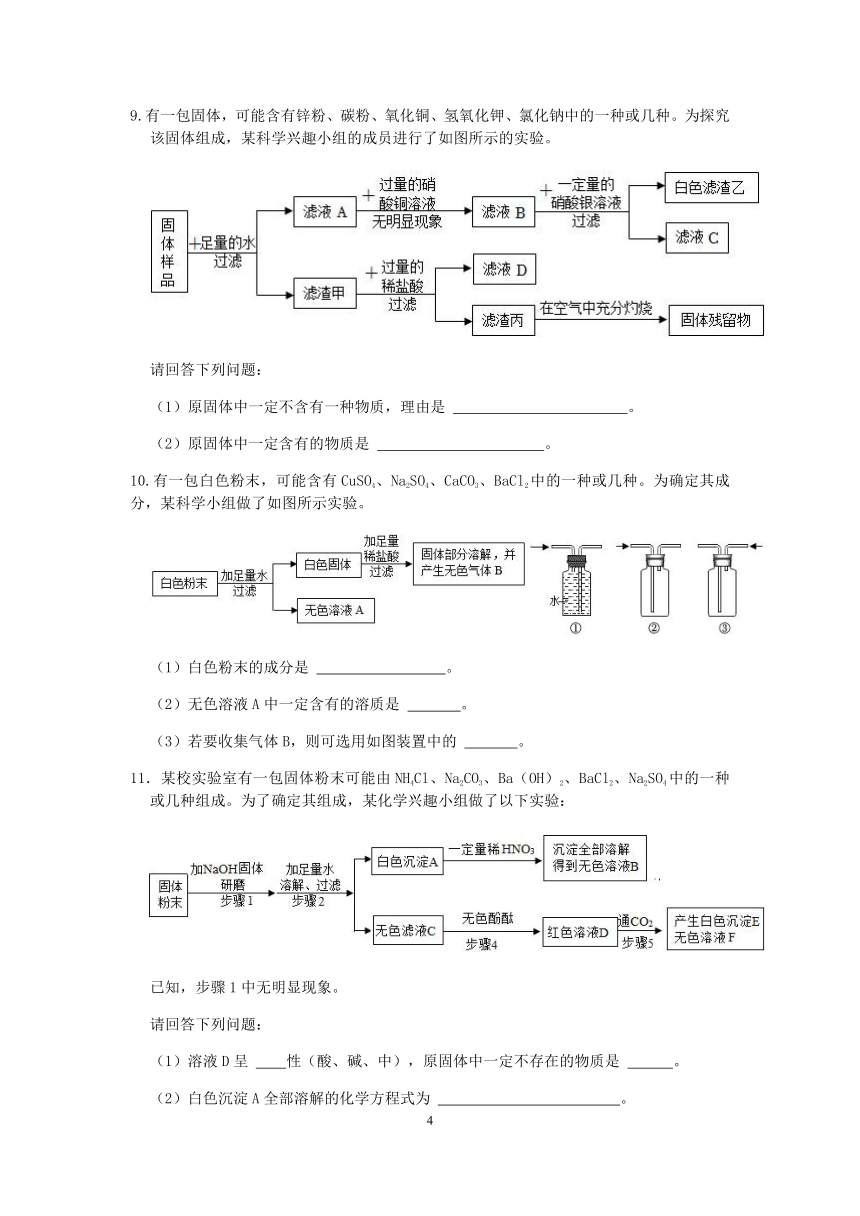
9.有一包固体,可能含有锌粉、碳粉、氧化铜、氢氧化钾、氯化钠中的一种或几种。为探究该固体组成,某科学兴趣小组的成员进行了如图所示的实验。
请回答下列问题:
(1)原固体中一定不含有一种物质,理由是 。
(2)原固体中一定含有的物质是 。
10.有一包白色粉末,可能含有CuSO4、Na2SO4、CaCO3、BaCl2中的一种或几种。为确定其成分,某科学小组做了如图所示实验。
(1)白色粉末的成分是 。
(2)无色溶液A中一定含有的溶质是 。
(3)若要收集气体B,则可选用如图装置中的 。
11.某校实验室有一包固体粉末可能由NH4Cl、Na2CO3、Ba(OH)2、BaCl2、Na2SO4中的一种或几种组成。为了确定其组成,某化学兴趣小组做了以下实验:
已知,步骤1中无明显现象。
请回答下列问题:
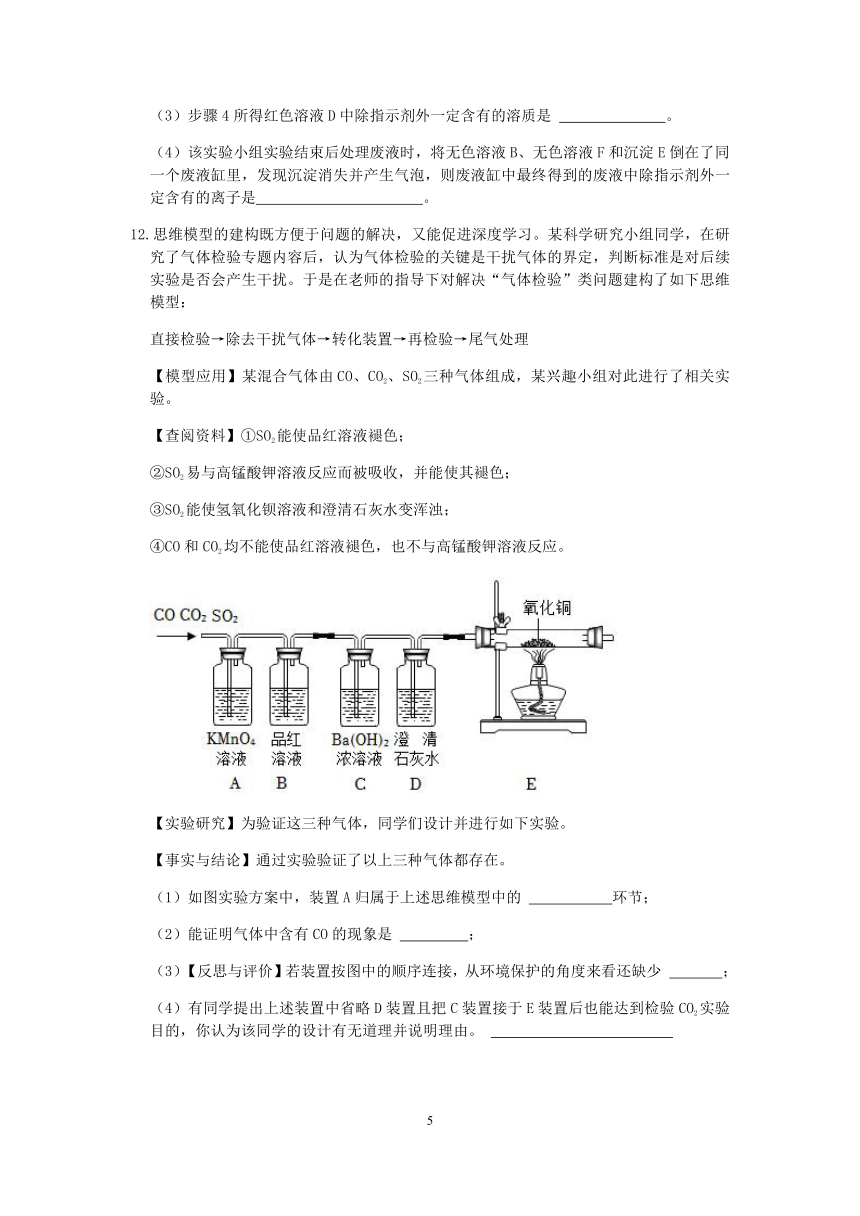
(1)溶液D呈 性(酸、碱、中),原固体中一定不存在的物质是 。
(2)白色沉淀A全部溶解的化学方程式为 。
(3)步骤4所得红色溶液D中除指示剂外一定含有的溶质是 。
(4)该实验小组实验结束后处理废液时,将无色溶液B、无色溶液F和沉淀E倒在了同一个废液缸里,发现沉淀消失并产生气泡,则废液缸中最终得到的废液中除指示剂外一定含有的离子是 。
12.思维模型的建构既方便于问题的解决,又能促进深度学习。某科学研究小组同学,在研究了气体检验专题内容后,认为气体检验的关键是干扰气体的界定,判断标准是对后续实验是否会产生干扰。于是在老师的指导下对解决“气体检验”类问题建构了如下思维模型:
直接检验→除去干扰气体→转化装置→再检验→尾气处理
【模型应用】某混合气体由CO、CO2、SO2三种气体组成,某兴趣小组对此进行了相关实验。
【查阅资料】①SO2能使品红溶液褪色;
②SO2易与高锰酸钾溶液反应而被吸收,并能使其褪色;
③SO2能使氢氧化钡溶液和澄清石灰水变浑浊;
④CO和CO2均不能使品红溶液褪色,也不与高锰酸钾溶液反应。
【实验研究】为验证这三种气体,同学们设计并进行如下实验。
【事实与结论】通过实验验证了以上三种气体都存在。
(1)如图实验方案中,装置A归属于上述思维模型中的 环节;
(2)能证明气体中含有CO的现象是 ;
(3)【反思与评价】若装置按图中的顺序连接,从环境保护的角度来看还缺少 ;
(4)有同学提出上述装置中省略D装置且把C装置接于E装置后也能达到检验CO2实验目的,你认为该同学的设计有无道理并说明理由。
答案及解析
1.A
解:将固体溶于水得无色透明溶液,说明不含铜离子;加入足量BaCl2溶液,过滤后得到白色沉淀,说明固体中可能含有硫酸根离子、碳酸根离子等;在沉淀中加入过量稀硝酸,仍有白色沉淀,说明存在不溶于稀硝酸的白色沉淀,即说明白色沉淀中含有硫酸钡、碳酸钡;滤液中含有过量的稀硝酸,在滤液中滴加AgNO3溶液,产生白色沉淀,说明生成了不溶于稀硝酸的氯化银沉淀,说明固体中存在氯离子,由于加入足量BaCl2溶液,但无法确定原固体中是否含有氯离子;钡离子和铜离子都不存在,故该固体中一定含有Na+、CO32﹣、SO42﹣,可能存在Cl﹣,一定不存在Ba2+、Cu2+。
故选:A。
2.D
解:①取少量白色固体溶于水,得到无色溶液,等分为两份,所以碳酸钠、硫酸钠和氯化钡不能同时存在;
②往一份无色溶液中加入稀硫酸,产生沉淀质量与所加稀硫酸质量关系如图所示;可知含有氯化钡;由①可知,则溶液一定不含有碳酸钠和硫酸钠;
③往另一份无色溶液中通入适量的CO2,产生白色沉淀,氢氧化钠和二氧化碳反应生成碳酸钠和水,碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,所以样品中一定含有氢氧化钠、氯化钡,一定不含硫酸钠、碳酸钠,可能含有硝酸钠,
A、样品中一定含有氢氧化钠、氯化钡,一定不含硫酸钠、碳酸钠,可能含有硝酸钠,故A错误;
B、加入稀硫酸时产生的沉淀是硫酸钡,故B错误;
C、样品中一定含有氢氧化钠和氯化钡,故C错误;
D、氢氧化钠和二氧化碳反应生成碳酸钠和水,碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,故D正确。
故选:D。
3.B
解:“纸牌接龙”游戏,规则是:出一张牌后,下一张牌上所提示的物质要与先出的那张牌上所提示的物质发生化学反应,小明先出甲牌后,手上还有A,B,C,D四张牌,出牌顺序:甲____________________;二氧化碳会与氢氧化钠反应,所以①出牌是氢氧化钠,氢氧化钠会与硫酸、硫酸铜反应,所以②是硫酸或硫酸铜,硫酸、硫酸铜都会与铁反应,所以③是铁,剩余的④就是硫酸铜或硫酸,经过验证,推导正确,所以为符合游戏规则,小明先出甲牌后,其余四张牌的出牌顺序有两种方式,两种方式中,第③次出牌的都是铁,故选:B。
4.D
解:A、原溶液为无色,而硫酸铜溶液为蓝色,故溶液中一定不含硫酸铜,选项正确,不符合题意;
B、溶液中加入过量稀盐酸,产生无色气体,说明原溶液中一定含有碳酸钠,溶液M中加硝酸钡出现白色沉淀说明,原溶液含有硫酸根离子,又因为溶液中没有硫酸铜,所以一定含有硫酸钠,故溶液中一定含有碳酸钠和硫酸钠,选项正确,不符合题意:
C、溶液中加入过量稀盐酸,产生无色气体,说明原溶液中一定含有碳酸钠,碳酸钠能与氯化钙反应,故原溶液一定不含氯化钙,选项正确,不符合题意;
D、开始加入的过量稀盐酸会引入氯离子,溶液N中加入硝酸银,一定会产生白色沉淀,不能判断是否含有氯化钠,选项错误;符合题意;
故选:D。
5.C
解:硫酸铜在溶液中显蓝色,碳酸根离子和钡离子反应生成溶于酸的碳酸钡沉淀,硫酸根离子和钡离子反应生成不溶于酸的硫酸钡沉淀,所以①取该样品溶于水,得到无色溶液,说明样品中一定不含硫酸铜;②取适量上述溶液加过量的BaCl2溶液,出现白色沉淀,样品中含有硫酸钾、碳酸钾中的一种或两种;③向步骤②所得沉淀中加入过量的HNO3,沉淀全部消失并产生气泡,所以样品中一定含有碳酸钾,一定不含硫酸钾,可能会有氯化钾。
A、经过上述分析知原固体中一定不含K2SO4、CuSO4,可能含有KCl,故A选项不符合题意;
B、经过上述分析知原固体中一定不含K2SO4、CuSO4,可能含有KCl,故B选项不符合题意;
C、经过上述分析知原固体中一定不含K2SO4、CuSO4,可能含有KCl,故C选项符合题意;
D、②所得滤液中有加入过量的氯化钡和原固体中可能含有的氯化钾,所以滴入AgNO3溶液,出现的白色沉淀不能确定是氯化钡和硝酸银反应生成的还是氯化钾与硝酸银生成的,故D选项不符合题意;
故选:C。
6.D
解:A、若甲为单质,乙为化合物,该应不一定是置换反应,如甲为氧气,乙为甲烷,甲烷和氧气在点燃的条件下反应生成二氧化碳和水,生成物均是化合物,不属于置换反应,不符合题意;
B、如丙、丁分别是盐和水,则甲和乙不一定是酸和碱,如氢氧化钠和二氧化碳反应生成碳酸钠和水,不符合题意;
C、若甲为BaCl2溶液,该过程为复分解反应,丙、丁中不一定有一种物质是碳酸钡或硫酸钡,如氯化钡和硝酸银反应生成氧化银和硝酸钡,不符合题意;
D、若甲、乙、丙、丁均为化合物,该应前后,各元素的化合价可能不变,如氢氧化钠和稀盐酸反应生成氯化钠和水,也可能改变,如二氧化氮和水反应生成硝酸和一氧化氮,氮元素的合价发生了改变,符合题意;
故选:D。
7.C
解:A、乙是最常用的溶剂,乙是水,丙是单质,则甲可以是过氧化氢,过氧化氢分解生成水和氧气,故选项说法正确;
B、若甲是一种常见的黑色固体,黑色固体碳能生成两种组成元素相同的气体一氧化碳和二氧化碳,丙→乙可以是二氧化碳和碳高温反应生成一氧化碳,故选项说法正确;
C、乙是一种常见的温室气体,则乙是二氧化碳,丙是大理石的主要成分,丙是碳酸钙,碳酸钠或碳酸钾可以和稀盐酸可以反立生成二氧化碳,可以和氯化钙反应生成碳酸钙沉淀,碳酸钙可以和盐酸反应生成二氧化碳,二氧化碳可以和氢氧化钙反应生成碳酸钙,甲可以是K2CO3也可以是碳酸钠,故选项说法错误;
D、乙是紫红色金属,乙是铜,丙是蓝色溶液,可以是硝酸铜,甲能反应生成乙和丙,且是黑色固体,则甲是氧化铜,氧化铜和一氧化碳反应生成铜,氧化铜和硝酸反应生成硝酸铜,铜和硝酸银溶液反应生成硝酸铜,铁和硝酸铜能反应生成铜,故选项说法正确;
故选:C。
8.D
解:甲、乙、丙、丁四种溶液中,分别含有Ba2+、Mg2+、Na+、H+、Cl﹣、CO32﹣、SO42﹣、OH﹣中的一种阳离子和一种阴离子,可以组成的物质有BaCl2、Ba(OH)2、MgCl2、MgSO4、HCl、H2SO4、NaCl、NaOH、Na2CO3、Na2SO4;
①将甲溶液分别与其他三种溶液混合,都观察到白色沉淀生成,能形成沉淀的离子组合是CO32﹣和Ba2+、Ba2+和SO42﹣、Mg2+和OH﹣;故甲可以是氢氧化钡;
②将乙、丁溶液混合,有气泡产生,则乙、丁溶液中分别含有H+和CO32﹣中的一种;乙、丁可以分别是硫酸和碳酸钠中的一种,无法具体判断分别是谁;
③向丙溶液中滴入AgNO3溶液,可明显观察到白色,加稀硝酸后,沉淀不消失,则丙溶液中含有Cl﹣,丙可以是氯化镁;
代入题干,推断合理;
A、甲溶液中一定含有Ba2+,说法正确;
B、乙溶液可能是硫酸溶液,也可能是碳酸钠溶液,因此可能含有SO42﹣,说法正确;
C、丙溶液是氯化镁溶液,一定含有Cl﹣,说法正确;
D、丁溶液可能是硫酸溶液,也可能是碳酸钠溶液,因此可能含有Na+,说法错误;
故选:D。
9.解:(1)固体样品加水过滤得滤液和滤渣,滤液A中加过量硝酸铜溶液无明显现象,因氢氧化钾会与硝酸铜反应产生蓝色沉淀,所以一定不含氢氧化钾;故答案为:滤液A中加过量硝酸铜溶液无明显现象;
(2)滤液B中加适量硝酸银溶液生成白色滤渣乙和滤液C,说明滤液B中含有氯离子,样品中含有氯化钠;滤渣甲加入过量稀盐酸,得滤液D和滤渣丙,滤渣丙在空气中充分灼烧,得固体残留物,因锌、碳、氧化铜都不溶于水,但锌和氧化铜能溶于酸,且锌能与氯化铜溶液反应置换出铜,碳在空气中灼烧会生成气体,铜在空气中灼烧会生成氧化铜,所以原固体中一定含有氯化钠,氧化铜,锌;故答案为:氯化钠,氧化铜,锌。
10.解:根据白色固体溶于水,得到白色沉淀和无色溶液A,白色沉淀与盐酸反应会生成无色气体B、固体部分被溶解。根据提供的物质碳酸钙难溶于水,与盐酸反应生成氯化钙、水和二氧化碳,气体B为二氧化碳;氯化钡与硫酸钠溶液反应分别生成硫酸钡白色沉淀,硫酸钡沉淀不溶于稀盐酸,说明白色沉淀为碳酸钙和硫酸钡的混合物,白色不溶物为硫酸钡,则白色固体中一定含有氯化钡、碳酸钠和含硫酸钠;含铜离子的溶液为蓝色,溶液A为无色,说明一定不存在硫酸铜;所以:
(1)白色不溶物的成分是氯化钡、硫酸钠和碳酸钙;故答案为:氯化钡、硫酸钠和碳酸钙;
(2)氯化钡与硫酸钠反应生成硫酸钡沉淀和氯化钠,无色溶液A中一定含有的溶质是氯化钠;故答案为:氯化钠;
(3)气体B为二氧化碳,二氧化碳能溶于水,密度比空气大,若因此要收集气体B,则可选用如图装置中的②;故答案为:②。
11.解:(1)由分析可知,溶液D加入无色酚酞后显红色,说明溶液D呈碱性;这包固体中一定不存在的物质是:NH4Cl、Na2SO4;
(2)白色沉淀A全部溶解的化学方程式为:BaCO3+2HNO3=BaNO3+H2O+CO2↑;
(3)由分析可知,步骤4所得红色溶液D中一定含有的溶质是:酚酞、氢氧化钠、氯化钡和氯化钠;
(4)将无色溶液B、无色溶液F和沉淀E倒在了同一个废液缸里,发现沉淀消失并产生气泡,无色溶液B有2种情况“硝酸钡”和“硝酸钡、硝酸”,沉淀E为碳酸钡,它们倒在同一个废液缸里,沉淀消失并产生气泡,由此可知,无色溶液B中的溶质为“硝酸钡、硝酸”,硝酸与碳酸钡反应生成硝酸钡、水和二氧化碳,溶液中一定含有硝酸钡,无色溶液F中一定含有氯化钠,则废液缸中最终得到的废液中一定含有的溶质是硝酸钡和氯化钠,则废液缸中最终得到的废液中除指示剂外一定含有的离子是钠离子、氯离子、钡离子、硝酸根离子。
故答案为:
(1)NH4Cl、Na2SO4;
(2)BaCO3+2HNO3=BaNO3+H2O+CO2↑;
(3)氢氧化钠,以及氢氧化钡和氯化钡中的一种;
(4)钠离子、氯离子、钡离子、硝酸根离子。
12.解:(1)装置A是为了验证气体中存在二氧化硫并将其除去,以免干扰二氧化碳验证,属于思维模型中的直接检验和除去干扰气体;故答案为:直接检验和除去干扰气体;
(2)CO具有还原性,可利用在加热的条件下,CO能使氧化铜还原成铜,证明CO存在,所以证明CO的现象是E装置中黑色固体变红色;故答案为:E装置中黑色固体变红色;
(3)该装置中将尾气排放到空气中,会污染空气,所以缺少尾气处理装置;故答案为:尾气处理;
(4)在用酒精灯加热前是要先通入一段时间的检验气体,根据B中的品红溶液不变色和C中的氢氧化钡溶液是否变浑浊,也可检验出CO2,故答案为:有道理,在用酒精灯加热前是要先通入一段时间的检验气体,根据B中的品红溶液不变色和C中的氢氧化钡溶液是否变浑浊,也可检验出CO2。
物质鉴别、检验、推断
①将固体溶于水得无色透明溶液,加入足量BaCl2溶液过滤,得到白色沉淀和无色滤液。
②在白色沉淀中加入过量稀硝酸,白色沉淀部分溶解并产生气泡。
③在无色滤液中滴加AgNO3溶液产生白色沉淀。
由此推断该固体中一定含有的离子是( )
A.Na+、CO32﹣、SO42﹣
B.Na+、CO32﹣、SO42﹣、Cl﹣
C.Ba2+、CO32﹣、SO42﹣、Cl﹣
D.Cu2+、Ba2+、CO32﹣、SO42﹣
2.有一包白色固体样品,可能含氢氧化钠、硝酸钠、碳酸钠、硫酸钠、氯化钡中的一种或几种。小金同学为探究其成分,完成了以下实验:①取少量白色固体溶于水,得到无色溶液,等分为两份:②往一份无色溶液中加入稀硫酸,产生沉淀质量与所加稀硫酸质量关系如图所示;③往另一份无色溶液中通入适量的CO2,产生白色沉淀。下列说法正确的是( )
A.样品中一定存在NaOH、NaNO3、BaCl2,一定不存在Na2SO4
B.加入硫酸后产生的沉淀一定有BaSO4,可能有BaCO3
C.样品中一定含BaCl2,可能含NaOH
D.通入二氧化碳后产生的沉淀一定只有BaCO3
3.“停课不停学”期间小明在家里玩“纸牌接龙”游戏,规则是:出一张牌后,下一张牌上所提示的物质要与先出的那张牌上所提示的物质发生化学反应。小明先出甲牌后,手上还有A,B,C,D四张牌。出牌顺序:甲____________________;为符合游戏规则,小明先出甲牌后,其余四张牌的出牌顺序有两种方式,两种方式中,第③次出牌的都是( )
A.硫酸铜B.铁C.氢氧化钠D.硫酸
4.某无色溶液中可能含有NaCl、Na2CO3、Na2SO4、CuSO4、CaCl2中的一种或几种,为确定其成分,某兴趣小组设计实验进行探究。下列对原溶液的判断错误的是( )
A.一定不含CuSO4
B.一定含有Na2CO3和Na2SO4
C.一定不含CaCl2
D.一定含有NaCl
5.实验室有一包白色固体由K2CO3、K2SO4、KCl和CuSO4中的一种或几种组成,实验记录如下:①取该样品溶于水,得到无色溶液;②取适量上述溶液加过量的BaCl2溶液,出现白色沉淀,过滤;③向步骤②所得沉淀中加入过量的稀HNO3,沉淀全部消失并产生气泡。下列分析中正确的是( )
A.原固体中一定含有K2CO3,可能含有CuSO4和KCl
B.原固体中一定含有K2CO3和K2SO4,一定不含CuSO4
C.原固体中一定不含K2SO4和CuSO4,可能含有KCl
D.若在步骤②所得滤液中滴入AgNO3溶液,出现白色沉淀,则原固体中一定含有KCl
6.甲、乙、丙、丁为初中化学常见物质,其转化关系为初中化学常见反应。根据图示(反应条件已省略),下列说法正确的是( )
A.若甲为单质、乙为化合物,该反应一定是置换反应
B.若丙、丁分别是盐和水,则甲和乙分别是酸和碱
C.若甲为BaCl2溶液,该过程为复分解反应,则丙、丁中一定有一种物质是BaCO3或BaSO4
D.若甲、乙、丙、丁均为化合物,该反应前后各元素的化合价不一定改变
7.甲、乙、丙三种物质存在如下转化关系(均为一步反应,部分反应物、生成物或反应条件均已略去),则下列对于甲物质的判断,错误的是( )
A.若乙是最常用的溶剂,丙是单质,则甲可能是H2O2
B.若甲是一种常见的黑色固体,乙和丙是组成元素相同的两种气体,则甲应该是C
C.若乙是常见的一种温室气体,丙是大理石的主要成分,则甲只能是K2CO3
D.若甲是黑色固体,乙是紫红色金属,丙的溶液显蓝色,则甲一定是CuO
8.甲、乙、丙、丁四种溶液中,分别含有Ba2+、Mg2+、Na+、H+、Cl﹣、OH﹣、CO32﹣、SO42﹣中的一种阳离子和一种阴离子。为确定四种溶液中分别含有哪种阳离子或阴离子,进行了如下实验:
①将甲溶液分别与其他三种溶液混合,都观察到白色沉淀生成
②将乙、丁溶液混合,有气泡产生
③向丙溶液中滴入AgNO3溶液,可明显观察到白色沉淀,加稀硝酸后,沉淀不消失
分析实验得到的以下结论中错误的是( )
A.甲溶液中一定含有Ba2+ B.乙溶液中可能含有SO42﹣
C.丙溶液中一定含有Cl﹣ D.丁溶液中一定含有Na+
9.有一包固体,可能含有锌粉、碳粉、氧化铜、氢氧化钾、氯化钠中的一种或几种。为探究该固体组成,某科学兴趣小组的成员进行了如图所示的实验。
请回答下列问题:
(1)原固体中一定不含有一种物质,理由是 。
(2)原固体中一定含有的物质是 。
10.有一包白色粉末,可能含有CuSO4、Na2SO4、CaCO3、BaCl2中的一种或几种。为确定其成分,某科学小组做了如图所示实验。
(1)白色粉末的成分是 。
(2)无色溶液A中一定含有的溶质是 。
(3)若要收集气体B,则可选用如图装置中的 。
11.某校实验室有一包固体粉末可能由NH4Cl、Na2CO3、Ba(OH)2、BaCl2、Na2SO4中的一种或几种组成。为了确定其组成,某化学兴趣小组做了以下实验:
已知,步骤1中无明显现象。
请回答下列问题:
(1)溶液D呈 性(酸、碱、中),原固体中一定不存在的物质是 。
(2)白色沉淀A全部溶解的化学方程式为 。
(3)步骤4所得红色溶液D中除指示剂外一定含有的溶质是 。
(4)该实验小组实验结束后处理废液时,将无色溶液B、无色溶液F和沉淀E倒在了同一个废液缸里,发现沉淀消失并产生气泡,则废液缸中最终得到的废液中除指示剂外一定含有的离子是 。
12.思维模型的建构既方便于问题的解决,又能促进深度学习。某科学研究小组同学,在研究了气体检验专题内容后,认为气体检验的关键是干扰气体的界定,判断标准是对后续实验是否会产生干扰。于是在老师的指导下对解决“气体检验”类问题建构了如下思维模型:
直接检验→除去干扰气体→转化装置→再检验→尾气处理
【模型应用】某混合气体由CO、CO2、SO2三种气体组成,某兴趣小组对此进行了相关实验。
【查阅资料】①SO2能使品红溶液褪色;
②SO2易与高锰酸钾溶液反应而被吸收,并能使其褪色;
③SO2能使氢氧化钡溶液和澄清石灰水变浑浊;
④CO和CO2均不能使品红溶液褪色,也不与高锰酸钾溶液反应。
【实验研究】为验证这三种气体,同学们设计并进行如下实验。
【事实与结论】通过实验验证了以上三种气体都存在。
(1)如图实验方案中,装置A归属于上述思维模型中的 环节;
(2)能证明气体中含有CO的现象是 ;
(3)【反思与评价】若装置按图中的顺序连接,从环境保护的角度来看还缺少 ;
(4)有同学提出上述装置中省略D装置且把C装置接于E装置后也能达到检验CO2实验目的,你认为该同学的设计有无道理并说明理由。
答案及解析
1.A
解:将固体溶于水得无色透明溶液,说明不含铜离子;加入足量BaCl2溶液,过滤后得到白色沉淀,说明固体中可能含有硫酸根离子、碳酸根离子等;在沉淀中加入过量稀硝酸,仍有白色沉淀,说明存在不溶于稀硝酸的白色沉淀,即说明白色沉淀中含有硫酸钡、碳酸钡;滤液中含有过量的稀硝酸,在滤液中滴加AgNO3溶液,产生白色沉淀,说明生成了不溶于稀硝酸的氯化银沉淀,说明固体中存在氯离子,由于加入足量BaCl2溶液,但无法确定原固体中是否含有氯离子;钡离子和铜离子都不存在,故该固体中一定含有Na+、CO32﹣、SO42﹣,可能存在Cl﹣,一定不存在Ba2+、Cu2+。
故选:A。
2.D
解:①取少量白色固体溶于水,得到无色溶液,等分为两份,所以碳酸钠、硫酸钠和氯化钡不能同时存在;
②往一份无色溶液中加入稀硫酸,产生沉淀质量与所加稀硫酸质量关系如图所示;可知含有氯化钡;由①可知,则溶液一定不含有碳酸钠和硫酸钠;
③往另一份无色溶液中通入适量的CO2,产生白色沉淀,氢氧化钠和二氧化碳反应生成碳酸钠和水,碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,所以样品中一定含有氢氧化钠、氯化钡,一定不含硫酸钠、碳酸钠,可能含有硝酸钠,
A、样品中一定含有氢氧化钠、氯化钡,一定不含硫酸钠、碳酸钠,可能含有硝酸钠,故A错误;
B、加入稀硫酸时产生的沉淀是硫酸钡,故B错误;
C、样品中一定含有氢氧化钠和氯化钡,故C错误;
D、氢氧化钠和二氧化碳反应生成碳酸钠和水,碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,故D正确。
故选:D。
3.B
解:“纸牌接龙”游戏,规则是:出一张牌后,下一张牌上所提示的物质要与先出的那张牌上所提示的物质发生化学反应,小明先出甲牌后,手上还有A,B,C,D四张牌,出牌顺序:甲____________________;二氧化碳会与氢氧化钠反应,所以①出牌是氢氧化钠,氢氧化钠会与硫酸、硫酸铜反应,所以②是硫酸或硫酸铜,硫酸、硫酸铜都会与铁反应,所以③是铁,剩余的④就是硫酸铜或硫酸,经过验证,推导正确,所以为符合游戏规则,小明先出甲牌后,其余四张牌的出牌顺序有两种方式,两种方式中,第③次出牌的都是铁,故选:B。
4.D
解:A、原溶液为无色,而硫酸铜溶液为蓝色,故溶液中一定不含硫酸铜,选项正确,不符合题意;
B、溶液中加入过量稀盐酸,产生无色气体,说明原溶液中一定含有碳酸钠,溶液M中加硝酸钡出现白色沉淀说明,原溶液含有硫酸根离子,又因为溶液中没有硫酸铜,所以一定含有硫酸钠,故溶液中一定含有碳酸钠和硫酸钠,选项正确,不符合题意:
C、溶液中加入过量稀盐酸,产生无色气体,说明原溶液中一定含有碳酸钠,碳酸钠能与氯化钙反应,故原溶液一定不含氯化钙,选项正确,不符合题意;
D、开始加入的过量稀盐酸会引入氯离子,溶液N中加入硝酸银,一定会产生白色沉淀,不能判断是否含有氯化钠,选项错误;符合题意;
故选:D。
5.C
解:硫酸铜在溶液中显蓝色,碳酸根离子和钡离子反应生成溶于酸的碳酸钡沉淀,硫酸根离子和钡离子反应生成不溶于酸的硫酸钡沉淀,所以①取该样品溶于水,得到无色溶液,说明样品中一定不含硫酸铜;②取适量上述溶液加过量的BaCl2溶液,出现白色沉淀,样品中含有硫酸钾、碳酸钾中的一种或两种;③向步骤②所得沉淀中加入过量的HNO3,沉淀全部消失并产生气泡,所以样品中一定含有碳酸钾,一定不含硫酸钾,可能会有氯化钾。
A、经过上述分析知原固体中一定不含K2SO4、CuSO4,可能含有KCl,故A选项不符合题意;
B、经过上述分析知原固体中一定不含K2SO4、CuSO4,可能含有KCl,故B选项不符合题意;
C、经过上述分析知原固体中一定不含K2SO4、CuSO4,可能含有KCl,故C选项符合题意;
D、②所得滤液中有加入过量的氯化钡和原固体中可能含有的氯化钾,所以滴入AgNO3溶液,出现的白色沉淀不能确定是氯化钡和硝酸银反应生成的还是氯化钾与硝酸银生成的,故D选项不符合题意;
故选:C。
6.D
解:A、若甲为单质,乙为化合物,该应不一定是置换反应,如甲为氧气,乙为甲烷,甲烷和氧气在点燃的条件下反应生成二氧化碳和水,生成物均是化合物,不属于置换反应,不符合题意;
B、如丙、丁分别是盐和水,则甲和乙不一定是酸和碱,如氢氧化钠和二氧化碳反应生成碳酸钠和水,不符合题意;
C、若甲为BaCl2溶液,该过程为复分解反应,丙、丁中不一定有一种物质是碳酸钡或硫酸钡,如氯化钡和硝酸银反应生成氧化银和硝酸钡,不符合题意;
D、若甲、乙、丙、丁均为化合物,该应前后,各元素的化合价可能不变,如氢氧化钠和稀盐酸反应生成氯化钠和水,也可能改变,如二氧化氮和水反应生成硝酸和一氧化氮,氮元素的合价发生了改变,符合题意;
故选:D。
7.C
解:A、乙是最常用的溶剂,乙是水,丙是单质,则甲可以是过氧化氢,过氧化氢分解生成水和氧气,故选项说法正确;
B、若甲是一种常见的黑色固体,黑色固体碳能生成两种组成元素相同的气体一氧化碳和二氧化碳,丙→乙可以是二氧化碳和碳高温反应生成一氧化碳,故选项说法正确;
C、乙是一种常见的温室气体,则乙是二氧化碳,丙是大理石的主要成分,丙是碳酸钙,碳酸钠或碳酸钾可以和稀盐酸可以反立生成二氧化碳,可以和氯化钙反应生成碳酸钙沉淀,碳酸钙可以和盐酸反应生成二氧化碳,二氧化碳可以和氢氧化钙反应生成碳酸钙,甲可以是K2CO3也可以是碳酸钠,故选项说法错误;
D、乙是紫红色金属,乙是铜,丙是蓝色溶液,可以是硝酸铜,甲能反应生成乙和丙,且是黑色固体,则甲是氧化铜,氧化铜和一氧化碳反应生成铜,氧化铜和硝酸反应生成硝酸铜,铜和硝酸银溶液反应生成硝酸铜,铁和硝酸铜能反应生成铜,故选项说法正确;
故选:C。
8.D
解:甲、乙、丙、丁四种溶液中,分别含有Ba2+、Mg2+、Na+、H+、Cl﹣、CO32﹣、SO42﹣、OH﹣中的一种阳离子和一种阴离子,可以组成的物质有BaCl2、Ba(OH)2、MgCl2、MgSO4、HCl、H2SO4、NaCl、NaOH、Na2CO3、Na2SO4;
①将甲溶液分别与其他三种溶液混合,都观察到白色沉淀生成,能形成沉淀的离子组合是CO32﹣和Ba2+、Ba2+和SO42﹣、Mg2+和OH﹣;故甲可以是氢氧化钡;
②将乙、丁溶液混合,有气泡产生,则乙、丁溶液中分别含有H+和CO32﹣中的一种;乙、丁可以分别是硫酸和碳酸钠中的一种,无法具体判断分别是谁;
③向丙溶液中滴入AgNO3溶液,可明显观察到白色,加稀硝酸后,沉淀不消失,则丙溶液中含有Cl﹣,丙可以是氯化镁;
代入题干,推断合理;
A、甲溶液中一定含有Ba2+,说法正确;
B、乙溶液可能是硫酸溶液,也可能是碳酸钠溶液,因此可能含有SO42﹣,说法正确;
C、丙溶液是氯化镁溶液,一定含有Cl﹣,说法正确;
D、丁溶液可能是硫酸溶液,也可能是碳酸钠溶液,因此可能含有Na+,说法错误;
故选:D。
9.解:(1)固体样品加水过滤得滤液和滤渣,滤液A中加过量硝酸铜溶液无明显现象,因氢氧化钾会与硝酸铜反应产生蓝色沉淀,所以一定不含氢氧化钾;故答案为:滤液A中加过量硝酸铜溶液无明显现象;
(2)滤液B中加适量硝酸银溶液生成白色滤渣乙和滤液C,说明滤液B中含有氯离子,样品中含有氯化钠;滤渣甲加入过量稀盐酸,得滤液D和滤渣丙,滤渣丙在空气中充分灼烧,得固体残留物,因锌、碳、氧化铜都不溶于水,但锌和氧化铜能溶于酸,且锌能与氯化铜溶液反应置换出铜,碳在空气中灼烧会生成气体,铜在空气中灼烧会生成氧化铜,所以原固体中一定含有氯化钠,氧化铜,锌;故答案为:氯化钠,氧化铜,锌。
10.解:根据白色固体溶于水,得到白色沉淀和无色溶液A,白色沉淀与盐酸反应会生成无色气体B、固体部分被溶解。根据提供的物质碳酸钙难溶于水,与盐酸反应生成氯化钙、水和二氧化碳,气体B为二氧化碳;氯化钡与硫酸钠溶液反应分别生成硫酸钡白色沉淀,硫酸钡沉淀不溶于稀盐酸,说明白色沉淀为碳酸钙和硫酸钡的混合物,白色不溶物为硫酸钡,则白色固体中一定含有氯化钡、碳酸钠和含硫酸钠;含铜离子的溶液为蓝色,溶液A为无色,说明一定不存在硫酸铜;所以:
(1)白色不溶物的成分是氯化钡、硫酸钠和碳酸钙;故答案为:氯化钡、硫酸钠和碳酸钙;
(2)氯化钡与硫酸钠反应生成硫酸钡沉淀和氯化钠,无色溶液A中一定含有的溶质是氯化钠;故答案为:氯化钠;
(3)气体B为二氧化碳,二氧化碳能溶于水,密度比空气大,若因此要收集气体B,则可选用如图装置中的②;故答案为:②。
11.解:(1)由分析可知,溶液D加入无色酚酞后显红色,说明溶液D呈碱性;这包固体中一定不存在的物质是:NH4Cl、Na2SO4;
(2)白色沉淀A全部溶解的化学方程式为:BaCO3+2HNO3=BaNO3+H2O+CO2↑;
(3)由分析可知,步骤4所得红色溶液D中一定含有的溶质是:酚酞、氢氧化钠、氯化钡和氯化钠;
(4)将无色溶液B、无色溶液F和沉淀E倒在了同一个废液缸里,发现沉淀消失并产生气泡,无色溶液B有2种情况“硝酸钡”和“硝酸钡、硝酸”,沉淀E为碳酸钡,它们倒在同一个废液缸里,沉淀消失并产生气泡,由此可知,无色溶液B中的溶质为“硝酸钡、硝酸”,硝酸与碳酸钡反应生成硝酸钡、水和二氧化碳,溶液中一定含有硝酸钡,无色溶液F中一定含有氯化钠,则废液缸中最终得到的废液中一定含有的溶质是硝酸钡和氯化钠,则废液缸中最终得到的废液中除指示剂外一定含有的离子是钠离子、氯离子、钡离子、硝酸根离子。
故答案为:
(1)NH4Cl、Na2SO4;
(2)BaCO3+2HNO3=BaNO3+H2O+CO2↑;
(3)氢氧化钠,以及氢氧化钡和氯化钡中的一种;
(4)钠离子、氯离子、钡离子、硝酸根离子。
12.解:(1)装置A是为了验证气体中存在二氧化硫并将其除去,以免干扰二氧化碳验证,属于思维模型中的直接检验和除去干扰气体;故答案为:直接检验和除去干扰气体;
(2)CO具有还原性,可利用在加热的条件下,CO能使氧化铜还原成铜,证明CO存在,所以证明CO的现象是E装置中黑色固体变红色;故答案为:E装置中黑色固体变红色;
(3)该装置中将尾气排放到空气中,会污染空气,所以缺少尾气处理装置;故答案为:尾气处理;
(4)在用酒精灯加热前是要先通入一段时间的检验气体,根据B中的品红溶液不变色和C中的氢氧化钡溶液是否变浑浊,也可检验出CO2,故答案为:有道理,在用酒精灯加热前是要先通入一段时间的检验气体,根据B中的品红溶液不变色和C中的氢氧化钡溶液是否变浑浊,也可检验出CO2。
物质鉴别、检验、推断
同课章节目录
