4.2 蛋白质-高二化学课件(共28张PPT)(人教版2019选择性必修3)
文档属性
| 名称 | 4.2 蛋白质-高二化学课件(共28张PPT)(人教版2019选择性必修3) |
|
|
| 格式 | pptx | ||
| 文件大小 | 24.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-10 00:00:00 | ||
图片预览







文档简介
(共28张PPT)
基 于 真 实 情 景 的 同 步 教 学
基 于 真 实 情 景 的 同 步 教 学
高 中 化 学 选 择 性 必 修 三 ( 2019 人 教 版 )
第四章 生物大分子
xi
第二节 蛋白质
第一课时
蛋白质
蛋白质
蛋白质是生物体内一类极为重要的_____________,是生命活动的主要物质基础。它不仅是_____的重要成分,而且具有多种生物学功能。
人体内起催化作用的_________、一些调节代谢的______和发生免疫反应的______等均为蛋白质。
生物大分子
细胞
大多数酶
激素
抗体
没有蛋白质就没有生命
食物中的蛋白质
生活中的蛋白质
一、氨基酸
1.氨基酸
_________是组成蛋白质的基本结构单位。
为了人体的健康,应注意合理膳食、科学营养,保证人体必需氨基酸的摄取。
羧酸分子烃基上的_______被_______取代得到的化合物称为氨基酸。
氢原子
氨基
氨基酸
氨基酸分子中含有______和_______,属于_________。
氨基
羧基
取代羧酸
自然界中存在的氨基酸
组成生物体内
人体内不能合成
一般只有20种
8种氨基酸
几百种
必需氨基酸
组成蛋白质的氨基酸主要是___________
ɑ-氨基酸
氨基连接在与羧基相邻的ɑ位的碳原子上
R CH COOH
NH2
ɑ
当R不是H时,(即除甘氨酸外),ɑ-碳为手性碳原子
大部分ɑ-氨基酸具有对映异构
1.氨基酸
2.氨基酸的物理性质
天然氨基酸均为_____晶体,熔点_____,在200~3000C时熔化分解
无色
较高
一般____溶于水而_____溶于乙醇、乙醚等有机溶剂
能
难
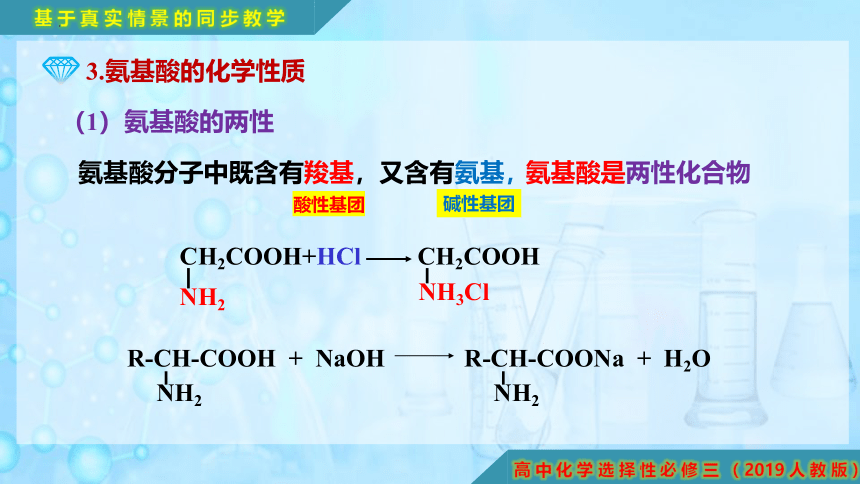
常见的氨基酸
俗名 结构简式 命名
甘氨酸
丙氨酸
谷氨酸
苯丙氨酸
半胱氨酸
CH2—COOH
H2N
氨基乙酸
2-氨基丙酸
2-氨基戊二酸
2-氨基-3-苯基丙酸
2-氨基-3-巯基丙酸
CH3—CH—COOH
NH2
HOOC—(CH2)2—CH—COOH
NH2
3.氨基酸的化学性质
(1)氨基酸的两性
氨基酸分子中既含有羧基,又含有氨基,
酸性基团
碱性基团
氨基酸是两性化合物
R-CH-COOH + NaOH
NH2
R-CH-COONa + H2O
NH2
CH2COOH+HCl CH2COOH
NH2
NH3Cl
(2)成肽反应
一定条件
+
肽键
两个氨基酸分子(可以相同,也可以不同)在一定条件下,通过氨基和羧基间缩合脱去水形成含有肽键的化合物
+ H2O
二肽
两分子氨基酸
缩合
二肽
三肽
缩合
+氨基酸
缩合
+氨基酸
四肽
缩合
+氨基酸
多肽
· · · · · ·
呈链状
肽链
又称
相互结合形成
盘曲、折叠
蛋白质
Mr>10000
具有一定的空间结构
4.氨基酸的化学性质
组成主要元素:
C、H、O、N、S 等
有些蛋白质还含有:
蛋白质属于:
人体内所具有的蛋白质种类达到了10万种以上。
二、蛋白质
1.蛋白质的组成
P、Fe、Zn、Cu等
天然高分子化合物
2.蛋白质的结构
种类、数目及排列顺序
特定的空间结构
多肽链的氨基酸
蛋白质的结构
各种蛋白质都有其特殊功能和活性
一级结构
二级结构
三级结构
四级结构
2.蛋白质的结构
一级结构
例如,血红蛋白分子中的________会因遗传因素变成________,这一微小差别会导致红细胞的形态由正常的圆饼状变为异常的镰刀状,使人患镰状细胞贫血。
蛋白质分子中氨基酸单体的__________称为蛋白质的一级结构
排列顺序
一级结构是______________的基础,对蛋白质的___________起着决定性作用
蛋白质高级结构
性质和功能
谷氨酸
缬氨酸
2.蛋白质的结构
二级结构
肽键中的氧原子与氢原子之间__________,会使肽链___________成特定的空间结构,形成蛋白质的二级结构
存在氢键
盘绕或折叠
氢键
三级结构
肽链在二级结构基础上还会进一步盘曲折叠,形成更复杂的三级结构
2.蛋白质的结构
四级结构
多个具有特定三级结构的多肽链通过 (如氢键等)排列组装,形成蛋白质的四级结构。
非共价键相互作用
2.蛋白质的结构
3.蛋白质的性质
1.水解反应
在酸、碱或酶作用下,逐步水解成相对分子质量较小的_____,最终水解得到________。
多肽
氨基酸
食物中的蛋白质在人体内各种_______的作用下水解成_______,氨基酸被_____吸收进入_____,再在体内_________人体所需要的蛋白质。
蛋白酶
氨基酸
肠壁
血液
重新合成
实验4-3
在试管中加入2mL饱和(NH4)2SO4溶液,向其中加入几滴鸡蛋清溶液,振荡,观察现象。再继续加入蒸馏水,振荡,观察现象。
2.盐析
少量的 (如硫酸铵、硫酸钠、氯化钠等)能_____蛋白质的_____。但当这些盐在蛋白质溶液中达到一定浓度时,反而使蛋白质的 而使其从溶液中______,这种作用称为盐析。
某些可溶性盐
促进
溶解
溶解度降低
析出
蛋白质的盐析是一个_________,盐析出的蛋白质在水中仍能溶解,并不影响其_______。采用_________________,可以分离提纯蛋白质。
可逆过程
可逆过程
活性
多次盐析和溶解
分离提纯蛋白质
3.蛋白质的性质
实验4-4
在三支试管中各加入2mL鸡蛋清溶液,将一支试管加热,向另两支试管中分别加入硝酸银溶液和乙醇,观察现象。再向试管中加入蒸馏水,观察产生的沉淀能否溶解。
3.变性
概念
影响因素 物理 ______、加压、搅拌、振荡、紫外线和放射线、超声波等
化学因素 ______、 、 、乙醇、甲醛、丙酮等
特点 变性会使蛋白质的结构发生变化,使其失去原有的__________,在水中不能重新溶解,是 过程
在某些物理或化学因素的影响下,蛋白质的性质和生理功能发生改变的现象
加热
强酸
强碱
重金属盐
不可逆
生理活性
3.蛋白质的性质
在日常生活中有时需要利用蛋白质变性
1.食物加热后,其中的蛋白质发生了变性,有利于人体消化吸收
2.乙醇、苯酚和碘等作为消毒防腐药可以使微生物的蛋白质变性,导致其死亡,达到消毒的目的
3.紫外线可用于杀菌消毒。有时也要注意防止蛋白质变性。
4.疫苗等生物制剂需要在低温下保存
5.攀登高山时为防止强紫外线引起皮肤和眼睛的蛋白质变性灼伤,需要防晒护目。
实验4-5
向盛有2mL鸡蛋清溶液的试管中加入5滴浓硝酸,加热。观察实验现象。
3.蛋白质的性质
4.燃烧反应
可用于蛋白质的鉴别
一般生成CO2、H2O、N2、SO2、P2O5等物质。烧焦羽毛味。
【应用】真假羊毛衫、蚕丝被的鉴别
4.显色反应
向蛋白质溶液加入浓硝酸会有___色沉淀产生,加热后沉淀变_____色。
可用于蛋白质的分析检测
固体蛋白质如皮肤、指甲遇浓硝酸变______色。
白
含有苯环
黄
黄
其他一些试剂也可以与蛋白质作用,呈现特定颜色
3.蛋白质的性质
酶
三、酶
酶是一类由_____产生的、对生物体内的化学反应具有_____作用的有机化合物,其中绝大多数是________。
在酶的作用下,生物才能进行新陈代谢,完成消化、呼吸、运动、生长、发育、繁殖等生命活动。
细胞
催化
蛋白质
特点
具有高效催化作用
条件温和
具有高度的专一性
一般是普通催化剂的107倍
一般在接近体温和中性的条件下进行,此时酶的活性最高。超过适宜的温度时,酶将失去活性
基 于 真 实 情 景 的 同 步 教 学
基 于 真 实 情 景 的 同 步 教 学
高 中 化 学 选 择 性 必 修 三 ( 2019 人 教 版 )
第四章 生物大分子
xi
第二节 蛋白质
第一课时
蛋白质
蛋白质
蛋白质是生物体内一类极为重要的_____________,是生命活动的主要物质基础。它不仅是_____的重要成分,而且具有多种生物学功能。
人体内起催化作用的_________、一些调节代谢的______和发生免疫反应的______等均为蛋白质。
生物大分子
细胞
大多数酶
激素
抗体
没有蛋白质就没有生命
食物中的蛋白质
生活中的蛋白质
一、氨基酸
1.氨基酸
_________是组成蛋白质的基本结构单位。
为了人体的健康,应注意合理膳食、科学营养,保证人体必需氨基酸的摄取。
羧酸分子烃基上的_______被_______取代得到的化合物称为氨基酸。
氢原子
氨基
氨基酸
氨基酸分子中含有______和_______,属于_________。
氨基
羧基
取代羧酸
自然界中存在的氨基酸
组成生物体内
人体内不能合成
一般只有20种
8种氨基酸
几百种
必需氨基酸
组成蛋白质的氨基酸主要是___________
ɑ-氨基酸
氨基连接在与羧基相邻的ɑ位的碳原子上
R CH COOH
NH2
ɑ
当R不是H时,(即除甘氨酸外),ɑ-碳为手性碳原子
大部分ɑ-氨基酸具有对映异构
1.氨基酸
2.氨基酸的物理性质
天然氨基酸均为_____晶体,熔点_____,在200~3000C时熔化分解
无色
较高
一般____溶于水而_____溶于乙醇、乙醚等有机溶剂
能
难
常见的氨基酸
俗名 结构简式 命名
甘氨酸
丙氨酸
谷氨酸
苯丙氨酸
半胱氨酸
CH2—COOH
H2N
氨基乙酸
2-氨基丙酸
2-氨基戊二酸
2-氨基-3-苯基丙酸
2-氨基-3-巯基丙酸
CH3—CH—COOH
NH2
HOOC—(CH2)2—CH—COOH
NH2
3.氨基酸的化学性质
(1)氨基酸的两性
氨基酸分子中既含有羧基,又含有氨基,
酸性基团
碱性基团
氨基酸是两性化合物
R-CH-COOH + NaOH
NH2
R-CH-COONa + H2O
NH2
CH2COOH+HCl CH2COOH
NH2
NH3Cl
(2)成肽反应
一定条件
+
肽键
两个氨基酸分子(可以相同,也可以不同)在一定条件下,通过氨基和羧基间缩合脱去水形成含有肽键的化合物
+ H2O
二肽
两分子氨基酸
缩合
二肽
三肽
缩合
+氨基酸
缩合
+氨基酸
四肽
缩合
+氨基酸
多肽
· · · · · ·
呈链状
肽链
又称
相互结合形成
盘曲、折叠
蛋白质
Mr>10000
具有一定的空间结构
4.氨基酸的化学性质
组成主要元素:
C、H、O、N、S 等
有些蛋白质还含有:
蛋白质属于:
人体内所具有的蛋白质种类达到了10万种以上。
二、蛋白质
1.蛋白质的组成
P、Fe、Zn、Cu等
天然高分子化合物
2.蛋白质的结构
种类、数目及排列顺序
特定的空间结构
多肽链的氨基酸
蛋白质的结构
各种蛋白质都有其特殊功能和活性
一级结构
二级结构
三级结构
四级结构
2.蛋白质的结构
一级结构
例如,血红蛋白分子中的________会因遗传因素变成________,这一微小差别会导致红细胞的形态由正常的圆饼状变为异常的镰刀状,使人患镰状细胞贫血。
蛋白质分子中氨基酸单体的__________称为蛋白质的一级结构
排列顺序
一级结构是______________的基础,对蛋白质的___________起着决定性作用
蛋白质高级结构
性质和功能
谷氨酸
缬氨酸
2.蛋白质的结构
二级结构
肽键中的氧原子与氢原子之间__________,会使肽链___________成特定的空间结构,形成蛋白质的二级结构
存在氢键
盘绕或折叠
氢键
三级结构
肽链在二级结构基础上还会进一步盘曲折叠,形成更复杂的三级结构
2.蛋白质的结构
四级结构
多个具有特定三级结构的多肽链通过 (如氢键等)排列组装,形成蛋白质的四级结构。
非共价键相互作用
2.蛋白质的结构
3.蛋白质的性质
1.水解反应
在酸、碱或酶作用下,逐步水解成相对分子质量较小的_____,最终水解得到________。
多肽
氨基酸
食物中的蛋白质在人体内各种_______的作用下水解成_______,氨基酸被_____吸收进入_____,再在体内_________人体所需要的蛋白质。
蛋白酶
氨基酸
肠壁
血液
重新合成
实验4-3
在试管中加入2mL饱和(NH4)2SO4溶液,向其中加入几滴鸡蛋清溶液,振荡,观察现象。再继续加入蒸馏水,振荡,观察现象。
2.盐析
少量的 (如硫酸铵、硫酸钠、氯化钠等)能_____蛋白质的_____。但当这些盐在蛋白质溶液中达到一定浓度时,反而使蛋白质的 而使其从溶液中______,这种作用称为盐析。
某些可溶性盐
促进
溶解
溶解度降低
析出
蛋白质的盐析是一个_________,盐析出的蛋白质在水中仍能溶解,并不影响其_______。采用_________________,可以分离提纯蛋白质。
可逆过程
可逆过程
活性
多次盐析和溶解
分离提纯蛋白质
3.蛋白质的性质
实验4-4
在三支试管中各加入2mL鸡蛋清溶液,将一支试管加热,向另两支试管中分别加入硝酸银溶液和乙醇,观察现象。再向试管中加入蒸馏水,观察产生的沉淀能否溶解。
3.变性
概念
影响因素 物理 ______、加压、搅拌、振荡、紫外线和放射线、超声波等
化学因素 ______、 、 、乙醇、甲醛、丙酮等
特点 变性会使蛋白质的结构发生变化,使其失去原有的__________,在水中不能重新溶解,是 过程
在某些物理或化学因素的影响下,蛋白质的性质和生理功能发生改变的现象
加热
强酸
强碱
重金属盐
不可逆
生理活性
3.蛋白质的性质
在日常生活中有时需要利用蛋白质变性
1.食物加热后,其中的蛋白质发生了变性,有利于人体消化吸收
2.乙醇、苯酚和碘等作为消毒防腐药可以使微生物的蛋白质变性,导致其死亡,达到消毒的目的
3.紫外线可用于杀菌消毒。有时也要注意防止蛋白质变性。
4.疫苗等生物制剂需要在低温下保存
5.攀登高山时为防止强紫外线引起皮肤和眼睛的蛋白质变性灼伤,需要防晒护目。
实验4-5
向盛有2mL鸡蛋清溶液的试管中加入5滴浓硝酸,加热。观察实验现象。
3.蛋白质的性质
4.燃烧反应
可用于蛋白质的鉴别
一般生成CO2、H2O、N2、SO2、P2O5等物质。烧焦羽毛味。
【应用】真假羊毛衫、蚕丝被的鉴别
4.显色反应
向蛋白质溶液加入浓硝酸会有___色沉淀产生,加热后沉淀变_____色。
可用于蛋白质的分析检测
固体蛋白质如皮肤、指甲遇浓硝酸变______色。
白
含有苯环
黄
黄
其他一些试剂也可以与蛋白质作用,呈现特定颜色
3.蛋白质的性质
酶
三、酶
酶是一类由_____产生的、对生物体内的化学反应具有_____作用的有机化合物,其中绝大多数是________。
在酶的作用下,生物才能进行新陈代谢,完成消化、呼吸、运动、生长、发育、繁殖等生命活动。
细胞
催化
蛋白质
特点
具有高效催化作用
条件温和
具有高度的专一性
一般是普通催化剂的107倍
一般在接近体温和中性的条件下进行,此时酶的活性最高。超过适宜的温度时,酶将失去活性
