河北省滦县二中2013-2014学年高二上学期期中考试化学试题(实验班)
文档属性
| 名称 | 河北省滦县二中2013-2014学年高二上学期期中考试化学试题(实验班) |

|
|
| 格式 | zip | ||
| 文件大小 | 191.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2014-05-20 00:00:00 | ||
图片预览


文档简介
本资料来自于资源最齐全的21世纪教育网www.21cnjy.com
滦县二中2013——2014学年度第一学期期中考试
高二理科实验班 化 学
本试卷满分为100分,时间为70分钟
可能用到的相对原子质量:H—1、C—12、O—16、Cu—64
第Ⅰ卷(共51分)
一、选择题 (本题共17小题,每小题3分,共51分。在每小题给出的4个选项中,只有一个选项是符合题中要求的)【来源:21cnj*y.co*m】
.实验要快速制取H2,最好的方法是( )
A.纯锌和稀反应 B.纯锌和浓硫酸反应
C.粗锌和浓反应 D.粗锌和稀硫酸反应
.下列反应既是氧化还原反应,又是放热反应的是( )
A.铝与稀盐酸的反应
B.Ba(OH)2·8H2O与NH4Cl的反应
C.灼热的碳与水蒸气的反应
D. NaOH与稀硫酸的反应
.某金属能与盐酸反应产生氢气,该金属与锌组成的原电池中,锌为负极。该金属为( )
A.铝 B.铜 C.铁 D.镁【来源:21·世纪·教育·网】
.用于人造地球卫星的一种高能电池―银锌蓄电池,其电极反应式为:Zn+2OH–-2e–
=ZnO+H2O;Ag2O+H2O+2e ( http: / / www.21cnjy.com )–=2Ag+2OH–。据此判断氧化银是( )
A.负极,并被氧化 B.正极,并被还原
C.负极,并被还原 D.正极,并被氧化
.在10L容器中进行如下反应:N2 + 3H2 2NH3,3秒钟后,NH3的物质的量增加0.12mol,用H2浓度的变化表示3秒钟内的平均反应速率为( ) 2·1·c·n·j·y
A.0.003mol/(L·s) B.0.045mol/(L·s) 21·世纪*教育网
C.0.006mol/(L·s) D.0.009 mol/(L·s)【版权所有:21教育】
.下列关于原电池的叙述正确的是( )
A.原电池将化学能转化为电能
B.原电池负极发生的反应是还原反应
C.原电池在工作时其正极不断产生电子并经过外电路流向负极
D.原电池的电极只能由两种不同的金属构成
.下面所列事实中,与电化学腐蚀无关的是( )
A. 埋在潮湿地下的铁管道比地上的铁管道更耐腐蚀
B. 为保护海轮的船壳,常在船壳水线以下部分装上锌块
C. 在空气中,金属银的表面生成一层黑色物质
D. 镀银的铁制品,镀层部分受损后,露出的铁表面更易被腐蚀
.下图是电解溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )
A.a为负极,b为正极 B.a为阳极,b为阴极
C.电解过程中,d电极质量增加 D.电解过程中,氯离子浓度不变
. 向平衡体系2NO+O22NO2中通入18O组成的氧气,重新达到平衡后,18O存在
于( )
A.仅在O2中 B.仅在NO2中
C.仅在NO中 D.存在于NO、O2、NO2中
.一定温度和压强下N2+3H22NH3反应达到平衡后,下列说法中正确的是( )
A.N2与H2不再化合,NH3不再分解
B.N2、H2化合成氨的反应速率等于NH3 分解的反应速率
C.H2、NH3的体积分数相等
D.N2、H2、NH3的物质的量浓度相等
. 已知反应X+Y= M+N为放热反应,,对该反应的下列说法中正确的( )
A、X的能量一定高于M
B、Y的能量一定高于N
C、X和Y的总能量一定高于M和N的总能量
D、因该反应为放热反应,故不必加热就可发生
. 下列说法正确的是( )
A、在其他条件不变时,升高温度可以使平衡向放热反应方向移动
B、在其他条件不变时,使用催化剂只能改变反应速率,而不能使化学平衡移动
C、在容积可变的容器中充入与反应无关的气体,平衡一定不移动
D、在其他条件不变时,增大压强一定会破坏气体反应的平衡状态
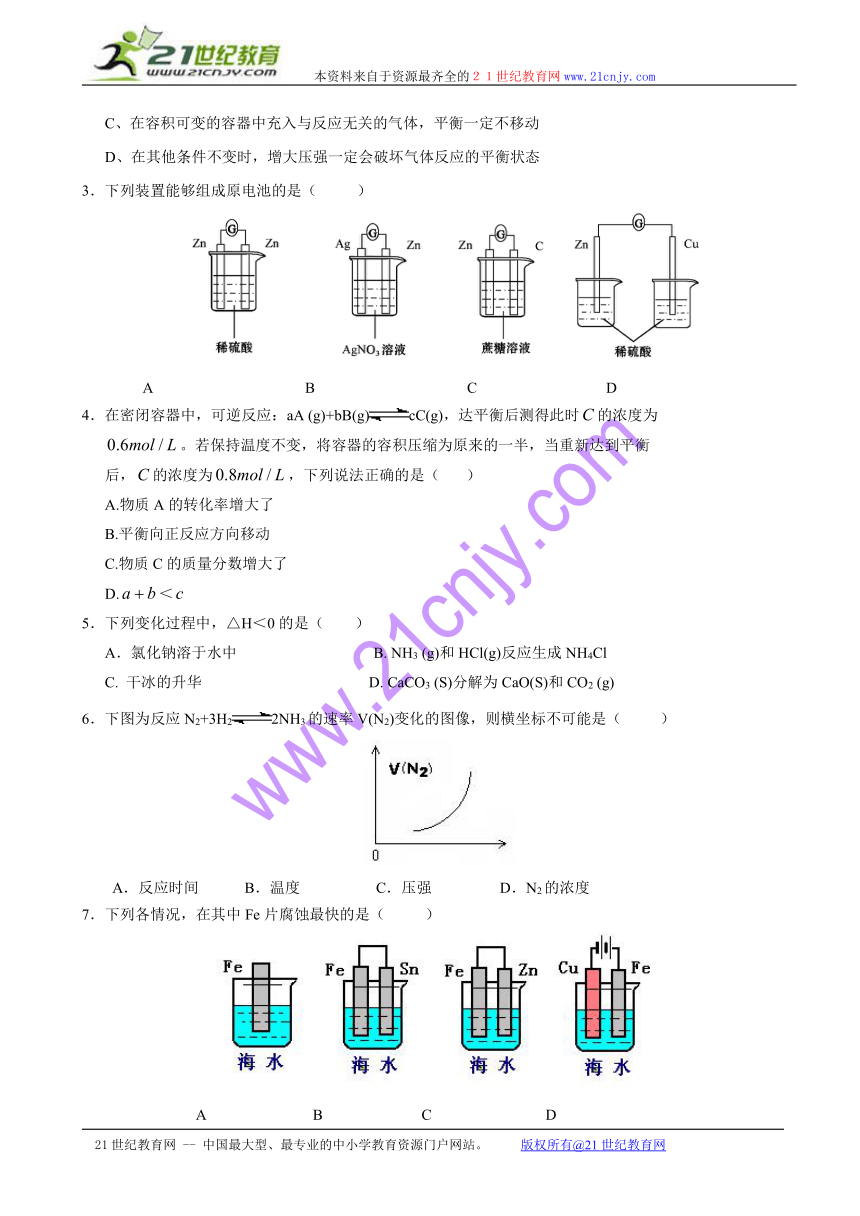
.下列装置能够组成原电池的是( )
( http: / / www.21cnjy.com )
A B C D 21世纪教育网版权所有
.在密闭容器中,可逆反应:aA (g)+bB(g)cC(g),达平衡后测得此时的浓度为
。若保持温度不变,将容器的容积压缩为原来的一半,当重新达到平衡
后,的浓度为,下列说法正确的是( )
A.物质A的转化率增大了
B.平衡向正反应方向移动
C.物质C的质量分数增大了
D.<
.下列变化过程中,△H<0的是( )
A.氯化钠溶于水中 B. NH3 (g)和HCl(g)反应生成NH4Cl21教育网
C. 干冰的升华 D. CaCO3 (S)分解为CaO(S)和CO2 (g) 21cnjy.com
.下图为反应N2+3H22NH3的速率V(N2)变化的图像,则横坐标不可能是( )
( http: / / www.21cnjy.com )
A.反应时间 B.温度 C.压强 D.N2的浓度
.下列各情况,在其中Fe片腐蚀最快的是( )
( http: / / www.21cnjy.com )
A B C D
滦县二中2013——2014学年度第一学期期中考试
高二理科实验班化学
第Ⅱ卷(共49分)
二、填空题(共31分)
.(10分)A与B反应生成C,假定反应由 ( http: / / www.21cnjy.com )A、B开始,它们的起始浓度均为2mol/L。反应进行2min后A的浓度为1.8 mol/L,B的浓度为1.6 mol/L,C的浓度为0.6 mol/L.21·cn·jy·com
(1)2min内反应的平均速率为:
v(A)= , v(B)= v (C )=
(2)三者数值之间的关系是:v(A)= v(B)= v(C)
.(5分)
(1)1 mol碳与适量水 ( http: / / www.21cnjy.com )蒸气反应生成CO和H2,需吸收132KJ热量,此反应的热化学方程式为
(2)已知CH4(g)+2O2(g)== CO2(g)+2H2O(l) ΔH1=-Q1kJ·mol-1 , www.21-cn-jy.com
2H2(g)+O2(g)=2H2O(l) ΔH2=-Q2 kJ·,
常温下,取体积比4∶1的甲烷和氢气的混 ( http: / / www.21cnjy.com )合气体11.2L(标准状况下),经完全燃烧后恢复至室温,则放出的热量为 kJ 。2-1-c-n-j-y
.(4分)在一定条件下,反应:H2(g) +I2 (g) 2HI(g) △H<0在一密闭体系中达到化学平衡。
(1)请写出该反应的平衡常数表达式K=
(2)改变下列条件时,平衡向正向移动的是( )
A 保持压强不变,升高温度
B 保持温度不变,通入氢气
C 保持温度不变,缩小容器的体积
.(8分)(1)若电解足量的氯化铜溶液,写出电解时发生反应的化学方程式
,如果电解一段时间后,电路中转移2mol的电子,阳极在标准状况下放出氯气 升。 www-2-1-cnjy-com
(2)若电解足量的氯化钠溶液,写出电解时发生反应的化学方程式
,如果电解一段时间后,电路中转移1mol的电子,则阴极析出氢气 L。 21*cnjy*com
三、实验题(计18分)
.(10分)50ml0.50mol/L盐酸 ( http: / / www.21cnjy.com )与50ml0.55mol/L氢氧化钠的溶液在如下图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:21*cnjy*com
( http: / / www.21cnjy.com )
(1)从实验装置上看,图中尚缺少的种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)若大烧杯上不盖硬纸板,求得中和热数值 。(填“偏大”“偏小”或“无影响”)。
(4)实验中改用 60 m ( http: / / www.21cnjy.com )L 0.50 mol·L-1的盐酸跟 50mL 0.55 mol·L-1的 NaOH溶液进行反应,与上述实验相比,所放出的热量______(填“相等”或“不相等”),所求中和热_______(填“相等”或“不相等”)。
.(8分)按右图所示实验,水槽中试管内有一枚铁钉,放置数天后观察:
(1)若试管内的液面上升,发生 腐蚀,负极电极反应式
(2)若试管内液面下降,发生 腐蚀,正极电极反应式
.(4分)采用惰性电极 ( http: / / www.21cnjy.com )从NO3-、SO42-、H+、Cu2+、Ba2+、Ag+、Cl-等离子中,选出适当的离子组成电解质,对其溶液进行电解(每空至少写出两种物质):
(1)两极分别放出H2和O2时,电解质的化学式可能是________________________;
(2)两极分别放出气体,且体积比为1∶1时,电解质的化学式可能是__________________。
滦县二中2013——2014学年度第一学期期中考试
高二理科实验班化学参考答案
1-5 DACBC 6-10 ACCDB 11-15 CBBDB 16-17 AD
18. (共10分,每空2分)
(1)0.1mol/L/min 0.2 mol/L/min 0.3 mol/L/min 【出处:21教育名师】
(2)1/2 1/3
19.(共5分)
(1)C(S)+H2O(g) == CO(g) +H2(g) ΔH= +132 kJ·(3分)21教育名师原创作品
(2)0.4Q1+0.05Q2(2分)
20.(共4分,每空2分)(1) (2)B
21.(共8分,每空2分)(1)CuCl2═Cu+Cl2↑(2分);22.4L(2分)
(2)2NaCl+2H2O= H2↑+Cl2↑+NaOH(2分);11.2L(2分)
22.(共10分,每空2分)
(1) 环形玻璃搅拌棒
(2)(2)减少实验过程中的热量损失
(3)偏小
(4)不相等;相等`
24.(共8分,每空2分)
(1)电化学
(2) 吸氧 负极:Fe-2e-Fe2+
(3) 析氢 正极:2H++2e-H2↑
24.(共4分,每空2分)
(1)HNO3、H2SO4、Ba(NO3)2 (2) HCl、BaCl2
班级:____________ 姓名:______________ 考场:____________ 考号:____________
…………………………………………………………………………………………………………………………………………………………
…………………………………-密……………………………………封……………………………………线……………………………………
得分
通电
通电
21世纪教育网 -- 中国最大型、最专业的中小学教育资源门户网站。 版权所有@21世纪教育网
滦县二中2013——2014学年度第一学期期中考试
高二理科实验班 化 学
本试卷满分为100分,时间为70分钟
可能用到的相对原子质量:H—1、C—12、O—16、Cu—64
第Ⅰ卷(共51分)
一、选择题 (本题共17小题,每小题3分,共51分。在每小题给出的4个选项中,只有一个选项是符合题中要求的)【来源:21cnj*y.co*m】
.实验要快速制取H2,最好的方法是( )
A.纯锌和稀反应 B.纯锌和浓硫酸反应
C.粗锌和浓反应 D.粗锌和稀硫酸反应
.下列反应既是氧化还原反应,又是放热反应的是( )
A.铝与稀盐酸的反应
B.Ba(OH)2·8H2O与NH4Cl的反应
C.灼热的碳与水蒸气的反应
D. NaOH与稀硫酸的反应
.某金属能与盐酸反应产生氢气,该金属与锌组成的原电池中,锌为负极。该金属为( )
A.铝 B.铜 C.铁 D.镁【来源:21·世纪·教育·网】
.用于人造地球卫星的一种高能电池―银锌蓄电池,其电极反应式为:Zn+2OH–-2e–
=ZnO+H2O;Ag2O+H2O+2e ( http: / / www.21cnjy.com )–=2Ag+2OH–。据此判断氧化银是( )
A.负极,并被氧化 B.正极,并被还原
C.负极,并被还原 D.正极,并被氧化
.在10L容器中进行如下反应:N2 + 3H2 2NH3,3秒钟后,NH3的物质的量增加0.12mol,用H2浓度的变化表示3秒钟内的平均反应速率为( ) 2·1·c·n·j·y
A.0.003mol/(L·s) B.0.045mol/(L·s) 21·世纪*教育网
C.0.006mol/(L·s) D.0.009 mol/(L·s)【版权所有:21教育】
.下列关于原电池的叙述正确的是( )
A.原电池将化学能转化为电能
B.原电池负极发生的反应是还原反应
C.原电池在工作时其正极不断产生电子并经过外电路流向负极
D.原电池的电极只能由两种不同的金属构成
.下面所列事实中,与电化学腐蚀无关的是( )
A. 埋在潮湿地下的铁管道比地上的铁管道更耐腐蚀
B. 为保护海轮的船壳,常在船壳水线以下部分装上锌块
C. 在空气中,金属银的表面生成一层黑色物质
D. 镀银的铁制品,镀层部分受损后,露出的铁表面更易被腐蚀
.下图是电解溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )
A.a为负极,b为正极 B.a为阳极,b为阴极
C.电解过程中,d电极质量增加 D.电解过程中,氯离子浓度不变
. 向平衡体系2NO+O22NO2中通入18O组成的氧气,重新达到平衡后,18O存在
于( )
A.仅在O2中 B.仅在NO2中
C.仅在NO中 D.存在于NO、O2、NO2中
.一定温度和压强下N2+3H22NH3反应达到平衡后,下列说法中正确的是( )
A.N2与H2不再化合,NH3不再分解
B.N2、H2化合成氨的反应速率等于NH3 分解的反应速率
C.H2、NH3的体积分数相等
D.N2、H2、NH3的物质的量浓度相等
. 已知反应X+Y= M+N为放热反应,,对该反应的下列说法中正确的( )
A、X的能量一定高于M
B、Y的能量一定高于N
C、X和Y的总能量一定高于M和N的总能量
D、因该反应为放热反应,故不必加热就可发生
. 下列说法正确的是( )
A、在其他条件不变时,升高温度可以使平衡向放热反应方向移动
B、在其他条件不变时,使用催化剂只能改变反应速率,而不能使化学平衡移动
C、在容积可变的容器中充入与反应无关的气体,平衡一定不移动
D、在其他条件不变时,增大压强一定会破坏气体反应的平衡状态
.下列装置能够组成原电池的是( )
( http: / / www.21cnjy.com )
A B C D 21世纪教育网版权所有
.在密闭容器中,可逆反应:aA (g)+bB(g)cC(g),达平衡后测得此时的浓度为
。若保持温度不变,将容器的容积压缩为原来的一半,当重新达到平衡
后,的浓度为,下列说法正确的是( )
A.物质A的转化率增大了
B.平衡向正反应方向移动
C.物质C的质量分数增大了
D.<
.下列变化过程中,△H<0的是( )
A.氯化钠溶于水中 B. NH3 (g)和HCl(g)反应生成NH4Cl21教育网
C. 干冰的升华 D. CaCO3 (S)分解为CaO(S)和CO2 (g) 21cnjy.com
.下图为反应N2+3H22NH3的速率V(N2)变化的图像,则横坐标不可能是( )
( http: / / www.21cnjy.com )
A.反应时间 B.温度 C.压强 D.N2的浓度
.下列各情况,在其中Fe片腐蚀最快的是( )
( http: / / www.21cnjy.com )
A B C D
滦县二中2013——2014学年度第一学期期中考试
高二理科实验班化学
第Ⅱ卷(共49分)
二、填空题(共31分)
.(10分)A与B反应生成C,假定反应由 ( http: / / www.21cnjy.com )A、B开始,它们的起始浓度均为2mol/L。反应进行2min后A的浓度为1.8 mol/L,B的浓度为1.6 mol/L,C的浓度为0.6 mol/L.21·cn·jy·com
(1)2min内反应的平均速率为:
v(A)= , v(B)= v (C )=
(2)三者数值之间的关系是:v(A)= v(B)= v(C)
.(5分)
(1)1 mol碳与适量水 ( http: / / www.21cnjy.com )蒸气反应生成CO和H2,需吸收132KJ热量,此反应的热化学方程式为
(2)已知CH4(g)+2O2(g)== CO2(g)+2H2O(l) ΔH1=-Q1kJ·mol-1 , www.21-cn-jy.com
2H2(g)+O2(g)=2H2O(l) ΔH2=-Q2 kJ·,
常温下,取体积比4∶1的甲烷和氢气的混 ( http: / / www.21cnjy.com )合气体11.2L(标准状况下),经完全燃烧后恢复至室温,则放出的热量为 kJ 。2-1-c-n-j-y
.(4分)在一定条件下,反应:H2(g) +I2 (g) 2HI(g) △H<0在一密闭体系中达到化学平衡。
(1)请写出该反应的平衡常数表达式K=
(2)改变下列条件时,平衡向正向移动的是( )
A 保持压强不变,升高温度
B 保持温度不变,通入氢气
C 保持温度不变,缩小容器的体积
.(8分)(1)若电解足量的氯化铜溶液,写出电解时发生反应的化学方程式
,如果电解一段时间后,电路中转移2mol的电子,阳极在标准状况下放出氯气 升。 www-2-1-cnjy-com
(2)若电解足量的氯化钠溶液,写出电解时发生反应的化学方程式
,如果电解一段时间后,电路中转移1mol的电子,则阴极析出氢气 L。 21*cnjy*com
三、实验题(计18分)
.(10分)50ml0.50mol/L盐酸 ( http: / / www.21cnjy.com )与50ml0.55mol/L氢氧化钠的溶液在如下图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:21*cnjy*com
( http: / / www.21cnjy.com )
(1)从实验装置上看,图中尚缺少的种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)若大烧杯上不盖硬纸板,求得中和热数值 。(填“偏大”“偏小”或“无影响”)。
(4)实验中改用 60 m ( http: / / www.21cnjy.com )L 0.50 mol·L-1的盐酸跟 50mL 0.55 mol·L-1的 NaOH溶液进行反应,与上述实验相比,所放出的热量______(填“相等”或“不相等”),所求中和热_______(填“相等”或“不相等”)。
.(8分)按右图所示实验,水槽中试管内有一枚铁钉,放置数天后观察:
(1)若试管内的液面上升,发生 腐蚀,负极电极反应式
(2)若试管内液面下降,发生 腐蚀,正极电极反应式
.(4分)采用惰性电极 ( http: / / www.21cnjy.com )从NO3-、SO42-、H+、Cu2+、Ba2+、Ag+、Cl-等离子中,选出适当的离子组成电解质,对其溶液进行电解(每空至少写出两种物质):
(1)两极分别放出H2和O2时,电解质的化学式可能是________________________;
(2)两极分别放出气体,且体积比为1∶1时,电解质的化学式可能是__________________。
滦县二中2013——2014学年度第一学期期中考试
高二理科实验班化学参考答案
1-5 DACBC 6-10 ACCDB 11-15 CBBDB 16-17 AD
18. (共10分,每空2分)
(1)0.1mol/L/min 0.2 mol/L/min 0.3 mol/L/min 【出处:21教育名师】
(2)1/2 1/3
19.(共5分)
(1)C(S)+H2O(g) == CO(g) +H2(g) ΔH= +132 kJ·(3分)21教育名师原创作品
(2)0.4Q1+0.05Q2(2分)
20.(共4分,每空2分)(1) (2)B
21.(共8分,每空2分)(1)CuCl2═Cu+Cl2↑(2分);22.4L(2分)
(2)2NaCl+2H2O= H2↑+Cl2↑+NaOH(2分);11.2L(2分)
22.(共10分,每空2分)
(1) 环形玻璃搅拌棒
(2)(2)减少实验过程中的热量损失
(3)偏小
(4)不相等;相等`
24.(共8分,每空2分)
(1)电化学
(2) 吸氧 负极:Fe-2e-Fe2+
(3) 析氢 正极:2H++2e-H2↑
24.(共4分,每空2分)
(1)HNO3、H2SO4、Ba(NO3)2 (2) HCl、BaCl2
班级:____________ 姓名:______________ 考场:____________ 考号:____________
…………………………………………………………………………………………………………………………………………………………
…………………………………-密……………………………………封……………………………………线……………………………………
得分
通电
通电
21世纪教育网 -- 中国最大型、最专业的中小学教育资源门户网站。 版权所有@21世纪教育网
同课章节目录
