6.2蛋白质(含视频)(教学课件)(共28张PPT)—-高二化学苏教版(2019)选择性必修3
文档属性
| 名称 | 6.2蛋白质(含视频)(教学课件)(共28张PPT)—-高二化学苏教版(2019)选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 89.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-12 11:20:41 | ||
图片预览





文档简介
(共28张PPT)
专题6 生命活动的物质基础
第二单元 蛋白质
1、认识氨基酸和蛋白质的关系,以及它们对人体健康的影响;
2、能列举简单氨基酸的组成、结构、主要的化学性质和典型的检验方法;
3、能辨识蛋白质中的肽键,能判断氨基酸的缩合产物和多肽的水解产物,能通过实验探究蛋白质的主要性质和检验方法;
4、能初步认识核酸的结构特点和生物功能;体会生物大分子的研究的重要意义。
蛋白质是生命的物质基础,是构成细胞的基本有机物,是生命活动的主要承担者——没有蛋白质就没有生命。
1、组成蛋白质的主要元素有哪些?你如何理解氨基酸与蛋白质之间的关系?
2、你知道哪些常见的氨基酸?氨基酸有哪些重要的性质?
氨基酸的组成与结构
定义:氨基酸可看作是羧酸分子中烃基上的一个或几个氢原子被氨基取代后生成的化合物。
官能团:—COOH、—NH2
α-氨基酸
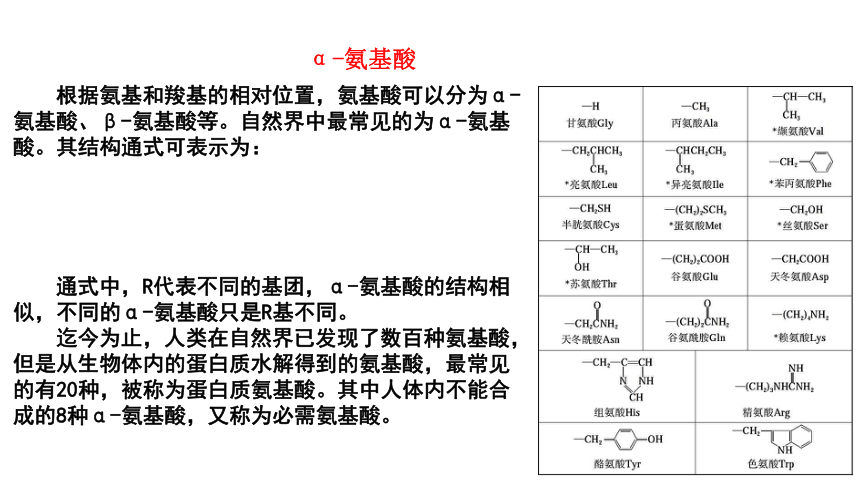
根据氨基和羧基的相对位置,氨基酸可以分为α-氨基酸、β-氨基酸等。自然界中最常见的为α-氨基酸。其结构通式可表示为:
通式中,R代表不同的基团,α-氨基酸的结构相似,不同的α-氨基酸只是R基不同。
迄今为止,人类在自然界已发现了数百种氨基酸,但是从生物体内的蛋白质水解得到的氨基酸,最常见的有20种,被称为蛋白质氨基酸。其中人体内不能合成的8种α-氨基酸,又称为必需氨基酸。
氨基酸的性质1
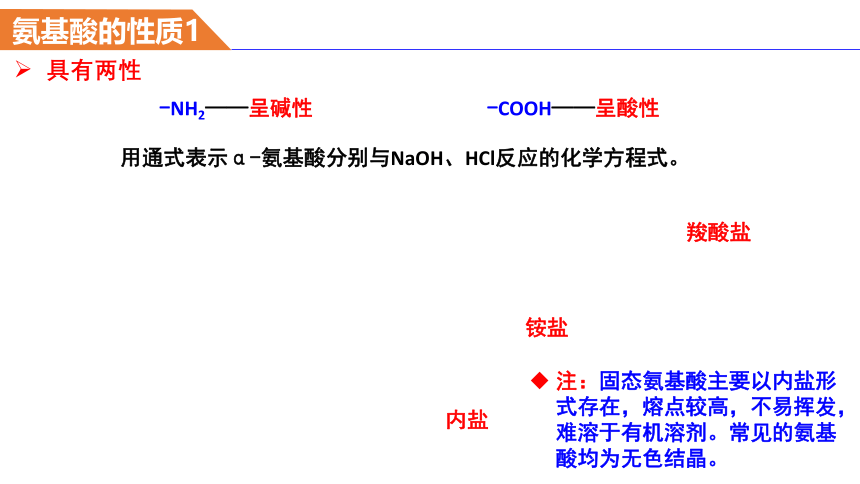
具有两性
-NH2——呈碱性 -COOH——呈酸性
羧酸盐
铵盐
用通式表示α-氨基酸分别与NaOH、HCl反应的化学方程式。
内盐
注:固态氨基酸主要以内盐形式存在,熔点较高,不易挥发,难溶于有机溶剂。常见的氨基酸均为无色结晶。
溶液酸碱性对氨基酸存在形态的影响
氨基酸是两性化合物,既能与酸发生反应,又能与碱发生反应。水溶液的pH不同,氨基酸在溶液中存在的形态也不同。
不同的氨基酸出现两性离子的pH各不相同,利用这一差异,可以通过控制溶液的pH分离不同的氨基酸、多肽和蛋白质。
两性离子
在水中的溶解度最小
阳离子
阴离子
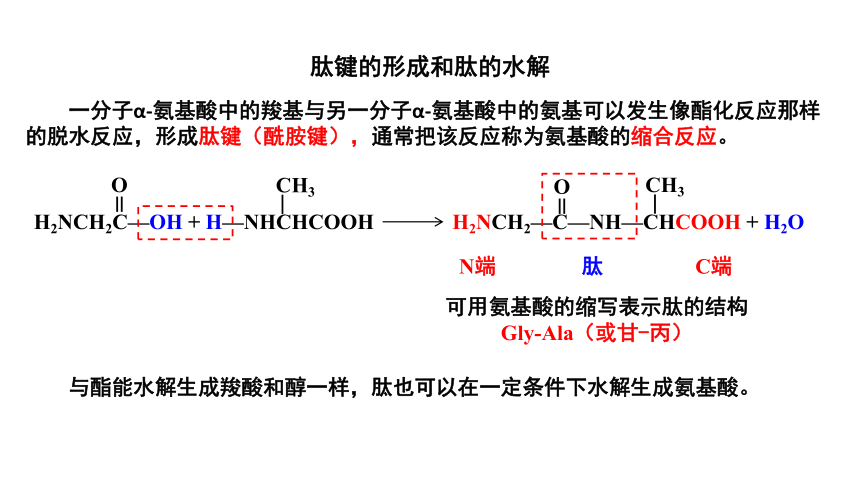
一分子α-氨基酸中的羧基与另一分子α-氨基酸中的氨基可以发生像酯化反应那样的脱水反应,形成肽键(酰胺键),通常把该反应称为氨基酸的缩合反应。
肽键的形成和肽的水解
与酯能水解生成羧酸和醇一样,肽也可以在一定条件下水解生成氨基酸。
肽
N端
C端
可用氨基酸的缩写表示肽的结构
Gly-Ala(或甘-丙)
H2NCH2C—OH + H—NHCHCOOH
CH3
H2NCH2—C—NH—CHCOOH + H2O
O
=
O
=
CH3
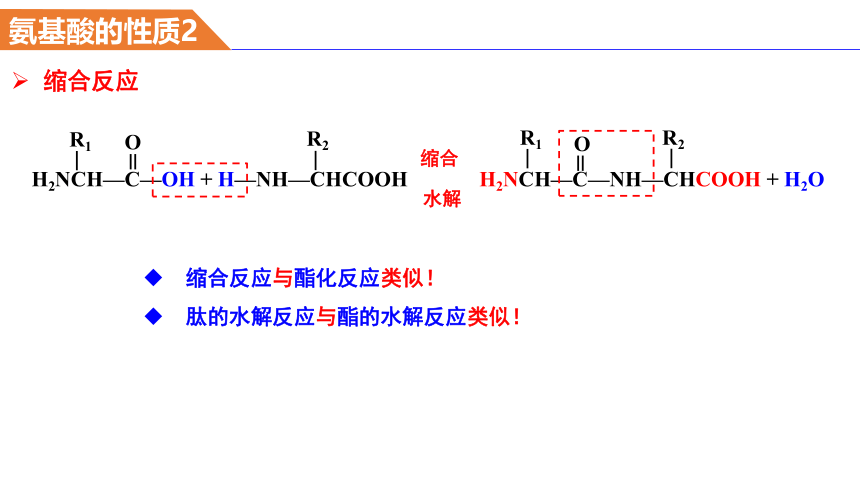
缩合反应
氨基酸的性质2
H2NCH—C—OH + H—NH—CHCOOH
R2
H2NCH—C—NH—CHCOOH + H2O
O
=
O
=
R1
R2
R1
缩合
水解
缩合反应与酯化反应类似!
肽的水解反应与酯的水解反应类似!
1、甘氨酸和丙氨酸的混合物在一定条件下可发生反应生成链状二肽,试判断能得到几种二肽,并写出二肽分子的结构简式。
2、三肽Val-Ala-Gly在一定条件下可以水解生成氨基酸。请写出其水解产物的结构简式。
甘-丙
H2NCH2C—NHCHCOOH
O
=
CH3
甘-甘
H2NCH2C—NHCH2COOH
O
=
丙-甘
H2NCHC—NHCH2COOH
O
=
H3C
丙-丙
H2NCHC—NHCHCOOH
O
=
CH3
H3C
H2NCH2COOH
Gly
CH3CHCOOH
Ala
NH2
Val
CH3CHCHCOOH
CH3
NH2
3、写出下列化学方程式
(1)两分子间缩合成二肽
(2)分子间或分子内缩合成环
(3)缩聚成多肽或蛋白质
茚三酮反应
α-氨基酸
紫色或紫蓝色
茚三酮
用途:反应灵敏,是鉴定氨基酸最简便的方法。
氨基酸的性质3
实 验
【实验】取1 mL 0.1%的茚三酮溶液,加入1%的甘氨酸溶液,将试管放入热水浴中,观察现象。
溶液呈紫色或紫蓝色
实验现象:
蛋白质的组成与结构
1、组成:主要由C、H、O、N组成。
2、结构
⑴一级结构:氨基酸残基在肽链中的顺序(桑格测定牛胰岛素的一级结构)。
⑵二级结构:α-螺旋结构、β-折叠结构(鲍林和科里共同发现)。
⑶三级结构:在二级结构的基础上,肽链按一定空间结构形成的更复杂的结构。
⑷四级结构:具有三级结构的肽链按一定的空间排列方式结合在一起形成的集体结构。
实验操作 实验现象 性质
蛋白质溶液 ①加饱和硫酸铵溶液,再加蒸馏水
②加硫酸钠溶液,再加蒸馏水
③加热,再加蒸馏水
④加醋酸铅溶液,再加蒸馏水
产生沉淀,加水后溶解
产生沉淀,加水后溶解
产生沉淀,加水后不溶解
产生沉淀,加水后不溶解
1、医院里用高温蒸煮、照射紫外线、喷洒苯酚溶液、在伤口处涂抹酒精溶液等方法来消毒杀菌的原理是什么?
2、为什么生物实验室用甲醛溶液(福尔马林)保存动物标本?
物理变化
盐析
化学变化
变性
性质 盐析 变性
所需条件
原理
变化
过程 (可逆或不可逆)
常见用途
某些浓的无机盐溶液,如Na2SO4、(NH4)2SO4
加热、强酸、强碱、重金属盐、紫外线、福尔马林(36%~40%甲醛溶液)、酒精等
降低蛋白质在水中的溶解度
使蛋白质化学组成或空间结构会发生改变,丧失生理活性,
物理变化
化学变化
可逆
不可逆
分离提纯
杀菌消毒
蛋白质的性质1
盐析与变性
实 验
【实验1】取蛋白质溶液2 mL于试管中,加入1 mL浓硝酸,微热,观察现象。
【实验2】取蛋白质溶液1mL于试管中,加入1mL10%的氢氧化钠溶液,再加入3~4滴1%的硫酸铜溶液,不断振荡,观察现象。
实验1:蛋白质变黄
实验2:溶液呈紫玫瑰色
实验现象:
【归纳总结】
蛋白黄反应:含有苯基的蛋白质遇到浓硝酸显黄色。
缩二脲反应:蛋白质遇双缩脲试剂呈紫玫瑰色。
上述反应可用于检验蛋白质!
蛋白质的基本组成单位是氨基酸,由氨基酸通过缩合反应生成,请推测蛋白质还具有哪些性质?
水解反应:一定条件下能发生水解反应,最终转化为各种小分子的氨基酸。
蛋白质的性质2
颜色反应
1、蛋白黄反应:含有苯基的蛋白质遇到浓硝酸显黄色,可用于检验蛋白质。
2、缩二脲反应:蛋白质遇双缩脲试剂呈紫玫瑰色。
3、茚三酮反应:蛋白质遇茚三酮呈蓝紫色。
具有两性:蛋白质与酸、碱作用都能生成盐。
在生命活动中,几乎所有的化学变化都是在酶的催化作用下完成的。阅读教材P162,回答下列问题:
1、酶属于哪一种物质类别?
2、酶催化反应具有哪些特点?
3、你认为影响酶催化活性的因素主要有哪些?
2、催化特点
⑴条件温和, 不需加热 (体温和中性条件);
⑵高度的专一性,一种酶只催化一种反应;
⑶高效性,比普通催化剂高107~1013倍。
酶——具有催化作用的生物分子
1、类别:绝大多数是蛋白质,少数是核糖核酸(RNA)。
3、影响因素:能使蛋白质变性的条件均能降低酶的催化活性!如高温、强酸、强碱、重金属离子等。
核酸的结构及生物功能
阅读教材,认识核酸的结构和生物功能!
核酸存在于一切生物体中,和蛋白质类似,核酸也有一级结构、二级结构和三级结构。
核糖核酸
(RNA)
脱氧核糖核酸
(DNA)
存在于细胞质
存在于细胞核
将DNA的遗传信息翻译并表达成具有特定功能的蛋白质
遗传信息的储存和携带者,决定了生物合成蛋白质的特定结构
核酸
1.下列物质属于蛋白质的一组是( )
A.淀粉 淀粉酶 B.血红蛋白 尿素
C.血红蛋白 淀粉酶 D.葡萄糖 淀粉
2.下列有机物在一定条件下不能发生水解反应的是( )
A.蛋白质 B.葡萄糖 C.油脂 D.淀粉
3.下列生活中的化学小实验不合理的是( )
A.用米汤检验加碘盐中的碘酸钾(KIO3)
B.用食用醋除去热水瓶中积存的水垢
C.用纯碱(Na2CO3)溶液洗涤沾有油污的器具
D.用灼烧并闻气味的方法区分化纤织物与纯毛织物
B
A
C
4.误服氯化钡溶液后会引起中毒,采用下列解毒方法中,正确的是( )
A.服用稀的硫酸铜溶液,使Ba2+变成BaSO4不溶物
B.服用小苏打溶液,使Ba2+变成BaCO3不溶物
C.服用大量豆浆,Ba2+能使蛋白质变性
D.饮用大量的水,使血液中凝聚的蛋白质重新溶解
C
5.有关蛋白质的叙述不正确的是( )
A.鸡蛋白溶液中,加入浓的硫酸铵溶液有沉淀析出,加水后沉淀不溶解
B.蛋白质水解的最后产物是氨基酸
C.加热可使蛋白质凝固
D.蛋白质是天然高分子化合物,有些蛋白质也可以人工合成
A
6、欲将蛋白质从水中析出而又不改变它的性质应加入( )
A、甲醛溶液 B、CuSO4溶液
C、饱和Na2SO4溶液 D、浓硫酸
7.在下列物质中:①K2SO4 ②HCHO ③MgSO4 ④乙醇 ⑤硝酸 ⑥Hg(NO3)2 ⑦NH4Cl ⑧KOH中,能使蛋白质变性的是( )
A.①②②④⑥⑧ B.①③⑤⑦⑧
C.①②③④⑤ D.②④⑤⑥⑧
8.下列物质中既能与盐酸又能与氢氧化钠反应的是( )
①NaHCO3②(NH4)2CO3③Al(OH)3 ④NH4Cl ⑤甘氨酸 ⑥醋酸
A.①②③ B.①②④⑤ C.⑤⑥ D.①②③⑤
C
D
D
专题6 生命活动的物质基础
第二单元 蛋白质
1、认识氨基酸和蛋白质的关系,以及它们对人体健康的影响;
2、能列举简单氨基酸的组成、结构、主要的化学性质和典型的检验方法;
3、能辨识蛋白质中的肽键,能判断氨基酸的缩合产物和多肽的水解产物,能通过实验探究蛋白质的主要性质和检验方法;
4、能初步认识核酸的结构特点和生物功能;体会生物大分子的研究的重要意义。
蛋白质是生命的物质基础,是构成细胞的基本有机物,是生命活动的主要承担者——没有蛋白质就没有生命。
1、组成蛋白质的主要元素有哪些?你如何理解氨基酸与蛋白质之间的关系?
2、你知道哪些常见的氨基酸?氨基酸有哪些重要的性质?
氨基酸的组成与结构
定义:氨基酸可看作是羧酸分子中烃基上的一个或几个氢原子被氨基取代后生成的化合物。
官能团:—COOH、—NH2
α-氨基酸
根据氨基和羧基的相对位置,氨基酸可以分为α-氨基酸、β-氨基酸等。自然界中最常见的为α-氨基酸。其结构通式可表示为:
通式中,R代表不同的基团,α-氨基酸的结构相似,不同的α-氨基酸只是R基不同。
迄今为止,人类在自然界已发现了数百种氨基酸,但是从生物体内的蛋白质水解得到的氨基酸,最常见的有20种,被称为蛋白质氨基酸。其中人体内不能合成的8种α-氨基酸,又称为必需氨基酸。
氨基酸的性质1
具有两性
-NH2——呈碱性 -COOH——呈酸性
羧酸盐
铵盐
用通式表示α-氨基酸分别与NaOH、HCl反应的化学方程式。
内盐
注:固态氨基酸主要以内盐形式存在,熔点较高,不易挥发,难溶于有机溶剂。常见的氨基酸均为无色结晶。
溶液酸碱性对氨基酸存在形态的影响
氨基酸是两性化合物,既能与酸发生反应,又能与碱发生反应。水溶液的pH不同,氨基酸在溶液中存在的形态也不同。
不同的氨基酸出现两性离子的pH各不相同,利用这一差异,可以通过控制溶液的pH分离不同的氨基酸、多肽和蛋白质。
两性离子
在水中的溶解度最小
阳离子
阴离子
一分子α-氨基酸中的羧基与另一分子α-氨基酸中的氨基可以发生像酯化反应那样的脱水反应,形成肽键(酰胺键),通常把该反应称为氨基酸的缩合反应。
肽键的形成和肽的水解
与酯能水解生成羧酸和醇一样,肽也可以在一定条件下水解生成氨基酸。
肽
N端
C端
可用氨基酸的缩写表示肽的结构
Gly-Ala(或甘-丙)
H2NCH2C—OH + H—NHCHCOOH
CH3
H2NCH2—C—NH—CHCOOH + H2O
O
=
O
=
CH3
缩合反应
氨基酸的性质2
H2NCH—C—OH + H—NH—CHCOOH
R2
H2NCH—C—NH—CHCOOH + H2O
O
=
O
=
R1
R2
R1
缩合
水解
缩合反应与酯化反应类似!
肽的水解反应与酯的水解反应类似!
1、甘氨酸和丙氨酸的混合物在一定条件下可发生反应生成链状二肽,试判断能得到几种二肽,并写出二肽分子的结构简式。
2、三肽Val-Ala-Gly在一定条件下可以水解生成氨基酸。请写出其水解产物的结构简式。
甘-丙
H2NCH2C—NHCHCOOH
O
=
CH3
甘-甘
H2NCH2C—NHCH2COOH
O
=
丙-甘
H2NCHC—NHCH2COOH
O
=
H3C
丙-丙
H2NCHC—NHCHCOOH
O
=
CH3
H3C
H2NCH2COOH
Gly
CH3CHCOOH
Ala
NH2
Val
CH3CHCHCOOH
CH3
NH2
3、写出下列化学方程式
(1)两分子间缩合成二肽
(2)分子间或分子内缩合成环
(3)缩聚成多肽或蛋白质
茚三酮反应
α-氨基酸
紫色或紫蓝色
茚三酮
用途:反应灵敏,是鉴定氨基酸最简便的方法。
氨基酸的性质3
实 验
【实验】取1 mL 0.1%的茚三酮溶液,加入1%的甘氨酸溶液,将试管放入热水浴中,观察现象。
溶液呈紫色或紫蓝色
实验现象:
蛋白质的组成与结构
1、组成:主要由C、H、O、N组成。
2、结构
⑴一级结构:氨基酸残基在肽链中的顺序(桑格测定牛胰岛素的一级结构)。
⑵二级结构:α-螺旋结构、β-折叠结构(鲍林和科里共同发现)。
⑶三级结构:在二级结构的基础上,肽链按一定空间结构形成的更复杂的结构。
⑷四级结构:具有三级结构的肽链按一定的空间排列方式结合在一起形成的集体结构。
实验操作 实验现象 性质
蛋白质溶液 ①加饱和硫酸铵溶液,再加蒸馏水
②加硫酸钠溶液,再加蒸馏水
③加热,再加蒸馏水
④加醋酸铅溶液,再加蒸馏水
产生沉淀,加水后溶解
产生沉淀,加水后溶解
产生沉淀,加水后不溶解
产生沉淀,加水后不溶解
1、医院里用高温蒸煮、照射紫外线、喷洒苯酚溶液、在伤口处涂抹酒精溶液等方法来消毒杀菌的原理是什么?
2、为什么生物实验室用甲醛溶液(福尔马林)保存动物标本?
物理变化
盐析
化学变化
变性
性质 盐析 变性
所需条件
原理
变化
过程 (可逆或不可逆)
常见用途
某些浓的无机盐溶液,如Na2SO4、(NH4)2SO4
加热、强酸、强碱、重金属盐、紫外线、福尔马林(36%~40%甲醛溶液)、酒精等
降低蛋白质在水中的溶解度
使蛋白质化学组成或空间结构会发生改变,丧失生理活性,
物理变化
化学变化
可逆
不可逆
分离提纯
杀菌消毒
蛋白质的性质1
盐析与变性
实 验
【实验1】取蛋白质溶液2 mL于试管中,加入1 mL浓硝酸,微热,观察现象。
【实验2】取蛋白质溶液1mL于试管中,加入1mL10%的氢氧化钠溶液,再加入3~4滴1%的硫酸铜溶液,不断振荡,观察现象。
实验1:蛋白质变黄
实验2:溶液呈紫玫瑰色
实验现象:
【归纳总结】
蛋白黄反应:含有苯基的蛋白质遇到浓硝酸显黄色。
缩二脲反应:蛋白质遇双缩脲试剂呈紫玫瑰色。
上述反应可用于检验蛋白质!
蛋白质的基本组成单位是氨基酸,由氨基酸通过缩合反应生成,请推测蛋白质还具有哪些性质?
水解反应:一定条件下能发生水解反应,最终转化为各种小分子的氨基酸。
蛋白质的性质2
颜色反应
1、蛋白黄反应:含有苯基的蛋白质遇到浓硝酸显黄色,可用于检验蛋白质。
2、缩二脲反应:蛋白质遇双缩脲试剂呈紫玫瑰色。
3、茚三酮反应:蛋白质遇茚三酮呈蓝紫色。
具有两性:蛋白质与酸、碱作用都能生成盐。
在生命活动中,几乎所有的化学变化都是在酶的催化作用下完成的。阅读教材P162,回答下列问题:
1、酶属于哪一种物质类别?
2、酶催化反应具有哪些特点?
3、你认为影响酶催化活性的因素主要有哪些?
2、催化特点
⑴条件温和, 不需加热 (体温和中性条件);
⑵高度的专一性,一种酶只催化一种反应;
⑶高效性,比普通催化剂高107~1013倍。
酶——具有催化作用的生物分子
1、类别:绝大多数是蛋白质,少数是核糖核酸(RNA)。
3、影响因素:能使蛋白质变性的条件均能降低酶的催化活性!如高温、强酸、强碱、重金属离子等。
核酸的结构及生物功能
阅读教材,认识核酸的结构和生物功能!
核酸存在于一切生物体中,和蛋白质类似,核酸也有一级结构、二级结构和三级结构。
核糖核酸
(RNA)
脱氧核糖核酸
(DNA)
存在于细胞质
存在于细胞核
将DNA的遗传信息翻译并表达成具有特定功能的蛋白质
遗传信息的储存和携带者,决定了生物合成蛋白质的特定结构
核酸
1.下列物质属于蛋白质的一组是( )
A.淀粉 淀粉酶 B.血红蛋白 尿素
C.血红蛋白 淀粉酶 D.葡萄糖 淀粉
2.下列有机物在一定条件下不能发生水解反应的是( )
A.蛋白质 B.葡萄糖 C.油脂 D.淀粉
3.下列生活中的化学小实验不合理的是( )
A.用米汤检验加碘盐中的碘酸钾(KIO3)
B.用食用醋除去热水瓶中积存的水垢
C.用纯碱(Na2CO3)溶液洗涤沾有油污的器具
D.用灼烧并闻气味的方法区分化纤织物与纯毛织物
B
A
C
4.误服氯化钡溶液后会引起中毒,采用下列解毒方法中,正确的是( )
A.服用稀的硫酸铜溶液,使Ba2+变成BaSO4不溶物
B.服用小苏打溶液,使Ba2+变成BaCO3不溶物
C.服用大量豆浆,Ba2+能使蛋白质变性
D.饮用大量的水,使血液中凝聚的蛋白质重新溶解
C
5.有关蛋白质的叙述不正确的是( )
A.鸡蛋白溶液中,加入浓的硫酸铵溶液有沉淀析出,加水后沉淀不溶解
B.蛋白质水解的最后产物是氨基酸
C.加热可使蛋白质凝固
D.蛋白质是天然高分子化合物,有些蛋白质也可以人工合成
A
6、欲将蛋白质从水中析出而又不改变它的性质应加入( )
A、甲醛溶液 B、CuSO4溶液
C、饱和Na2SO4溶液 D、浓硫酸
7.在下列物质中:①K2SO4 ②HCHO ③MgSO4 ④乙醇 ⑤硝酸 ⑥Hg(NO3)2 ⑦NH4Cl ⑧KOH中,能使蛋白质变性的是( )
A.①②②④⑥⑧ B.①③⑤⑦⑧
C.①②③④⑤ D.②④⑤⑥⑧
8.下列物质中既能与盐酸又能与氢氧化钠反应的是( )
①NaHCO3②(NH4)2CO3③Al(OH)3 ④NH4Cl ⑤甘氨酸 ⑥醋酸
A.①②③ B.①②④⑤ C.⑤⑥ D.①②③⑤
C
D
D
