浙教版科学八年级下期中解答题专练一(含解析)
文档属性
| 名称 | 浙教版科学八年级下期中解答题专练一(含解析) |
|
|
| 格式 | docx | ||
| 文件大小 | 262.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-04-12 00:00:00 | ||
图片预览




文档简介
期中解答题专练一
、解答题
(1)在图中画出磁感线的方向,并标出 N 极。
(2)在图 2 中用涂黑的方式画出小磁针的 N 极。
小明自制了一个带有电磁铁的木船模型,将它放入水中漂浮,闭合开关后,船头会向北方偏转。请在图上画出螺线管的绕线方法。
我国目前的动车上均安装了烟雾报警器,一旦有吸烟,列车上的烟雾报警系统就会报警,列车就会自动减速甚至停车。小刘在查阅资料后,自行设计了一个“烟雾报警器”,电路如图。该报警器由“控制电路”和“工作电路”所组成,其中“控制电路”由光敏电阻R、电磁铁(线圈阻值R0=12Ω)、电源U=6V、开关等组成;“工作电路”由工作电源、电铃、导线等组成。小刘的设计思路:当光敏电阻接收到的光强减弱到一定程度时,工作电路接通,电铃报警。已知该光敏电阻的阻值R与光强E之间的关系如表所示。
光强E/cd 1 2 3 4 5 6
光敏电阻R/Ω 36 18 12 9 m 6
(1)根据光敏电阻的阻值R与光强E之间的关系,推测m= 。
(2)根据报警器的工作原理判断,电铃应接在 (填“甲”或“乙”)处。
(3)闭合开关S,如果当线圈中的电流大于或等于250mA时,继电器的衔铁被吸合,则光敏电阻接收到的光照强度需要在多少cd以上?
(4)若要提高该烟雾报警器的灵敏度(即在烟雾更少条件下就能报警),请你提出一种改进建议。
请用笔画线代替导线,将图中的电灯、开关和插座正确接入家庭电路中。
已知在C2H4、C2H4O和C2H4O6组成的混合物中,经分析发现含氧元素的质量分数为M%,则混合物中氢元素的质量分数是多少?面对这类的题目,我们可以对抽象的问题进行理想化处理。我们把此混合物放入一容器,那么在此容器中便存在大量构成这三种物质的分子:a个C2H4分子,b个C2H4O分子,c个C2H4O6分子。现在我们需取出三个分子,随机的结果有:
①一个C2H4分子,一个C2H4O分子,一个C2H4O6分子;
②一个C2H4分子,二个C2H4O分子;
③一个C2H4O分子,二个C2H4O6分子……
(1)我们来看这三种情况,我们发现,无论怎么组合 (填两种元素名 称)的原子个数比为一定值,且这两种元素所占总物质的质量分数可表示为 ,且碳元素的质量分数可表示为 。
(2)拓展:已知在NaHS、MgSO4和NaHSO3组成的混合物中,含硫40%,则氧元素的质量分数为 。
市场上出现的某钙片的标签如图,经检验知,此钙片中含钙物质只有碳酸钙(CaCO3)
(1)此标签中标注的含钙量是否合理? (填“合理”或“不合理”)
(2)如果一个青少年每天需补钙0.8克,其中有0.6克来自于牛奶及其他食品,其余服用钙片。请计算每天他需补充碳酸钙多少克?(写出计算过程)
(3)7.4克氢氧化钙[Ca(OH)2]与多少克碳酸钙[CaCO3]含钙元素质量相等?(写出计算过程)
如图甲所示是测电笔的结构,图乙和图丙中,正确使用试电笔的是图 ,当用它插入插座的左孔时氖管不亮,插入右孔时氖管发光,则说明火线在插座的 孔。测电笔内部有一个大电阻,它的作用是 。若测电笔氖管发光放电时的电流为0.36毫安,人体的安全电压为36伏,则当测电笔的笔尖接触家庭电路的火线时要使人能处于安全状态,此大电阻的阻值至少应为 欧。(不计氖管发光时的电阻)
时下有些年轻人喜欢染发,染发时一般要用到一种着色剂对苯二胺,其化学式为C6H8Nx。它是一种有毒的化学药品,会对染发者的身体带来伤害。回答下列问题:
(1)对苯二胺是由 种元素组成的。
(2)对苯二胺的相对分子质量为108,则x= 。
(3).对苯二胺中碳元素和氢元素最简质量比等于 。 (要求写出最简整数比)
2018年2月《自然》杂志上发表了一项新研究,展示了一种全新的加工木材的方法(如图),把天然木材放在NaOH和Na2SO3的混合液中煮沸以除去部分木质素,接着在100℃以上的高温中进行机械压缩制成致密木材。
(1)致密木材是由天然木材加工而成的,其密度为天然木材的3倍。
①加工致密木材的材料主要取自于植物的 (填植物器官名称).
②充分压缩后木材的厚度减小到原天然木材的20%,这一过程主要是 变化。若在压缩过程中底面积保持不变,则说明处理过程中木材的质量减少了 (用百分数表示)。
(2)致密木材的硬度、拉伸强度都很大,为天然木材的10倍左右,甚至超过了部分金属.
①致密木材的拉伸强度和纤维素有关。纤维素的化学式为(C12H10O5)n,则其中三种元素的质量比是C:H:O= 。
②拉伸强度= ,它用来表示材料的坚韧程度。拉伸强度与我们所学的科学量 的单位是相同的。
(3)与其他材料相比,致密木材的优点是( )
A.加工过程中没有任何污染
B.可代替部分金属材料,具有广阔的应用前景
C.原料来源丰富,能通过无限制砍伐树木加工制成
中国是一个人口众多的发展中国家,人们注意到:西方国家的发展模式不完全适用于中国。例如:设想以植物性食物为主的中国人,平均食用牛肉的水平若与美国人相当。则每年需增加粮食3.4 亿吨(这相当于美国一年的粮食产量)如果每吨粮食生产需提供0.1吨氮元素,则:中国每年将需要多供应多少吨尿素(CO(NH2)2)
丁酸乙酯(C6H12O2)是一种具有菠萝香味的液体,可用于制作香料、香精和作溶剂。
(1)丁酸乙酯中氢和碳的原子个数比为 。
(2)丁酸乙酯作为溶剂,可以溶解多种有机物,这体现了它的 。(填“物理性质”或“化学性质”)
(3)若丁酸乙酯和葡萄糖(C6H12O6)中碳原子个数相等,则丁酸乙酯和葡萄糖的质量比为 。
光合作用释放的氧气来自原料CO2还是H2O呢 科学家鲁宾和卡门曾对这个问题进行了研究,在实验中他们利用18O作为标记物,制备了三份相同浓度的碳酸氢盐溶液,三份溶液的碳酸氢盐和水都含有不同的18O百分比,将小球藻放入这三种溶液并光照,然后分析产生的氧,得出结论:光合作用产生的氧来自水。
资料:
Ⅰ.中子数为8的氧原子可用16O来表示,18O是表示中子数为10的氧原子;自然界的氧气在标准状况下的密度为1.43千克/米3 , 其中16O占99.76%(可视为100%),
Ⅱ.碳酸氢盐给小球藻的光合作用提供全部的CO2 , 而且不产生水。
Ⅲ.在相同的温度和压强下,相同体积的气体具有相同的分子数。
(1)16O、标记物18O都属于氧元素,其位置大致在元素周期表的________方。
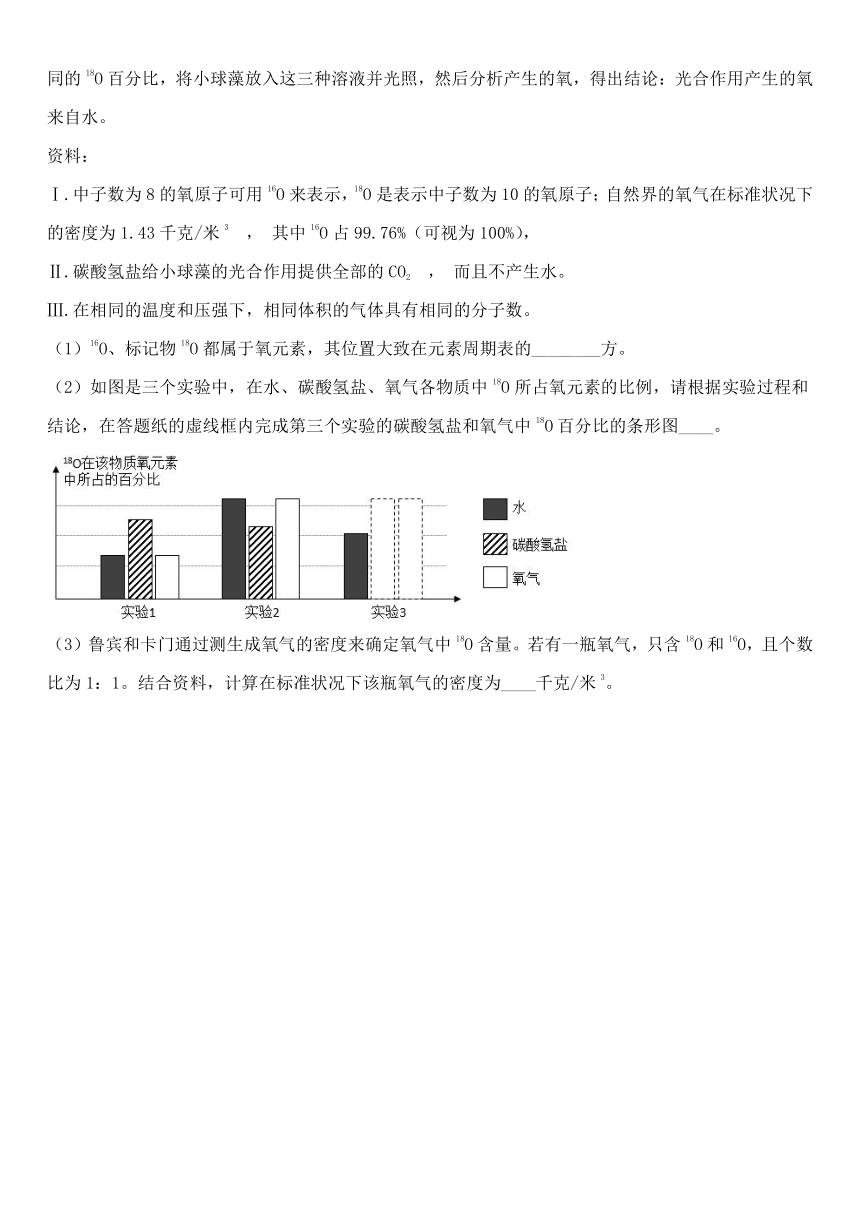
(2)如图是三个实验中,在水、碳酸氢盐、氧气各物质中18O所占氧元素的比例,请根据实验过程和结论,在答题纸的虚线框内完成第三个实验的碳酸氢盐和氧气中18O百分比的条形图____。
(3)鲁宾和卡门通过测生成氧气的密度来确定氧气中18O含量。若有一瓶氧气,只含18O和16O,且个数比为1:1。结合资料,计算在标准状况下该瓶氧气的密度为____千克/米3。
亚铁离子具有防治缺铁性贫血的功效,而三价铁离子会使人感到胃部不适,还会对肝脏产生危害。维生素C可以防止亚铁离子氧化成三价铁离子。如图是某种补铁药物说明书的部分信息。某成人按此说明书服药期间,每天能从该药物中补充铁元素多少毫克?
补铁缓释片 规格:每片含硫酸亚铁(FeSO4)456毫克 用量:成人一天一片
期中解答题专练一答案解析
、解答题
【答案】(1)解:如图所示:
(2)解:如图所示:
【解析】(1)磁感线从N极出发,回到S极,由小磁针N极指向左边,可知条形磁铁左端为S极,右端为N极,再画出磁感线的方向即可;
(2)先由右手螺旋定则判断出通电螺线管的磁极,左端为S极,右端为N极,由磁极间的相互作用规律得知,小磁针的N极在小磁针的右端,再由磁感线的特点画出磁感线的方向。
【解答】(1)
(2)
故答案为:见上
【答案】解:
【解析】通电螺线管中的安培定则:用右手握住通电螺线管,使四指弯曲与电流方向一致,那么指所指的那一端是通电螺线管的N极。
【解答】闭合开关后,船头会向北方偏转,说明右侧为带电电磁铁的N极,左侧为S极,根据安培定则即可画出螺线管的绕线方法。
【答案】(1)7.2
(2)甲
(3)R点= =24Ω,
R=R总-R0=24Ω- 12Ω= 12Ω,
对应表格E=3.0cd
(4)降低电源电压或串联一个定值电阻
【解析】(1)根据表格数据,分析光敏电阻的阻值随光照强度的数量关系,然后推测m的数值;
(2)分析报警器工作时衔铁的位置即可;
(3)首先根据 计算出衔铁吸合时的总电阻,再根据计 R=R总-R0 算出此时光敏电阻的阻值,最后根据表格确定此时的光照强度。
(4)电磁铁的衔铁弹开时磁场的强弱不变,即通过电磁铁的电流不变。当烟雾减少时,光照强度增大,而光敏电阻的阻值减小,根据U=IR可知,保持电流不变,即可以降低电源电压。根据可知,如果电源电压不变,电流不变,那么总电阻不变。为了保持总电阻不变,此时可以再串联一个定值电阻,据此分析解答。
【解答】(1)根据表格可知,光敏电阻的阻值和对应光照强度的乘积都是36,则m=.
(2)当烟雾增大时,光照强度减小,光敏电阻阻值增大,而通过电磁铁的电流减小。此时电磁铁的磁场减弱,衔铁弹回原来位置,接通甲所在的电路,因此报警器应该与甲相接。
(4)要提高该烟雾报警器的灵敏度(即在烟雾更少条件下就能报警),改进建议为:降低电源电压或串联一个定值电阻。
【答案】如图所示
【解析】根据家庭电路连接的知识分析解答。
【解答】①三孔插座的左孔接零线,右孔接火线,中控接地线。
②从火线上接线,首先连接开关,然后再将灯泡与零线相连,如下图所示:
(1)149
(2)15:8
(3)蛋氨酸中氮元素的质量分数为9.4%
(4)每100克合格奶粉中氮元素的质量为2.88g;不合格
(1)相对分子质量等于相对原子质量和个数的乘积之和;
(2)元素的质量之比等于相对原子质量和个数的乘积之比;
(3)元素的质量分数=;
(4)氮元素的质量=蛋白质的质量×氮元素的质量分数。将100g奶粉中氮元素的质量与2.88g比较即可。
【解答】(1)根据化学式 C5H11O2NS 可知,蛋氨酸的相对分子质量:12×5+1×11+16×2+14+32=149。
(2)蛋氨酸中碳氧元素的质量比C∶O =(12×5):(16×2)=15:8.
(3)蛋氨酸中氮元素的质量分数:。
(4)每100克合格奶粉中氮元素的质量:
因为1.5g<2.88g,所以这种奶粉不合格。
(1)不合理
(2)每天需补钙元素的质量为:0.8g-0.6g=0.2g,
设:每天需补充碳酸钙的质量为x,0.2g=x×40%,
解得: x=0.5g;
(3)7.4克氢氧化钙中所含钙元素的质量为:;
所需碳酸钙的质量为:。
(1)根据标签信息以及碳酸钙的化学式计算钙元素的质量分数;
(2)用每天补钙质量减去来自于牛奶和其它食品的钙元素质量,从而得到来自钙片的钙元素的质量,再根据“钙元素质量=碳酸钙质量×钙元素的质量分数”列方程计算即可。
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答。【解答】(1)由标签信息可知,每片钙片含钙元素的质量为0.75g;
碳酸钙中钙元素的质量分数为:;
每片钙片中含有钙元素的质量为:
因为0.32g<0.75g,
所以说明此标签中的含钙量不合理;
【答案】丙;右;分压(限流);5.11×105
【解析】(1)使用测电笔时,人体必须接触尾部的金属体,否则它不能正常工作;
(2)正常情况下,测电笔接触火线发光,接触零线不发光;
(3)人体直接接触火线,由于电压太大,会造成触电事故。在测电笔中串联一个大电阻,可以起到分压限流的作用,保证人体不会触电;
(4)首先根据U=U总-U人计算出测电笔两端的电压,然后根据计算电阻即可。
【解答】(1)如图甲所示是测电笔的结构,图乙和图丙中,正确使用试电笔的是图丙;
(2)当用它插入插座的左孔时氖管不亮,插入右孔时氖管发光,则说明火线在插座的右孔。
(3)测电笔内部有一个大电阻,它的作用是分压限流;
(4)测电笔两端的电压:U=U总-U人=220V-36V=184V;
测电笔的电阻为:。
(1)3
(2)2
(3)9.1
(1)在化学式中,一种符号代表一种元素;
(2)相对分子质量等于相对原子质量与个数的乘积之和;
(3)元素的质量之比等于相对原子质量与个数的乘积之比。
【解答】(1)根据化学式 C6H8Nx 可知,对苯二胺由C、H、N共3种元素组成;
(2)根据化学式 C6H8Nx 可知,对苯二胺的相对分子质量:
12×6+1×8+14x=108,解得:x=2;
(3)根据化学式 C6H8Nx 可知,对苯二胺中碳元素和氢元素最简质量比:
(12×6):(1×8)=9:1。
(1)茎;物理;40%
(2)72:5:40;压强
(3)B
元素质量比=元素的相对原子质量*原子个数的比;物体所受的压力与受力面积之比叫做压强,压强用来比较压力产生的效果,压强越大,压力的作用效果越明显。压强的计算公式是:p=F/S,压强的单位是帕斯卡,符号是Pa。
【解答】(1)加工木材主要取用的是木材的木质部,而木质部是茎的一部分;对木材进行压缩后没有新物质的产生,所以该过程是物理变化;压缩前木材的质量为: ;而压缩后厚度减少到20%。底面积不变,则体积减小到压缩前的20%; ;故答案为:茎;物理变化;40%;(2)m(C):m(H):m(O)=12×12×n:10×1×n:16×5×n=72:5:40;由公式可知,材料宽度×材料厚度=材料的底面积;而力与面积之比是压强;故答案为:72:5:40;压强;(3)A、在制作过程中使用了多种化学试剂,会造成污染;故A错误;
B、制作之后的材料硬度超过部分金属材料的硬度,所以可以替代部分金属;故B正确;
C、树木对于地球的生态系统作用巨大,不可或缺,因此不能无限制砍伐;故C错误;故答案为:B;
故答案为:茎;物理变化;40%;(2)72:5:40;压强;(3)B。
尿素中氮元素的质量分数为 , (吨)
根据元素的质量分数的计算方法来分析。根据物质的质量和元素的质量分数可以计算出元素的质量。
【解答】
尿素中氮元素的质量分数为: 2N/(CO(NH2)2) =28 /60 × 100 % ≈ 46.7 % ,
多少吨尿素(CO(NH2)2)含0.1吨氮元素: 0.1 ÷ 46.7 % =0.214吨
3.4 亿吨粮食需要化肥:0.214吨X3.4X 10 8=7.28 × 10 7 (吨)
(1)474
(2)m(K)∶m(Al)∶m(S)∶m(O)∶m(H)=39∶27∶64∶320∶24
(3)8.2%
(4)解:设与258g明矾中氧元素质量相等的水的质量为x。x×(1618×100%)=258g×(16×20474×100%)x=195.9g答:258g明矾与195.9g水所含氧元素的质量相等。
(1)相对分子质量等于相对原子质量和个数的乘积之和;
(2)元素的质量之比等于相对原子质量和个数的乘积之比;
(3)元素的质量分数=;
(4)元素质量=物质质量×元素的质量分数,据此根据氧元素质量相等列出方程计算即可。
【解答】(1)明矾的相对分子质量是:39+27+(32+16×4)×2+(1×2+16)×12=474。
(2)明矾中各元素的质量比是:
m(K)∶m(Al)∶m(S)∶m(O)∶m(H)=(39×1):(27×1):(32×2):(16×20):(1×24)=39∶27∶64∶320∶24。
(3)明矾中钾元素的质量分数是:。
(4)设与258g明矾中氧元素质量相等的水的质量为x,
;
解得:x=195.9g。
右上 1.52
【详解】
(1)氧原子中含有8个质子,是8号元素,是第二周期,第六主族元素,位于元素周期右上方;
(2)由实验结论可知,产生的氧气均来自水,所以实验三中氧气中含有的 18O 百分比与水中的 18O 百分比相同; 三份溶液的碳酸氢盐和水都含有不同的18O百分比,所以碳酸氢盐的18O与实验1、2都不相同;
(3) 氧气在标准状况下的密度为1.43千克/米3 ,所以,含有18O 的氧气密度为: 1.43kg/m3≈1.61kg/m3,设一瓶氧气的的体积为V,由于这瓶氧气只 含18O和16O,且个数比为1:1,所以其密度为1.52千克/米3。
解:铁元素质量=456毫克× ×100%=168毫克
根据元素质量分数=相对原子质量×原子个数/相对分子质量分析;根据元素质量=化合物质量×元素质量分数分析。
【解答】 成人一天一片,一片中所含硫酸亚铁质量为456毫克,所以每天能从药物中补充铁元素质量=456毫克× ×100%=168毫克 ;
故答案为: 铁元素质量=456毫克× ×100%=168毫克 。
第 13 页(共 13 页)
、解答题
(1)在图中画出磁感线的方向,并标出 N 极。
(2)在图 2 中用涂黑的方式画出小磁针的 N 极。
小明自制了一个带有电磁铁的木船模型,将它放入水中漂浮,闭合开关后,船头会向北方偏转。请在图上画出螺线管的绕线方法。
我国目前的动车上均安装了烟雾报警器,一旦有吸烟,列车上的烟雾报警系统就会报警,列车就会自动减速甚至停车。小刘在查阅资料后,自行设计了一个“烟雾报警器”,电路如图。该报警器由“控制电路”和“工作电路”所组成,其中“控制电路”由光敏电阻R、电磁铁(线圈阻值R0=12Ω)、电源U=6V、开关等组成;“工作电路”由工作电源、电铃、导线等组成。小刘的设计思路:当光敏电阻接收到的光强减弱到一定程度时,工作电路接通,电铃报警。已知该光敏电阻的阻值R与光强E之间的关系如表所示。
光强E/cd 1 2 3 4 5 6
光敏电阻R/Ω 36 18 12 9 m 6
(1)根据光敏电阻的阻值R与光强E之间的关系,推测m= 。
(2)根据报警器的工作原理判断,电铃应接在 (填“甲”或“乙”)处。
(3)闭合开关S,如果当线圈中的电流大于或等于250mA时,继电器的衔铁被吸合,则光敏电阻接收到的光照强度需要在多少cd以上?
(4)若要提高该烟雾报警器的灵敏度(即在烟雾更少条件下就能报警),请你提出一种改进建议。
请用笔画线代替导线,将图中的电灯、开关和插座正确接入家庭电路中。
已知在C2H4、C2H4O和C2H4O6组成的混合物中,经分析发现含氧元素的质量分数为M%,则混合物中氢元素的质量分数是多少?面对这类的题目,我们可以对抽象的问题进行理想化处理。我们把此混合物放入一容器,那么在此容器中便存在大量构成这三种物质的分子:a个C2H4分子,b个C2H4O分子,c个C2H4O6分子。现在我们需取出三个分子,随机的结果有:
①一个C2H4分子,一个C2H4O分子,一个C2H4O6分子;
②一个C2H4分子,二个C2H4O分子;
③一个C2H4O分子,二个C2H4O6分子……
(1)我们来看这三种情况,我们发现,无论怎么组合 (填两种元素名 称)的原子个数比为一定值,且这两种元素所占总物质的质量分数可表示为 ,且碳元素的质量分数可表示为 。
(2)拓展:已知在NaHS、MgSO4和NaHSO3组成的混合物中,含硫40%,则氧元素的质量分数为 。
市场上出现的某钙片的标签如图,经检验知,此钙片中含钙物质只有碳酸钙(CaCO3)
(1)此标签中标注的含钙量是否合理? (填“合理”或“不合理”)
(2)如果一个青少年每天需补钙0.8克,其中有0.6克来自于牛奶及其他食品,其余服用钙片。请计算每天他需补充碳酸钙多少克?(写出计算过程)
(3)7.4克氢氧化钙[Ca(OH)2]与多少克碳酸钙[CaCO3]含钙元素质量相等?(写出计算过程)
如图甲所示是测电笔的结构,图乙和图丙中,正确使用试电笔的是图 ,当用它插入插座的左孔时氖管不亮,插入右孔时氖管发光,则说明火线在插座的 孔。测电笔内部有一个大电阻,它的作用是 。若测电笔氖管发光放电时的电流为0.36毫安,人体的安全电压为36伏,则当测电笔的笔尖接触家庭电路的火线时要使人能处于安全状态,此大电阻的阻值至少应为 欧。(不计氖管发光时的电阻)
时下有些年轻人喜欢染发,染发时一般要用到一种着色剂对苯二胺,其化学式为C6H8Nx。它是一种有毒的化学药品,会对染发者的身体带来伤害。回答下列问题:
(1)对苯二胺是由 种元素组成的。
(2)对苯二胺的相对分子质量为108,则x= 。
(3).对苯二胺中碳元素和氢元素最简质量比等于 。 (要求写出最简整数比)
2018年2月《自然》杂志上发表了一项新研究,展示了一种全新的加工木材的方法(如图),把天然木材放在NaOH和Na2SO3的混合液中煮沸以除去部分木质素,接着在100℃以上的高温中进行机械压缩制成致密木材。
(1)致密木材是由天然木材加工而成的,其密度为天然木材的3倍。
①加工致密木材的材料主要取自于植物的 (填植物器官名称).
②充分压缩后木材的厚度减小到原天然木材的20%,这一过程主要是 变化。若在压缩过程中底面积保持不变,则说明处理过程中木材的质量减少了 (用百分数表示)。
(2)致密木材的硬度、拉伸强度都很大,为天然木材的10倍左右,甚至超过了部分金属.
①致密木材的拉伸强度和纤维素有关。纤维素的化学式为(C12H10O5)n,则其中三种元素的质量比是C:H:O= 。
②拉伸强度= ,它用来表示材料的坚韧程度。拉伸强度与我们所学的科学量 的单位是相同的。
(3)与其他材料相比,致密木材的优点是( )
A.加工过程中没有任何污染
B.可代替部分金属材料,具有广阔的应用前景
C.原料来源丰富,能通过无限制砍伐树木加工制成
中国是一个人口众多的发展中国家,人们注意到:西方国家的发展模式不完全适用于中国。例如:设想以植物性食物为主的中国人,平均食用牛肉的水平若与美国人相当。则每年需增加粮食3.4 亿吨(这相当于美国一年的粮食产量)如果每吨粮食生产需提供0.1吨氮元素,则:中国每年将需要多供应多少吨尿素(CO(NH2)2)
丁酸乙酯(C6H12O2)是一种具有菠萝香味的液体,可用于制作香料、香精和作溶剂。
(1)丁酸乙酯中氢和碳的原子个数比为 。
(2)丁酸乙酯作为溶剂,可以溶解多种有机物,这体现了它的 。(填“物理性质”或“化学性质”)
(3)若丁酸乙酯和葡萄糖(C6H12O6)中碳原子个数相等,则丁酸乙酯和葡萄糖的质量比为 。
光合作用释放的氧气来自原料CO2还是H2O呢 科学家鲁宾和卡门曾对这个问题进行了研究,在实验中他们利用18O作为标记物,制备了三份相同浓度的碳酸氢盐溶液,三份溶液的碳酸氢盐和水都含有不同的18O百分比,将小球藻放入这三种溶液并光照,然后分析产生的氧,得出结论:光合作用产生的氧来自水。
资料:
Ⅰ.中子数为8的氧原子可用16O来表示,18O是表示中子数为10的氧原子;自然界的氧气在标准状况下的密度为1.43千克/米3 , 其中16O占99.76%(可视为100%),
Ⅱ.碳酸氢盐给小球藻的光合作用提供全部的CO2 , 而且不产生水。
Ⅲ.在相同的温度和压强下,相同体积的气体具有相同的分子数。
(1)16O、标记物18O都属于氧元素,其位置大致在元素周期表的________方。
(2)如图是三个实验中,在水、碳酸氢盐、氧气各物质中18O所占氧元素的比例,请根据实验过程和结论,在答题纸的虚线框内完成第三个实验的碳酸氢盐和氧气中18O百分比的条形图____。
(3)鲁宾和卡门通过测生成氧气的密度来确定氧气中18O含量。若有一瓶氧气,只含18O和16O,且个数比为1:1。结合资料,计算在标准状况下该瓶氧气的密度为____千克/米3。
亚铁离子具有防治缺铁性贫血的功效,而三价铁离子会使人感到胃部不适,还会对肝脏产生危害。维生素C可以防止亚铁离子氧化成三价铁离子。如图是某种补铁药物说明书的部分信息。某成人按此说明书服药期间,每天能从该药物中补充铁元素多少毫克?
补铁缓释片 规格:每片含硫酸亚铁(FeSO4)456毫克 用量:成人一天一片
期中解答题专练一答案解析
、解答题
【答案】(1)解:如图所示:
(2)解:如图所示:
【解析】(1)磁感线从N极出发,回到S极,由小磁针N极指向左边,可知条形磁铁左端为S极,右端为N极,再画出磁感线的方向即可;
(2)先由右手螺旋定则判断出通电螺线管的磁极,左端为S极,右端为N极,由磁极间的相互作用规律得知,小磁针的N极在小磁针的右端,再由磁感线的特点画出磁感线的方向。
【解答】(1)
(2)
故答案为:见上
【答案】解:
【解析】通电螺线管中的安培定则:用右手握住通电螺线管,使四指弯曲与电流方向一致,那么指所指的那一端是通电螺线管的N极。
【解答】闭合开关后,船头会向北方偏转,说明右侧为带电电磁铁的N极,左侧为S极,根据安培定则即可画出螺线管的绕线方法。
【答案】(1)7.2
(2)甲
(3)R点= =24Ω,
R=R总-R0=24Ω- 12Ω= 12Ω,
对应表格E=3.0cd
(4)降低电源电压或串联一个定值电阻
【解析】(1)根据表格数据,分析光敏电阻的阻值随光照强度的数量关系,然后推测m的数值;
(2)分析报警器工作时衔铁的位置即可;
(3)首先根据 计算出衔铁吸合时的总电阻,再根据计 R=R总-R0 算出此时光敏电阻的阻值,最后根据表格确定此时的光照强度。
(4)电磁铁的衔铁弹开时磁场的强弱不变,即通过电磁铁的电流不变。当烟雾减少时,光照强度增大,而光敏电阻的阻值减小,根据U=IR可知,保持电流不变,即可以降低电源电压。根据可知,如果电源电压不变,电流不变,那么总电阻不变。为了保持总电阻不变,此时可以再串联一个定值电阻,据此分析解答。
【解答】(1)根据表格可知,光敏电阻的阻值和对应光照强度的乘积都是36,则m=.
(2)当烟雾增大时,光照强度减小,光敏电阻阻值增大,而通过电磁铁的电流减小。此时电磁铁的磁场减弱,衔铁弹回原来位置,接通甲所在的电路,因此报警器应该与甲相接。
(4)要提高该烟雾报警器的灵敏度(即在烟雾更少条件下就能报警),改进建议为:降低电源电压或串联一个定值电阻。
【答案】如图所示
【解析】根据家庭电路连接的知识分析解答。
【解答】①三孔插座的左孔接零线,右孔接火线,中控接地线。
②从火线上接线,首先连接开关,然后再将灯泡与零线相连,如下图所示:
(1)149
(2)15:8
(3)蛋氨酸中氮元素的质量分数为9.4%
(4)每100克合格奶粉中氮元素的质量为2.88g;不合格
(1)相对分子质量等于相对原子质量和个数的乘积之和;
(2)元素的质量之比等于相对原子质量和个数的乘积之比;
(3)元素的质量分数=;
(4)氮元素的质量=蛋白质的质量×氮元素的质量分数。将100g奶粉中氮元素的质量与2.88g比较即可。
【解答】(1)根据化学式 C5H11O2NS 可知,蛋氨酸的相对分子质量:12×5+1×11+16×2+14+32=149。
(2)蛋氨酸中碳氧元素的质量比C∶O =(12×5):(16×2)=15:8.
(3)蛋氨酸中氮元素的质量分数:。
(4)每100克合格奶粉中氮元素的质量:
因为1.5g<2.88g,所以这种奶粉不合格。
(1)不合理
(2)每天需补钙元素的质量为:0.8g-0.6g=0.2g,
设:每天需补充碳酸钙的质量为x,0.2g=x×40%,
解得: x=0.5g;
(3)7.4克氢氧化钙中所含钙元素的质量为:;
所需碳酸钙的质量为:。
(1)根据标签信息以及碳酸钙的化学式计算钙元素的质量分数;
(2)用每天补钙质量减去来自于牛奶和其它食品的钙元素质量,从而得到来自钙片的钙元素的质量,再根据“钙元素质量=碳酸钙质量×钙元素的质量分数”列方程计算即可。
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答。【解答】(1)由标签信息可知,每片钙片含钙元素的质量为0.75g;
碳酸钙中钙元素的质量分数为:;
每片钙片中含有钙元素的质量为:
因为0.32g<0.75g,
所以说明此标签中的含钙量不合理;
【答案】丙;右;分压(限流);5.11×105
【解析】(1)使用测电笔时,人体必须接触尾部的金属体,否则它不能正常工作;
(2)正常情况下,测电笔接触火线发光,接触零线不发光;
(3)人体直接接触火线,由于电压太大,会造成触电事故。在测电笔中串联一个大电阻,可以起到分压限流的作用,保证人体不会触电;
(4)首先根据U=U总-U人计算出测电笔两端的电压,然后根据计算电阻即可。
【解答】(1)如图甲所示是测电笔的结构,图乙和图丙中,正确使用试电笔的是图丙;
(2)当用它插入插座的左孔时氖管不亮,插入右孔时氖管发光,则说明火线在插座的右孔。
(3)测电笔内部有一个大电阻,它的作用是分压限流;
(4)测电笔两端的电压:U=U总-U人=220V-36V=184V;
测电笔的电阻为:。
(1)3
(2)2
(3)9.1
(1)在化学式中,一种符号代表一种元素;
(2)相对分子质量等于相对原子质量与个数的乘积之和;
(3)元素的质量之比等于相对原子质量与个数的乘积之比。
【解答】(1)根据化学式 C6H8Nx 可知,对苯二胺由C、H、N共3种元素组成;
(2)根据化学式 C6H8Nx 可知,对苯二胺的相对分子质量:
12×6+1×8+14x=108,解得:x=2;
(3)根据化学式 C6H8Nx 可知,对苯二胺中碳元素和氢元素最简质量比:
(12×6):(1×8)=9:1。
(1)茎;物理;40%
(2)72:5:40;压强
(3)B
元素质量比=元素的相对原子质量*原子个数的比;物体所受的压力与受力面积之比叫做压强,压强用来比较压力产生的效果,压强越大,压力的作用效果越明显。压强的计算公式是:p=F/S,压强的单位是帕斯卡,符号是Pa。
【解答】(1)加工木材主要取用的是木材的木质部,而木质部是茎的一部分;对木材进行压缩后没有新物质的产生,所以该过程是物理变化;压缩前木材的质量为: ;而压缩后厚度减少到20%。底面积不变,则体积减小到压缩前的20%; ;故答案为:茎;物理变化;40%;(2)m(C):m(H):m(O)=12×12×n:10×1×n:16×5×n=72:5:40;由公式可知,材料宽度×材料厚度=材料的底面积;而力与面积之比是压强;故答案为:72:5:40;压强;(3)A、在制作过程中使用了多种化学试剂,会造成污染;故A错误;
B、制作之后的材料硬度超过部分金属材料的硬度,所以可以替代部分金属;故B正确;
C、树木对于地球的生态系统作用巨大,不可或缺,因此不能无限制砍伐;故C错误;故答案为:B;
故答案为:茎;物理变化;40%;(2)72:5:40;压强;(3)B。
尿素中氮元素的质量分数为 , (吨)
根据元素的质量分数的计算方法来分析。根据物质的质量和元素的质量分数可以计算出元素的质量。
【解答】
尿素中氮元素的质量分数为: 2N/(CO(NH2)2) =28 /60 × 100 % ≈ 46.7 % ,
多少吨尿素(CO(NH2)2)含0.1吨氮元素: 0.1 ÷ 46.7 % =0.214吨
3.4 亿吨粮食需要化肥:0.214吨X3.4X 10 8=7.28 × 10 7 (吨)
(1)474
(2)m(K)∶m(Al)∶m(S)∶m(O)∶m(H)=39∶27∶64∶320∶24
(3)8.2%
(4)解:设与258g明矾中氧元素质量相等的水的质量为x。x×(1618×100%)=258g×(16×20474×100%)x=195.9g答:258g明矾与195.9g水所含氧元素的质量相等。
(1)相对分子质量等于相对原子质量和个数的乘积之和;
(2)元素的质量之比等于相对原子质量和个数的乘积之比;
(3)元素的质量分数=;
(4)元素质量=物质质量×元素的质量分数,据此根据氧元素质量相等列出方程计算即可。
【解答】(1)明矾的相对分子质量是:39+27+(32+16×4)×2+(1×2+16)×12=474。
(2)明矾中各元素的质量比是:
m(K)∶m(Al)∶m(S)∶m(O)∶m(H)=(39×1):(27×1):(32×2):(16×20):(1×24)=39∶27∶64∶320∶24。
(3)明矾中钾元素的质量分数是:。
(4)设与258g明矾中氧元素质量相等的水的质量为x,
;
解得:x=195.9g。
右上 1.52
【详解】
(1)氧原子中含有8个质子,是8号元素,是第二周期,第六主族元素,位于元素周期右上方;
(2)由实验结论可知,产生的氧气均来自水,所以实验三中氧气中含有的 18O 百分比与水中的 18O 百分比相同; 三份溶液的碳酸氢盐和水都含有不同的18O百分比,所以碳酸氢盐的18O与实验1、2都不相同;
(3) 氧气在标准状况下的密度为1.43千克/米3 ,所以,含有18O 的氧气密度为: 1.43kg/m3≈1.61kg/m3,设一瓶氧气的的体积为V,由于这瓶氧气只 含18O和16O,且个数比为1:1,所以其密度为1.52千克/米3。
解:铁元素质量=456毫克× ×100%=168毫克
根据元素质量分数=相对原子质量×原子个数/相对分子质量分析;根据元素质量=化合物质量×元素质量分数分析。
【解答】 成人一天一片,一片中所含硫酸亚铁质量为456毫克,所以每天能从药物中补充铁元素质量=456毫克× ×100%=168毫克 ;
故答案为: 铁元素质量=456毫克× ×100%=168毫克 。
第 13 页(共 13 页)
同课章节目录
