辽宁省鞍山市部分普通高中2022-2023学年高二下学期第二次月考化学(B卷)试题(含答案)
文档属性
| 名称 | 辽宁省鞍山市部分普通高中2022-2023学年高二下学期第二次月考化学(B卷)试题(含答案) |
|
|
| 格式 | doc | ||
| 文件大小 | 368.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-13 00:00:00 | ||
图片预览


文档简介
鞍山市部分普通高中2022-2023学年度下学期第二次月考试卷
高二化学(B)
时间:75分钟 满分:100分
考试范围:选必二第三章,选必三第一章,第二章1-2节
可能用到的相对的原子质量:
一、单项选择题:每题3分,共45分
1、下列说法正确的是( )
A.冰的晶体中每个水分子可与周围两个水分子形成氢键
B.手性碳原子不一定是饱和碳原子
C.区分晶体与非晶体最科学的方法是X-射线衍射法
D.晶体中有阳离子就一定有阴离子
2、下列有关化学用语的表示中正确的是( )
A.甲烷的球棍模型: B.的名称:2-甲基-2-丙烯
C.乙酸的实验式: D.羟基的电子式:
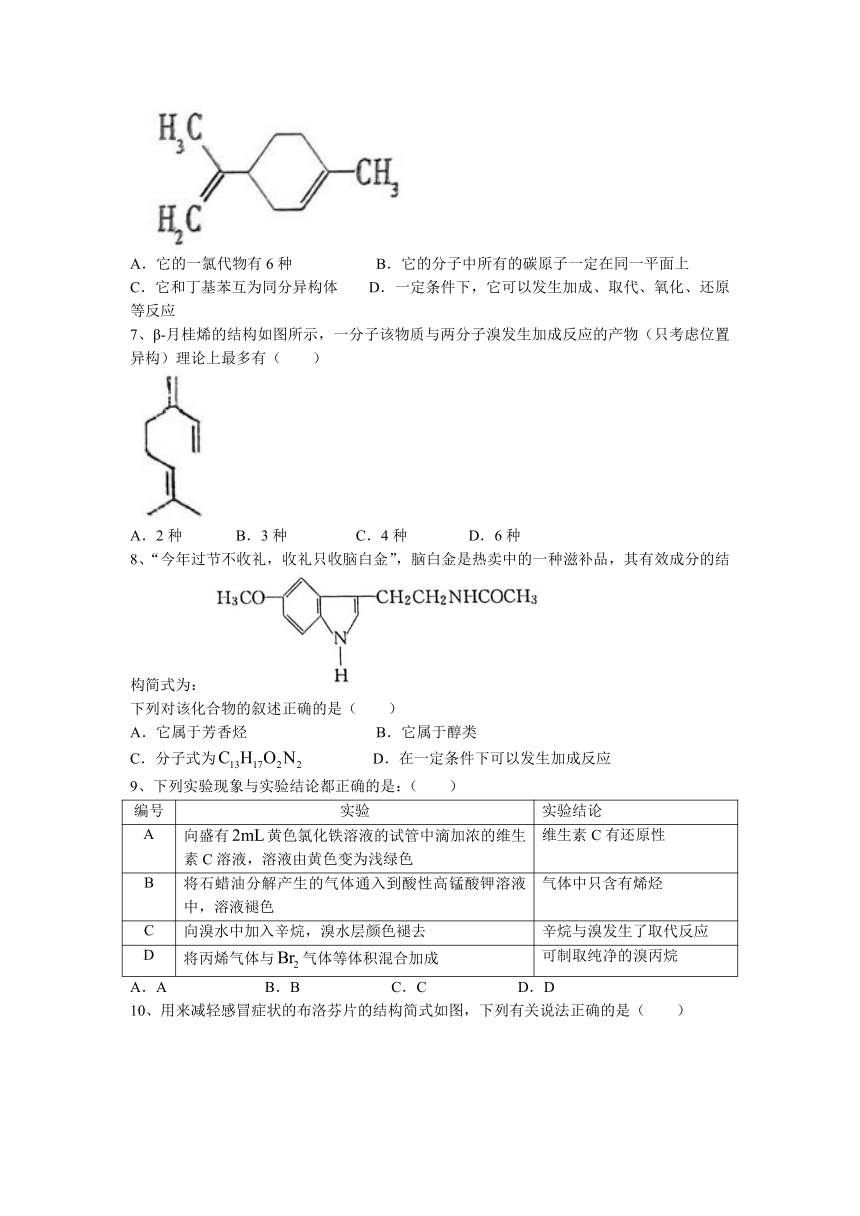
3、维生素C具备抗氧化,抗自由基等作用,广泛存在于西红柿、柚子、猕猴桃等新鲜蔬菜水果中。其结构简式如图所示,下列关于维生素C的说法正确的是( )
A.维生素C分子中含有醚键 B.维生素C的分子式为
C.维生素C结构中包含了一个五元碳环 D.维生素C最多能与发生反应
4、分子式为的同分异构体共有(不考虑立体异构)( )
A.10种 B.9种 C.8种 D.7种
5、由乙烯推测丙烯()的结构或性质正确的是( )
A.分子中3个碳原子在同一直线上 B.分子中所有原子在同一平面上
C.能发生加聚反应 D.与氯化氢加成只生成一种产物
6、柠檬烯是一种食用香料,其结构简式如图所示。有关柠檬烯的分析正确的是( )
A.它的一氯代物有6种 B.它的分子中所有的碳原子一定在同一平面上
C.它和丁基苯互为同分异构体 D.一定条件下,它可以发生加成、取代、氧化、还原等反应
7、β-月桂烯的结构如图所示,一分子该物质与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有( )
A.2种 B.3种 C.4种 D.6种
8、“今年过节不收礼,收礼只收脑白金”,脑白金是热卖中的一种滋补品,其有效成分的结构简式为:
下列对该化合物的叙述正确的是( )
A.它属于芳香烃 B.它属于醇类
C.分子式为 D.在一定条件下可以发生加成反应
9、下列实验现象与实验结论都正确的是:( )
编号 实验 实验结论
A 向盛有黄色氯化铁溶液的试管中滴加浓的维生素C溶液,溶液由黄色变为浅绿色 维生素C有还原性
B 将石蜡油分解产生的气体通入到酸性高锰酸钾溶液中,溶液褪色 气体中只含有烯烃
C 向溴水中加入辛烷,溴水层颜色褪去 辛烷与溴发生了取代反应
D 将丙烯气体与气体等体积混合加成 可制取纯净的溴丙烷
A.A B.B C.C D.D
10、用来减轻感冒症状的布洛芬片的结构简式如图,下列有关说法正确的是( )
A.布洛芬与苯甲酸乙酯互为同系物 B.布洛芬的分子式为
C.布洛芬能与发生反应 D.布洛芬苯环上的一溴代物有4种(不含立体结构)
11、下面有关晶体的叙述中,不正确的是( )
A.金刚石为空间网状结构,由共价键形成的碳原子环上,最小的环上有6个碳原子
B.氯化钠晶体中,每个周围距离相等的共有6个
C.氯化铯晶体中,每个周围紧邻8个
D.干冰晶体中,每个分子周围紧邻12个分子
12、根据下列性质判断所描述的位置可能属于分子晶体的是( )
A.熔点,易溶于水,水溶液能导电 B.熔点,沸点,硬度很大
C.熔点,液态不导电,水溶液能导电 D.熔点,质软,导电,密度
13、离子晶体熔点的高低决定于晶体中阳离子与阴离子之间的静电引力,静电引力大则熔点高,引力小则反之试根据你学到的电学知识,判断、、、四种晶体熔点的高低顺序( )
A. B.
C. D.
14、某物质的实验式为,其水溶液不导电,加入溶液反应也不产生沉淀,以强碱处理并没有放出,则关于此化合物的说法中正确的是( )
A.配合物中中心原子的电荷数和配位数均为6 B.中心原子杂化类型为杂化
C.1摩尔该分子中含有键数目为12 D.和分子均与配位
15、元素X的价离子中所有电子正好充满K、L、M三个电子层,它与形成的晶体结构如图所示。下列说法错误的是( )
A.X元素的原子序数是19 B.该晶体中阳离子与阴离子个数比为
C.离子是图中的黑球 D.的半径大于
二、非选择题:共4题,共55分
16、【14分】(1)有下列几组物质,请将序号填入下列空格内:
A、和油酸() B、和石墨
C、和 D、和 E、乙醇和乙二醇
①互为同位素的是____________; ②互为同系物的是____________;
③互为同素异形体的是____________; ④互为同分异构体的是____________;
⑤既不是同系物,又不是同分异构体,也不是同素异形体,但可看成是同一类物质的是______。
(2)分子式为的同分异构体共有多种,其中含有三个甲基的结构有______种;含有手性碳的结构有______种。
17、【12分】测定有机化合物中碳和氢组成常用燃烧分析法,如图是德国化学家李比希测定烃类有机物组成的装置,氧化铜作催化剂,在左右使有机物在氧气流中全部氧化为和,用含有固体氢氧化钠和高氯酸镁的吸收管分别吸收和。试回答下列问题:
(1)甲装置中盛放的是______(填名称),甲、乙中的吸收剂不能颠倒,理由:______。
(2)实验开始时,要先通入氧气一会儿,然后再加热。为什么?____________。
(3)若测得甲装置增重,乙装置增重,试求出烃中碳、氢的原子个数比为______。
(4)若已知试样是纯净物______,某次测定时,测出碳、氢原子个数比为,能否确定其为何种烃?______(填“能”或“不能”);若能,写出其分子式______(若不能,此空不必回答)
18、【14分】(1)A、B、C、D、E为五种气态烃,其中A、B、C都能使酸性退色,与完全加成,生成物分子中每个碳原子都有一个溴原子,A与C通式相同,A与加成可得到B,B与密度相同,D是最简单的有机物,E为D的同系物,完全燃烧等摩尔B、E,生成相同,试确定A、B、C、D、E的结构简式。
A:_______;B:_______;C:_______;D:_______;E:_______。
(2)某烃X。步骤一:通过仪器分析得知X的相对分子质量为106;
步骤二:用核磁共振仪测出X的核磁共振谱有2个峰,其面积之比为(如图I)
步骤三:利用红外光谱仪测得X分子的红外光谱如图Ⅱ,试回答:
①步骤一中的仪器为________。
②X的结构简式为________。
19、【15分】我国部分城市灰霾天占全年一半,引起灰霾的PM2.5微细粒子包含、,有机颗粒物及扬尘等。通过测定灰中锌等重金属的含量,可知目前造成我国灰霾天气主要是交通污染。
(1)在基态时核外电子排布式为______
(2)的空间构型是________(用文字描述)。
(3)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有、,,,等二次污染物。
①下列说法正确的是________(不定项选择)。
a.结构式可表示为
b.分子呈直线形
c.分子中碳原子均采用杂化
d.相同压强下,沸点比高,说明前者是极性分子,后者是非极性分子
②中含键数目为_____。
③能被溶液吸收生成配合物,该配合物中心离子的配位数为_____ (填数字)。
(4)下列分子或离子中,能提供孤对电子与某些金属离子形成配位键的是__________。
① ② ③ ④
(5)测定大气中PM2.5的浓度方法之一是β—射线吸收法,β—射线放射源可用,已知晶体的晶胞结构如图所示,设晶体中与每个原子相紧邻的原子有m个,晶胞中含原子为n个,则_____(填数字)。
高二化学B答案
一、单项选择题:每题3分,共45分
1、【答案】C 2、【答案】D 3、【答案】B
4、【答案】B 5、【答案】C 6、【答案】D
7、【答案】C 8、【答案】D 9、【答案】A
10、【答案】C 11、【答案】B 12、【答案】C
13、【答案】C 14、【答案】D 15、【答案】A
二、非选择题:每空2分,最后一空3分,共55分
16、【14分】① D ② A ③ B ④ C ⑤ E (2)3; 2
17、【12分】(1) 高氯酸镁 ;
因氢氧化钠同时能吸收CO2和H2O,无法确定生成的H2O和CO2的质量
(2)将装置中的空气排尽,否则空气中含有二氧化碳和水蒸气,影响测定结果的准确性
(3)9b∶44a
(4)能 ; C22H46
18、【14分】(1)A: CH≡CH;B: CH2═CH2;C: CH2= CHCH =CH2;D: CH4 ;E: CH3CH3
(2) 1.质谱仪
2.
19、【15分】(1)1s22s22p63s23p63d10或[Ar]3d10
(2)正四面体
(3)①ac ②7 ③6
(4)①②③④
(5)3 (3分)
高二化学(B)
时间:75分钟 满分:100分
考试范围:选必二第三章,选必三第一章,第二章1-2节
可能用到的相对的原子质量:
一、单项选择题:每题3分,共45分
1、下列说法正确的是( )
A.冰的晶体中每个水分子可与周围两个水分子形成氢键
B.手性碳原子不一定是饱和碳原子
C.区分晶体与非晶体最科学的方法是X-射线衍射法
D.晶体中有阳离子就一定有阴离子
2、下列有关化学用语的表示中正确的是( )
A.甲烷的球棍模型: B.的名称:2-甲基-2-丙烯
C.乙酸的实验式: D.羟基的电子式:
3、维生素C具备抗氧化,抗自由基等作用,广泛存在于西红柿、柚子、猕猴桃等新鲜蔬菜水果中。其结构简式如图所示,下列关于维生素C的说法正确的是( )
A.维生素C分子中含有醚键 B.维生素C的分子式为
C.维生素C结构中包含了一个五元碳环 D.维生素C最多能与发生反应
4、分子式为的同分异构体共有(不考虑立体异构)( )
A.10种 B.9种 C.8种 D.7种
5、由乙烯推测丙烯()的结构或性质正确的是( )
A.分子中3个碳原子在同一直线上 B.分子中所有原子在同一平面上
C.能发生加聚反应 D.与氯化氢加成只生成一种产物
6、柠檬烯是一种食用香料,其结构简式如图所示。有关柠檬烯的分析正确的是( )
A.它的一氯代物有6种 B.它的分子中所有的碳原子一定在同一平面上
C.它和丁基苯互为同分异构体 D.一定条件下,它可以发生加成、取代、氧化、还原等反应
7、β-月桂烯的结构如图所示,一分子该物质与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有( )
A.2种 B.3种 C.4种 D.6种
8、“今年过节不收礼,收礼只收脑白金”,脑白金是热卖中的一种滋补品,其有效成分的结构简式为:
下列对该化合物的叙述正确的是( )
A.它属于芳香烃 B.它属于醇类
C.分子式为 D.在一定条件下可以发生加成反应
9、下列实验现象与实验结论都正确的是:( )
编号 实验 实验结论
A 向盛有黄色氯化铁溶液的试管中滴加浓的维生素C溶液,溶液由黄色变为浅绿色 维生素C有还原性
B 将石蜡油分解产生的气体通入到酸性高锰酸钾溶液中,溶液褪色 气体中只含有烯烃
C 向溴水中加入辛烷,溴水层颜色褪去 辛烷与溴发生了取代反应
D 将丙烯气体与气体等体积混合加成 可制取纯净的溴丙烷
A.A B.B C.C D.D
10、用来减轻感冒症状的布洛芬片的结构简式如图,下列有关说法正确的是( )
A.布洛芬与苯甲酸乙酯互为同系物 B.布洛芬的分子式为
C.布洛芬能与发生反应 D.布洛芬苯环上的一溴代物有4种(不含立体结构)
11、下面有关晶体的叙述中,不正确的是( )
A.金刚石为空间网状结构,由共价键形成的碳原子环上,最小的环上有6个碳原子
B.氯化钠晶体中,每个周围距离相等的共有6个
C.氯化铯晶体中,每个周围紧邻8个
D.干冰晶体中,每个分子周围紧邻12个分子
12、根据下列性质判断所描述的位置可能属于分子晶体的是( )
A.熔点,易溶于水,水溶液能导电 B.熔点,沸点,硬度很大
C.熔点,液态不导电,水溶液能导电 D.熔点,质软,导电,密度
13、离子晶体熔点的高低决定于晶体中阳离子与阴离子之间的静电引力,静电引力大则熔点高,引力小则反之试根据你学到的电学知识,判断、、、四种晶体熔点的高低顺序( )
A. B.
C. D.
14、某物质的实验式为,其水溶液不导电,加入溶液反应也不产生沉淀,以强碱处理并没有放出,则关于此化合物的说法中正确的是( )
A.配合物中中心原子的电荷数和配位数均为6 B.中心原子杂化类型为杂化
C.1摩尔该分子中含有键数目为12 D.和分子均与配位
15、元素X的价离子中所有电子正好充满K、L、M三个电子层,它与形成的晶体结构如图所示。下列说法错误的是( )
A.X元素的原子序数是19 B.该晶体中阳离子与阴离子个数比为
C.离子是图中的黑球 D.的半径大于
二、非选择题:共4题,共55分
16、【14分】(1)有下列几组物质,请将序号填入下列空格内:
A、和油酸() B、和石墨
C、和 D、和 E、乙醇和乙二醇
①互为同位素的是____________; ②互为同系物的是____________;
③互为同素异形体的是____________; ④互为同分异构体的是____________;
⑤既不是同系物,又不是同分异构体,也不是同素异形体,但可看成是同一类物质的是______。
(2)分子式为的同分异构体共有多种,其中含有三个甲基的结构有______种;含有手性碳的结构有______种。
17、【12分】测定有机化合物中碳和氢组成常用燃烧分析法,如图是德国化学家李比希测定烃类有机物组成的装置,氧化铜作催化剂,在左右使有机物在氧气流中全部氧化为和,用含有固体氢氧化钠和高氯酸镁的吸收管分别吸收和。试回答下列问题:
(1)甲装置中盛放的是______(填名称),甲、乙中的吸收剂不能颠倒,理由:______。
(2)实验开始时,要先通入氧气一会儿,然后再加热。为什么?____________。
(3)若测得甲装置增重,乙装置增重,试求出烃中碳、氢的原子个数比为______。
(4)若已知试样是纯净物______,某次测定时,测出碳、氢原子个数比为,能否确定其为何种烃?______(填“能”或“不能”);若能,写出其分子式______(若不能,此空不必回答)
18、【14分】(1)A、B、C、D、E为五种气态烃,其中A、B、C都能使酸性退色,与完全加成,生成物分子中每个碳原子都有一个溴原子,A与C通式相同,A与加成可得到B,B与密度相同,D是最简单的有机物,E为D的同系物,完全燃烧等摩尔B、E,生成相同,试确定A、B、C、D、E的结构简式。
A:_______;B:_______;C:_______;D:_______;E:_______。
(2)某烃X。步骤一:通过仪器分析得知X的相对分子质量为106;
步骤二:用核磁共振仪测出X的核磁共振谱有2个峰,其面积之比为(如图I)
步骤三:利用红外光谱仪测得X分子的红外光谱如图Ⅱ,试回答:
①步骤一中的仪器为________。
②X的结构简式为________。
19、【15分】我国部分城市灰霾天占全年一半,引起灰霾的PM2.5微细粒子包含、,有机颗粒物及扬尘等。通过测定灰中锌等重金属的含量,可知目前造成我国灰霾天气主要是交通污染。
(1)在基态时核外电子排布式为______
(2)的空间构型是________(用文字描述)。
(3)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有、,,,等二次污染物。
①下列说法正确的是________(不定项选择)。
a.结构式可表示为
b.分子呈直线形
c.分子中碳原子均采用杂化
d.相同压强下,沸点比高,说明前者是极性分子,后者是非极性分子
②中含键数目为_____。
③能被溶液吸收生成配合物,该配合物中心离子的配位数为_____ (填数字)。
(4)下列分子或离子中,能提供孤对电子与某些金属离子形成配位键的是__________。
① ② ③ ④
(5)测定大气中PM2.5的浓度方法之一是β—射线吸收法,β—射线放射源可用,已知晶体的晶胞结构如图所示,设晶体中与每个原子相紧邻的原子有m个,晶胞中含原子为n个,则_____(填数字)。
高二化学B答案
一、单项选择题:每题3分,共45分
1、【答案】C 2、【答案】D 3、【答案】B
4、【答案】B 5、【答案】C 6、【答案】D
7、【答案】C 8、【答案】D 9、【答案】A
10、【答案】C 11、【答案】B 12、【答案】C
13、【答案】C 14、【答案】D 15、【答案】A
二、非选择题:每空2分,最后一空3分,共55分
16、【14分】① D ② A ③ B ④ C ⑤ E (2)3; 2
17、【12分】(1) 高氯酸镁 ;
因氢氧化钠同时能吸收CO2和H2O,无法确定生成的H2O和CO2的质量
(2)将装置中的空气排尽,否则空气中含有二氧化碳和水蒸气,影响测定结果的准确性
(3)9b∶44a
(4)能 ; C22H46
18、【14分】(1)A: CH≡CH;B: CH2═CH2;C: CH2= CHCH =CH2;D: CH4 ;E: CH3CH3
(2) 1.质谱仪
2.
19、【15分】(1)1s22s22p63s23p63d10或[Ar]3d10
(2)正四面体
(3)①ac ②7 ③6
(4)①②③④
(5)3 (3分)
同课章节目录
