4.1第2课时酚的性质和应用(含课件)(教学课件)(共22张PPT)——2022-2023学年高二化学苏教版(2019)选择性必修3
文档属性
| 名称 | 4.1第2课时酚的性质和应用(含课件)(教学课件)(共22张PPT)——2022-2023学年高二化学苏教版(2019)选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 40.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-14 00:00:00 | ||
图片预览







文档简介
(共22张PPT)
第2课时 酚的性质和应用
专题四 生活中常用的有机物
--烃的含氧衍生物
第一单元醇和酚
教学目标
1,了解酚的典型代表物的组成和结构特点
2,掌握本分的化学性质及其检验方法
3,了解醇和酚的结构差别及其对化学性质的影响
情境激趣
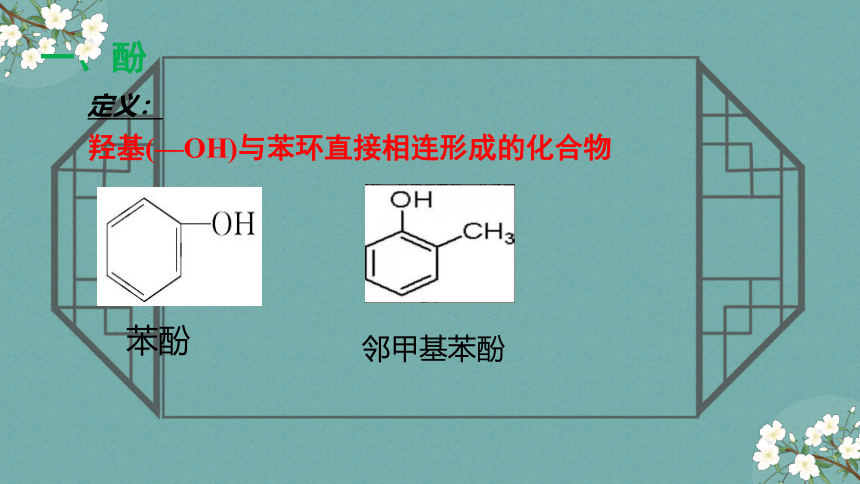
一、酚
羟基(—OH)与苯环直接相连形成的化合物
定义:
苯酚
邻甲基苯酚
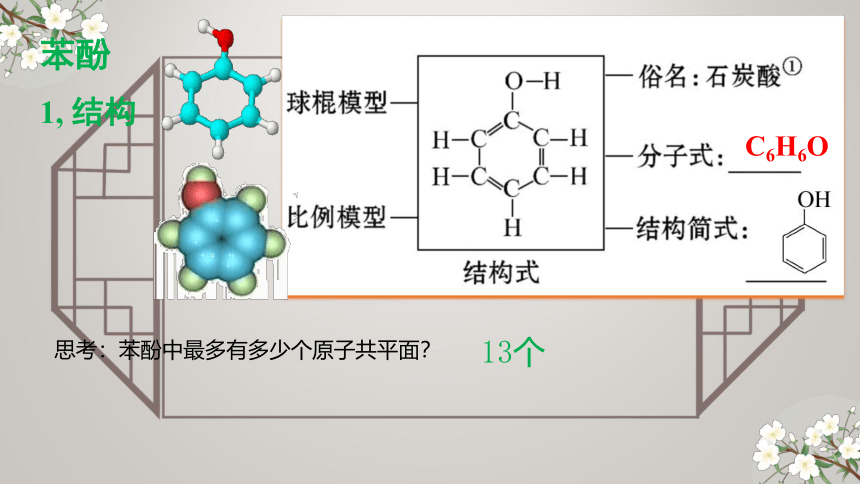
1, 结构
C6H6O
苯酚
思考:苯酚中最多有多少个原子共平面?
13个
二、苯酚物理性质
颜色:
无色,在空气中被氧化显粉红色。
气味:
有特殊气味
状态:
常温下,无色晶体,熔点(43℃)
毒性:
有毒,腐蚀性,皮肤沾到苯酚,立即用酒精清洗。
溶解性:
室温下微溶于水,温度高于65oC与以任意比例水互溶,易溶于有机溶剂
苯酚的溶解性实验
思考:苯酚的水溶液呈浑浊,能用过滤的方法分离吗
不能。苯酚从水溶液中析出形成的是乳浊液,而非悬浊液,应用分液的方法分离。
1.应具备两种基团的性质。
结 构
性 质
苯基 羟基
2.两种基团是否相互影响。
三.苯酚的化学性质
决定
一,弱酸性
思考:如何检测苯酚显酸性呢?
①酸碱指示剂
②与碱反应
注意:苯酚酸性较弱,不能使酸碱指示剂变色
②与碱反应
实
验
步
骤:
实验现象:
①加入蒸馏水后,溶液变浑浊。说明室温下苯酚在水中溶解度小
②加入氢氧化钠溶液,溶液变澄清。
③加入盐酸和二氧化碳后,溶液均变浑浊。
酸性:C6H5OH<HCl
苯酚钠(易溶于水)
酸性:H2CO3>C6H5OH
实验现象:
(2)取代反应
实
验
操
作
试管中立即产生白色沉淀
应用:用于苯酚的定性检验和定量测定
注意:此反应中应选择稀苯酚溶液,饱和溴水且Br2水必须过量,若苯酚过量,生成三溴苯酚会溶于苯酚中,无法观察实验现象。
反应方程式:
苯酚 苯
反应物
反应条件
被取代氢原子数
反应速率
结论 小结:羟基对苯环的影响——更易被取代
溴水、苯酚
液溴、苯
不用催化剂
FeBr3催化剂
3个
1个
快
慢
酚羟基对苯环的影响,使苯环上氢原子变得活泼,苯酚与溴取代反应比苯容易。
苯酚遇FeCl3溶液呈___色
紫
(3)显色反应
应用:
用于检验酚类物质的存在。
粉红
C6H6O+7O2 6CO2+3H2O
点燃
(4)氧化反应
酚羟基易被氧化
思考:如何除去苯中混有的苯酚 能否采用先加足量的溴水再过滤的方法?
不能。虽然苯酚和溴水反应生成的三溴苯酚不溶于水,但是三溴苯酚易溶于苯而不容易分离。应加入适量的NaOH溶液后分液,取上层清液即得苯。
含苯酚的工业废水中回收苯酚:
2.苯酚的分离提纯:
1,下列物质与Naoh溶液反应的是( )
(1)乙醇(2)乙酸(3)苯酚(4)小苏打(5)甲苯
A (1)(5) B(1)(2)(3) C(2)(3)(4) D(4)(5)
C
2.苯酚( )在一定条件下能与H2加成得到环己醇( ),下列关于这两种物质的叙述中错误的是 ( )
A.常温下都能溶于水,但溶解性都比乙醇差
B.都能与金属钠反应放出氢气
C.都显弱酸性,且酸性都弱于碳酸
D.苯酚与FeCl3溶液作用显紫色,环己醇加入FeCl3溶液中无明显现象
【解析】苯酚显弱酸性,环己醇不显酸性
C
2.下列说法正确的是 ( )
A.苯甲醇和苯酚都能与浓溴水反应产生白色沉淀
B.苯甲醇、苯酚在分子组成上相差一个CH2原子团,故两者互为同系物
C. 、 、 互为同分异构体
D.乙醇、苯甲醇、苯酚都既能与钠反应,又能与NaOH溶液反应
C
第2课时 酚的性质和应用
专题四 生活中常用的有机物
--烃的含氧衍生物
第一单元醇和酚
教学目标
1,了解酚的典型代表物的组成和结构特点
2,掌握本分的化学性质及其检验方法
3,了解醇和酚的结构差别及其对化学性质的影响
情境激趣
一、酚
羟基(—OH)与苯环直接相连形成的化合物
定义:
苯酚
邻甲基苯酚
1, 结构
C6H6O
苯酚
思考:苯酚中最多有多少个原子共平面?
13个
二、苯酚物理性质
颜色:
无色,在空气中被氧化显粉红色。
气味:
有特殊气味
状态:
常温下,无色晶体,熔点(43℃)
毒性:
有毒,腐蚀性,皮肤沾到苯酚,立即用酒精清洗。
溶解性:
室温下微溶于水,温度高于65oC与以任意比例水互溶,易溶于有机溶剂
苯酚的溶解性实验
思考:苯酚的水溶液呈浑浊,能用过滤的方法分离吗
不能。苯酚从水溶液中析出形成的是乳浊液,而非悬浊液,应用分液的方法分离。
1.应具备两种基团的性质。
结 构
性 质
苯基 羟基
2.两种基团是否相互影响。
三.苯酚的化学性质
决定
一,弱酸性
思考:如何检测苯酚显酸性呢?
①酸碱指示剂
②与碱反应
注意:苯酚酸性较弱,不能使酸碱指示剂变色
②与碱反应
实
验
步
骤:
实验现象:
①加入蒸馏水后,溶液变浑浊。说明室温下苯酚在水中溶解度小
②加入氢氧化钠溶液,溶液变澄清。
③加入盐酸和二氧化碳后,溶液均变浑浊。
酸性:C6H5OH<HCl
苯酚钠(易溶于水)
酸性:H2CO3>C6H5OH
实验现象:
(2)取代反应
实
验
操
作
试管中立即产生白色沉淀
应用:用于苯酚的定性检验和定量测定
注意:此反应中应选择稀苯酚溶液,饱和溴水且Br2水必须过量,若苯酚过量,生成三溴苯酚会溶于苯酚中,无法观察实验现象。
反应方程式:
苯酚 苯
反应物
反应条件
被取代氢原子数
反应速率
结论 小结:羟基对苯环的影响——更易被取代
溴水、苯酚
液溴、苯
不用催化剂
FeBr3催化剂
3个
1个
快
慢
酚羟基对苯环的影响,使苯环上氢原子变得活泼,苯酚与溴取代反应比苯容易。
苯酚遇FeCl3溶液呈___色
紫
(3)显色反应
应用:
用于检验酚类物质的存在。
粉红
C6H6O+7O2 6CO2+3H2O
点燃
(4)氧化反应
酚羟基易被氧化
思考:如何除去苯中混有的苯酚 能否采用先加足量的溴水再过滤的方法?
不能。虽然苯酚和溴水反应生成的三溴苯酚不溶于水,但是三溴苯酚易溶于苯而不容易分离。应加入适量的NaOH溶液后分液,取上层清液即得苯。
含苯酚的工业废水中回收苯酚:
2.苯酚的分离提纯:
1,下列物质与Naoh溶液反应的是( )
(1)乙醇(2)乙酸(3)苯酚(4)小苏打(5)甲苯
A (1)(5) B(1)(2)(3) C(2)(3)(4) D(4)(5)
C
2.苯酚( )在一定条件下能与H2加成得到环己醇( ),下列关于这两种物质的叙述中错误的是 ( )
A.常温下都能溶于水,但溶解性都比乙醇差
B.都能与金属钠反应放出氢气
C.都显弱酸性,且酸性都弱于碳酸
D.苯酚与FeCl3溶液作用显紫色,环己醇加入FeCl3溶液中无明显现象
【解析】苯酚显弱酸性,环己醇不显酸性
C
2.下列说法正确的是 ( )
A.苯甲醇和苯酚都能与浓溴水反应产生白色沉淀
B.苯甲醇、苯酚在分子组成上相差一个CH2原子团,故两者互为同系物
C. 、 、 互为同分异构体
D.乙醇、苯甲醇、苯酚都既能与钠反应,又能与NaOH溶液反应
C
