4.2.1醛的性质和应用(含视频)(教学课件)(共23张PPT)—— 2022-2023学年高二化学苏教版(2019)选择性必修3
文档属性
| 名称 | 4.2.1醛的性质和应用(含视频)(教学课件)(共23张PPT)—— 2022-2023学年高二化学苏教版(2019)选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 168.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-14 00:00:00 | ||
图片预览



文档简介
(共23张PPT)
专题4 烃的含氧衍生物
第二单元 醛 羧酸
第一节 醛的性质和应用
1.认识醛典型代表物的组成和结构特点。
2.知道醛的化学性质及其用途。
你知道吗?
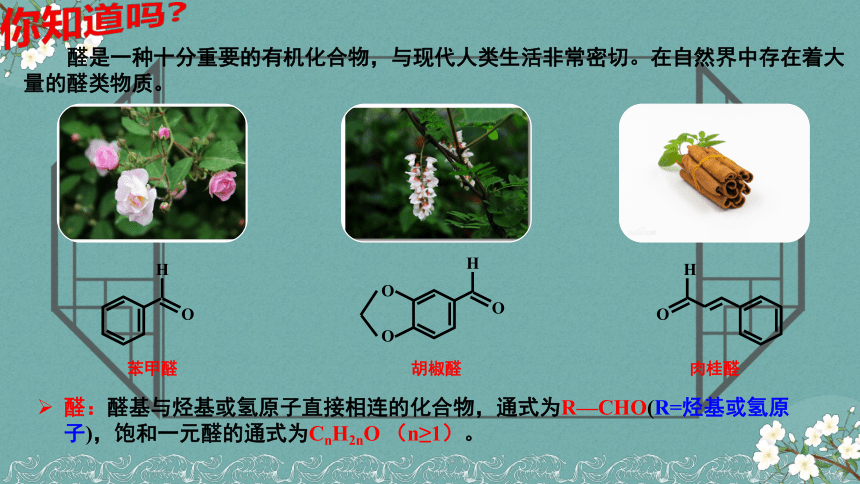
醛是一种十分重要的有机化合物,与现代人类生活非常密切。在自然界中存在着大量的醛类物质。
苯甲醛
胡椒醛
肉桂醛
H
O
O
O
H
O
H
O
醛:醛基与烃基或氢原子直接相连的化合物,通式为R—CHO(R=烃基或氢原子),饱和一元醛的通式为CnH2nO (n≥1)。
① HCOOH
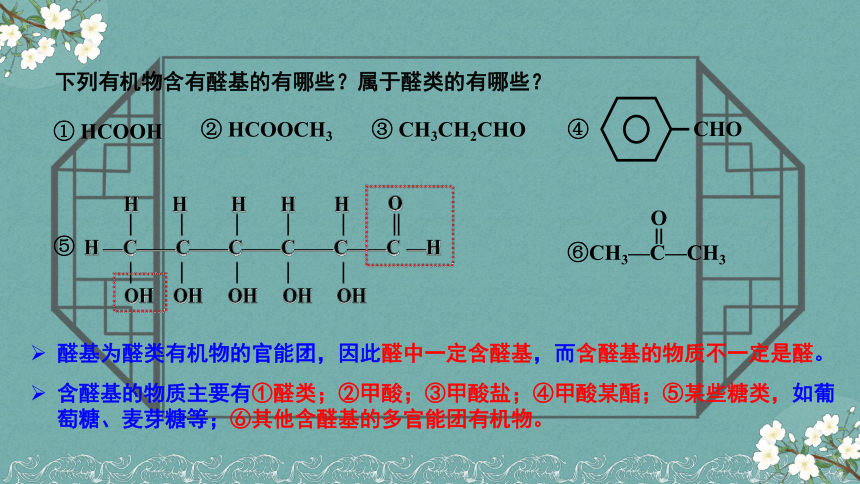
醛基为醛类有机物的官能团,因此醛中一定含醛基,而含醛基的物质不一定是醛。
含醛基的物质主要有①醛类;②甲酸;③甲酸盐;④甲酸某酯;⑤某些糖类,如葡萄糖、麦芽糖等;⑥其他含醛基的多官能团有机物。
下列有机物含有醛基的有哪些?属于醛类的有哪些?
CHO
④
③ CH3CH2CHO
② HCOOCH3
⑤
⑥CH3—C—CH3
O
=
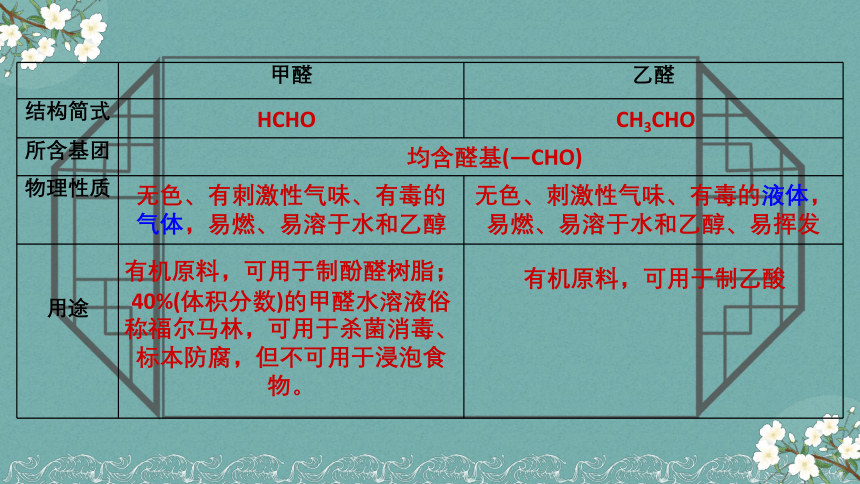
甲醛 乙醛
结构简式
所含基团
物理性质
用途
有机原料,可用于制酚醛树脂;40%(体积分数)的甲醛水溶液俗称福尔马林,可用于杀菌消毒、标本防腐,但不可用于浸泡食物。
无色、有刺激性气味、有毒的气体,易燃、易溶于水和乙醇
有机原料,可用于制乙酸
均含醛基(—CHO)
HCHO
CH3CHO
无色、刺激性气味、有毒的液体,易燃、易溶于水和乙醇、易挥发
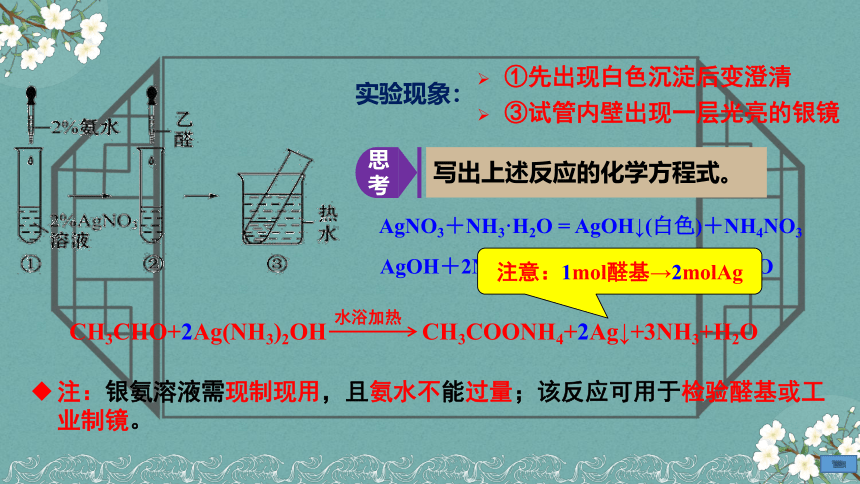
①先出现白色沉淀后变澄清
③试管内壁出现一层光亮的银镜
实验现象:
思考
写出上述反应的化学方程式。
CH3CHO+2Ag(NH3)2OH CH3COONH4+2Ag↓+3NH3+H2O
水浴加热
AgOH+2NH3·H2O = Ag(NH3)2OH+2H2O
AgNO3+NH3·H2O = AgOH↓(白色)+NH4NO3
注意:1mol醛基→2molAg
注:银氨溶液需现制现用,且氨水不能过量;该反应可用于检验醛基或工业制镜。
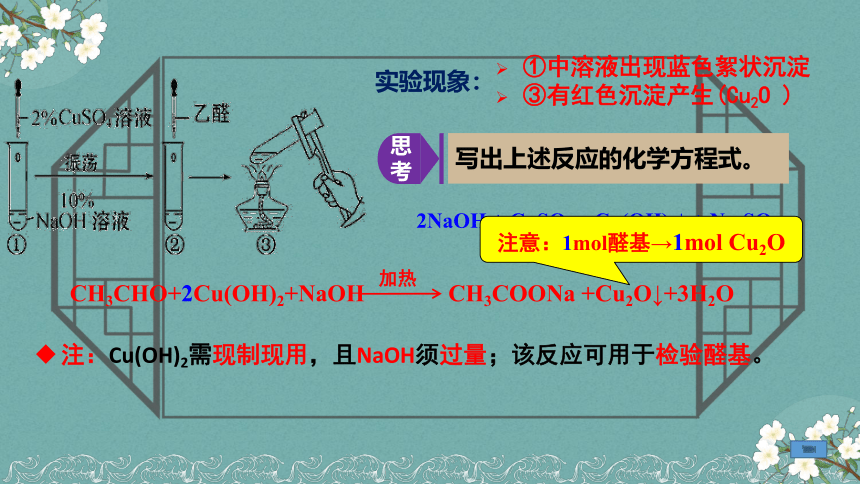
①中溶液出现蓝色絮状沉淀
③有红色沉淀产生(Cu2O )
实验现象:
思考
写出上述反应的化学方程式。
CH3CHO+2Cu(OH)2+NaOH CH3COONa +Cu2O↓+3H2O
加热
2NaOH + CuSO4 = Cu(OH)2↓ + Na2SO4
注意:1mol醛基→1mol Cu2O
注:Cu(OH)2需现制现用,且NaOH须过量;该反应可用于检验醛基。
1、请写出甲醛与银氨溶液、新制Cu(OH)2反应的化学方程式?
甲醛分子中可看作有2个—CHO
HCHO + 4Ag(NH3)2OH (NH4)2CO3 + 4Ag↓ + 6NH3 + 2H2O
水浴加热
HCHO + 4Cu(OH)2 CO2 + 2Cu2O↓ + 5H2O
加热
H—C—H
氧化
氧化
=
O
H—C—OH
HO—C—OH
=
O
=
O
2、实验结束后,如何处理试管内壁的银镜?
用硝酸浸泡,再用水清洗。3Ag + 4HNO3(稀) = 3AgNO3 + NO↑ + 2H2O
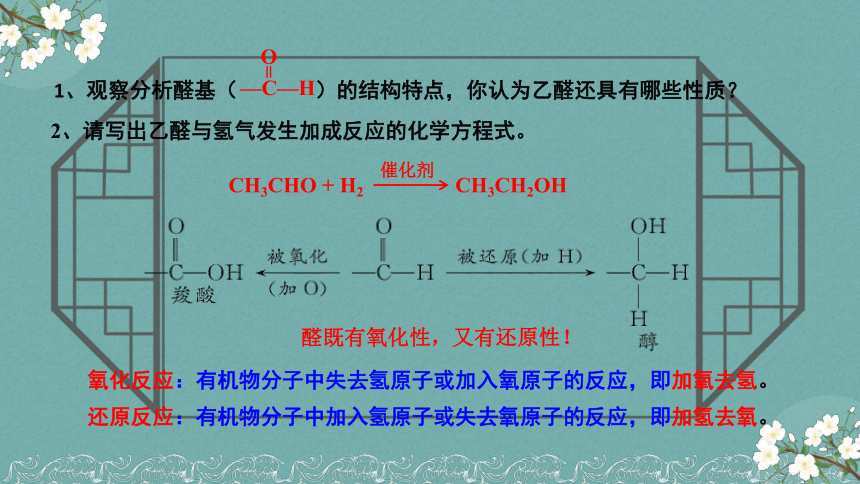
1、观察分析醛基( )的结构特点,你认为乙醛还具有哪些性质?
CH3CHO + H2
CH3CH2OH
催化剂
氧化反应:有机物分子中失去氢原子或加入氧原子的反应,即加氧去氢。
还原反应:有机物分子中加入氢原子或失去氧原子的反应,即加氢去氧。
醛既有氧化性,又有还原性!
2、请写出乙醛与氢气发生加成反应的化学方程式。
—C—H
=
O
双键变单键,异性相吸
+
δ
δ
-
写出乙醛分别与HCN加成的化学方程式!
+
δ
δ
-
在有机合成中可以用来增长碳链
【实验1】将乙醛逐滴滴入溴水中,微热,观察实验现象。
【实验2】将乙醛逐滴滴入酸性KMnO4溶液中,观察实验现象。
溴水的橙黄色褪去
酸性KMnO4溶液紫红色褪去
实验现象:
思考
酸性KMnO4溶液和溴水均褪色,为什么?
注意:乙醛不能使溴的四氯化碳溶液褪色
实 验
R—C—H + Br2 + H2O → 2HBr + R—COOH
=
O
均发生氧化反应,乙醛被氧化生成乙酸!
溶液变浑浊,生成白色固体;加入乙醇微热后,白色固体溶解。
苯酚
甲醛
浓盐酸
实验现象:
思考
写出上述反应的化学方程式。
缩聚反应:有机化合物间脱去小分子获得高分子化合物的反应。
线型高分子——酚醛树脂
酚醛树脂是人类合成的第一种高分子材料,至今还广泛使用,条件不同时(催化剂)可以生成线型或体型的酚醛树脂
线型酚醛树脂(盐酸作催化剂)
体型的酚醛树脂(氨水作催化剂)
甲醛和尿素反应生成脲醛树脂,脲醛树脂可制成热固性高分子黏合剂,用于胶合板、刨花板、人造维板等木材加工。
酚醛树脂
醛的化学性质
—CHO既有氧化性又有还原性
氧化反应
⑴与弱氧化剂
水浴加热
RCHO+2Ag(NH3)2OH
2Ag↓+RCOONH4+3NH3+H2O
RCHO + 2Cu(OH)2 + NaOH
RCOONa + Cu2O↓ + 3H2O
①与银氨溶液(又称“银镜反应”)
②与新制Cu(OH)2:
均须
碱性条件
下进行
点燃
还原反应(加成反应)
RCHO + H2
RCH2OH
Ni
加热、加压
⑵与强氧化剂
①能被酸性KMnO4、溴水氧化,并使其褪色。
2CH3CHO + O2
2CH3COOH
催化剂
4CH3CHO + 5O2
4CO2 + 4H2O
催化氧化:
燃烧:
②与氧气
可用于工业制醋酸
①浓盐酸作催化剂生成线型酚醛树脂
缩聚反应
②氨水作催化剂生成体型酚醛树脂
RCHO + HCN
RCHCN
OH
常见酮类物质
酮:羰基碳原子与两个烃基相连的化合物,通式为R—C—R’(R为烃基);饱和一元酮的通式为:CnH2nO(n≥3)
O
=
CH3—C—CH3
O
=
丙酮:最简单的酮,可用作有机溶剂,工业也可用于制备双酚A!
环己酮:重要化工原料
特点:酮类物质很难被氧化,但可催化加氢生成醇。
尝试写出分子式为C3H6O的有机物有哪些?分析这些同分异构体的类型。
饱和一元醛、饱和一元酮互为官能团异构!
1、辨析下列说法的正误:
(1)乙醛分子中的所有原子都在同一平面上。( )
(2)乙醛与新制Cu(OH)2悬浊液反应,表现酸性。( )
(3)凡是能发生银镜反应的物质一定是醛。( )
(4)醛类既能被氧化为羧酸,又能被还原为醇。( )
(5)丙醛的结构简式可以写为CH3CH2COH。( )
√
×
×
×
×
2、某学生做乙醛还原性的实验,取l mol/L的硫酸铜溶液2 mL和0.4mol/L的氢氧化钠溶液 4 mL,在一支试管里混合后加入0.5 mL 40%的乙醛溶液加热至沸腾,无红色沉淀,实验失败的原因是 ( )
A.氧氧化钠的量不够 B.硫酸铜不够量
C.乙醛溶液太少 D.加热时间不够
A
3、丙烯醛的结构简式为CH2=CH—CHO。下列关于它的性质叙述错误的是( )
A.能使溴水褪色,也能使高锰酸钾酸性溶液褪色
B.在一定条件下与H2充分反应,生成l一丙醇
C.能发生银镜反应表现出氧化性
D.一定条件下能被空气氧化
4、某种饱和一元醇和某种饱和一元醛的混合物共3 g,跟银氨溶液完全反应后,可还原出16.2 g银,下列说法中正确的是 ( )
A.混合物中一定含有甲醛
B.混合物中可能含有乙醛
C.混合物中醇与醛的质量比为1∶3
D.3 g混合物不可能还原出16.2 g银
C
A
4、香料茉莉酮是一种人工合成的有机化合物,其结构简式如图
下列关于茉莉酮的说法正确的是( )
A.该有机物的化学式为C11H16O
B.1 mol该有机物与H2充分反应,消耗H2 4 mol
C.该有机物能发生银镜反应
D.该有机物能发生加成反应,但不能发生氧化反应
5、橙花醛是一种香料,结构简式为:( CH3)2C==CHCH2C(CH3)==CHCHO 下列说法正确的是( )
A.橙花醛不可以与溴发生加成反应
B.橙花醛可以发生银镜反应
C.1mol橙花醛最多可以与2mol氢气发生加成反应
D.橙花醛是乙烯的同系物
A
B
专题4 烃的含氧衍生物
第二单元 醛 羧酸
第一节 醛的性质和应用
1.认识醛典型代表物的组成和结构特点。
2.知道醛的化学性质及其用途。
你知道吗?
醛是一种十分重要的有机化合物,与现代人类生活非常密切。在自然界中存在着大量的醛类物质。
苯甲醛
胡椒醛
肉桂醛
H
O
O
O
H
O
H
O
醛:醛基与烃基或氢原子直接相连的化合物,通式为R—CHO(R=烃基或氢原子),饱和一元醛的通式为CnH2nO (n≥1)。
① HCOOH
醛基为醛类有机物的官能团,因此醛中一定含醛基,而含醛基的物质不一定是醛。
含醛基的物质主要有①醛类;②甲酸;③甲酸盐;④甲酸某酯;⑤某些糖类,如葡萄糖、麦芽糖等;⑥其他含醛基的多官能团有机物。
下列有机物含有醛基的有哪些?属于醛类的有哪些?
CHO
④
③ CH3CH2CHO
② HCOOCH3
⑤
⑥CH3—C—CH3
O
=
甲醛 乙醛
结构简式
所含基团
物理性质
用途
有机原料,可用于制酚醛树脂;40%(体积分数)的甲醛水溶液俗称福尔马林,可用于杀菌消毒、标本防腐,但不可用于浸泡食物。
无色、有刺激性气味、有毒的气体,易燃、易溶于水和乙醇
有机原料,可用于制乙酸
均含醛基(—CHO)
HCHO
CH3CHO
无色、刺激性气味、有毒的液体,易燃、易溶于水和乙醇、易挥发
①先出现白色沉淀后变澄清
③试管内壁出现一层光亮的银镜
实验现象:
思考
写出上述反应的化学方程式。
CH3CHO+2Ag(NH3)2OH CH3COONH4+2Ag↓+3NH3+H2O
水浴加热
AgOH+2NH3·H2O = Ag(NH3)2OH+2H2O
AgNO3+NH3·H2O = AgOH↓(白色)+NH4NO3
注意:1mol醛基→2molAg
注:银氨溶液需现制现用,且氨水不能过量;该反应可用于检验醛基或工业制镜。
①中溶液出现蓝色絮状沉淀
③有红色沉淀产生(Cu2O )
实验现象:
思考
写出上述反应的化学方程式。
CH3CHO+2Cu(OH)2+NaOH CH3COONa +Cu2O↓+3H2O
加热
2NaOH + CuSO4 = Cu(OH)2↓ + Na2SO4
注意:1mol醛基→1mol Cu2O
注:Cu(OH)2需现制现用,且NaOH须过量;该反应可用于检验醛基。
1、请写出甲醛与银氨溶液、新制Cu(OH)2反应的化学方程式?
甲醛分子中可看作有2个—CHO
HCHO + 4Ag(NH3)2OH (NH4)2CO3 + 4Ag↓ + 6NH3 + 2H2O
水浴加热
HCHO + 4Cu(OH)2 CO2 + 2Cu2O↓ + 5H2O
加热
H—C—H
氧化
氧化
=
O
H—C—OH
HO—C—OH
=
O
=
O
2、实验结束后,如何处理试管内壁的银镜?
用硝酸浸泡,再用水清洗。3Ag + 4HNO3(稀) = 3AgNO3 + NO↑ + 2H2O
1、观察分析醛基( )的结构特点,你认为乙醛还具有哪些性质?
CH3CHO + H2
CH3CH2OH
催化剂
氧化反应:有机物分子中失去氢原子或加入氧原子的反应,即加氧去氢。
还原反应:有机物分子中加入氢原子或失去氧原子的反应,即加氢去氧。
醛既有氧化性,又有还原性!
2、请写出乙醛与氢气发生加成反应的化学方程式。
—C—H
=
O
双键变单键,异性相吸
+
δ
δ
-
写出乙醛分别与HCN加成的化学方程式!
+
δ
δ
-
在有机合成中可以用来增长碳链
【实验1】将乙醛逐滴滴入溴水中,微热,观察实验现象。
【实验2】将乙醛逐滴滴入酸性KMnO4溶液中,观察实验现象。
溴水的橙黄色褪去
酸性KMnO4溶液紫红色褪去
实验现象:
思考
酸性KMnO4溶液和溴水均褪色,为什么?
注意:乙醛不能使溴的四氯化碳溶液褪色
实 验
R—C—H + Br2 + H2O → 2HBr + R—COOH
=
O
均发生氧化反应,乙醛被氧化生成乙酸!
溶液变浑浊,生成白色固体;加入乙醇微热后,白色固体溶解。
苯酚
甲醛
浓盐酸
实验现象:
思考
写出上述反应的化学方程式。
缩聚反应:有机化合物间脱去小分子获得高分子化合物的反应。
线型高分子——酚醛树脂
酚醛树脂是人类合成的第一种高分子材料,至今还广泛使用,条件不同时(催化剂)可以生成线型或体型的酚醛树脂
线型酚醛树脂(盐酸作催化剂)
体型的酚醛树脂(氨水作催化剂)
甲醛和尿素反应生成脲醛树脂,脲醛树脂可制成热固性高分子黏合剂,用于胶合板、刨花板、人造维板等木材加工。
酚醛树脂
醛的化学性质
—CHO既有氧化性又有还原性
氧化反应
⑴与弱氧化剂
水浴加热
RCHO+2Ag(NH3)2OH
2Ag↓+RCOONH4+3NH3+H2O
RCHO + 2Cu(OH)2 + NaOH
RCOONa + Cu2O↓ + 3H2O
①与银氨溶液(又称“银镜反应”)
②与新制Cu(OH)2:
均须
碱性条件
下进行
点燃
还原反应(加成反应)
RCHO + H2
RCH2OH
Ni
加热、加压
⑵与强氧化剂
①能被酸性KMnO4、溴水氧化,并使其褪色。
2CH3CHO + O2
2CH3COOH
催化剂
4CH3CHO + 5O2
4CO2 + 4H2O
催化氧化:
燃烧:
②与氧气
可用于工业制醋酸
①浓盐酸作催化剂生成线型酚醛树脂
缩聚反应
②氨水作催化剂生成体型酚醛树脂
RCHO + HCN
RCHCN
OH
常见酮类物质
酮:羰基碳原子与两个烃基相连的化合物,通式为R—C—R’(R为烃基);饱和一元酮的通式为:CnH2nO(n≥3)
O
=
CH3—C—CH3
O
=
丙酮:最简单的酮,可用作有机溶剂,工业也可用于制备双酚A!
环己酮:重要化工原料
特点:酮类物质很难被氧化,但可催化加氢生成醇。
尝试写出分子式为C3H6O的有机物有哪些?分析这些同分异构体的类型。
饱和一元醛、饱和一元酮互为官能团异构!
1、辨析下列说法的正误:
(1)乙醛分子中的所有原子都在同一平面上。( )
(2)乙醛与新制Cu(OH)2悬浊液反应,表现酸性。( )
(3)凡是能发生银镜反应的物质一定是醛。( )
(4)醛类既能被氧化为羧酸,又能被还原为醇。( )
(5)丙醛的结构简式可以写为CH3CH2COH。( )
√
×
×
×
×
2、某学生做乙醛还原性的实验,取l mol/L的硫酸铜溶液2 mL和0.4mol/L的氢氧化钠溶液 4 mL,在一支试管里混合后加入0.5 mL 40%的乙醛溶液加热至沸腾,无红色沉淀,实验失败的原因是 ( )
A.氧氧化钠的量不够 B.硫酸铜不够量
C.乙醛溶液太少 D.加热时间不够
A
3、丙烯醛的结构简式为CH2=CH—CHO。下列关于它的性质叙述错误的是( )
A.能使溴水褪色,也能使高锰酸钾酸性溶液褪色
B.在一定条件下与H2充分反应,生成l一丙醇
C.能发生银镜反应表现出氧化性
D.一定条件下能被空气氧化
4、某种饱和一元醇和某种饱和一元醛的混合物共3 g,跟银氨溶液完全反应后,可还原出16.2 g银,下列说法中正确的是 ( )
A.混合物中一定含有甲醛
B.混合物中可能含有乙醛
C.混合物中醇与醛的质量比为1∶3
D.3 g混合物不可能还原出16.2 g银
C
A
4、香料茉莉酮是一种人工合成的有机化合物,其结构简式如图
下列关于茉莉酮的说法正确的是( )
A.该有机物的化学式为C11H16O
B.1 mol该有机物与H2充分反应,消耗H2 4 mol
C.该有机物能发生银镜反应
D.该有机物能发生加成反应,但不能发生氧化反应
5、橙花醛是一种香料,结构简式为:( CH3)2C==CHCH2C(CH3)==CHCHO 下列说法正确的是( )
A.橙花醛不可以与溴发生加成反应
B.橙花醛可以发生银镜反应
C.1mol橙花醛最多可以与2mol氢气发生加成反应
D.橙花醛是乙烯的同系物
A
B
