3.3 醛 酮(教案)-2022-2023学年高二化学人教版(2019)选择性必修3
文档属性
| 名称 | 3.3 醛 酮(教案)-2022-2023学年高二化学人教版(2019)选择性必修3 |

|
|
| 格式 | doc | ||
| 文件大小 | 757.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-15 00:00:00 | ||
图片预览

文档简介
人教版(2019) 选择性必修3 第三章 烃的衍生物
第三节 醛 酮
教学设计
教学目标
1.从官能团和化学键可能的断键部位预测乙醛的化学性质,并能在结构分析和实验事实的基础上书写相关反应的化学方程式,强化“结构决定性质”的观念。
2.能够结合分子结构特点,运用类比迁移的方法预测其他醛类物质的主要性质。
3.能根据官能团的特点和性质区别醛和酮,以丙酮为例认识酮的主要化学性质。
教学重难点
重点:乙醛的结构特点和主要化学性质
难点:乙醛的氧化反应及相关化学方程式的书写
教学过程
一、导入新课
现在的室内空气污染常见的有:大气颗粒、甲醛、苯等,这些空气中的污染物主要是来源于室内新房装修装饰材料具有污染物。
二、新课讲授
【学习任务】如何认识乙醛的化学性质。
【环节1】分析乙醛的结构特点
【学生活动】书写乙醛的结构简式,搭建其分子的结构模型。
【学生活动】分析讨论醛基的结构特点。
【师】乙醛分子式为C2H4O,结构式为,简写为CH3CHO,乙醛的核磁共振氢谱有2组峰,峰面积比为3:1。乙醛是无色、具有刺激性气味的液体,密度比水的小,沸点20.8 ℃,易挥发,易燃烧,能与水、乙醇等互溶。
【环节2】预测乙醛可能具有的化学性质
【学生活动】从C=O的结构特点和烯烃C=C的性质出发,分析乙醛可能与H2、HCN发生的加成反应,写出化学方程式。
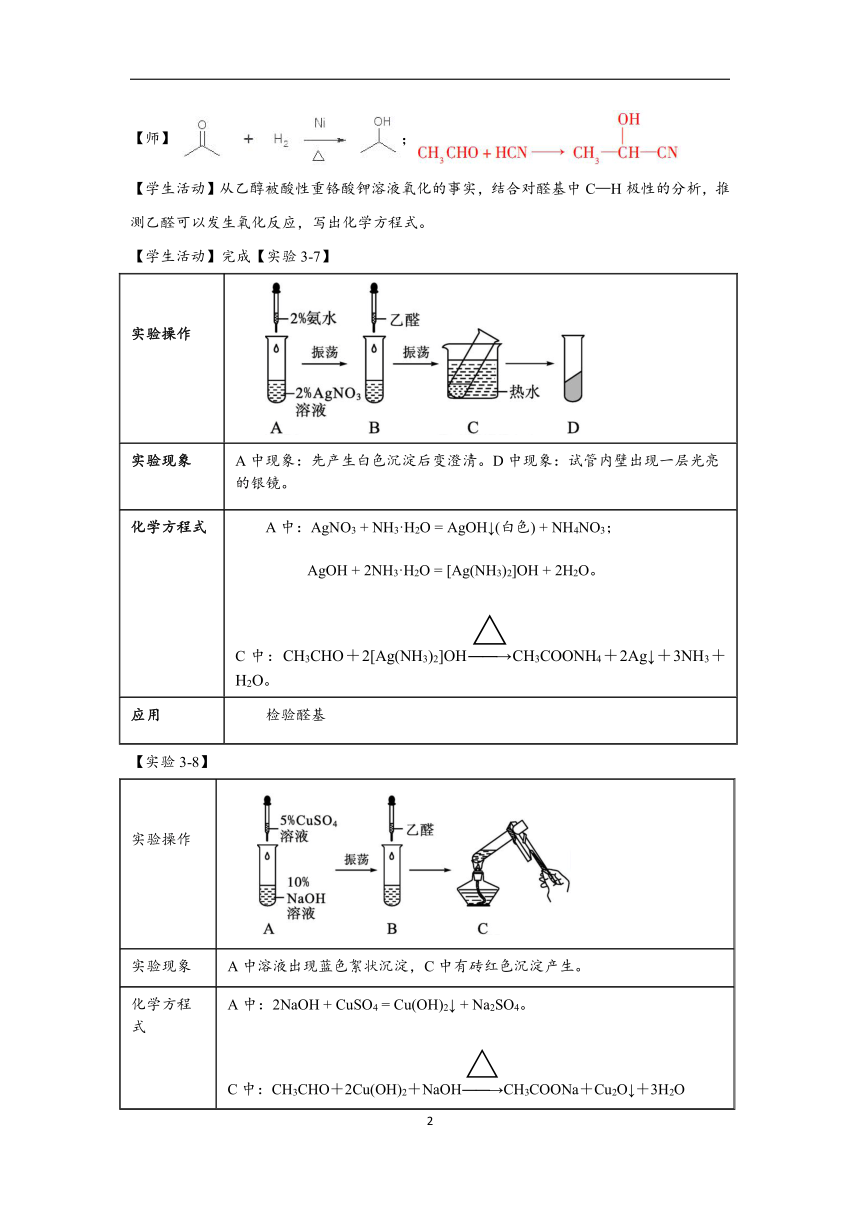
【师】;
【学生活动】从乙醇被酸性重铬酸钾溶液氧化的事实,结合对醛基中C—H极性的分析,推测乙醛可以发生氧化反应,写出化学方程式。
【学生活动】完成【实验3-7】
实验操作
实验现象 A中现象:先产生白色沉淀后变澄清。D中现象:试管内壁出现一层光亮的银镜。
化学方程式 A中:AgNO3 + NH3·H2O = AgOH↓(白色) + NH4NO3; AgOH + 2NH3·H2O = [Ag(NH3)2]OH + 2H2O。C中:CH3CHO+2[Ag(NH3)2]OHCH3COONH4+2Ag↓+3NH3+H2O。
应用 检验醛基
【实验3-8】
实验操作
实验现象 A中溶液出现蓝色絮状沉淀,C中有砖红色沉淀产生。
化学方程式 A中:2NaOH + CuSO4 = Cu(OH)2↓ + Na2SO4。C中:CH3CHO+2Cu(OH)2+NaOHCH3COONa+Cu2O↓+3H2O
【思考与讨论】已知银氨溶液和新制的氢氧化铜属于弱氧化剂,思考乙醛能不能使酸性高锰酸钾溶液褪色
【学生】酸性高锰酸钾溶液属于强氧化剂,故乙醛能使酸性高锰酸钾溶液褪色。
【师】
名称 甲醛 苯甲醛
结构简式 HCHO
俗称 蚁醛 苦杏仁油
物理性质 颜色 无色 无色
气味 强烈刺激性气味 苦杏仁气味
状态 气体 液体
溶解性 易溶于水 —
用途 合成多种有机化合物;福尔马林(甲醛水溶液)可用于消毒和制作生物标本 制造染料、香料及药物的重要原料
化学性质 与乙醛相似,可以被还原为醇,氧化为酸,可以发生银镜反应,能与氰化氢加成
【师】酮
【思考与讨论】饱和一元醛的通式为CnH2nO(n≥1),饱和一元酮的通式为CnH2nO(n≥3),那么分子中含相同碳原子数的饱和一元醛与饱和一元酮有什么关系
【学生活动】分子中含相同碳原子数的饱和一元醛与饱和一元酮的分子式相同,结构不同,互为同分异构体。
板书设计
醛 酮
1、乙醛
(1)结构特点
(2)化学性质
2、常见的醛
3、酮
2
第三节 醛 酮
教学设计
教学目标
1.从官能团和化学键可能的断键部位预测乙醛的化学性质,并能在结构分析和实验事实的基础上书写相关反应的化学方程式,强化“结构决定性质”的观念。
2.能够结合分子结构特点,运用类比迁移的方法预测其他醛类物质的主要性质。
3.能根据官能团的特点和性质区别醛和酮,以丙酮为例认识酮的主要化学性质。
教学重难点
重点:乙醛的结构特点和主要化学性质
难点:乙醛的氧化反应及相关化学方程式的书写
教学过程
一、导入新课
现在的室内空气污染常见的有:大气颗粒、甲醛、苯等,这些空气中的污染物主要是来源于室内新房装修装饰材料具有污染物。
二、新课讲授
【学习任务】如何认识乙醛的化学性质。
【环节1】分析乙醛的结构特点
【学生活动】书写乙醛的结构简式,搭建其分子的结构模型。
【学生活动】分析讨论醛基的结构特点。
【师】乙醛分子式为C2H4O,结构式为,简写为CH3CHO,乙醛的核磁共振氢谱有2组峰,峰面积比为3:1。乙醛是无色、具有刺激性气味的液体,密度比水的小,沸点20.8 ℃,易挥发,易燃烧,能与水、乙醇等互溶。
【环节2】预测乙醛可能具有的化学性质
【学生活动】从C=O的结构特点和烯烃C=C的性质出发,分析乙醛可能与H2、HCN发生的加成反应,写出化学方程式。
【师】;
【学生活动】从乙醇被酸性重铬酸钾溶液氧化的事实,结合对醛基中C—H极性的分析,推测乙醛可以发生氧化反应,写出化学方程式。
【学生活动】完成【实验3-7】
实验操作
实验现象 A中现象:先产生白色沉淀后变澄清。D中现象:试管内壁出现一层光亮的银镜。
化学方程式 A中:AgNO3 + NH3·H2O = AgOH↓(白色) + NH4NO3; AgOH + 2NH3·H2O = [Ag(NH3)2]OH + 2H2O。C中:CH3CHO+2[Ag(NH3)2]OHCH3COONH4+2Ag↓+3NH3+H2O。
应用 检验醛基
【实验3-8】
实验操作
实验现象 A中溶液出现蓝色絮状沉淀,C中有砖红色沉淀产生。
化学方程式 A中:2NaOH + CuSO4 = Cu(OH)2↓ + Na2SO4。C中:CH3CHO+2Cu(OH)2+NaOHCH3COONa+Cu2O↓+3H2O
【思考与讨论】已知银氨溶液和新制的氢氧化铜属于弱氧化剂,思考乙醛能不能使酸性高锰酸钾溶液褪色
【学生】酸性高锰酸钾溶液属于强氧化剂,故乙醛能使酸性高锰酸钾溶液褪色。
【师】
名称 甲醛 苯甲醛
结构简式 HCHO
俗称 蚁醛 苦杏仁油
物理性质 颜色 无色 无色
气味 强烈刺激性气味 苦杏仁气味
状态 气体 液体
溶解性 易溶于水 —
用途 合成多种有机化合物;福尔马林(甲醛水溶液)可用于消毒和制作生物标本 制造染料、香料及药物的重要原料
化学性质 与乙醛相似,可以被还原为醇,氧化为酸,可以发生银镜反应,能与氰化氢加成
【师】酮
【思考与讨论】饱和一元醛的通式为CnH2nO(n≥1),饱和一元酮的通式为CnH2nO(n≥3),那么分子中含相同碳原子数的饱和一元醛与饱和一元酮有什么关系
【学生活动】分子中含相同碳原子数的饱和一元醛与饱和一元酮的分子式相同,结构不同,互为同分异构体。
板书设计
醛 酮
1、乙醛
(1)结构特点
(2)化学性质
2、常见的醛
3、酮
2
