1.1.3 泡利原理 洪特规则 课件(共16张PPT) 2022-2023学年高二化学人教版(2019)选择性必修2
文档属性
| 名称 | 1.1.3 泡利原理 洪特规则 课件(共16张PPT) 2022-2023学年高二化学人教版(2019)选择性必修2 |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-15 09:47:29 | ||
图片预览



文档简介
(共16张PPT)
第一章第一节 原子结构
化学选择性必修2《物质结构与性质》
第3课时 泡利原理、洪特规则
能量最低原理
2022年3月3日
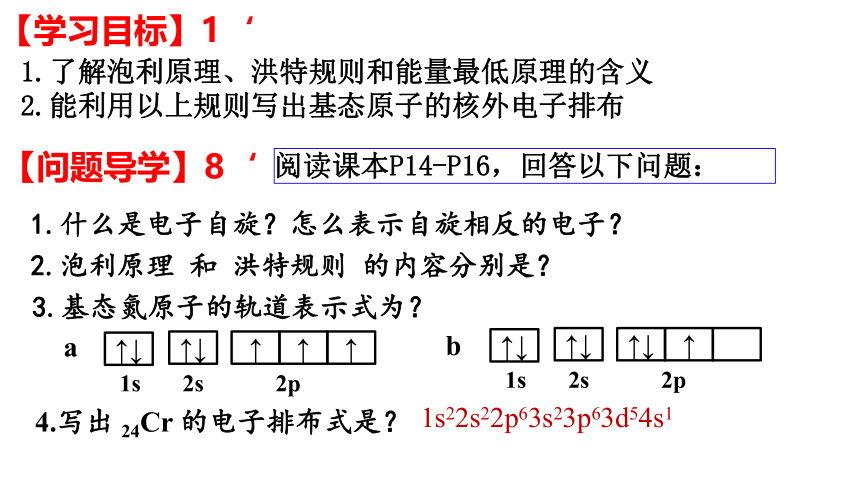
1.了解泡利原理、洪特规则和能量最低原理的含义
2.能利用以上规则写出基态原子的核外电子排布
【学习目标】1‘
1.什么是电子自旋?怎么表示自旋相反的电子?
【问题导学】8‘
阅读课本P14-P16,回答以下问题:
2.泡利原理 和 洪特规则 的内容分别是?
3.基态氮原子的轨道表示式为?
↑↓
1s 2s 2p
↑↓
↑
↑
↑
↑↓
1s 2s 2p
↑↓
↑↓
↑
a
b
4.写出 24Cr 的电子排布式是?
1s22s22p63s23p63d54s1
1925年,乌伦贝克和哥德斯密根据实验事实提出假设:
电子除了空间运动状态外,还存在一种运动状态叫自旋。
【点拨精讲】20‘
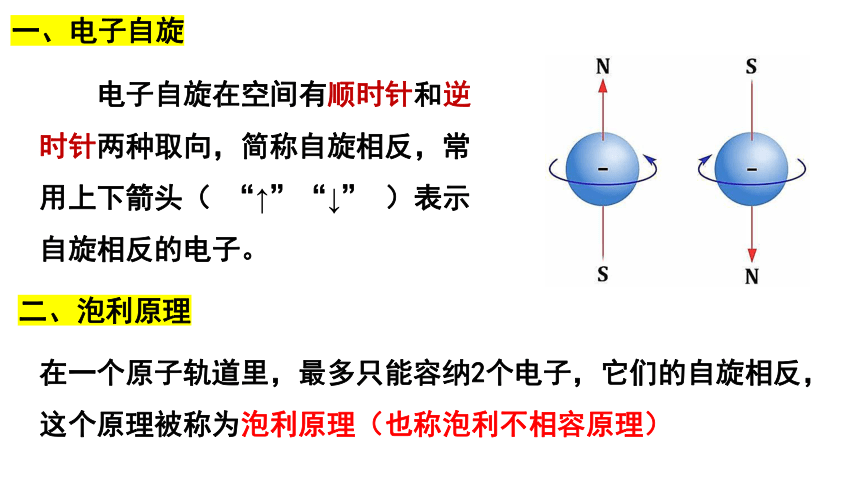
一、电子自旋
电子自旋在空间有顺时针和逆时针两种取向,简称自旋相反,常用上下箭头( “↑”“↓” )表示自旋相反的电子。
二、泡利原理
在一个原子轨道里,最多只能容纳2个电子,它们的自旋相反,这个原理被称为泡利原理(也称泡利不相容原理)
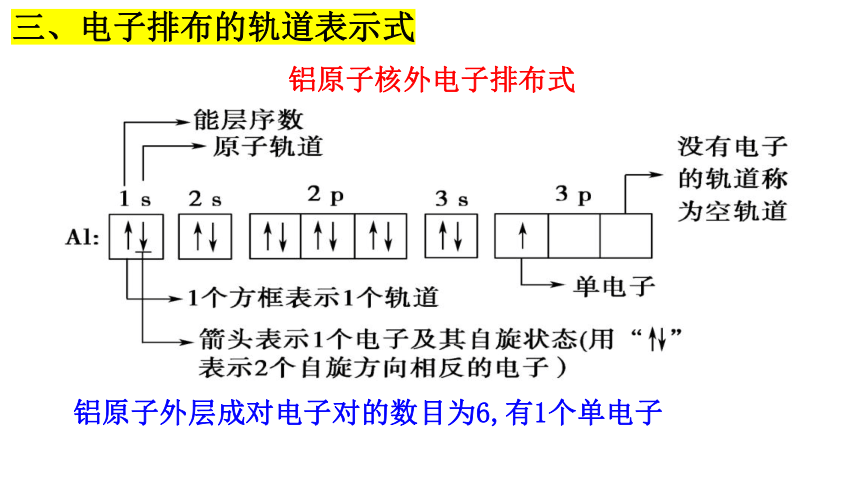
三、电子排布的轨道表示式
轨道表示式(又称电子排布图):表示电子排布的一种图式,如钠的基态原子的轨道表示式如下:
↑↓
↑↓
↑
↑↓
↑↓
↑↓
Na
1s22s22p63s1
Na
1s
2s
2p
3s
4、箭头表示一种自旋状态的电子,一个箭头表示一个电子,
“↓↑”称电子对 , “↓”或“↑”表示单电子,箭头同向,自旋平行,箭头相反,自旋相反。
2、电子排布图中各能级的排列顺序要与相应的电子排布式一致
3、通常在方框下方或者上方标记能级符号
↑↓
1s 2s 2p 3s
↑↓
↑
↑↓
↑↓
↑↓
Na
1、用□(也可用○)代表一个原子轨道,能量相同的原子轨道(简并轨道)的方框相连。不同能级中的方框要相互分开,同一能级中的方框要相互连接
三、电子排布的轨道表示式
铝原子核外电子排布式
铝原子外层成对电子对的数目为6,有1个单电子
请写出Li、Be、B的轨道表示式。
Li
1s
↑↓
↑
2s
Be
1s
↑↓
↑↓
2s
B
1s
↑
↑↓
↑↓
2s
2p
【学以致用】
请写出基态碳原子可能的轨道表示式
② C
1s
↑↑
↑↓
↑↓
2s
2p
① C
1s
↑↓
↑↓
↑↓
2s
2p
2p
③ C
↑
1s
↑
↑↓
↑↓
2s
↑
2p
④ C
↓
1s
↑↓
↑↓
2s
哪个正确呢?
【思考与讨论】
√
四、洪特规则
基态原子中,填入简并轨道的电子总是先单独分占,且自旋平行
2p3的电子排布图
×
×
√
洪特规则不仅适用于基态原子,也适用于基态离子
洪特规则适用于电子填入简并轨道,并不适用于电子填入能量不同的轨道
能量较低
状态稳定
全充满(p6,d10,f14)
全空时(p0,d0,f0 )
半充满(p3,d5,f7 )
对于能量相同的轨道(同一能级),当电子排布处于全满、半满、全空时比较稳定,整个体系的能量最低。
Cr:1s2 2s2 2p6 3s2 3p6 3d4 4s2
Cu:1s2 2s2 2p6 3s2 3p6 3d9 4s2
Cr:1s2 2s2 2p6 3s2 3p6 3d5 4s1
Cu:1s2 2s2 2p6 3s2 3p6 3d10 4s1
√
√
五、能量最低原理
五、能量最低原理
1、在构建基态原子时,电子尽可能地先占有能量低的轨道,然后进入能量高的轨道,使整个原子的能量处于最低状态
2、能级的能量高低顺序如构造原理所示(对于1~36号元素来说,应重点掌握和记忆“ ”这一顺序)
1s→2s→2p→3s→3p→4s→3d→4p
3、在构建基态原子时,电子将尽可能占据能量最低的原子轨道,使整个原子的能量最低,这就是能量最低原理。
【课堂小结】2‘
注意:书写轨道表示式时,常出现的错误及正确书写
1.“各能级最多容纳的电子数,是该能级原子轨道数的二倍”,支撑这一结论的理论是 ( )
A.构造原理 B.泡利原理
C.洪特规则 D.能量最低原理
B
2.某原子核外电子排布为ns2np7,它违背了( )
A.泡利原理 B.能量最低原理
C.洪特规则 D.洪特规则特例
A
【当堂检测】14‘
3.下列关于硅原子的核外电子排布表示方法中,错误的是( )
A. 1s2 2s2 2p6 3s2 3p2 B. [Ne] 3s2 3p2
C. D.
C
4.下列原子或离子的电子排布式或轨道表示式正确的是________(填序号,下同),违反能量最低原理的是____,违反洪特规则的是____,违反泡利原理的是____。
①Ca2+:1s2 2s2 2p6 3s2 3p6 ②F-:1s2 2s2 3p6
③P:
④Fe:1s2 2s2 2p6 3s2 3p6 3d6 4s2 ⑤Mg2+:1s2 2s2 2p6
⑥C:
①④⑤
⑥
②
③
5. 按要求填空。
15P 的轨道表示式: ,有 对电子对,有 个单电子。
25Mn的简化电子排布式: .
6
3
[Ar] 3d5 4s2
第一章第一节 原子结构
化学选择性必修2《物质结构与性质》
第3课时 泡利原理、洪特规则
能量最低原理
2022年3月3日
1.了解泡利原理、洪特规则和能量最低原理的含义
2.能利用以上规则写出基态原子的核外电子排布
【学习目标】1‘
1.什么是电子自旋?怎么表示自旋相反的电子?
【问题导学】8‘
阅读课本P14-P16,回答以下问题:
2.泡利原理 和 洪特规则 的内容分别是?
3.基态氮原子的轨道表示式为?
↑↓
1s 2s 2p
↑↓
↑
↑
↑
↑↓
1s 2s 2p
↑↓
↑↓
↑
a
b
4.写出 24Cr 的电子排布式是?
1s22s22p63s23p63d54s1
1925年,乌伦贝克和哥德斯密根据实验事实提出假设:
电子除了空间运动状态外,还存在一种运动状态叫自旋。
【点拨精讲】20‘
一、电子自旋
电子自旋在空间有顺时针和逆时针两种取向,简称自旋相反,常用上下箭头( “↑”“↓” )表示自旋相反的电子。
二、泡利原理
在一个原子轨道里,最多只能容纳2个电子,它们的自旋相反,这个原理被称为泡利原理(也称泡利不相容原理)
三、电子排布的轨道表示式
轨道表示式(又称电子排布图):表示电子排布的一种图式,如钠的基态原子的轨道表示式如下:
↑↓
↑↓
↑
↑↓
↑↓
↑↓
Na
1s22s22p63s1
Na
1s
2s
2p
3s
4、箭头表示一种自旋状态的电子,一个箭头表示一个电子,
“↓↑”称电子对 , “↓”或“↑”表示单电子,箭头同向,自旋平行,箭头相反,自旋相反。
2、电子排布图中各能级的排列顺序要与相应的电子排布式一致
3、通常在方框下方或者上方标记能级符号
↑↓
1s 2s 2p 3s
↑↓
↑
↑↓
↑↓
↑↓
Na
1、用□(也可用○)代表一个原子轨道,能量相同的原子轨道(简并轨道)的方框相连。不同能级中的方框要相互分开,同一能级中的方框要相互连接
三、电子排布的轨道表示式
铝原子核外电子排布式
铝原子外层成对电子对的数目为6,有1个单电子
请写出Li、Be、B的轨道表示式。
Li
1s
↑↓
↑
2s
Be
1s
↑↓
↑↓
2s
B
1s
↑
↑↓
↑↓
2s
2p
【学以致用】
请写出基态碳原子可能的轨道表示式
② C
1s
↑↑
↑↓
↑↓
2s
2p
① C
1s
↑↓
↑↓
↑↓
2s
2p
2p
③ C
↑
1s
↑
↑↓
↑↓
2s
↑
2p
④ C
↓
1s
↑↓
↑↓
2s
哪个正确呢?
【思考与讨论】
√
四、洪特规则
基态原子中,填入简并轨道的电子总是先单独分占,且自旋平行
2p3的电子排布图
×
×
√
洪特规则不仅适用于基态原子,也适用于基态离子
洪特规则适用于电子填入简并轨道,并不适用于电子填入能量不同的轨道
能量较低
状态稳定
全充满(p6,d10,f14)
全空时(p0,d0,f0 )
半充满(p3,d5,f7 )
对于能量相同的轨道(同一能级),当电子排布处于全满、半满、全空时比较稳定,整个体系的能量最低。
Cr:1s2 2s2 2p6 3s2 3p6 3d4 4s2
Cu:1s2 2s2 2p6 3s2 3p6 3d9 4s2
Cr:1s2 2s2 2p6 3s2 3p6 3d5 4s1
Cu:1s2 2s2 2p6 3s2 3p6 3d10 4s1
√
√
五、能量最低原理
五、能量最低原理
1、在构建基态原子时,电子尽可能地先占有能量低的轨道,然后进入能量高的轨道,使整个原子的能量处于最低状态
2、能级的能量高低顺序如构造原理所示(对于1~36号元素来说,应重点掌握和记忆“ ”这一顺序)
1s→2s→2p→3s→3p→4s→3d→4p
3、在构建基态原子时,电子将尽可能占据能量最低的原子轨道,使整个原子的能量最低,这就是能量最低原理。
【课堂小结】2‘
注意:书写轨道表示式时,常出现的错误及正确书写
1.“各能级最多容纳的电子数,是该能级原子轨道数的二倍”,支撑这一结论的理论是 ( )
A.构造原理 B.泡利原理
C.洪特规则 D.能量最低原理
B
2.某原子核外电子排布为ns2np7,它违背了( )
A.泡利原理 B.能量最低原理
C.洪特规则 D.洪特规则特例
A
【当堂检测】14‘
3.下列关于硅原子的核外电子排布表示方法中,错误的是( )
A. 1s2 2s2 2p6 3s2 3p2 B. [Ne] 3s2 3p2
C. D.
C
4.下列原子或离子的电子排布式或轨道表示式正确的是________(填序号,下同),违反能量最低原理的是____,违反洪特规则的是____,违反泡利原理的是____。
①Ca2+:1s2 2s2 2p6 3s2 3p6 ②F-:1s2 2s2 3p6
③P:
④Fe:1s2 2s2 2p6 3s2 3p6 3d6 4s2 ⑤Mg2+:1s2 2s2 2p6
⑥C:
①④⑤
⑥
②
③
5. 按要求填空。
15P 的轨道表示式: ,有 对电子对,有 个单电子。
25Mn的简化电子排布式: .
6
3
[Ar] 3d5 4s2
