河北省石家庄市行唐县2022-2023学年高二下学期4月月考化学试题(含解析)
文档属性
| 名称 | 河北省石家庄市行唐县2022-2023学年高二下学期4月月考化学试题(含解析) |
|
|
| 格式 | doc | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-18 00:00:00 | ||
图片预览


文档简介
行唐县2022-2023学年高二下学期4月月考
化学试卷
可能用到的相对原子质量:H-1 O-16 C-12 N-14
一、选择题:本题共14个小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
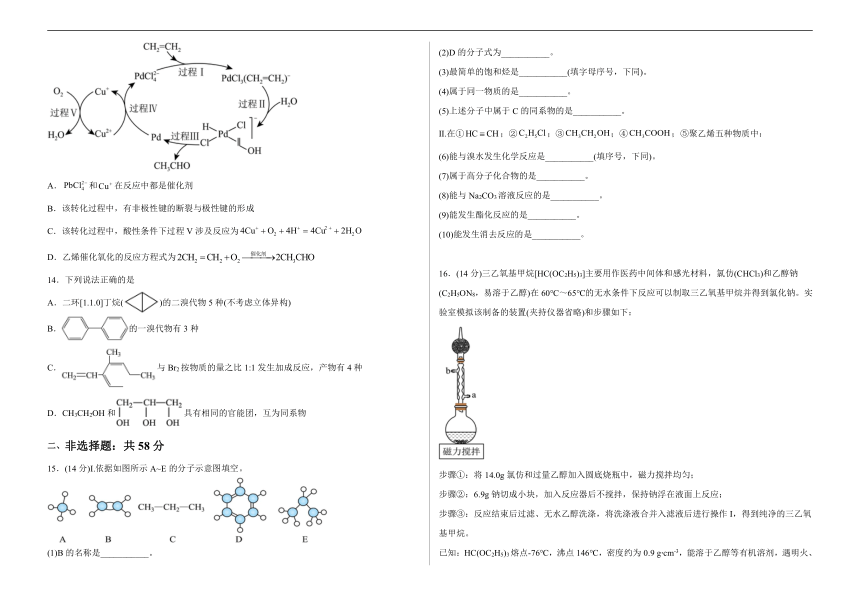
1.下列化学用语或图示表达正确的是
A.乙烯的结构简式: B.碳化硅的分子式:SiC
C.Cr的核外电子排布式: D.乙醇的核磁共振氢谱图:
2.下列有机物的物理性质的大小比较正确的是
A.熔点:苯甲醇>一氯甲烷>溴苯
B.密度:CH3CH2Br>CH3CH3>CH3(CH2)2CH3
C.室温下,在水中的溶解度:丙三醇>苯酚>1-氯丁烷
D.沸点:1-戊醇>2,3-二甲基丁烷>2-甲基戊烷>丙烷
3.下列说法正确的是
A.某有机物燃烧只生成和,且二者物质的量相等,则此有机物的组成为
B.一种烃在足量的氧气中燃烧并通过浓硫酸,减少的总体积就是生成的水蒸气的体积
C.某气态烃与足量恰好完全反应,如果反应前后气体体积不变(温度大于100℃),则;若体积减少,则;否则
D.相同质量的烃完全燃烧,消耗越多,则烃中含量越高
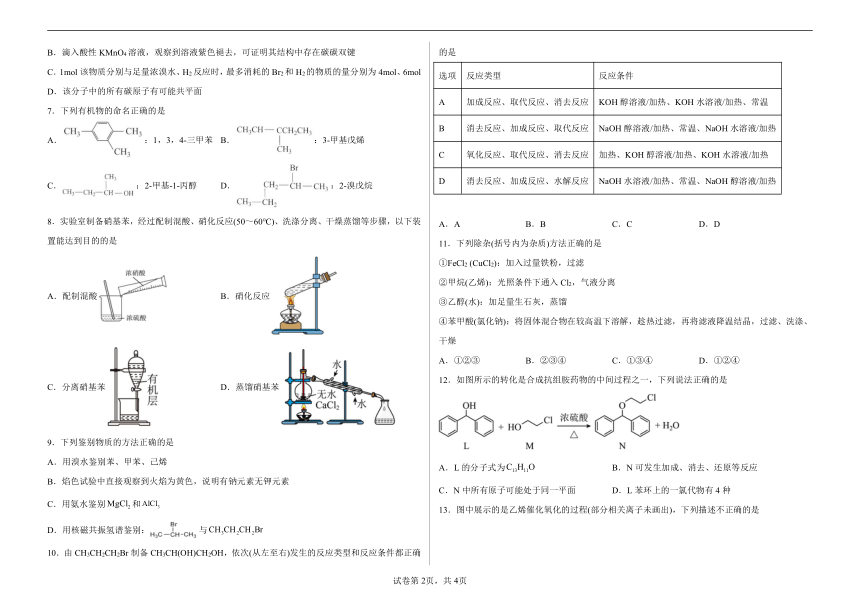
4.下列实验装置能达到实验目的是(夹持仪器未画出)
A.①装置用于实验室制备乙炔
B.②装置制备并收集乙酸乙酯
C.③装置用于实验室制硝基苯
D.④装置可装置证明酸性:盐酸>碳酸>苯酚
5.下列有关同分异构体数目(不考虑立体异构)的叙述正确的是
A.与互为同分异构体的芳香烃有2种
B.它与硝酸反应,可生成4种一硝基取代物
C.与两分子溴发生加成反应的产物,理论上最多有3种
D.分子式为C7H16的烃,分子中有4个甲基的同分异构体有4种
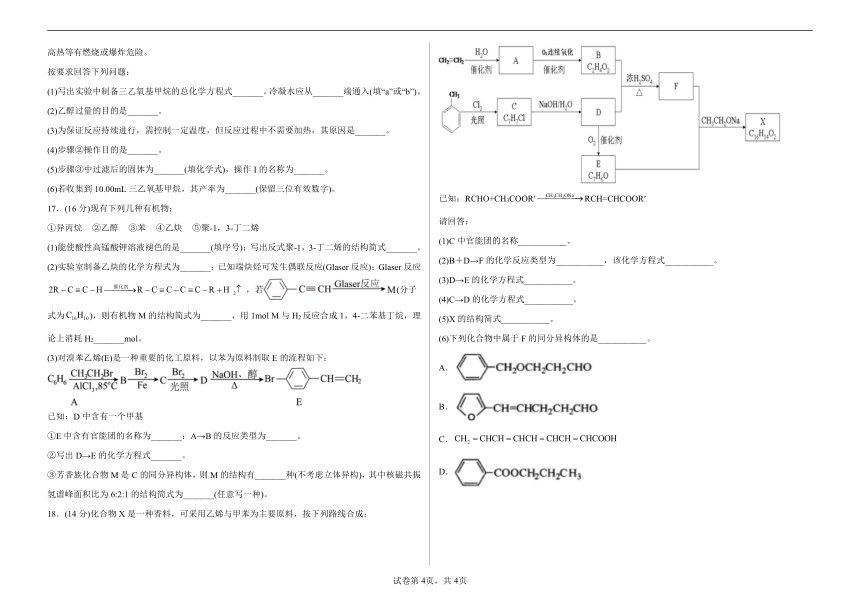
6.坚决反对运动员服用兴奋剂是现代奥运会公平性的一个重要体现。已知某种兴奋剂的结构简式如图,下列有关该物质的说法正确的是
A.因该物质与苯酚互为同系物,故其遇FeCl3溶液显紫色
B.滴入酸性KMnO4溶液,观察到溶液紫色褪去,可证明其结构中存在碳碳双键
C.1mol该物质分别与足量浓溴水、H2反应时,最多消耗的Br2和H2的物质的量分别为4mol、6mol
D.该分子中的所有碳原子有可能共平面
7.下列有机物的命名正确的是
A.:1,3,4-三甲苯 B.:3-甲基戊烯
C.:2-甲基-1-丙醇 D.:2-溴戊烷
8.实验室制备硝基苯,经过配制混酸、硝化反应(50~60℃)、洗涤分离、干燥蒸馏等步骤,以下装置能达到目的的是
A.配制混酸 B.硝化反应
C.分离硝基苯 D.蒸馏硝基苯
9.下列鉴别物质的方法正确的是
A.用溴水鉴别苯、甲苯、己烯
B.焰色试验中直接观察到火焰为黄色,说明有钠元素无钾元素
C.用氨水鉴别和
D.用核磁共振氢谱鉴别:与
10.由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次(从左至右)发生的反应类型和反应条件都正确的是
选项 反应类型 反应条件
A 加成反应、取代反应、消去反应 KOH醇溶液/加热、KOH水溶液/加热、常温
B 消去反应、加成反应、取代反应 NaOH醇溶液/加热、常温、NaOH水溶液/加热
C 氧化反应、取代反应、消去反应 加热、KOH醇溶液/加热、KOH水溶液/加热
D 消去反应、加成反应、水解反应 NaOH水溶液/加热、常温、NaOH醇溶液/加热
A.A B.B C.C D.D
11.下列除杂(括号内为杂质)方法正确的是
①FeCl2 (CuCl2):加入过量铁粉,过滤
②甲烷(乙烯):光照条件下通入Cl2,气液分离
③乙醇(水):加足量生石灰,蒸馏
④苯甲酸(氯化钠):将固体混合物在较高温下溶解,趁热过滤,再将滤液降温结晶,过滤、洗涤、干燥
A.①②③ B.②③④ C.①③④ D.①②④
12.如图所示的转化是合成抗组胺药物的中间过程之一,下列说法正确的是
A.L的分子式为 B.N可发生加成、消去、还原等反应
C.N中所有原子可能处于同一平面 D.L苯环上的一氯代物有4种
13.图中展示的是乙烯催化氧化的过程(部分相关离子未画出),下列描述不正确的是
A.和在反应中都是催化剂
B.该转化过程中,有非极性键的断裂与极性键的形成
C.该转化过程中,酸性条件下过程V涉及反应为
D.乙烯催化氧化的反应方程式为
14.下列说法正确的是
A.二环[1.1.0]丁烷()的二溴代物5种(不考虑立体异构)
B.的一溴代物有3种
C.与Br2按物质的量之比1:1发生加成反应,产物有4种
D.CH3CH2OH和具有相同的官能团,互为同系物
二、非选择题:共58分
15.(14分)Ⅰ.依据如图所示A~E的分子示意图填空。
(1)B的名称是___________。
(2)D的分子式为___________。
(3)最简单的饱和烃是___________(填字母序号,下同)。
(4)属于同一物质的是___________。
(5)上述分子中属于C的同系物的是___________。
Ⅱ.在①;②;③;④;⑤聚乙烯五种物质中:
(6)能与溴水发生化学反应是___________(填序号,下同)。
(7)属于高分子化合物的是___________。
(8)能与Na2CO3溶液反应的是___________。
(9)能发生酯化反应的是___________。
(10)能发生消去反应的是___________。
16.(14分)三乙氧基甲烷[HC(OC2H5)3]主要用作医药中间体和感光材料,氯仿(CHCl3)和乙醇钠(C2H5ON8,易溶于乙醇)在60℃~65℃的无水条件下反应可以制取三乙氧基甲烷并得到氯化钠。实验室模拟该制备的装置(夹持仪器省略)和步骤如下:
步骤①:将14.0g氯仿和过量乙醇加入圆底烧瓶中,磁力搅拌均匀;
步骤②:6.9g钠切成小块,加入反应器后不搅拌,保持钠浮在液面上反应;
步骤③:反应结束后过滤、无水乙醇洗涤,将洗涤液合并入滤液后进行操作I,得到纯净的三乙氧基甲烷。
已知:HC(OC2H5)3熔点-76℃,沸点146℃,密度约为0.9 g cm-3,能溶于乙醇等有机溶剂,遇明火、高热等有燃烧或爆炸危险。
按要求回答下列问题:
(1)写出实验中制备三乙氧基甲烷的总化学方程式_______。冷凝水应从_______端通入(填“a”或“b”)。
(2)乙醇过量的目的是_______。
(3)为保证反应持续进行,需控制一定温度,但反应过程中不需要加热,其原因是_______。
(4)步骤②操作目的是_______。
(5)步骤③中过滤后的固体为_______(填化学式),操作I的名称为_______。
(6)若收集到10.00mL三乙氧基甲烷,其产率为_______(保留三位有效数字)。
17.(16分)现有下列几种有机物:
①异丙烷 ②乙醇 ③苯 ④乙炔 ⑤聚-1,3-丁二烯
(1)能使酸性高锰酸钾溶液褪色的是_______(填序号);写出反式聚-1,3-丁二烯的结构简式_______。
(2)实验室制备乙炔的化学方程式为_______;已知端炔烃可发生偶联反应(Glaser反应);Glaser反应,若(分子式为),则有机物M的结构简式为_______,用1mol M与H2反应合成1,4-二苯基丁烷,理论上消耗H2_______mol。
(3)对溴苯乙烯(E)是一种重要的化工原料,以苯为原料制取E的流程如下:
已知:D中含有一个甲基
①E中含有官能团的名称为_______;A→B的反应类型为_______。
②写出D→E的化学方程式_______。
③芳香族化合物M是C的同分异构体,则M的结构有_______种(不考虑立体异构),其中核磁共振氢谱峰面积比为6:2:1的结构简式为_______(任意写一种)。
18.(14分)化合物X是一种香料,可采用乙烯与甲苯为主要原料,按下列路线合成:
已知:RCHO+CH3COOR′RCH=CHCOOR′
请回答:
(1)C中官能团的名称___________。
(2)B+D→F的化学反应类型为___________,该化学方程式___________。
(3)D→E的化学方程式___________。
(4)C→D的化学方程式___________。
(5)X的结构简式___________。
(6)下列化合物中属于F的同分异构体的是___________。
A.
B.
C.
D.
试卷第2页,共2页
答案
1.C
【详解】A.结构简式中不能省略C=C,所以乙烯的结构简式为CH2=CH2,A项错误;
B.碳化硅为原子晶体,其化学式为SiC,B项错误;
C.Cr为24号元素,核外电子排布半满结构稳定为[Ar]3d54s1,C项正确;
D.乙醇为CH3CH2OH,分子中含有3类氢原子,核磁共振氢谱中有三种峰,D项错误;
故选C。
2.C
【详解】A.一氯甲烷呈气态,苯甲醇、溴苯呈液态,所以一氯甲烷的熔点最低,A不正确;
B.常温常压下,CH3CH2Br呈液态,CH3CH3、CH3(CH2)2CH3呈气态,且CH3(CH2)2CH3的密度比CH3CH3大,所以密度:CH3CH2Br>CH3(CH2)2CH3>CH3CH3,B不正确;
C.常温下,丙三醇与水分子间能形成氢键,丙三醇与水互溶,苯酚微溶于水,而1-氯丁烷难溶于水,所以在水中的溶解度:丙三醇>苯酚>1-氯丁烷,C正确;
D.2,3-二甲基丁烷与2-甲基戊烷互为同分异构体,2,3-二甲基丁烷的支链比2-甲基戊烷多,则沸点:1-戊醇>2-甲基戊烷>2,3-二甲基丁烷>丙烷,D不正确;
故选C。
3.D
【详解】A.某有机物燃烧只生成CO2和H2O,二者物质的量相等,说明该有机物中C、H个数比为1∶2,符合形式有CnH2n、CnH2nO、CnH2nO2等,故A错误;
B.浓硫酸吸收的是水蒸气,烃燃烧前后气体体积也可能发生变化,因此烃在足量的氧气中燃烧并通过浓硫酸,减少的体积不一定是生成的水蒸气的体积,故B错误;
C.温度高于100℃,水为气体,根据CxHy+(x+)O2xCO2+H2O(g),如果反应前后气体体积不变,则1+(x+)=x+,解得y=4,若气体体积减少,则1+(x+)>x+,解得y<4,若气体体积增大,则1+(x+)<x+,解得y>4,故C错误;
D.C~O2~CO2,4H~O2~2H2O,消耗1mol氧气,需要12gC,需要4gH,可知有机物含氢量越大,等质量时消耗的氧气越多,故D正确;
答案为D。
4.C
【详解】A.电石遇水后,与水剧烈反应,且产生的Ca(OH)2易堵塞塑料板上的小孔,所以实验室不能用①装置制备乙炔,A不符合题意;
B.制备乙酸乙酯时,出气导管口应位于饱和Na2CO3溶液的液面上,②装置会产生倒吸,B不符合题意;
C.实验室制硝基苯时,应使用60℃左右的水浴加热,则③装置可用于实验室制硝基苯,C符合题意;
D.④装置中,与Na2CO3反应的酸为浓盐酸,易挥发出HCl气体,与苯酚钠直接反应,所以④装置不能用于判断碳酸与苯酚的酸性强弱,D不符合题意;
故选C。
5.D
【详解】A.的分子式为C8H8,与其互为同分异构体的芳香烃为苯乙烯,有1种,A错误;
B.为对称结构,如与硝酸反应,可生成5种一硝基取代物,B错误;
C.因分子存在三种不同的碳碳双键,如图所示,1分子物质与2分子Br2加成时,可以在①②的位置上发生加成,也可以在①③位置上发生加成,或在②③位置上发生加成,还可以消耗1分子Br2在①②发生1,4-加成反应、而另1分子Br2在③上加成,故所得产物共有四种,C错误;
D.分子式为C7H16的烃,分子中有4个甲基的同分异构体可看作正戊烷中间3个碳原子上的氢原子被2个甲基取代,2个甲基在同一碳原子有2种,在不同碳原子有2种,合计有4种,D正确;
故答案选D。
6.D
【详解】A.该物质含有酚羟基,遇FeCl3溶液显紫色,但与苯酚不互为同系物,A不正确;
B.连在苯环上的-CH3、酚-OH、碳碳双键,都能被酸性KMnO4溶液氧化,从而使KMnO4溶液紫色褪去,所以不能证明其结构中存在碳碳双键,B不正确;
C.酚羟基邻、对位上的H原子可以被Br原子取代,苯环、碳碳双键都能与H2发生加成反应,所以1mol该物质分别与足量浓溴水、H2反应时,最多消耗的Br2和H2的物质的量分别为5mol、7mol,C不正确;
D.由苯和乙烯原子的共平面,可推测 红框内的原子一定共平面,三个红框分别共用2个碳原子,所以三个红框内的碳原子也可能共平面,由此可推出,该分子中的所有碳原子可能共平面,D正确;
故选D。
7.D
【详解】A.该物质的名称为1,2,4-三甲苯,A项错误;
B.烯烃需要指出双键碳并使双键碳序号尽可能的小,该物质为3-甲基-2-戊烯,B项错误;
C.选择连羟基的最长的碳链为主链,该物质的名称为2-丁醇,C项错误;
D.把卤素原子当取代基,该物质为2-溴戊烷,D项正确;
故选D。
8.C
【详解】A.浓硫酸密度大,防止酸液飞溅,配置混酸时应将浓硫酸加入浓硝酸中,A错误;
B.制备硝基苯时反应温度应在50~60℃,为控制反应温度应该用水浴加热,B错误;
C.硝基苯不溶于水,分离硝基苯应该用分液的方法,C正确;
D.蒸馏硝基苯时,温度计水银球应该与支管口平齐,D错误;
故答案为:C。
9.D
【详解】A.苯和甲苯的密度都比水小,都不能与溴水反应,所以用溴水可以鉴别己烯,但不能鉴别苯和甲苯,故A错误;
B.黄色光会掩盖紫色光,所以焰色试验中直接观察到火焰为黄色,说明化合物中一定有钠元素,但不能确定是否含有钾元素,故B错误;
C.氯化镁溶液与氨水反应生成氢氧化镁白色沉淀和氯化铵,氢氧化铝是不能溶于氨水的两性氢氧化物,氯化铝溶液与氨水反应生成氢氧化铝白色沉淀和氯化铵,则用氨水不能鉴别氯化镁溶液和氯化铝溶液,故C错误;
D.2—溴丙烷分子中含有2类氢原子,核磁共振氢谱有2组峰,1—溴丙烷分子中含有3类氢原子,核磁共振氢谱有3组峰,则用核磁共振氢谱能鉴别2—溴丙烷和1—溴丙烷,故D正确;
故选D。
10.B
【详解】由CH3CH2CH2Br制备CH3CH(OH)CH2OH,先发生消去反应,得到丙烯,条件为NaOH的醇溶液、加热;再与卤素单质加成得到卤代烃,条件为卤素单质的四氯化碳溶液;最后水解得到目标产物,条件为NaOH的水溶液、加热,故选B。
11.C
【详解】①FeCl2 (CuCl2):加入过量铁粉,将CuCl2全部转化为FeCl2和Cu,过滤,滤液为FeCl2溶液,①正确;
②甲烷(乙烯):光照条件下通入Cl2,Cl2与甲烷发生取代反应,生成氯代甲烷和HCl,气液分离后得不到纯净的甲烷,②不正确;
③乙醇(水):加足量生石灰,与水反应生成氢氧化钙,蒸馏可得纯净的乙醇,③正确;
④苯甲酸(氯化钠):苯甲酸的溶解度随温度的升高而增大,氯化钠的溶解度受温度的影响不大,将固体混合物在较高温下溶解,趁热过滤,以防苯甲酸结晶析出,再将滤液降温结晶,过滤出苯甲酸,再洗涤、干燥,④正确;
通过以上分析可知,①③④正确,故选C。
12.B
【详解】A.由结构简式可知,L的分子式为C13H12O,故A错误;
B.由结构简式可知,N分子中含有的苯环能发生加成反应和还原反应,含有的氯原子能发生消去反应,故B正确;
C.由结构简式可知,N分子中含有空间构型为四面体形的饱和碳原子,分子中所有原子不可能处于同一平面,故C错误;
D.由结构简式可知,L苯环上有3类氢原子,一氯代物有3种,故D错误;
故选B。
13.A
【详解】A.过程V中消耗,过程IV中生成,不是催化剂,过程I消耗,过程IV生成,则是催化剂,A选项错误;
B.该转化过程中,有非极性键的断裂与极性键的形成,例如过程V:氧气分子中的非极性键断裂,生成水有极性键的形成(氢氧键),B选项正确;
C.该转化过程中,酸性条件下过程V是与氧气反应生成和水,涉及的反应为:,C选项正确;
D.乙烯被氧气最终催化氧化为,反应的方程式为:,D选项正确;
答案选A。
14.B
【详解】A.二环[1.1.0]丁烷()的二溴代物中,2个Br连在同一碳原子上只有1种,2个Br连在不同碳原子上共有3种,所以共有4种异构体(不考虑立体异构),A不正确;
B. 的一溴代物中溴原子可取代中①、②、③位置上的氢原子,则共有3种异构体,B正确;
C. 与Br2按物质的量之比1:1发生加成反应,只断裂1个碳碳双键的产物有3种,同时断裂2个碳碳双键、并形成1个碳碳双键(相当于发生1,4-加成)的产物有2种,所以与等摩Br2加成的产物有5种,C不正确;
D.CH3CH2OH和 具有相同种类的官能团,但官能团的数目不同,二者不互为同系物,D不正确;
故选B。
15.(1)乙烯
(2)
(3)A
(4)C E
(5)A
(6)①
(7)⑤
(8)④
(9)③④
(10)②③
【分析】由烃分子的示意图可知,A为甲烷、B为乙烯、C为丙烷、D为苯、E为丙烷。
【详解】(1)B的结构简式为CH2=CH2,B的名称是乙烯。故答案为:乙烯;
(2)D为苯,D的分子式为。故答案为:;
(3)甲烷分子中只有一个碳原子,最简单的饱和烃是A。故答案为:A;
(4)C为丙烷的结构简式,E为丙烷的球棍模型,属于同一物质的是C E。故答案为:C E;
(5)甲烷和丙烷同属于烷烃,分子组成上相差2个CH2原子团,上述分子中属于C的同系物的是A。故答案为:A;
(6)乙炔中有不饱和键,能与溴水发生化学反应是①。故答案为:①;
(7)分子量大于10000的化合物属于高分子化合物,属于高分子化合物的是⑤。故答案为:⑤;
(8)有机物中含有羧基或酚羟基能与Na2CO3溶液反应,能与Na2CO3溶液反应的是④。故答案为:④;
(9)含有羟基或羧基的有机物能发生酯化反应,能发生酯化反应的是③④。故答案为:③④;
(10)与-X或-OH相连的碳的邻碳上有氢,在一定条件下可发生消去反应,能发生消去反应的是②③。故答案为:②③。
16.(1) 2CHCl3+6CH3CH2OH+6Na→2HC(OC2H5)3+6NaCl+3H2↑ a
(2)增大反应物的接触面积,提高原料的利用率
(3)钠与乙醇的反应为放热反应
(4)有利于散热,防止温度升高引起爆炸
(5) NaCl 蒸馏
(6)51.9%
【分析】14.0g氯仿和过量乙醇混合后形成溶液;将切成小块的6.9g钠加入反应器后不搅拌,保持钠浮在液面上与乙醇反应,反应平稳进行,反应产生的热量及时散失;反应结束后过滤出不溶物NaCl,用无水乙醇洗涤,将洗涤液合并入滤液后进行蒸馏,得到纯净的三乙氧基甲烷。
【详解】(1)实验中,乙醇与钠反应生成乙醇钠和氢气,氯仿与乙醇钠反应制得三乙氧基甲烷等,总化学方程式为2CHCl3+6CH3CH2OH+6Na→2HC(OC2H5)3+6NaCl+3H2↑。为了保证冷却水能充满冷凝管,冷凝水应从a端通入。答案为:2CHCl3+6CH3CH2OH+6Na→2HC(OC2H5)3+6NaCl+3H2↑;a;
(2)乙醇过量,可使反应物充分溶解,增大接触面积,则目的是:增大反应物的接触面积,提高原料的利用率。答案为:增大反应物的接触面积,提高原料的利用率;
(3)为保证反应持续进行,需控制一定温度,但反应过程中不需要加热,其原因是:钠与乙醇的反应为放热反应。答案为:钠与乙醇的反应为放热反应;
(4)HC(OC2H5)3熔点-76℃,沸点146℃,能溶于乙醇等有机溶剂,遇明火、高热等有燃烧或爆炸危险,则步骤②操作目的是:有利于散热,防止温度升高引起爆炸。答案为:有利于散热,防止温度升高引起爆炸;
(5)反应结束后过滤、无水乙醇洗涤,将洗涤液合并入滤液后进行操作I,得到纯净的三乙氧基甲烷,因为NaCl难溶于乙醇,所以步骤③中过滤后的固体为NaCl,操作I是从混合液中分离出HC(OC2H5)3,名称为蒸馏。答案为:NaCl;蒸馏。
(6)三乙氧基甲烷体积为10.00mL,密度约为0.9 g cm-3,氯仿质量为14.0g,则CHCl3——HC(OC2H5)3,可求出理论上生成HC(OC2H5)3的质量为,则
HC(OC2H5)3的产率为≈51.9%。答案为:51.9%。
【点睛】产率=。
17.(1) ②④⑤
(2) CaC2+2H2O→Ca(OH)2+CH≡CH↑ 4
(3) 碳碳双键、碳溴键 取代反应 +NaOH+NaBr+H2O 13 、
【分析】由E的结构简式,可确定A为,B为,C为,D为。
【详解】(1)②乙醇、④乙炔、⑤聚-1,3-丁二烯都能使酸性高锰酸钾溶液褪色,故选②④⑤;反式聚-1,3-丁二烯的结构简式为。答案为:②④⑤;;
(2)实验室以电石与水反应制备乙炔,化学方程式为CaC2+2H2O→Ca(OH)2+CH≡CH↑;若(分子式为),则有机物M的结构简式为,用1mol M与H2反应合成1,4-二苯基丁烷,则需将2mol碳碳三键转化为碳碳单键,理论上消耗H24mol。答案为:CaC2+2H2O→Ca(OH)2+CH≡CH↑;;4;
(3)①E的结构简式为,含有官能团的名称为碳碳双键、碳溴键;A()与CH3CH2Br在AlCl3催化作用下发生反应→B()和HBr,反应类型为取代反应。
②D()发生消去反应→E()等,化学方程式+NaOH+NaBr+H2O。
③芳香族化合物M是C的同分异构体,C为,则M的结构可能为:含苯环和1个取代基-CH2CH2Br或-CHBrCH3(2种);含苯环和2个取代基-Br、-CH2CH3(邻位或间位)或-CH2Br、-CH3(邻、间、对)(5种);含苯环、-Br、2个-CH3,共有6种异构体,所以,共有13种,其中核磁共振氢谱峰面积比为6:2:1的结构简式为、。答案为:碳碳双键、碳溴键;取代反应;+NaOH+NaBr+H2O;13;、。
【点睛】合成有机物时,可采用逆推法。
18.(1)氯原子或碳氯键
(2) 取代反应或酯化反应 CH3COOH++H2O
(3)2+O22+2H2O
(4)+NaOH+NaCl
(5)
(6)BC
【分析】乙烯与水发生加成反应,生成乙醇,即A的结构简式为CH3CH2OH,乙醇连续氧化成乙酸,根据B的分子式,B的结构简式为CH3COOH,甲苯与氯气在光照条件下,发生取代反应,氯原子取代甲基上的氢原子,即C的结构简式为,C在氢氧化钠水溶液中发生水解反应,得到D,D的结构简式为,B与D发生酯化反应,即F的结构简式为,根据E的分子式,E为醛,结构简式为,根据题中所给信息,X结构简式为,
据此分析;
【详解】(1)根据上述分析,C的结构简式为,所含官能团为碳氯键;故答案为碳氯键;
(2)根据上述分析,B+D→F的反应的类型为取代反应或酯化反应;该反应方程式为CH3COOH++H2O;故答案为取代反应或酯化反应;CH3COOH++H2O;
(3)D的结构简式为,E的结构简式为,D→E发生氧化反应,其反应方程式为2+O22+2H2O;故答案为2+O22+2H2O;
(4)C→D的反应类型为水解反应,其反应方程式为+NaOH+NaCl;故答案为+NaOH+NaCl;
(5)根据上述分析,X的结构简式为;故答案为;
(6)根据上述分析,F的结构简式为,
A.F的结构简式为C9H10O2,题中所给结构简式的分子式为C10H12O2,两者分子式不同,不属于同分异构体,故A不符合题意;
B.分子式为C9H10O2,与F的结构简式不同,因此两者互为同分异构体,故B符合题意;
C.分子式为C9H10O2,与F的结构简式不同,因此两者互为同分异构体,故C符合题意;
D.题中所给有机物的分子式为C10H12O2,两者分子式不同,不属于同分异构体,故D不符合题意;
答案为BC。
化学试卷
可能用到的相对原子质量:H-1 O-16 C-12 N-14
一、选择题:本题共14个小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.下列化学用语或图示表达正确的是
A.乙烯的结构简式: B.碳化硅的分子式:SiC
C.Cr的核外电子排布式: D.乙醇的核磁共振氢谱图:
2.下列有机物的物理性质的大小比较正确的是
A.熔点:苯甲醇>一氯甲烷>溴苯
B.密度:CH3CH2Br>CH3CH3>CH3(CH2)2CH3
C.室温下,在水中的溶解度:丙三醇>苯酚>1-氯丁烷
D.沸点:1-戊醇>2,3-二甲基丁烷>2-甲基戊烷>丙烷
3.下列说法正确的是
A.某有机物燃烧只生成和,且二者物质的量相等,则此有机物的组成为
B.一种烃在足量的氧气中燃烧并通过浓硫酸,减少的总体积就是生成的水蒸气的体积
C.某气态烃与足量恰好完全反应,如果反应前后气体体积不变(温度大于100℃),则;若体积减少,则;否则
D.相同质量的烃完全燃烧,消耗越多,则烃中含量越高
4.下列实验装置能达到实验目的是(夹持仪器未画出)
A.①装置用于实验室制备乙炔
B.②装置制备并收集乙酸乙酯
C.③装置用于实验室制硝基苯
D.④装置可装置证明酸性:盐酸>碳酸>苯酚
5.下列有关同分异构体数目(不考虑立体异构)的叙述正确的是
A.与互为同分异构体的芳香烃有2种
B.它与硝酸反应,可生成4种一硝基取代物
C.与两分子溴发生加成反应的产物,理论上最多有3种
D.分子式为C7H16的烃,分子中有4个甲基的同分异构体有4种
6.坚决反对运动员服用兴奋剂是现代奥运会公平性的一个重要体现。已知某种兴奋剂的结构简式如图,下列有关该物质的说法正确的是
A.因该物质与苯酚互为同系物,故其遇FeCl3溶液显紫色
B.滴入酸性KMnO4溶液,观察到溶液紫色褪去,可证明其结构中存在碳碳双键
C.1mol该物质分别与足量浓溴水、H2反应时,最多消耗的Br2和H2的物质的量分别为4mol、6mol
D.该分子中的所有碳原子有可能共平面
7.下列有机物的命名正确的是
A.:1,3,4-三甲苯 B.:3-甲基戊烯
C.:2-甲基-1-丙醇 D.:2-溴戊烷
8.实验室制备硝基苯,经过配制混酸、硝化反应(50~60℃)、洗涤分离、干燥蒸馏等步骤,以下装置能达到目的的是
A.配制混酸 B.硝化反应
C.分离硝基苯 D.蒸馏硝基苯
9.下列鉴别物质的方法正确的是
A.用溴水鉴别苯、甲苯、己烯
B.焰色试验中直接观察到火焰为黄色,说明有钠元素无钾元素
C.用氨水鉴别和
D.用核磁共振氢谱鉴别:与
10.由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次(从左至右)发生的反应类型和反应条件都正确的是
选项 反应类型 反应条件
A 加成反应、取代反应、消去反应 KOH醇溶液/加热、KOH水溶液/加热、常温
B 消去反应、加成反应、取代反应 NaOH醇溶液/加热、常温、NaOH水溶液/加热
C 氧化反应、取代反应、消去反应 加热、KOH醇溶液/加热、KOH水溶液/加热
D 消去反应、加成反应、水解反应 NaOH水溶液/加热、常温、NaOH醇溶液/加热
A.A B.B C.C D.D
11.下列除杂(括号内为杂质)方法正确的是
①FeCl2 (CuCl2):加入过量铁粉,过滤
②甲烷(乙烯):光照条件下通入Cl2,气液分离
③乙醇(水):加足量生石灰,蒸馏
④苯甲酸(氯化钠):将固体混合物在较高温下溶解,趁热过滤,再将滤液降温结晶,过滤、洗涤、干燥
A.①②③ B.②③④ C.①③④ D.①②④
12.如图所示的转化是合成抗组胺药物的中间过程之一,下列说法正确的是
A.L的分子式为 B.N可发生加成、消去、还原等反应
C.N中所有原子可能处于同一平面 D.L苯环上的一氯代物有4种
13.图中展示的是乙烯催化氧化的过程(部分相关离子未画出),下列描述不正确的是
A.和在反应中都是催化剂
B.该转化过程中,有非极性键的断裂与极性键的形成
C.该转化过程中,酸性条件下过程V涉及反应为
D.乙烯催化氧化的反应方程式为
14.下列说法正确的是
A.二环[1.1.0]丁烷()的二溴代物5种(不考虑立体异构)
B.的一溴代物有3种
C.与Br2按物质的量之比1:1发生加成反应,产物有4种
D.CH3CH2OH和具有相同的官能团,互为同系物
二、非选择题:共58分
15.(14分)Ⅰ.依据如图所示A~E的分子示意图填空。
(1)B的名称是___________。
(2)D的分子式为___________。
(3)最简单的饱和烃是___________(填字母序号,下同)。
(4)属于同一物质的是___________。
(5)上述分子中属于C的同系物的是___________。
Ⅱ.在①;②;③;④;⑤聚乙烯五种物质中:
(6)能与溴水发生化学反应是___________(填序号,下同)。
(7)属于高分子化合物的是___________。
(8)能与Na2CO3溶液反应的是___________。
(9)能发生酯化反应的是___________。
(10)能发生消去反应的是___________。
16.(14分)三乙氧基甲烷[HC(OC2H5)3]主要用作医药中间体和感光材料,氯仿(CHCl3)和乙醇钠(C2H5ON8,易溶于乙醇)在60℃~65℃的无水条件下反应可以制取三乙氧基甲烷并得到氯化钠。实验室模拟该制备的装置(夹持仪器省略)和步骤如下:
步骤①:将14.0g氯仿和过量乙醇加入圆底烧瓶中,磁力搅拌均匀;
步骤②:6.9g钠切成小块,加入反应器后不搅拌,保持钠浮在液面上反应;
步骤③:反应结束后过滤、无水乙醇洗涤,将洗涤液合并入滤液后进行操作I,得到纯净的三乙氧基甲烷。
已知:HC(OC2H5)3熔点-76℃,沸点146℃,密度约为0.9 g cm-3,能溶于乙醇等有机溶剂,遇明火、高热等有燃烧或爆炸危险。
按要求回答下列问题:
(1)写出实验中制备三乙氧基甲烷的总化学方程式_______。冷凝水应从_______端通入(填“a”或“b”)。
(2)乙醇过量的目的是_______。
(3)为保证反应持续进行,需控制一定温度,但反应过程中不需要加热,其原因是_______。
(4)步骤②操作目的是_______。
(5)步骤③中过滤后的固体为_______(填化学式),操作I的名称为_______。
(6)若收集到10.00mL三乙氧基甲烷,其产率为_______(保留三位有效数字)。
17.(16分)现有下列几种有机物:
①异丙烷 ②乙醇 ③苯 ④乙炔 ⑤聚-1,3-丁二烯
(1)能使酸性高锰酸钾溶液褪色的是_______(填序号);写出反式聚-1,3-丁二烯的结构简式_______。
(2)实验室制备乙炔的化学方程式为_______;已知端炔烃可发生偶联反应(Glaser反应);Glaser反应,若(分子式为),则有机物M的结构简式为_______,用1mol M与H2反应合成1,4-二苯基丁烷,理论上消耗H2_______mol。
(3)对溴苯乙烯(E)是一种重要的化工原料,以苯为原料制取E的流程如下:
已知:D中含有一个甲基
①E中含有官能团的名称为_______;A→B的反应类型为_______。
②写出D→E的化学方程式_______。
③芳香族化合物M是C的同分异构体,则M的结构有_______种(不考虑立体异构),其中核磁共振氢谱峰面积比为6:2:1的结构简式为_______(任意写一种)。
18.(14分)化合物X是一种香料,可采用乙烯与甲苯为主要原料,按下列路线合成:
已知:RCHO+CH3COOR′RCH=CHCOOR′
请回答:
(1)C中官能团的名称___________。
(2)B+D→F的化学反应类型为___________,该化学方程式___________。
(3)D→E的化学方程式___________。
(4)C→D的化学方程式___________。
(5)X的结构简式___________。
(6)下列化合物中属于F的同分异构体的是___________。
A.
B.
C.
D.
试卷第2页,共2页
答案
1.C
【详解】A.结构简式中不能省略C=C,所以乙烯的结构简式为CH2=CH2,A项错误;
B.碳化硅为原子晶体,其化学式为SiC,B项错误;
C.Cr为24号元素,核外电子排布半满结构稳定为[Ar]3d54s1,C项正确;
D.乙醇为CH3CH2OH,分子中含有3类氢原子,核磁共振氢谱中有三种峰,D项错误;
故选C。
2.C
【详解】A.一氯甲烷呈气态,苯甲醇、溴苯呈液态,所以一氯甲烷的熔点最低,A不正确;
B.常温常压下,CH3CH2Br呈液态,CH3CH3、CH3(CH2)2CH3呈气态,且CH3(CH2)2CH3的密度比CH3CH3大,所以密度:CH3CH2Br>CH3(CH2)2CH3>CH3CH3,B不正确;
C.常温下,丙三醇与水分子间能形成氢键,丙三醇与水互溶,苯酚微溶于水,而1-氯丁烷难溶于水,所以在水中的溶解度:丙三醇>苯酚>1-氯丁烷,C正确;
D.2,3-二甲基丁烷与2-甲基戊烷互为同分异构体,2,3-二甲基丁烷的支链比2-甲基戊烷多,则沸点:1-戊醇>2-甲基戊烷>2,3-二甲基丁烷>丙烷,D不正确;
故选C。
3.D
【详解】A.某有机物燃烧只生成CO2和H2O,二者物质的量相等,说明该有机物中C、H个数比为1∶2,符合形式有CnH2n、CnH2nO、CnH2nO2等,故A错误;
B.浓硫酸吸收的是水蒸气,烃燃烧前后气体体积也可能发生变化,因此烃在足量的氧气中燃烧并通过浓硫酸,减少的体积不一定是生成的水蒸气的体积,故B错误;
C.温度高于100℃,水为气体,根据CxHy+(x+)O2xCO2+H2O(g),如果反应前后气体体积不变,则1+(x+)=x+,解得y=4,若气体体积减少,则1+(x+)>x+,解得y<4,若气体体积增大,则1+(x+)<x+,解得y>4,故C错误;
D.C~O2~CO2,4H~O2~2H2O,消耗1mol氧气,需要12gC,需要4gH,可知有机物含氢量越大,等质量时消耗的氧气越多,故D正确;
答案为D。
4.C
【详解】A.电石遇水后,与水剧烈反应,且产生的Ca(OH)2易堵塞塑料板上的小孔,所以实验室不能用①装置制备乙炔,A不符合题意;
B.制备乙酸乙酯时,出气导管口应位于饱和Na2CO3溶液的液面上,②装置会产生倒吸,B不符合题意;
C.实验室制硝基苯时,应使用60℃左右的水浴加热,则③装置可用于实验室制硝基苯,C符合题意;
D.④装置中,与Na2CO3反应的酸为浓盐酸,易挥发出HCl气体,与苯酚钠直接反应,所以④装置不能用于判断碳酸与苯酚的酸性强弱,D不符合题意;
故选C。
5.D
【详解】A.的分子式为C8H8,与其互为同分异构体的芳香烃为苯乙烯,有1种,A错误;
B.为对称结构,如与硝酸反应,可生成5种一硝基取代物,B错误;
C.因分子存在三种不同的碳碳双键,如图所示,1分子物质与2分子Br2加成时,可以在①②的位置上发生加成,也可以在①③位置上发生加成,或在②③位置上发生加成,还可以消耗1分子Br2在①②发生1,4-加成反应、而另1分子Br2在③上加成,故所得产物共有四种,C错误;
D.分子式为C7H16的烃,分子中有4个甲基的同分异构体可看作正戊烷中间3个碳原子上的氢原子被2个甲基取代,2个甲基在同一碳原子有2种,在不同碳原子有2种,合计有4种,D正确;
故答案选D。
6.D
【详解】A.该物质含有酚羟基,遇FeCl3溶液显紫色,但与苯酚不互为同系物,A不正确;
B.连在苯环上的-CH3、酚-OH、碳碳双键,都能被酸性KMnO4溶液氧化,从而使KMnO4溶液紫色褪去,所以不能证明其结构中存在碳碳双键,B不正确;
C.酚羟基邻、对位上的H原子可以被Br原子取代,苯环、碳碳双键都能与H2发生加成反应,所以1mol该物质分别与足量浓溴水、H2反应时,最多消耗的Br2和H2的物质的量分别为5mol、7mol,C不正确;
D.由苯和乙烯原子的共平面,可推测 红框内的原子一定共平面,三个红框分别共用2个碳原子,所以三个红框内的碳原子也可能共平面,由此可推出,该分子中的所有碳原子可能共平面,D正确;
故选D。
7.D
【详解】A.该物质的名称为1,2,4-三甲苯,A项错误;
B.烯烃需要指出双键碳并使双键碳序号尽可能的小,该物质为3-甲基-2-戊烯,B项错误;
C.选择连羟基的最长的碳链为主链,该物质的名称为2-丁醇,C项错误;
D.把卤素原子当取代基,该物质为2-溴戊烷,D项正确;
故选D。
8.C
【详解】A.浓硫酸密度大,防止酸液飞溅,配置混酸时应将浓硫酸加入浓硝酸中,A错误;
B.制备硝基苯时反应温度应在50~60℃,为控制反应温度应该用水浴加热,B错误;
C.硝基苯不溶于水,分离硝基苯应该用分液的方法,C正确;
D.蒸馏硝基苯时,温度计水银球应该与支管口平齐,D错误;
故答案为:C。
9.D
【详解】A.苯和甲苯的密度都比水小,都不能与溴水反应,所以用溴水可以鉴别己烯,但不能鉴别苯和甲苯,故A错误;
B.黄色光会掩盖紫色光,所以焰色试验中直接观察到火焰为黄色,说明化合物中一定有钠元素,但不能确定是否含有钾元素,故B错误;
C.氯化镁溶液与氨水反应生成氢氧化镁白色沉淀和氯化铵,氢氧化铝是不能溶于氨水的两性氢氧化物,氯化铝溶液与氨水反应生成氢氧化铝白色沉淀和氯化铵,则用氨水不能鉴别氯化镁溶液和氯化铝溶液,故C错误;
D.2—溴丙烷分子中含有2类氢原子,核磁共振氢谱有2组峰,1—溴丙烷分子中含有3类氢原子,核磁共振氢谱有3组峰,则用核磁共振氢谱能鉴别2—溴丙烷和1—溴丙烷,故D正确;
故选D。
10.B
【详解】由CH3CH2CH2Br制备CH3CH(OH)CH2OH,先发生消去反应,得到丙烯,条件为NaOH的醇溶液、加热;再与卤素单质加成得到卤代烃,条件为卤素单质的四氯化碳溶液;最后水解得到目标产物,条件为NaOH的水溶液、加热,故选B。
11.C
【详解】①FeCl2 (CuCl2):加入过量铁粉,将CuCl2全部转化为FeCl2和Cu,过滤,滤液为FeCl2溶液,①正确;
②甲烷(乙烯):光照条件下通入Cl2,Cl2与甲烷发生取代反应,生成氯代甲烷和HCl,气液分离后得不到纯净的甲烷,②不正确;
③乙醇(水):加足量生石灰,与水反应生成氢氧化钙,蒸馏可得纯净的乙醇,③正确;
④苯甲酸(氯化钠):苯甲酸的溶解度随温度的升高而增大,氯化钠的溶解度受温度的影响不大,将固体混合物在较高温下溶解,趁热过滤,以防苯甲酸结晶析出,再将滤液降温结晶,过滤出苯甲酸,再洗涤、干燥,④正确;
通过以上分析可知,①③④正确,故选C。
12.B
【详解】A.由结构简式可知,L的分子式为C13H12O,故A错误;
B.由结构简式可知,N分子中含有的苯环能发生加成反应和还原反应,含有的氯原子能发生消去反应,故B正确;
C.由结构简式可知,N分子中含有空间构型为四面体形的饱和碳原子,分子中所有原子不可能处于同一平面,故C错误;
D.由结构简式可知,L苯环上有3类氢原子,一氯代物有3种,故D错误;
故选B。
13.A
【详解】A.过程V中消耗,过程IV中生成,不是催化剂,过程I消耗,过程IV生成,则是催化剂,A选项错误;
B.该转化过程中,有非极性键的断裂与极性键的形成,例如过程V:氧气分子中的非极性键断裂,生成水有极性键的形成(氢氧键),B选项正确;
C.该转化过程中,酸性条件下过程V是与氧气反应生成和水,涉及的反应为:,C选项正确;
D.乙烯被氧气最终催化氧化为,反应的方程式为:,D选项正确;
答案选A。
14.B
【详解】A.二环[1.1.0]丁烷()的二溴代物中,2个Br连在同一碳原子上只有1种,2个Br连在不同碳原子上共有3种,所以共有4种异构体(不考虑立体异构),A不正确;
B. 的一溴代物中溴原子可取代中①、②、③位置上的氢原子,则共有3种异构体,B正确;
C. 与Br2按物质的量之比1:1发生加成反应,只断裂1个碳碳双键的产物有3种,同时断裂2个碳碳双键、并形成1个碳碳双键(相当于发生1,4-加成)的产物有2种,所以与等摩Br2加成的产物有5种,C不正确;
D.CH3CH2OH和 具有相同种类的官能团,但官能团的数目不同,二者不互为同系物,D不正确;
故选B。
15.(1)乙烯
(2)
(3)A
(4)C E
(5)A
(6)①
(7)⑤
(8)④
(9)③④
(10)②③
【分析】由烃分子的示意图可知,A为甲烷、B为乙烯、C为丙烷、D为苯、E为丙烷。
【详解】(1)B的结构简式为CH2=CH2,B的名称是乙烯。故答案为:乙烯;
(2)D为苯,D的分子式为。故答案为:;
(3)甲烷分子中只有一个碳原子,最简单的饱和烃是A。故答案为:A;
(4)C为丙烷的结构简式,E为丙烷的球棍模型,属于同一物质的是C E。故答案为:C E;
(5)甲烷和丙烷同属于烷烃,分子组成上相差2个CH2原子团,上述分子中属于C的同系物的是A。故答案为:A;
(6)乙炔中有不饱和键,能与溴水发生化学反应是①。故答案为:①;
(7)分子量大于10000的化合物属于高分子化合物,属于高分子化合物的是⑤。故答案为:⑤;
(8)有机物中含有羧基或酚羟基能与Na2CO3溶液反应,能与Na2CO3溶液反应的是④。故答案为:④;
(9)含有羟基或羧基的有机物能发生酯化反应,能发生酯化反应的是③④。故答案为:③④;
(10)与-X或-OH相连的碳的邻碳上有氢,在一定条件下可发生消去反应,能发生消去反应的是②③。故答案为:②③。
16.(1) 2CHCl3+6CH3CH2OH+6Na→2HC(OC2H5)3+6NaCl+3H2↑ a
(2)增大反应物的接触面积,提高原料的利用率
(3)钠与乙醇的反应为放热反应
(4)有利于散热,防止温度升高引起爆炸
(5) NaCl 蒸馏
(6)51.9%
【分析】14.0g氯仿和过量乙醇混合后形成溶液;将切成小块的6.9g钠加入反应器后不搅拌,保持钠浮在液面上与乙醇反应,反应平稳进行,反应产生的热量及时散失;反应结束后过滤出不溶物NaCl,用无水乙醇洗涤,将洗涤液合并入滤液后进行蒸馏,得到纯净的三乙氧基甲烷。
【详解】(1)实验中,乙醇与钠反应生成乙醇钠和氢气,氯仿与乙醇钠反应制得三乙氧基甲烷等,总化学方程式为2CHCl3+6CH3CH2OH+6Na→2HC(OC2H5)3+6NaCl+3H2↑。为了保证冷却水能充满冷凝管,冷凝水应从a端通入。答案为:2CHCl3+6CH3CH2OH+6Na→2HC(OC2H5)3+6NaCl+3H2↑;a;
(2)乙醇过量,可使反应物充分溶解,增大接触面积,则目的是:增大反应物的接触面积,提高原料的利用率。答案为:增大反应物的接触面积,提高原料的利用率;
(3)为保证反应持续进行,需控制一定温度,但反应过程中不需要加热,其原因是:钠与乙醇的反应为放热反应。答案为:钠与乙醇的反应为放热反应;
(4)HC(OC2H5)3熔点-76℃,沸点146℃,能溶于乙醇等有机溶剂,遇明火、高热等有燃烧或爆炸危险,则步骤②操作目的是:有利于散热,防止温度升高引起爆炸。答案为:有利于散热,防止温度升高引起爆炸;
(5)反应结束后过滤、无水乙醇洗涤,将洗涤液合并入滤液后进行操作I,得到纯净的三乙氧基甲烷,因为NaCl难溶于乙醇,所以步骤③中过滤后的固体为NaCl,操作I是从混合液中分离出HC(OC2H5)3,名称为蒸馏。答案为:NaCl;蒸馏。
(6)三乙氧基甲烷体积为10.00mL,密度约为0.9 g cm-3,氯仿质量为14.0g,则CHCl3——HC(OC2H5)3,可求出理论上生成HC(OC2H5)3的质量为,则
HC(OC2H5)3的产率为≈51.9%。答案为:51.9%。
【点睛】产率=。
17.(1) ②④⑤
(2) CaC2+2H2O→Ca(OH)2+CH≡CH↑ 4
(3) 碳碳双键、碳溴键 取代反应 +NaOH+NaBr+H2O 13 、
【分析】由E的结构简式,可确定A为,B为,C为,D为。
【详解】(1)②乙醇、④乙炔、⑤聚-1,3-丁二烯都能使酸性高锰酸钾溶液褪色,故选②④⑤;反式聚-1,3-丁二烯的结构简式为。答案为:②④⑤;;
(2)实验室以电石与水反应制备乙炔,化学方程式为CaC2+2H2O→Ca(OH)2+CH≡CH↑;若(分子式为),则有机物M的结构简式为,用1mol M与H2反应合成1,4-二苯基丁烷,则需将2mol碳碳三键转化为碳碳单键,理论上消耗H24mol。答案为:CaC2+2H2O→Ca(OH)2+CH≡CH↑;;4;
(3)①E的结构简式为,含有官能团的名称为碳碳双键、碳溴键;A()与CH3CH2Br在AlCl3催化作用下发生反应→B()和HBr,反应类型为取代反应。
②D()发生消去反应→E()等,化学方程式+NaOH+NaBr+H2O。
③芳香族化合物M是C的同分异构体,C为,则M的结构可能为:含苯环和1个取代基-CH2CH2Br或-CHBrCH3(2种);含苯环和2个取代基-Br、-CH2CH3(邻位或间位)或-CH2Br、-CH3(邻、间、对)(5种);含苯环、-Br、2个-CH3,共有6种异构体,所以,共有13种,其中核磁共振氢谱峰面积比为6:2:1的结构简式为、。答案为:碳碳双键、碳溴键;取代反应;+NaOH+NaBr+H2O;13;、。
【点睛】合成有机物时,可采用逆推法。
18.(1)氯原子或碳氯键
(2) 取代反应或酯化反应 CH3COOH++H2O
(3)2+O22+2H2O
(4)+NaOH+NaCl
(5)
(6)BC
【分析】乙烯与水发生加成反应,生成乙醇,即A的结构简式为CH3CH2OH,乙醇连续氧化成乙酸,根据B的分子式,B的结构简式为CH3COOH,甲苯与氯气在光照条件下,发生取代反应,氯原子取代甲基上的氢原子,即C的结构简式为,C在氢氧化钠水溶液中发生水解反应,得到D,D的结构简式为,B与D发生酯化反应,即F的结构简式为,根据E的分子式,E为醛,结构简式为,根据题中所给信息,X结构简式为,
据此分析;
【详解】(1)根据上述分析,C的结构简式为,所含官能团为碳氯键;故答案为碳氯键;
(2)根据上述分析,B+D→F的反应的类型为取代反应或酯化反应;该反应方程式为CH3COOH++H2O;故答案为取代反应或酯化反应;CH3COOH++H2O;
(3)D的结构简式为,E的结构简式为,D→E发生氧化反应,其反应方程式为2+O22+2H2O;故答案为2+O22+2H2O;
(4)C→D的反应类型为水解反应,其反应方程式为+NaOH+NaCl;故答案为+NaOH+NaCl;
(5)根据上述分析,X的结构简式为;故答案为;
(6)根据上述分析,F的结构简式为,
A.F的结构简式为C9H10O2,题中所给结构简式的分子式为C10H12O2,两者分子式不同,不属于同分异构体,故A不符合题意;
B.分子式为C9H10O2,与F的结构简式不同,因此两者互为同分异构体,故B符合题意;
C.分子式为C9H10O2,与F的结构简式不同,因此两者互为同分异构体,故C符合题意;
D.题中所给有机物的分子式为C10H12O2,两者分子式不同,不属于同分异构体,故D不符合题意;
答案为BC。
同课章节目录
