实验活动6 酸、碱的化学性质 课时作业 (含解析)
文档属性
| 名称 | 实验活动6 酸、碱的化学性质 课时作业 (含解析) |
|
|
| 格式 | zip | ||
| 文件大小 | 180.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-15 00:00:00 | ||
图片预览




文档简介
实验活动6 酸、碱的化学性质 课时作业
一、单选题
1.在托盘天平两边各放一只质量相等的烧杯,内盛等质量、等溶质质量分数的足量的稀盐酸。将质量相等的石灰石和熟石灰分别放入天平的左盘和右盘的烧杯中,反应完毕后,天平会向哪一边倾斜
A.右边 B.左边 C.不倾斜,仍然平衡 D.无法确定
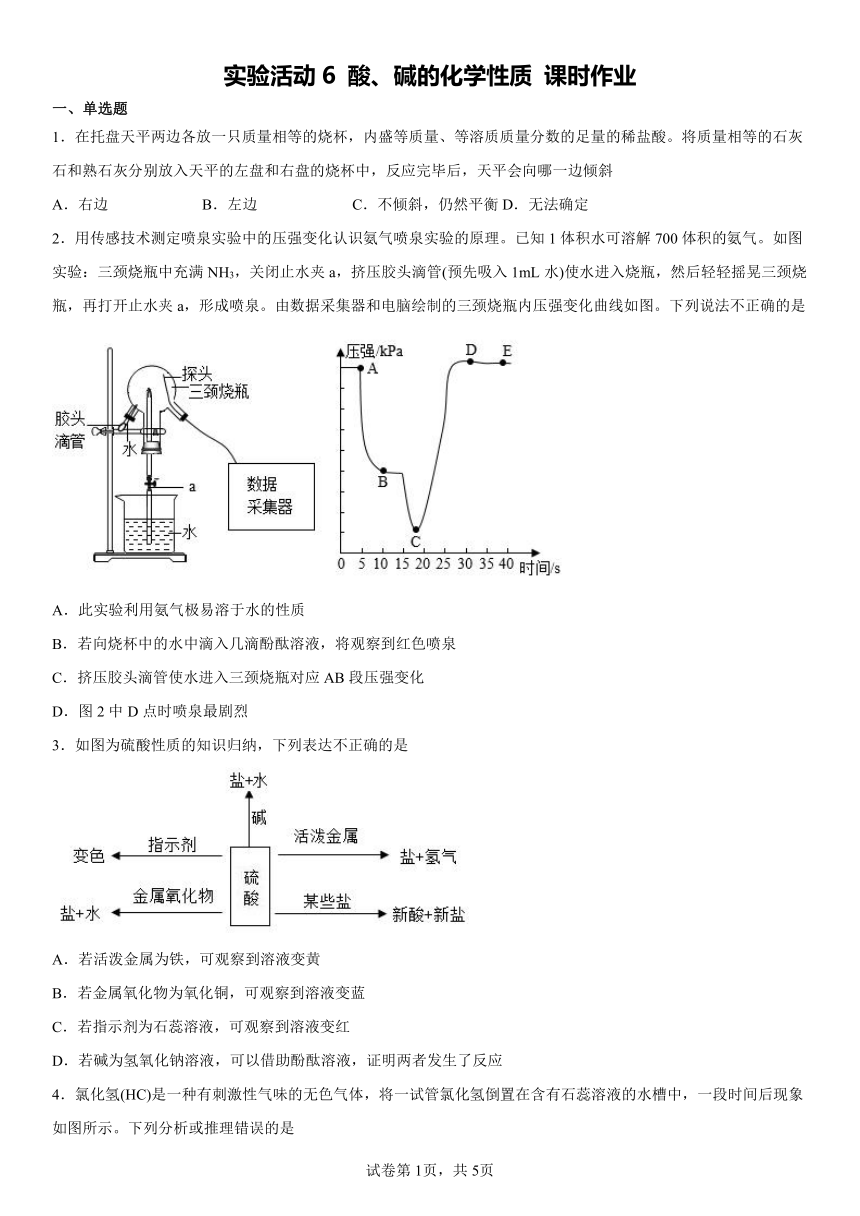
2.用传感技术测定喷泉实验中的压强变化认识氨气喷泉实验的原理。已知1体积水可溶解700体积的氨气。如图实验:三颈烧瓶中充满NH3,关闭止水夹a,挤压胶头滴管(预先吸入1mL水)使水进入烧瓶,然后轻轻摇晃三颈烧瓶,再打开止水夹a,形成喷泉。由数据采集器和电脑绘制的三颈烧瓶内压强变化曲线如图。下列说法不正确的是
A.此实验利用氨气极易溶于水的性质
B.若向烧杯中的水中滴入几滴酚酞溶液,将观察到红色喷泉
C.挤压胶头滴管使水进入三颈烧瓶对应AB段压强变化
D.图2中D点时喷泉最剧烈
3.如图为硫酸性质的知识归纳,下列表达不正确的是
A.若活泼金属为铁,可观察到溶液变黄
B.若金属氧化物为氧化铜,可观察到溶液变蓝
C.若指示剂为石蕊溶液,可观察到溶液变红
D.若碱为氢氧化钠溶液,可以借助酚酞溶液,证明两者发生了反应
4.氯化氢(HC)是一种有刺激性气味的无色气体,将一试管氯化氢倒置在含有石蕊溶液的水槽中,一段时间后现象如图所示。下列分析或推理错误的是
A.HCl不能用排水法集 B.乙中液体变红
C.乙中试管剩余气体气压小于大气压 D.将甲中HCl替换为NH3,现象相同
5.从物质的组成角度解释酸具有相似化学性质的原因是
A.酸都能在水中电离出H+ B.酸都含有酸根
C.酸中都含有氢气 D.酸中都含有氧元素
6.下列化学方程式与事实相符且正确的是( )
A.碳在氧气中完全燃烧
B.用足量澄清石灰水检验二氧化碳:
C.铝在空气中发生反应,其表面生成一层致密的氧化铝薄膜:
D.稀盐酸除铁锈反应:
7.某同学将一块石灰石高温煅烧一段时间后,欲证明是否有氧化钙生成,最简单的方法是
A.直接加水 B.滴加稀盐酸 C.冷却后加水 D.滴加稀硫酸
8.中考复习阶段,某同学梳理了以下知识:①碎鸡蛋壳中加入食盐水制二氧化碳;②分子可分,原子不可分;③煮沸可以降低井水的硬度;④在置换反应时,一定有元素化合价改变;⑤称量NaOH固体时托盘天平两端各放一张大小相同的纸片;⑥向某固体上滴加稀盐酸,有气泡产生,则该固体一定是碳酸盐; 以上说法正确的个数是
A.2 B.3 C.4 D.5
9.食醋是厨房中常用的调味品,它的土要成分是乙酸。已知乙酸的化学式为CH3COOH,则下列说法正确的是
A.乙酸是由碳、氢、氧三个元素组成的
B.乙酸的相对分子质量为60g
C.乙酸中碳元素的质量分数最大
D.乙酸可以除铁锈
10.对下列课外实验活动的叙述,不正确的是
A.用小卵石、活性炭和细沙等物品可制作简易净水器
B.物质的结构决定性质,性质决定用途;反之用途反映性质,性质反映结构
C.利用柠檬酸具有酸的性质,可在碳酸氢钠溶液中加入柠檬酸制汽水
D.将少量高锰酸钾晶体放入汽油中振荡,可形成紫红色的溶液
11.下列关于盐酸性质的叙述中不正确的是( )
A.盐酸能使紫色石蕊试液变红
B.开启浓盐酸的瓶盖会冒出白雾
C.稀盐酸和铁锈反应生成浅绿色溶液
D.浓盐酸是无色、有刺激性气味的液体
12.下列实验现象描述正确的是
A.细铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁
B.往稀盐酸中滴加紫色石蕊试剂,稀盐酸变红色
C.电解水实验中,正极上产生的气体使带火星的木条复燃
D.往氯化铜溶液中滴加氢氧化钠溶液,产生红褐色沉淀
二、填空题
13.(1)如图是某品牌矿泉水包装上的部分信息。
用化学符号填空:
碳酸根离子______。2个镁离子______。氯离子______。水分子______。钾原子______。
(2)①房屋装修后,可在室内放一些活性炭来吸收装修材料释放出的甲醛、苯等有毒气体,这是利用活性炭的______性。
②如图所示的“火立熄”是一种新型的家用灭火用品。“火立熄”接触到火焰3-5秒后炸开,释放的粉末覆盖在燃烧物上,同时放出不可燃烧气体,使火焰熄灭。“火立熄”的灭火原理是______。(填标号)
A.清除可燃物 B.使燃烧物与氧气隔绝 C.降低燃烧物的着火点
③打火机给人们的生活带来了方便,如图为普通打火机的示意图,请根据如图回答下列问题:
a.属于金属材料的是______。(填序号)
b.打火机偶然未打着火时会闻到一股异味,说明分子具有______性质。
(3)汽车是现代生活中常见的一种交通工具。
①漆可以延缓汽车钢铁外壳的锈蚀,其防锈原理是隔绝______和______。
②CNG双燃料环保汽车已在成都投入使用,这种汽车所用的燃料是汽油和压缩天然气。写出天然气完全燃烧的化学方程式______。
(4)①镁在空气中燃烧时,能发出耀眼的白光,可用来制造镁闪光灯,其反应的化学方程式为______。
②市场上出售的补血麦片中常含微量颗粒细小的铁粉,是因为铁粉与人体胃液中的盐酸反应,起到补血的作用,写出这个反应的化学方程式______。
③工厂师傅在切割钢板时,常用硫酸铜溶液画线,是因为______(用化学方程式表示)。
14.构建知识网络,可以帮助我们理解知识间的内在联系,如图是氢氧化钠与不同类别物质之间反应的知识网络。
(1)图中A应为____________类物质,写出一个符合要求的反应方程式____________。
(2)写出一种能与氢氧化钠反应生成蓝色沉淀的盐____________。
(3)氢氧化钠能与酸反应的实质是氢氧化钠中的____________(写离子符号,下同)与酸中的____________反应生成H2O。
三、推断题
15.A-F是初中化学常见的六种物质,分别由C、H、O、C1、Ca中的一种或几种元素组成。已知A固体可用于人工降雨;B是可燃性气体,燃烧能生成A;化合物C、D、E中含有相同的金属元素,且存在如下转化关系C→D→E;F可与E发生反应生成A,回答下列问题:
(1)A的化学式为_____。
(2)B中一定含有的元素是_____。
(3)写出F与E发生反应的化学方程式_____。
四、实验题
16.分类、类比推理是学习化学的重要方法。
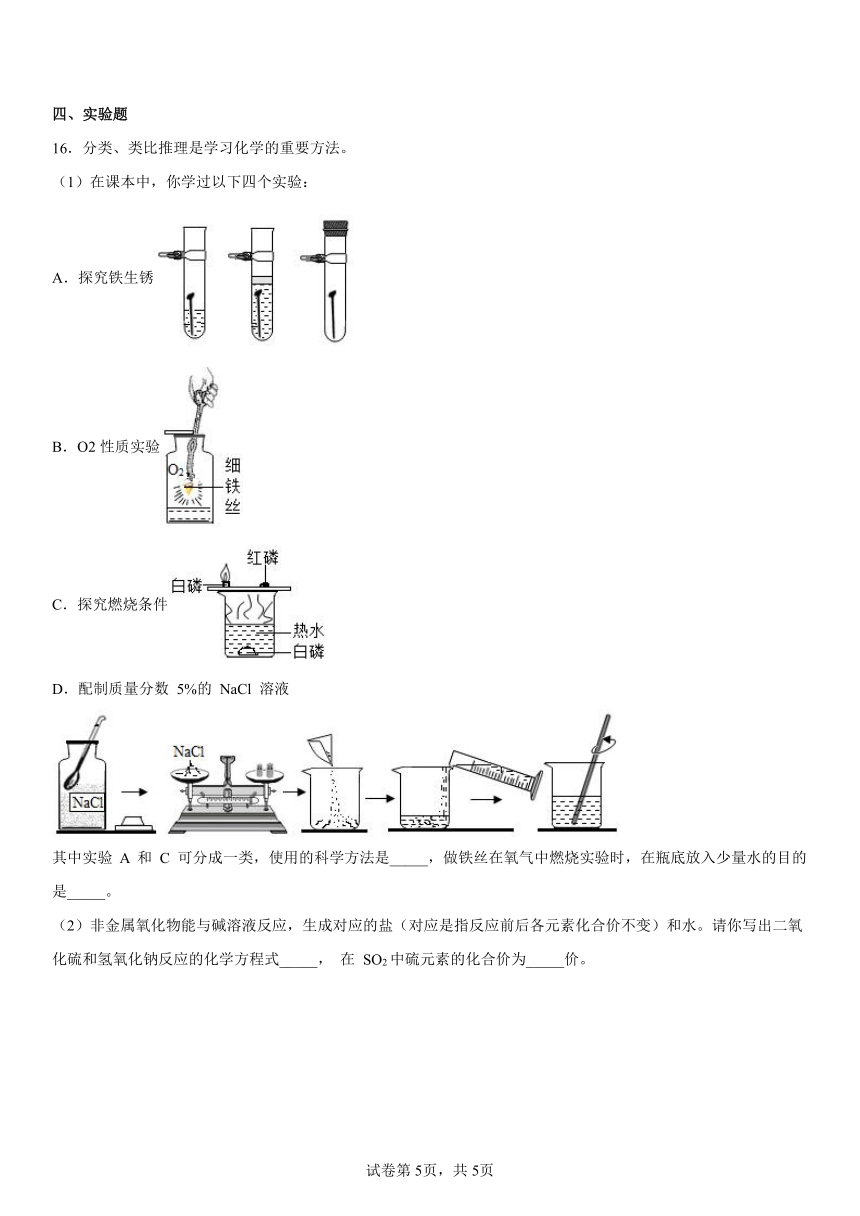
(1)在课本中,你学过以下四个实验:
A.探究铁生锈
B.O2性质实验
C.探究燃烧条件
D.配制质量分数 5%的 NaCl 溶液
其中实验 A 和 C 可分成一类,使用的科学方法是_____,做铁丝在氧气中燃烧实验时,在瓶底放入少量水的目的是_____。
(2)非金属氧化物能与碱溶液反应,生成对应的盐(对应是指反应前后各元素化合价不变)和水。请你写出二氧化硫和氢氧化钠反应的化学方程式_____, 在 SO2中硫元素的化合价为_____价。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
【详解】左边石灰石和稀盐酸反应生成氯化钙、水和二氧化碳,右边熟石灰和稀盐酸反应生成氯化钙和水,左边生成的二氧化碳气体会逸散到空气中,质量减少,故天平会往右边倾斜。
故选:A。
2.D
【详解】A.此实验利用氨气极易溶于水的性质,氨气溶于水瓶内压强变小,所以形成喷泉,正确。
B.若向烧杯中的水中滴入几滴酚酞溶液,将观察到红色喷泉,因为氨气能与水反应生成显碱性的氨水,正确。
C.挤压胶头滴管使水进入三颈烧瓶对应AB段压强变化,因为氨气溶于水瓶内压强变小,正确。
D.图2中C点时喷泉最剧烈,压强差越大,喷泉越剧烈,选项错误。
故选:D。
3.A
【详解】A、铁和稀硫酸反应生成硫酸亚铁和氢气,硫酸亚铁溶液呈浅绿色,故A错误;
B、氧化铜和硫酸反应生成硫酸铜和水,硫酸铜溶液呈蓝色,故B正确;
C、硫酸呈酸性,能够使紫色石蕊试液变红色,故C正确;
D、硫酸和氢氧化钠反应无明显现象,可在氢氧化钠中加入适量酚酞,此时溶液呈红色,然后滴入适量硫酸,可观察到溶液逐渐由红色变为无色,可证明硫酸和氢氧化钠发生了反应,故D正确;
故选A。
4.D
【详解】A、HCl易溶于水,不能用排水法集,正确;
B、HCl溶于水显酸性,石蕊遇酸变红,正确;
C、乙中试管剩余气体气压加试管内液体的压强等于大气压,故乙中试管剩余气体气压小于大气压 ,正确;
D、NH3溶于水显碱性,液体会变蓝,现象不同,错误;
故选D。
5.A
【详解】A、在不同的酸溶液中都含有H+,所以,酸具有一些相似的化学性质,符合题意;
B、酸都含有酸根,但不同的酸中,所含酸根的种类也不同,与酸具有相似的化学性质无关,不符合题意;
C、酸中都含有氢元素,而不是氢气,不符合题意;
D、酸中不一定都含有氧元素,如HCl,不符合题意。
故选A。
6.B
【详解】A、碳在氧气中完全燃烧生成二氧化碳,正确的化学方程式应为,错误;
B、澄清石灰水检验二氧化碳生成碳酸钙和水,该化学方程式书写完全正确,正确;
C、化学方程式配平错误,正确的化学方程式应为,错误;
D、铁锈主要成分为氧化铁,氧化铁和盐酸反应生成氯化铁和水,,错误;
故选B。
7.C
【详解】A、将一块石灰石高温煅烧一段时间后,温度较高,直接加水不能证明热量是氧化钙与水反应生成的,不能证明有氧化钙生成,故错误;
B、碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳气体,氧化钙与盐酸反应生成氯化钙和水,若有氧化钙生成,也无明显变化,滴加稀盐酸不能证明有氧化钙生成,故错误;
C、冷却后加水,若有氧化钙生成,氧化钙与水反应生成氢氧化钙,该反应放出大量的热,说明有氧化钙生成,故正确;
D、碳酸钙与稀硫酸反应生成硫酸钙、水和二氧化碳气体,氧化钙与硫酸反应生成硫酸钙和水,若有氧化钙生成,也无明显变化,滴加稀硫酸不能证明有氧化钙生成,故错误。
故选C。
8.A
【详解】①鸡蛋壳的主要成分是碳酸钙,不能与食盐水反应,不能用碎鸡蛋壳中加入食盐水的方法制二氧化碳,故说法错误。
②分子可分,原子也可以再分,原子可分为原子核和电子,故说法错误。
③煮沸,能除去一些水中的可溶性钙镁化合物,可以降低井水的硬度,故说法正确。
④置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,单质中元素的化合价为0、在化合物中正负化合价的代数和为零,则在置换反应时,一定有元素化合价改变,故说法正确。
⑤氢氧化钠具有腐蚀性,应放在玻璃器皿中称量,不能放在纸片上称量,故说法错误。
⑥碳酸盐与酸反应放出气体,但与酸反应放出气体的物质不一定是碳酸盐,也可能是活泼金属等,故说法错误。
故说法正确的个数是2个。
故选:A。
9.D
【详解】A、由化学式可知,乙酸是由C、H、O三种元素组成的,元素是宏观概念,不能论个数,不符合题意;
B、乙酸的相对分子质量为:12×2+4+16×2=60,相对分子质量是一个比值,单位为“1”,常省略不写,不符合题意;
C、乙酸中碳、氢、氧三种元素的质量比为:(12×2):4:(16×2)=6:1:8,故氧元素的质量分数最大,不符合题意;
D、乙酸显酸性,能与氧化铁反应生成乙酸铁和水,可以除去铁锈,符合题意。
故选D。
10.D
【详解】A、由于小卵石和细沙能起到过滤的作用,可以除去一些难溶性杂质,而活性炭具有吸附性,可以除去一些可溶性的杂质、异味、色素等,故A正确;
B、物质结构决定物质的性质,性质决定物质的用途,反之物质用途反映性质,性质反映结构,故B正确;
C、由于碳酸氢钠溶液中有碳酸根离子,若柠檬酸有酸性,它们混合以后就会有气泡冒出,故C正确;
D、高锰酸钾不会溶于汽油,因此不会形成溶液,故D错误;
故选D。
11.C
【详解】A、盐酸呈酸性,能使紫色石蕊试液变红,正确;
B、浓盐酸具有挥发性,开启浓盐酸的瓶盖会冒出白雾,正确;
C、稀盐酸和铁锈中氧化铁反应生成氯化铁溶液,显黄色,错误;
D、浓盐酸是无色、有刺激性气味的液体,正确;
故选C。
12.C
【详解】A、细铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体,说法不正确;
B、酸能使紫色石蕊试剂变红,不是稀盐酸变红,说法不正确;
C、电解水实验中,正极上产生的气体是氧气,氧气能使带火星的木条复燃,说法正确;
D、往氯化铜溶液中滴加氢氧化钠溶液,氯化铜和氢氧化钠反应生成氢氧化铜蓝色沉淀,说法不正确。
故选C。
13. CO Mg2+ Cl- H2O K 吸附 B ②⑤ 不断运动 氧气 水
【详解】(1)1个碳酸根离子带2个单位负电荷,CO 。
1个镁离子带2个单位正电荷,2个镁离子Mg2+。
1个氯离子带1个单位负电荷Cl-。
1个水分子中含有2个氢原子、1个氧原子,H2O。
钾原子K。
(2)①活性炭具有吸附性,可以吸收装修材料释放出的甲醛、苯等有毒气体。
②A、可燃物没有被清除,错误;
B、释放的粉末覆盖在燃烧物上,同时放出不可燃烧气体,使燃烧物与氧气隔绝,正确;
C、燃烧物的着火点不能被降低,错误。
故选B。
③a、金属材料有合金和纯金属;故属于金属材料的是②铜丝、⑤铁。
b、打火机偶然未打着火时会闻到一股异味,说明分子具有是不断运动的,运动到人周围被闻到。
(3)①铁生锈是铁与氧气和水共同作用的结果;漆可以延缓汽车钢铁外壳的锈蚀,其防锈原理是隔绝氧气和水。
②甲烷和氧气点燃生成水和二氧化碳,。
(4)①镁和氧气点燃生成氧化镁,。
②铁和盐酸反应生成氯化亚铁和氢气,。
③铁和硫酸铜生成铜和硫酸亚铁,。
14. 非金属氧化物 硫酸铜(合理都对)
【详解】(1)能与碱发生化学反应的物质类别有:酸碱指示剂、非金属氧化物、酸、盐。与题给氢氧化钠与不同类别物质之间反应的知识网络对比可知,A应该是非金属氧化物,符合要求的化学方程式例如氢氧化钠和二氧化碳反应生成碳酸钠和水,化学方程式为:。
(2)蓝色沉淀物只有Cu(OH)2,属于碱。氢氧化钠也是碱,根据碱能与盐发生复分解反应反应,生成新碱和新盐,可以判断氢氧化钠与可溶性铜盐反应,可以生成氢氧化铜,可溶性的铜盐有Cu(NO3)2、CuCl2、CuSO4。
(3)氢氧化钠与酸发生中和反应,中和反应的实质是H+与OH-生成H2O。据此判断,氢氧化钠能与酸反应的实质是氢氧化钠中OH-的与酸中H+反应生成H2O。
15. CO2 碳
【分析】A~F 是初中化学常见的6种物质,分别由C、H、O、Cl、Ca中的一种或几种元素组成。已知A固体可用于人工降雨,所以A为二氧化碳;B是可燃性气体,燃烧能生成A,据质量守恒定律可知反应前后元素的种类不变,所以B中一定含有碳元素;可能含有的元素是氢或氧;化合物C、D、E中含有相同的金属元素,所以C、D、E都是含钙元素的化合物,且存在如下转化关系C→D→E,氧化钙和水反应生成氢氧化钙,氢氧化钙和二氧化碳反应生成碳酸钙,所以C为氧化钙,D为氢氧化钙,E为碳酸钙;盐酸能与碳酸钙反应生成二氧化碳,所以F为盐酸;代入物质关系中推测正确;
【详解】根据分析得:
(1)二氧化碳A的化学式为CO2;
(2)B中一定含有的元素是碳元素;
(3)碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳气体,。
16. 控制变量 防止集气瓶底炸裂 SO2+2NaOH=Na2SO3+H2O +4
【详解】(1)实验中AC是通过控制变量研究铁生锈的因素和燃烧的条件;B是研究氧气的化学性质;D是配制溶液的操作;故实验 A 和 C 可分成一类,使用的科学方法是控制变量;铁丝在氧气中燃烧放出大量的热,在瓶底放入少量水的目的是防止生成物溅落炸裂集气瓶;
(2)题干提供,非金属氧化物能与碱溶液反应,生成对应的盐(对应是指反应前后各元素化合价不变)和水。二氧化硫中氧元素化合价为负二价,设硫元素化合价为x,化合物中正负化合价代数和为零;则x+(-2)×2=0,x=+4;那么二氧化硫和氢氧化钠反应生成硫元素化合价为正四价的钠盐Na2SO3和水,SO2+2NaOH=Na2SO3+H2O。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.在托盘天平两边各放一只质量相等的烧杯,内盛等质量、等溶质质量分数的足量的稀盐酸。将质量相等的石灰石和熟石灰分别放入天平的左盘和右盘的烧杯中,反应完毕后,天平会向哪一边倾斜
A.右边 B.左边 C.不倾斜,仍然平衡 D.无法确定
2.用传感技术测定喷泉实验中的压强变化认识氨气喷泉实验的原理。已知1体积水可溶解700体积的氨气。如图实验:三颈烧瓶中充满NH3,关闭止水夹a,挤压胶头滴管(预先吸入1mL水)使水进入烧瓶,然后轻轻摇晃三颈烧瓶,再打开止水夹a,形成喷泉。由数据采集器和电脑绘制的三颈烧瓶内压强变化曲线如图。下列说法不正确的是
A.此实验利用氨气极易溶于水的性质
B.若向烧杯中的水中滴入几滴酚酞溶液,将观察到红色喷泉
C.挤压胶头滴管使水进入三颈烧瓶对应AB段压强变化
D.图2中D点时喷泉最剧烈
3.如图为硫酸性质的知识归纳,下列表达不正确的是
A.若活泼金属为铁,可观察到溶液变黄
B.若金属氧化物为氧化铜,可观察到溶液变蓝
C.若指示剂为石蕊溶液,可观察到溶液变红
D.若碱为氢氧化钠溶液,可以借助酚酞溶液,证明两者发生了反应
4.氯化氢(HC)是一种有刺激性气味的无色气体,将一试管氯化氢倒置在含有石蕊溶液的水槽中,一段时间后现象如图所示。下列分析或推理错误的是
A.HCl不能用排水法集 B.乙中液体变红
C.乙中试管剩余气体气压小于大气压 D.将甲中HCl替换为NH3,现象相同
5.从物质的组成角度解释酸具有相似化学性质的原因是
A.酸都能在水中电离出H+ B.酸都含有酸根
C.酸中都含有氢气 D.酸中都含有氧元素
6.下列化学方程式与事实相符且正确的是( )
A.碳在氧气中完全燃烧
B.用足量澄清石灰水检验二氧化碳:
C.铝在空气中发生反应,其表面生成一层致密的氧化铝薄膜:
D.稀盐酸除铁锈反应:
7.某同学将一块石灰石高温煅烧一段时间后,欲证明是否有氧化钙生成,最简单的方法是
A.直接加水 B.滴加稀盐酸 C.冷却后加水 D.滴加稀硫酸
8.中考复习阶段,某同学梳理了以下知识:①碎鸡蛋壳中加入食盐水制二氧化碳;②分子可分,原子不可分;③煮沸可以降低井水的硬度;④在置换反应时,一定有元素化合价改变;⑤称量NaOH固体时托盘天平两端各放一张大小相同的纸片;⑥向某固体上滴加稀盐酸,有气泡产生,则该固体一定是碳酸盐; 以上说法正确的个数是
A.2 B.3 C.4 D.5
9.食醋是厨房中常用的调味品,它的土要成分是乙酸。已知乙酸的化学式为CH3COOH,则下列说法正确的是
A.乙酸是由碳、氢、氧三个元素组成的
B.乙酸的相对分子质量为60g
C.乙酸中碳元素的质量分数最大
D.乙酸可以除铁锈
10.对下列课外实验活动的叙述,不正确的是
A.用小卵石、活性炭和细沙等物品可制作简易净水器
B.物质的结构决定性质,性质决定用途;反之用途反映性质,性质反映结构
C.利用柠檬酸具有酸的性质,可在碳酸氢钠溶液中加入柠檬酸制汽水
D.将少量高锰酸钾晶体放入汽油中振荡,可形成紫红色的溶液
11.下列关于盐酸性质的叙述中不正确的是( )
A.盐酸能使紫色石蕊试液变红
B.开启浓盐酸的瓶盖会冒出白雾
C.稀盐酸和铁锈反应生成浅绿色溶液
D.浓盐酸是无色、有刺激性气味的液体
12.下列实验现象描述正确的是
A.细铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁
B.往稀盐酸中滴加紫色石蕊试剂,稀盐酸变红色
C.电解水实验中,正极上产生的气体使带火星的木条复燃
D.往氯化铜溶液中滴加氢氧化钠溶液,产生红褐色沉淀
二、填空题
13.(1)如图是某品牌矿泉水包装上的部分信息。
用化学符号填空:
碳酸根离子______。2个镁离子______。氯离子______。水分子______。钾原子______。
(2)①房屋装修后,可在室内放一些活性炭来吸收装修材料释放出的甲醛、苯等有毒气体,这是利用活性炭的______性。
②如图所示的“火立熄”是一种新型的家用灭火用品。“火立熄”接触到火焰3-5秒后炸开,释放的粉末覆盖在燃烧物上,同时放出不可燃烧气体,使火焰熄灭。“火立熄”的灭火原理是______。(填标号)
A.清除可燃物 B.使燃烧物与氧气隔绝 C.降低燃烧物的着火点
③打火机给人们的生活带来了方便,如图为普通打火机的示意图,请根据如图回答下列问题:
a.属于金属材料的是______。(填序号)
b.打火机偶然未打着火时会闻到一股异味,说明分子具有______性质。
(3)汽车是现代生活中常见的一种交通工具。
①漆可以延缓汽车钢铁外壳的锈蚀,其防锈原理是隔绝______和______。
②CNG双燃料环保汽车已在成都投入使用,这种汽车所用的燃料是汽油和压缩天然气。写出天然气完全燃烧的化学方程式______。
(4)①镁在空气中燃烧时,能发出耀眼的白光,可用来制造镁闪光灯,其反应的化学方程式为______。
②市场上出售的补血麦片中常含微量颗粒细小的铁粉,是因为铁粉与人体胃液中的盐酸反应,起到补血的作用,写出这个反应的化学方程式______。
③工厂师傅在切割钢板时,常用硫酸铜溶液画线,是因为______(用化学方程式表示)。
14.构建知识网络,可以帮助我们理解知识间的内在联系,如图是氢氧化钠与不同类别物质之间反应的知识网络。
(1)图中A应为____________类物质,写出一个符合要求的反应方程式____________。
(2)写出一种能与氢氧化钠反应生成蓝色沉淀的盐____________。
(3)氢氧化钠能与酸反应的实质是氢氧化钠中的____________(写离子符号,下同)与酸中的____________反应生成H2O。
三、推断题
15.A-F是初中化学常见的六种物质,分别由C、H、O、C1、Ca中的一种或几种元素组成。已知A固体可用于人工降雨;B是可燃性气体,燃烧能生成A;化合物C、D、E中含有相同的金属元素,且存在如下转化关系C→D→E;F可与E发生反应生成A,回答下列问题:
(1)A的化学式为_____。
(2)B中一定含有的元素是_____。
(3)写出F与E发生反应的化学方程式_____。
四、实验题
16.分类、类比推理是学习化学的重要方法。
(1)在课本中,你学过以下四个实验:
A.探究铁生锈
B.O2性质实验
C.探究燃烧条件
D.配制质量分数 5%的 NaCl 溶液
其中实验 A 和 C 可分成一类,使用的科学方法是_____,做铁丝在氧气中燃烧实验时,在瓶底放入少量水的目的是_____。
(2)非金属氧化物能与碱溶液反应,生成对应的盐(对应是指反应前后各元素化合价不变)和水。请你写出二氧化硫和氢氧化钠反应的化学方程式_____, 在 SO2中硫元素的化合价为_____价。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
【详解】左边石灰石和稀盐酸反应生成氯化钙、水和二氧化碳,右边熟石灰和稀盐酸反应生成氯化钙和水,左边生成的二氧化碳气体会逸散到空气中,质量减少,故天平会往右边倾斜。
故选:A。
2.D
【详解】A.此实验利用氨气极易溶于水的性质,氨气溶于水瓶内压强变小,所以形成喷泉,正确。
B.若向烧杯中的水中滴入几滴酚酞溶液,将观察到红色喷泉,因为氨气能与水反应生成显碱性的氨水,正确。
C.挤压胶头滴管使水进入三颈烧瓶对应AB段压强变化,因为氨气溶于水瓶内压强变小,正确。
D.图2中C点时喷泉最剧烈,压强差越大,喷泉越剧烈,选项错误。
故选:D。
3.A
【详解】A、铁和稀硫酸反应生成硫酸亚铁和氢气,硫酸亚铁溶液呈浅绿色,故A错误;
B、氧化铜和硫酸反应生成硫酸铜和水,硫酸铜溶液呈蓝色,故B正确;
C、硫酸呈酸性,能够使紫色石蕊试液变红色,故C正确;
D、硫酸和氢氧化钠反应无明显现象,可在氢氧化钠中加入适量酚酞,此时溶液呈红色,然后滴入适量硫酸,可观察到溶液逐渐由红色变为无色,可证明硫酸和氢氧化钠发生了反应,故D正确;
故选A。
4.D
【详解】A、HCl易溶于水,不能用排水法集,正确;
B、HCl溶于水显酸性,石蕊遇酸变红,正确;
C、乙中试管剩余气体气压加试管内液体的压强等于大气压,故乙中试管剩余气体气压小于大气压 ,正确;
D、NH3溶于水显碱性,液体会变蓝,现象不同,错误;
故选D。
5.A
【详解】A、在不同的酸溶液中都含有H+,所以,酸具有一些相似的化学性质,符合题意;
B、酸都含有酸根,但不同的酸中,所含酸根的种类也不同,与酸具有相似的化学性质无关,不符合题意;
C、酸中都含有氢元素,而不是氢气,不符合题意;
D、酸中不一定都含有氧元素,如HCl,不符合题意。
故选A。
6.B
【详解】A、碳在氧气中完全燃烧生成二氧化碳,正确的化学方程式应为,错误;
B、澄清石灰水检验二氧化碳生成碳酸钙和水,该化学方程式书写完全正确,正确;
C、化学方程式配平错误,正确的化学方程式应为,错误;
D、铁锈主要成分为氧化铁,氧化铁和盐酸反应生成氯化铁和水,,错误;
故选B。
7.C
【详解】A、将一块石灰石高温煅烧一段时间后,温度较高,直接加水不能证明热量是氧化钙与水反应生成的,不能证明有氧化钙生成,故错误;
B、碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳气体,氧化钙与盐酸反应生成氯化钙和水,若有氧化钙生成,也无明显变化,滴加稀盐酸不能证明有氧化钙生成,故错误;
C、冷却后加水,若有氧化钙生成,氧化钙与水反应生成氢氧化钙,该反应放出大量的热,说明有氧化钙生成,故正确;
D、碳酸钙与稀硫酸反应生成硫酸钙、水和二氧化碳气体,氧化钙与硫酸反应生成硫酸钙和水,若有氧化钙生成,也无明显变化,滴加稀硫酸不能证明有氧化钙生成,故错误。
故选C。
8.A
【详解】①鸡蛋壳的主要成分是碳酸钙,不能与食盐水反应,不能用碎鸡蛋壳中加入食盐水的方法制二氧化碳,故说法错误。
②分子可分,原子也可以再分,原子可分为原子核和电子,故说法错误。
③煮沸,能除去一些水中的可溶性钙镁化合物,可以降低井水的硬度,故说法正确。
④置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,单质中元素的化合价为0、在化合物中正负化合价的代数和为零,则在置换反应时,一定有元素化合价改变,故说法正确。
⑤氢氧化钠具有腐蚀性,应放在玻璃器皿中称量,不能放在纸片上称量,故说法错误。
⑥碳酸盐与酸反应放出气体,但与酸反应放出气体的物质不一定是碳酸盐,也可能是活泼金属等,故说法错误。
故说法正确的个数是2个。
故选:A。
9.D
【详解】A、由化学式可知,乙酸是由C、H、O三种元素组成的,元素是宏观概念,不能论个数,不符合题意;
B、乙酸的相对分子质量为:12×2+4+16×2=60,相对分子质量是一个比值,单位为“1”,常省略不写,不符合题意;
C、乙酸中碳、氢、氧三种元素的质量比为:(12×2):4:(16×2)=6:1:8,故氧元素的质量分数最大,不符合题意;
D、乙酸显酸性,能与氧化铁反应生成乙酸铁和水,可以除去铁锈,符合题意。
故选D。
10.D
【详解】A、由于小卵石和细沙能起到过滤的作用,可以除去一些难溶性杂质,而活性炭具有吸附性,可以除去一些可溶性的杂质、异味、色素等,故A正确;
B、物质结构决定物质的性质,性质决定物质的用途,反之物质用途反映性质,性质反映结构,故B正确;
C、由于碳酸氢钠溶液中有碳酸根离子,若柠檬酸有酸性,它们混合以后就会有气泡冒出,故C正确;
D、高锰酸钾不会溶于汽油,因此不会形成溶液,故D错误;
故选D。
11.C
【详解】A、盐酸呈酸性,能使紫色石蕊试液变红,正确;
B、浓盐酸具有挥发性,开启浓盐酸的瓶盖会冒出白雾,正确;
C、稀盐酸和铁锈中氧化铁反应生成氯化铁溶液,显黄色,错误;
D、浓盐酸是无色、有刺激性气味的液体,正确;
故选C。
12.C
【详解】A、细铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体,说法不正确;
B、酸能使紫色石蕊试剂变红,不是稀盐酸变红,说法不正确;
C、电解水实验中,正极上产生的气体是氧气,氧气能使带火星的木条复燃,说法正确;
D、往氯化铜溶液中滴加氢氧化钠溶液,氯化铜和氢氧化钠反应生成氢氧化铜蓝色沉淀,说法不正确。
故选C。
13. CO Mg2+ Cl- H2O K 吸附 B ②⑤ 不断运动 氧气 水
【详解】(1)1个碳酸根离子带2个单位负电荷,CO 。
1个镁离子带2个单位正电荷,2个镁离子Mg2+。
1个氯离子带1个单位负电荷Cl-。
1个水分子中含有2个氢原子、1个氧原子,H2O。
钾原子K。
(2)①活性炭具有吸附性,可以吸收装修材料释放出的甲醛、苯等有毒气体。
②A、可燃物没有被清除,错误;
B、释放的粉末覆盖在燃烧物上,同时放出不可燃烧气体,使燃烧物与氧气隔绝,正确;
C、燃烧物的着火点不能被降低,错误。
故选B。
③a、金属材料有合金和纯金属;故属于金属材料的是②铜丝、⑤铁。
b、打火机偶然未打着火时会闻到一股异味,说明分子具有是不断运动的,运动到人周围被闻到。
(3)①铁生锈是铁与氧气和水共同作用的结果;漆可以延缓汽车钢铁外壳的锈蚀,其防锈原理是隔绝氧气和水。
②甲烷和氧气点燃生成水和二氧化碳,。
(4)①镁和氧气点燃生成氧化镁,。
②铁和盐酸反应生成氯化亚铁和氢气,。
③铁和硫酸铜生成铜和硫酸亚铁,。
14. 非金属氧化物 硫酸铜(合理都对)
【详解】(1)能与碱发生化学反应的物质类别有:酸碱指示剂、非金属氧化物、酸、盐。与题给氢氧化钠与不同类别物质之间反应的知识网络对比可知,A应该是非金属氧化物,符合要求的化学方程式例如氢氧化钠和二氧化碳反应生成碳酸钠和水,化学方程式为:。
(2)蓝色沉淀物只有Cu(OH)2,属于碱。氢氧化钠也是碱,根据碱能与盐发生复分解反应反应,生成新碱和新盐,可以判断氢氧化钠与可溶性铜盐反应,可以生成氢氧化铜,可溶性的铜盐有Cu(NO3)2、CuCl2、CuSO4。
(3)氢氧化钠与酸发生中和反应,中和反应的实质是H+与OH-生成H2O。据此判断,氢氧化钠能与酸反应的实质是氢氧化钠中OH-的与酸中H+反应生成H2O。
15. CO2 碳
【分析】A~F 是初中化学常见的6种物质,分别由C、H、O、Cl、Ca中的一种或几种元素组成。已知A固体可用于人工降雨,所以A为二氧化碳;B是可燃性气体,燃烧能生成A,据质量守恒定律可知反应前后元素的种类不变,所以B中一定含有碳元素;可能含有的元素是氢或氧;化合物C、D、E中含有相同的金属元素,所以C、D、E都是含钙元素的化合物,且存在如下转化关系C→D→E,氧化钙和水反应生成氢氧化钙,氢氧化钙和二氧化碳反应生成碳酸钙,所以C为氧化钙,D为氢氧化钙,E为碳酸钙;盐酸能与碳酸钙反应生成二氧化碳,所以F为盐酸;代入物质关系中推测正确;
【详解】根据分析得:
(1)二氧化碳A的化学式为CO2;
(2)B中一定含有的元素是碳元素;
(3)碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳气体,。
16. 控制变量 防止集气瓶底炸裂 SO2+2NaOH=Na2SO3+H2O +4
【详解】(1)实验中AC是通过控制变量研究铁生锈的因素和燃烧的条件;B是研究氧气的化学性质;D是配制溶液的操作;故实验 A 和 C 可分成一类,使用的科学方法是控制变量;铁丝在氧气中燃烧放出大量的热,在瓶底放入少量水的目的是防止生成物溅落炸裂集气瓶;
(2)题干提供,非金属氧化物能与碱溶液反应,生成对应的盐(对应是指反应前后各元素化合价不变)和水。二氧化硫中氧元素化合价为负二价,设硫元素化合价为x,化合物中正负化合价代数和为零;则x+(-2)×2=0,x=+4;那么二氧化硫和氢氧化钠反应生成硫元素化合价为正四价的钠盐Na2SO3和水,SO2+2NaOH=Na2SO3+H2O。
答案第1页,共2页
答案第1页,共2页
同课章节目录
