10.1常见的酸和碱 课时作业(含解析)
文档属性
| 名称 | 10.1常见的酸和碱 课时作业(含解析) |
|
|
| 格式 | zip | ||
| 文件大小 | 134.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-17 00:00:00 | ||
图片预览




文档简介
10.1常见的酸和碱 课时作业
一、单选题
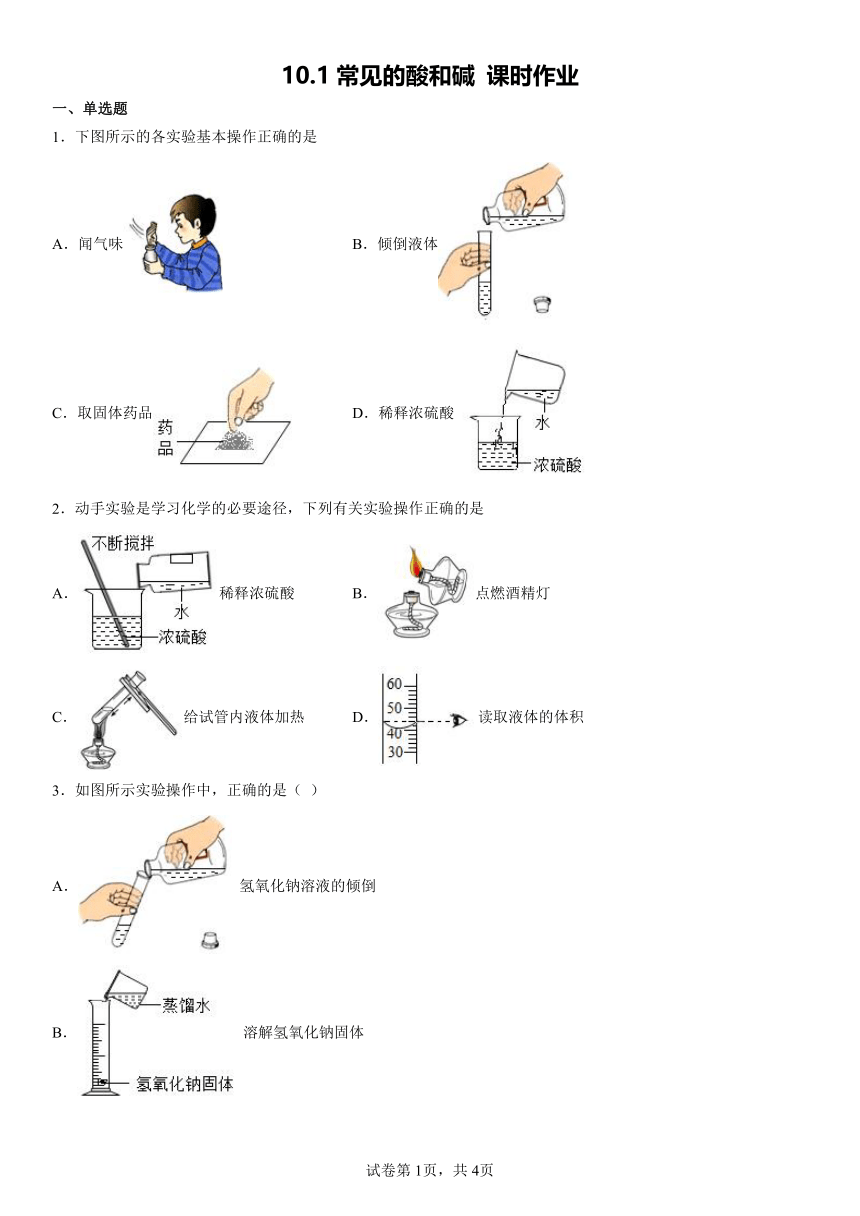
1.下图所示的各实验基本操作正确的是
A.闻气味 B.倾倒液体
C.取固体药品 D.稀释浓硫酸
2.动手实验是学习化学的必要途径,下列有关实验操作正确的是
A.稀释浓硫酸 B.点燃酒精灯
C.给试管内液体加热 D.读取液体的体积
3.如图所示实验操作中,正确的是( )
A. 氢氧化钠溶液的倾倒
B. 溶解氢氧化钠固体
C. 取用氢氧化钙固体
D. 称取一定质量的氢氧化钠
4.醋酸(CH3COOH)是食醋的成分之一,其化学性质与稀盐酸相似,下列说法正确的是
A.醋酸不能除铁锈 B.醋酸能与镁反应生成氢气
C.醋酸能使无色酚酞溶液变红 D.醋酸不能与碳酸钙反应生成二氧化碳
5.下列说法不正确的是
A.硝酸铵固体溶于水出现吸热现象
B.室温下的氯化钠饱和溶液还能再溶解氯化钾
C.饱和溶液的溶质质量分数一定大于不饱和溶液的溶质质量分数
D.氯化钠溶液能够导电是因为溶液中存在自由移动的离子
6.下列物质的性质与用途不具有对应关系的是
A.铝具有较好的延展性,可用于制作电线
B.金刚石的硬度很大,可用于切割
C.Ca(OH)2能与酸反应,可用于改良酸性土壤
D.生石灰与水反应放热,可作自热食品的发热包
7.下列实验现象描述正确的是
A.打开盛有浓盐酸的试剂瓶的瓶盖,瓶口出现白烟
B.铁与稀盐酸反应,溶液由无色变成浅绿色
C.硫在空气中燃烧发出明亮的蓝紫色火焰
D.红磷在空气中燃烧产生五氧化二磷
8.下列说法不正确的是( )
A.浓硫酸涂在木棒上,木棒变黑
B.乙醇与水混合可形成溶液
C.在煤炉旁放一盆水可以防止煤气中毒
D.氯化钠溶液能够导电是因为溶液中存在自由移动的离子
9.下列物质溶于水时,会使温度降低的是
A.NH4NO3固体 B.生石灰 C.KOH固体 D.苛性钠
10.下列有关实验现象的描述正确的是
A.红磷在空气中燃烧产生大量白色烟雾
B.电解水负极一侧得到的气体能使带火星的木条复燃
C.细铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁
D.小木条蘸取浓硫酸后,小木条变黑
11.下列关于硫酸和盐酸的性质和用途说法错误的是( )
A.浓硫酸具有腐蚀性,该性质属于物理性质
B.浓硫酸放置于空气中会变重是因为它有吸水性,所以它可作为干燥剂
C.打开装浓盐酸的试剂瓶看到白雾,是因为浓盐酸有挥发性
D.硫酸和盐酸化学性质比较活泼,都能用于金属除锈
12.下列物质的用途与物质化学性质无关的是( )
A.用铜丝做导线
B.用氮气充入灯泡可延长使用寿命
C.用稀有气体作金属焊接保护气
D.用生石灰作食品干燥剂
二、填空题
13.化学用语是化学的专用语言,也是我们学好化学的基础,选用适当化学符号和数字填空。
(1)人体内含量最高的金属元素______。
(2)三个铁离子______。
(3)食醋中的酸______。
14.回答下列有关的问题。
(1)稀盐酸和稀硫酸化学性质有差别的原因是______;
(2)生铁和钢性能不同的原因是______;
(3)电解水实验,证明水是由______组成的。
(4)测定稀硫酸的pH时,先用水将pH试纸润湿会使结果偏______(填“大”或“小”);
(5)除去氢氧化钠溶液中的氢氧化钙,可以加入适量的______后过滤;
(6)要用适量的试剂检验某硝酸钠溶液中含有的杂质氯化钠、硫酸钠和碳酸钠,先取少量溶液于试管中,然后向试管中依次加入①______②______③______。
三、推断题
15.A、B、C、D、E、F是初中化学常见的六种物质,按要求回答下列问题:
(1)A、B为两种气体,所含元素种类相同,A有可燃性.物质间满足如下转化关系:(部分反应物和生成物已省略,“→”表示转化关系,下同) A B C
①写出B转化为A的化学方程式___________________________;
②物质C可以是______________________(写一种即可)。
(2)D为一种气体单质,E为氧化物,E能与一种金属氧化物反应生成F并放出大量的热。物质间满足如下转化关系: D E F
①写出F的俗称___________;
②写出E转化为D的化学方程式_______________________________________。
四、实验题
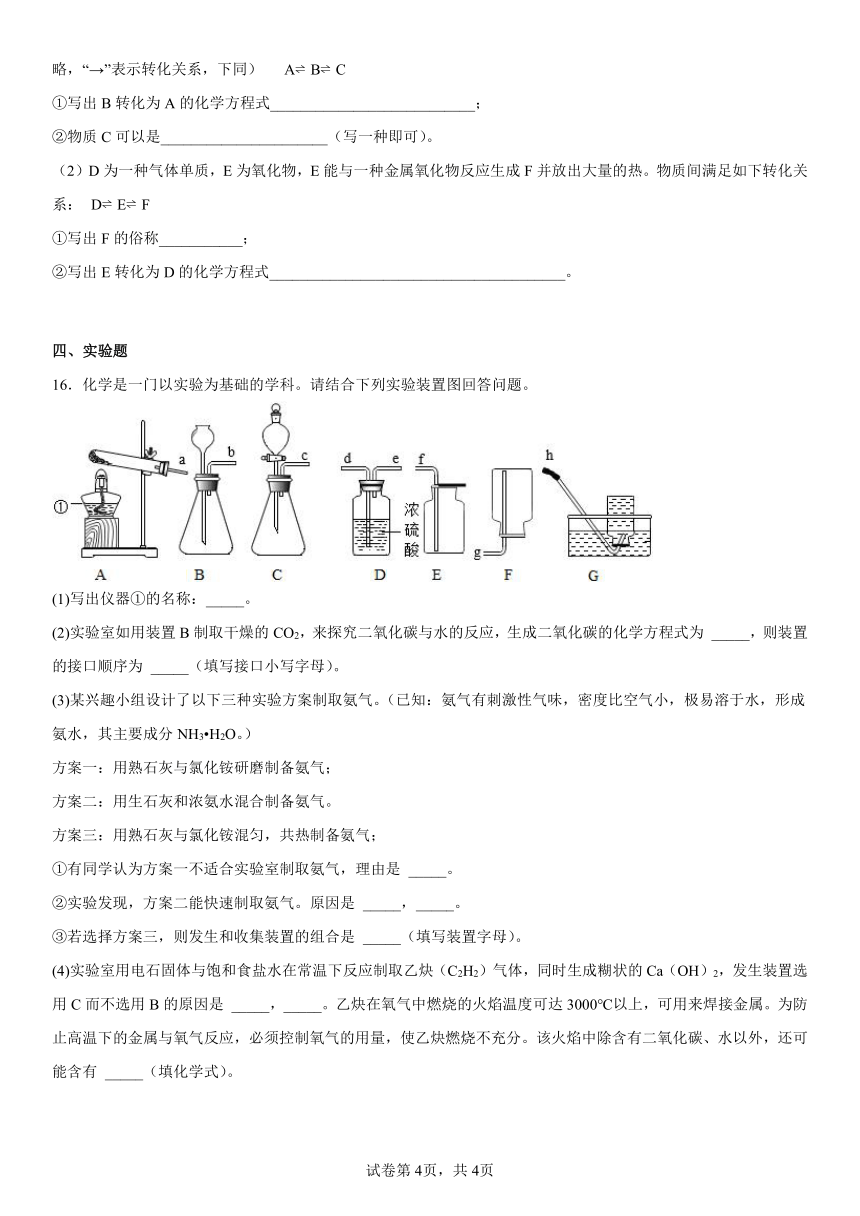
16.化学是一门以实验为基础的学科。请结合下列实验装置图回答问题。
(1)写出仪器①的名称:_____。
(2)实验室如用装置B制取干燥的CO2,来探究二氧化碳与水的反应,生成二氧化碳的化学方程式为 _____,则装置的接口顺序为 _____(填写接口小写字母)。
(3)某兴趣小组设计了以下三种实验方案制取氨气。(已知:氨气有刺激性气味,密度比空气小,极易溶于水,形成氨水,其主要成分NH3 H2O。)
方案一:用熟石灰与氯化铵研磨制备氨气;
方案二:用生石灰和浓氨水混合制备氨气。
方案三:用熟石灰与氯化铵混匀,共热制备氨气;
①有同学认为方案一不适合实验室制取氨气,理由是 _____。
②实验发现,方案二能快速制取氨气。原因是 _____,_____。
③若选择方案三,则发生和收集装置的组合是 _____(填写装置字母)。
(4)实验室用电石固体与饱和食盐水在常温下反应制取乙炔(C2H2)气体,同时生成糊状的Ca(OH)2,发生装置选用C而不选用B的原因是 _____,_____。乙炔在氧气中燃烧的火焰温度可达3000℃以上,可用来焊接金属。为防止高温下的金属与氧气反应,必须控制氧气的用量,使乙炔燃烧不充分。该火焰中除含有二氧化碳、水以外,还可能含有 _____(填化学式)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
【详解】A.闻气体的气味时,应用手在瓶口轻轻的扇动,使极少量的气体飘进鼻子中,不能将鼻子凑到集气瓶口去闻气体的气味,故图A中所示操作正确;
B.向试管中倾倒液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨,故图B中所示操作错误;
C.取用固体粉末状药品时,瓶塞要倒放,应用药匙取用,不能用手接触药品,故图C中所示操作错误;
D.稀释浓硫酸是将浓硫酸沿着容器壁慢慢注入水中,并用玻璃棒不断搅拌,图中将水倒入浓硫酸中,故图D中所示操作错误。
故选A。
【点睛】本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键。
2.C
【详解】A、在稀释浓硫酸时将将浓硫酸沿器壁慢慢注入水中,并用玻璃棒不断搅拌,不能将水注入浓硫酸中,水的密度比浓硫酸小水会浮在浓硫酸上面,浓硫酸溶于水会放出大量的热,水会沸腾产生危险,故A不正确;
B、点燃酒精灯要用火柴,不能用燃着的酒精灯去点燃酒精灯,会引发火灾,故B不正确;
C、给试管内液体加热,液体不能超过试管容积的三分之一,故C正确;
D、量筒读数时,视线与液体凹液面最低处保持水平,故D不正确。故选C。
3.A
【详解】A、氢氧化钠溶液倾倒时,取下的瓶塞要倒放,往试管内倾倒液体时,试管要略微倾斜,瓶口紧挨着试管口倾倒,避免液体溅出,图中所示操作正确;
B、溶解氢氧化钠时,不可放在量筒中溶解,图中所示操作错误;
C、取用氢氧化钙固体时,应用药匙取用,不能用手接触药品,图中所示操作错误;
D、托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了,氢氧化钠具有腐蚀性,应放在玻璃器皿中称量,图中所示操作错误。
故选A 。
4.B
【详解】A、铁锈的主要成分是氧化铁,醋酸属于酸,氧化铁能与酸反应,可用醋酸除去铁锈,不符合题意;
B、醋酸属于酸,镁能与醋酸反应生成醋酸镁和氢气,符合题意;
C、醋酸显酸性,不能使无色酚酞试液变色,不符合题意;
D、碳酸钙能与醋酸反应生成醋酸钙、二氧化碳和水,不符合题意。
故选B。
5.C
【详解】A、硝酸铵固体溶于水时吸收热量,即硝酸铵固体溶于水会出现吸热现象,选项正确;
C、由饱和溶液的概念可知,室温下的氯化钠饱和溶液不再溶解氯化钠,但还可以溶解其它物质,如还能再溶解氯化钾,选项正确;
C、饱和溶液的溶质质量分数不一定大于不饱和溶液的溶质质量分数,如室温时,接近饱和的硝酸钾溶液的溶质质量分数大于饱和氢氧化钙溶液的溶质质量分数,选项错误;
D、氯化钠溶液能够导电是因为氯化钠在水中解离出自由移动的钠离子和氯离子,即溶液中存在自由移动的离子,选项正确。
故选C。
6.A
【详解】A. 铝可用于制作电线主要利用的是铝具有导电性。错误。
B. 金刚石的硬度很大,可用于切割,正确。
C. Ca(OH)2能与酸反应,能减少酸性土壤中的酸性物质,可用于改良酸性土壤,正确。
D. 生石灰与水反应放热,能用放出的热量加热食物,正确。
故选:A。
7.B
【详解】A、浓盐酸有挥发性,挥发出的氯化氢气体极易溶解于水,与空气中的水蒸气结合形成盐酸小液滴,故瓶口有白雾,而不是白烟,所以错误。
B、铁与盐酸反应生成氯化亚铁和氢气,氯化亚铁溶液呈浅绿色,所以正确。
C、硫在空气中燃烧发出淡蓝色火焰,硫在氧气中燃烧发出蓝紫色火焰,所以错误。
D、D. 红磷在空气中燃烧产生五氧化二磷,现象的描述中不能说出结论,所以错误。
故选:B。
【点睛】实验现象的描述是学生学习的难点,也是化学考查的重点,化学反应的主要现象不外乎发光、放热、颜色变化、气泡产生、沉淀生成、形成烟或雾等,要特别注意几点:烟和雾的区别,光和火焰的区别,白色和无色的区别,现象和产物的区别等.
8.C
【详解】A、浓硫酸具有脱水性,浓硫酸涂在木棒上,能把木材中的氢元素和氧元素“脱出”结合生成水,木棒变黑,故选项说法正确。
B、乙醇易溶于水,乙醇与水混合可形成溶液,故选项说法正确。
C、一氧化碳难溶于水,不能与水反应,在煤炉旁放一盆水不能防止煤气中毒,故选项说法错误。
D、氯化钠溶液能够导电是因为溶液中存在自由移动的钠离子和氯离子,故选项说法正确。
故选C。
9.A
【详解】A、硝酸铵溶于水吸热,溶液温度降低,符合题意;
B、生石灰是氧化钙的俗称,氧化钙和水反应生成氢氧化钙,放出大量的热,温度升高,不符合题意;
C、氢氧化钾溶于水,放出大量的热,温度升高,不符合题意;
D、苛性钠是氢氧化钠的俗称,氢氧化钠溶于水放出大量的热,温度升高,不符合题意。
故选A。
10.D
【详解】A、红磷在空气中燃烧,产生大量的白烟,而不是白色烟雾,故选项实验现象的描述不正确;
B、电解水时负极产生的气体是氢气,不具有助燃性,不能使带火星木条复燃,故选项实验现象的描述不正确;
C、细铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁是实验结论而不是实验现象,故选项实验现象的描述不正确;
D、浓硫酸具有脱水性,能使小木条脱水碳化,故选项实验现象的描述正确。
故选D。
11.A
【详解】A. 浓硫酸具有腐蚀性,腐蚀性属于化学性质,此选项错误;
B. 浓硫酸放置于空气中会变重是因为浓硫酸有吸水性,所以浓硫酸可作为干燥剂,此选项正确;
C. 打开装浓盐酸的试剂瓶看到白雾,是因为浓盐酸有挥发性,挥发出来的氯化氢气体溶于空气中的水蒸气中形成了盐酸小液滴的缘故,此选项正确;
D. 硫酸和盐酸化学性质比较活泼,都能与金属氧化物反应,可用于金属除锈,此选项正确。
故选A。
12.A
【详解】 A、用铜丝做导线是利用导电性,属于物理性质;
B、用氮气充入灯泡可延长使用寿命是利用氮气的化学性质不活泼;
C、用稀有气体作金属焊接保护气是利用稀有气体化学性质稳定;
D、用生石灰作食品干燥剂,是利用氧化钙与水反应,属于化学性质。
故选A。
考点:性质与用途的关系
13. Ca 3Fe3+ CH3COOH
【详解】(1)人体内含量最高的金属元素是钙元素,其元素符号为Ca,故填:Ca;
(2)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,若表示多个该离子,就在其离子符号前加上相应的数字,故三个铁离子可表示为3Fe3+,故填:3Fe3+;
(3)食醋中的酸是醋酸,其化学式为CH3COOH,故填:CH3COOH。
14.(1)阴离子不同(或酸根离子不同)
(2)含碳量不同
(3)氢元素和氧元素(或H、O)
(4)大
(5)Na2CO3
(6) HNO3 Ba(NO3)2 AgNO3 (或Ba(NO3)2 HNO3 AgNO3)
【解析】(1)
阳离子都是氢离子,盐酸阴离子是氯离子,硫酸阴离子是硫酸根,所以阴离子不同化学性质不同;
(2)
生铁和钢中碳含量不同,性能不同;
(3)
电解水实验证明有氢气和氧气生成,因为化学反应前后元素种类不变,所以水由氢元素和氧元素组成;
(4)
先用水润湿,相当于溶液被稀释了,所以硫酸浓度降低,酸性减弱PH值偏大;
(5)
可以加入少量的碳酸钠,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,所以可以加入碳酸钠;
(6)
先加入过量硝酸会产生气泡,可以检验碳酸钠,然后加入过量硝酸钡产生硫酸钡沉淀,检验硫酸钠,最后加入硝酸银会产生氯化银沉淀,可以检验氯离子。
15. 碳酸 熟石灰
【分析】(1)A、B、C、D、E、F是初中化学常见的六种物质,A、B为两种气体,所含元素种类相同,A有可燃性,A、B可以相互转化,所以A是一氧化碳,B是二氧化碳,二氧化碳和C可以相互转化,所以C可以是碳酸,一氧化碳和氧气会生成二氧化碳,二氧化碳和木炭会生成一氧化碳,二氧化碳和水会生成碳酸,碳酸分解会生成水和二氧化碳,推出的各种物质均满足题中的转化关系。
(2)A、B、C、D、E、F是初中化学常见的六种物质,D为一种气体单质,E为氧化物,E能与一种金属氧化物反应生成F并放出大量的热,所以金属氧化物是氧化钙,E是水,F是氢氧化钙,氢氧化钙和水可以相互转化,水和D可以相互转化,D为一种气体单质,所以D是氢气或氧气,氢气和氧气反应会生成水,水通电会生成氢气和氧气,氧化钙和水会生成氢氧化钙,氢氧化钙和盐酸会生成水,推出的各种物质均满足题中的转化关系。
【详解】(1)①根据分析,A是一氧化碳,B是二氧化碳,所以B转化为A是木炭和二氧化碳在高温条件下反应生成一氧化碳,化学方程式为:;
②根据分析,B是二氧化碳,二氧化碳和水会生成碳酸,碳酸分解会生成水和二氧化碳,故物质C可以是:碳酸。
(2)①根据分析, F是氢氧化钙,俗称是:熟石灰(或消石灰);
②根据分析,E是水,D为一种气体单质,水和D可以相互转化,所以D是氢气或氧气,E转化为D的反应是水在通电的条件下分解生成氢气和氧气,化学方程式为:。
16.(1)酒精灯
(2) bdef##cdef
(3) 不方便收集 生石灰能与氨水中的水反应,使溶液浓度更大 生石灰与水反应为放热反应 AF##FA
(4) 分液漏斗能控制反应速率 防止糊状的氢氧化钙堵塞长颈漏斗的下端管口,使饱和食盐水无法顺利流出 CO
【详解】(1)由图可知,仪器①为酒精灯。
(2)实验室用大理石和稀盐酸制取二氧化碳,反应的化学方程式为;
该反应为固体和液体在常温下的反应,则发生装置选B或C,且浓硫酸具有吸水性,可干燥二氧化碳,则选用D装置干燥二氧化碳,且应长管进短管出,二氧化碳密度比空气大,能溶于水,则收集装置选E,则装置的接口顺序为bdef或cdef。
(3)①方案一为研磨固体混合物,则产生的气体不好收集;
②生石灰为氧化钙的俗称,氧化钙能与水反应放热,则一方面会消耗浓氨水中的水,使溶液浓度变大,另一方面温度升高,能加快氨气的挥发;
③方案三为加热固体的反应,发生装置选A,氨气能溶于水,且密度比空气小,则收集装置选F,则装置组合为AF。
(4)装置C中的长颈漏斗能控制液体的滴加速度,从而控制反应速率,且B装置中的长颈漏斗需浸入液面以下,而生成的糊状的氢氧化钙可能会堵塞长颈漏斗的下端管口,使饱和食盐水无法顺利流出,则选装置C而不选B。
乙炔中含有碳元素,不充分燃烧时还可能生成一氧化碳,符号为CO。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下图所示的各实验基本操作正确的是
A.闻气味 B.倾倒液体
C.取固体药品 D.稀释浓硫酸
2.动手实验是学习化学的必要途径,下列有关实验操作正确的是
A.稀释浓硫酸 B.点燃酒精灯
C.给试管内液体加热 D.读取液体的体积
3.如图所示实验操作中,正确的是( )
A. 氢氧化钠溶液的倾倒
B. 溶解氢氧化钠固体
C. 取用氢氧化钙固体
D. 称取一定质量的氢氧化钠
4.醋酸(CH3COOH)是食醋的成分之一,其化学性质与稀盐酸相似,下列说法正确的是
A.醋酸不能除铁锈 B.醋酸能与镁反应生成氢气
C.醋酸能使无色酚酞溶液变红 D.醋酸不能与碳酸钙反应生成二氧化碳
5.下列说法不正确的是
A.硝酸铵固体溶于水出现吸热现象
B.室温下的氯化钠饱和溶液还能再溶解氯化钾
C.饱和溶液的溶质质量分数一定大于不饱和溶液的溶质质量分数
D.氯化钠溶液能够导电是因为溶液中存在自由移动的离子
6.下列物质的性质与用途不具有对应关系的是
A.铝具有较好的延展性,可用于制作电线
B.金刚石的硬度很大,可用于切割
C.Ca(OH)2能与酸反应,可用于改良酸性土壤
D.生石灰与水反应放热,可作自热食品的发热包
7.下列实验现象描述正确的是
A.打开盛有浓盐酸的试剂瓶的瓶盖,瓶口出现白烟
B.铁与稀盐酸反应,溶液由无色变成浅绿色
C.硫在空气中燃烧发出明亮的蓝紫色火焰
D.红磷在空气中燃烧产生五氧化二磷
8.下列说法不正确的是( )
A.浓硫酸涂在木棒上,木棒变黑
B.乙醇与水混合可形成溶液
C.在煤炉旁放一盆水可以防止煤气中毒
D.氯化钠溶液能够导电是因为溶液中存在自由移动的离子
9.下列物质溶于水时,会使温度降低的是
A.NH4NO3固体 B.生石灰 C.KOH固体 D.苛性钠
10.下列有关实验现象的描述正确的是
A.红磷在空气中燃烧产生大量白色烟雾
B.电解水负极一侧得到的气体能使带火星的木条复燃
C.细铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁
D.小木条蘸取浓硫酸后,小木条变黑
11.下列关于硫酸和盐酸的性质和用途说法错误的是( )
A.浓硫酸具有腐蚀性,该性质属于物理性质
B.浓硫酸放置于空气中会变重是因为它有吸水性,所以它可作为干燥剂
C.打开装浓盐酸的试剂瓶看到白雾,是因为浓盐酸有挥发性
D.硫酸和盐酸化学性质比较活泼,都能用于金属除锈
12.下列物质的用途与物质化学性质无关的是( )
A.用铜丝做导线
B.用氮气充入灯泡可延长使用寿命
C.用稀有气体作金属焊接保护气
D.用生石灰作食品干燥剂
二、填空题
13.化学用语是化学的专用语言,也是我们学好化学的基础,选用适当化学符号和数字填空。
(1)人体内含量最高的金属元素______。
(2)三个铁离子______。
(3)食醋中的酸______。
14.回答下列有关的问题。
(1)稀盐酸和稀硫酸化学性质有差别的原因是______;
(2)生铁和钢性能不同的原因是______;
(3)电解水实验,证明水是由______组成的。
(4)测定稀硫酸的pH时,先用水将pH试纸润湿会使结果偏______(填“大”或“小”);
(5)除去氢氧化钠溶液中的氢氧化钙,可以加入适量的______后过滤;
(6)要用适量的试剂检验某硝酸钠溶液中含有的杂质氯化钠、硫酸钠和碳酸钠,先取少量溶液于试管中,然后向试管中依次加入①______②______③______。
三、推断题
15.A、B、C、D、E、F是初中化学常见的六种物质,按要求回答下列问题:
(1)A、B为两种气体,所含元素种类相同,A有可燃性.物质间满足如下转化关系:(部分反应物和生成物已省略,“→”表示转化关系,下同) A B C
①写出B转化为A的化学方程式___________________________;
②物质C可以是______________________(写一种即可)。
(2)D为一种气体单质,E为氧化物,E能与一种金属氧化物反应生成F并放出大量的热。物质间满足如下转化关系: D E F
①写出F的俗称___________;
②写出E转化为D的化学方程式_______________________________________。
四、实验题
16.化学是一门以实验为基础的学科。请结合下列实验装置图回答问题。
(1)写出仪器①的名称:_____。
(2)实验室如用装置B制取干燥的CO2,来探究二氧化碳与水的反应,生成二氧化碳的化学方程式为 _____,则装置的接口顺序为 _____(填写接口小写字母)。
(3)某兴趣小组设计了以下三种实验方案制取氨气。(已知:氨气有刺激性气味,密度比空气小,极易溶于水,形成氨水,其主要成分NH3 H2O。)
方案一:用熟石灰与氯化铵研磨制备氨气;
方案二:用生石灰和浓氨水混合制备氨气。
方案三:用熟石灰与氯化铵混匀,共热制备氨气;
①有同学认为方案一不适合实验室制取氨气,理由是 _____。
②实验发现,方案二能快速制取氨气。原因是 _____,_____。
③若选择方案三,则发生和收集装置的组合是 _____(填写装置字母)。
(4)实验室用电石固体与饱和食盐水在常温下反应制取乙炔(C2H2)气体,同时生成糊状的Ca(OH)2,发生装置选用C而不选用B的原因是 _____,_____。乙炔在氧气中燃烧的火焰温度可达3000℃以上,可用来焊接金属。为防止高温下的金属与氧气反应,必须控制氧气的用量,使乙炔燃烧不充分。该火焰中除含有二氧化碳、水以外,还可能含有 _____(填化学式)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
【详解】A.闻气体的气味时,应用手在瓶口轻轻的扇动,使极少量的气体飘进鼻子中,不能将鼻子凑到集气瓶口去闻气体的气味,故图A中所示操作正确;
B.向试管中倾倒液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨,故图B中所示操作错误;
C.取用固体粉末状药品时,瓶塞要倒放,应用药匙取用,不能用手接触药品,故图C中所示操作错误;
D.稀释浓硫酸是将浓硫酸沿着容器壁慢慢注入水中,并用玻璃棒不断搅拌,图中将水倒入浓硫酸中,故图D中所示操作错误。
故选A。
【点睛】本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键。
2.C
【详解】A、在稀释浓硫酸时将将浓硫酸沿器壁慢慢注入水中,并用玻璃棒不断搅拌,不能将水注入浓硫酸中,水的密度比浓硫酸小水会浮在浓硫酸上面,浓硫酸溶于水会放出大量的热,水会沸腾产生危险,故A不正确;
B、点燃酒精灯要用火柴,不能用燃着的酒精灯去点燃酒精灯,会引发火灾,故B不正确;
C、给试管内液体加热,液体不能超过试管容积的三分之一,故C正确;
D、量筒读数时,视线与液体凹液面最低处保持水平,故D不正确。故选C。
3.A
【详解】A、氢氧化钠溶液倾倒时,取下的瓶塞要倒放,往试管内倾倒液体时,试管要略微倾斜,瓶口紧挨着试管口倾倒,避免液体溅出,图中所示操作正确;
B、溶解氢氧化钠时,不可放在量筒中溶解,图中所示操作错误;
C、取用氢氧化钙固体时,应用药匙取用,不能用手接触药品,图中所示操作错误;
D、托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了,氢氧化钠具有腐蚀性,应放在玻璃器皿中称量,图中所示操作错误。
故选A 。
4.B
【详解】A、铁锈的主要成分是氧化铁,醋酸属于酸,氧化铁能与酸反应,可用醋酸除去铁锈,不符合题意;
B、醋酸属于酸,镁能与醋酸反应生成醋酸镁和氢气,符合题意;
C、醋酸显酸性,不能使无色酚酞试液变色,不符合题意;
D、碳酸钙能与醋酸反应生成醋酸钙、二氧化碳和水,不符合题意。
故选B。
5.C
【详解】A、硝酸铵固体溶于水时吸收热量,即硝酸铵固体溶于水会出现吸热现象,选项正确;
C、由饱和溶液的概念可知,室温下的氯化钠饱和溶液不再溶解氯化钠,但还可以溶解其它物质,如还能再溶解氯化钾,选项正确;
C、饱和溶液的溶质质量分数不一定大于不饱和溶液的溶质质量分数,如室温时,接近饱和的硝酸钾溶液的溶质质量分数大于饱和氢氧化钙溶液的溶质质量分数,选项错误;
D、氯化钠溶液能够导电是因为氯化钠在水中解离出自由移动的钠离子和氯离子,即溶液中存在自由移动的离子,选项正确。
故选C。
6.A
【详解】A. 铝可用于制作电线主要利用的是铝具有导电性。错误。
B. 金刚石的硬度很大,可用于切割,正确。
C. Ca(OH)2能与酸反应,能减少酸性土壤中的酸性物质,可用于改良酸性土壤,正确。
D. 生石灰与水反应放热,能用放出的热量加热食物,正确。
故选:A。
7.B
【详解】A、浓盐酸有挥发性,挥发出的氯化氢气体极易溶解于水,与空气中的水蒸气结合形成盐酸小液滴,故瓶口有白雾,而不是白烟,所以错误。
B、铁与盐酸反应生成氯化亚铁和氢气,氯化亚铁溶液呈浅绿色,所以正确。
C、硫在空气中燃烧发出淡蓝色火焰,硫在氧气中燃烧发出蓝紫色火焰,所以错误。
D、D. 红磷在空气中燃烧产生五氧化二磷,现象的描述中不能说出结论,所以错误。
故选:B。
【点睛】实验现象的描述是学生学习的难点,也是化学考查的重点,化学反应的主要现象不外乎发光、放热、颜色变化、气泡产生、沉淀生成、形成烟或雾等,要特别注意几点:烟和雾的区别,光和火焰的区别,白色和无色的区别,现象和产物的区别等.
8.C
【详解】A、浓硫酸具有脱水性,浓硫酸涂在木棒上,能把木材中的氢元素和氧元素“脱出”结合生成水,木棒变黑,故选项说法正确。
B、乙醇易溶于水,乙醇与水混合可形成溶液,故选项说法正确。
C、一氧化碳难溶于水,不能与水反应,在煤炉旁放一盆水不能防止煤气中毒,故选项说法错误。
D、氯化钠溶液能够导电是因为溶液中存在自由移动的钠离子和氯离子,故选项说法正确。
故选C。
9.A
【详解】A、硝酸铵溶于水吸热,溶液温度降低,符合题意;
B、生石灰是氧化钙的俗称,氧化钙和水反应生成氢氧化钙,放出大量的热,温度升高,不符合题意;
C、氢氧化钾溶于水,放出大量的热,温度升高,不符合题意;
D、苛性钠是氢氧化钠的俗称,氢氧化钠溶于水放出大量的热,温度升高,不符合题意。
故选A。
10.D
【详解】A、红磷在空气中燃烧,产生大量的白烟,而不是白色烟雾,故选项实验现象的描述不正确;
B、电解水时负极产生的气体是氢气,不具有助燃性,不能使带火星木条复燃,故选项实验现象的描述不正确;
C、细铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁是实验结论而不是实验现象,故选项实验现象的描述不正确;
D、浓硫酸具有脱水性,能使小木条脱水碳化,故选项实验现象的描述正确。
故选D。
11.A
【详解】A. 浓硫酸具有腐蚀性,腐蚀性属于化学性质,此选项错误;
B. 浓硫酸放置于空气中会变重是因为浓硫酸有吸水性,所以浓硫酸可作为干燥剂,此选项正确;
C. 打开装浓盐酸的试剂瓶看到白雾,是因为浓盐酸有挥发性,挥发出来的氯化氢气体溶于空气中的水蒸气中形成了盐酸小液滴的缘故,此选项正确;
D. 硫酸和盐酸化学性质比较活泼,都能与金属氧化物反应,可用于金属除锈,此选项正确。
故选A。
12.A
【详解】 A、用铜丝做导线是利用导电性,属于物理性质;
B、用氮气充入灯泡可延长使用寿命是利用氮气的化学性质不活泼;
C、用稀有气体作金属焊接保护气是利用稀有气体化学性质稳定;
D、用生石灰作食品干燥剂,是利用氧化钙与水反应,属于化学性质。
故选A。
考点:性质与用途的关系
13. Ca 3Fe3+ CH3COOH
【详解】(1)人体内含量最高的金属元素是钙元素,其元素符号为Ca,故填:Ca;
(2)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,若表示多个该离子,就在其离子符号前加上相应的数字,故三个铁离子可表示为3Fe3+,故填:3Fe3+;
(3)食醋中的酸是醋酸,其化学式为CH3COOH,故填:CH3COOH。
14.(1)阴离子不同(或酸根离子不同)
(2)含碳量不同
(3)氢元素和氧元素(或H、O)
(4)大
(5)Na2CO3
(6) HNO3 Ba(NO3)2 AgNO3 (或Ba(NO3)2 HNO3 AgNO3)
【解析】(1)
阳离子都是氢离子,盐酸阴离子是氯离子,硫酸阴离子是硫酸根,所以阴离子不同化学性质不同;
(2)
生铁和钢中碳含量不同,性能不同;
(3)
电解水实验证明有氢气和氧气生成,因为化学反应前后元素种类不变,所以水由氢元素和氧元素组成;
(4)
先用水润湿,相当于溶液被稀释了,所以硫酸浓度降低,酸性减弱PH值偏大;
(5)
可以加入少量的碳酸钠,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,所以可以加入碳酸钠;
(6)
先加入过量硝酸会产生气泡,可以检验碳酸钠,然后加入过量硝酸钡产生硫酸钡沉淀,检验硫酸钠,最后加入硝酸银会产生氯化银沉淀,可以检验氯离子。
15. 碳酸 熟石灰
【分析】(1)A、B、C、D、E、F是初中化学常见的六种物质,A、B为两种气体,所含元素种类相同,A有可燃性,A、B可以相互转化,所以A是一氧化碳,B是二氧化碳,二氧化碳和C可以相互转化,所以C可以是碳酸,一氧化碳和氧气会生成二氧化碳,二氧化碳和木炭会生成一氧化碳,二氧化碳和水会生成碳酸,碳酸分解会生成水和二氧化碳,推出的各种物质均满足题中的转化关系。
(2)A、B、C、D、E、F是初中化学常见的六种物质,D为一种气体单质,E为氧化物,E能与一种金属氧化物反应生成F并放出大量的热,所以金属氧化物是氧化钙,E是水,F是氢氧化钙,氢氧化钙和水可以相互转化,水和D可以相互转化,D为一种气体单质,所以D是氢气或氧气,氢气和氧气反应会生成水,水通电会生成氢气和氧气,氧化钙和水会生成氢氧化钙,氢氧化钙和盐酸会生成水,推出的各种物质均满足题中的转化关系。
【详解】(1)①根据分析,A是一氧化碳,B是二氧化碳,所以B转化为A是木炭和二氧化碳在高温条件下反应生成一氧化碳,化学方程式为:;
②根据分析,B是二氧化碳,二氧化碳和水会生成碳酸,碳酸分解会生成水和二氧化碳,故物质C可以是:碳酸。
(2)①根据分析, F是氢氧化钙,俗称是:熟石灰(或消石灰);
②根据分析,E是水,D为一种气体单质,水和D可以相互转化,所以D是氢气或氧气,E转化为D的反应是水在通电的条件下分解生成氢气和氧气,化学方程式为:。
16.(1)酒精灯
(2) bdef##cdef
(3) 不方便收集 生石灰能与氨水中的水反应,使溶液浓度更大 生石灰与水反应为放热反应 AF##FA
(4) 分液漏斗能控制反应速率 防止糊状的氢氧化钙堵塞长颈漏斗的下端管口,使饱和食盐水无法顺利流出 CO
【详解】(1)由图可知,仪器①为酒精灯。
(2)实验室用大理石和稀盐酸制取二氧化碳,反应的化学方程式为;
该反应为固体和液体在常温下的反应,则发生装置选B或C,且浓硫酸具有吸水性,可干燥二氧化碳,则选用D装置干燥二氧化碳,且应长管进短管出,二氧化碳密度比空气大,能溶于水,则收集装置选E,则装置的接口顺序为bdef或cdef。
(3)①方案一为研磨固体混合物,则产生的气体不好收集;
②生石灰为氧化钙的俗称,氧化钙能与水反应放热,则一方面会消耗浓氨水中的水,使溶液浓度变大,另一方面温度升高,能加快氨气的挥发;
③方案三为加热固体的反应,发生装置选A,氨气能溶于水,且密度比空气小,则收集装置选F,则装置组合为AF。
(4)装置C中的长颈漏斗能控制液体的滴加速度,从而控制反应速率,且B装置中的长颈漏斗需浸入液面以下,而生成的糊状的氢氧化钙可能会堵塞长颈漏斗的下端管口,使饱和食盐水无法顺利流出,则选装置C而不选B。
乙炔中含有碳元素,不充分燃烧时还可能生成一氧化碳,符号为CO。
答案第1页,共2页
答案第1页,共2页
同课章节目录
