2.3芳香烃(教学课件)(共26张PPT)—2022-2023学年高二化学人教版(2019)选择性必修3
文档属性
| 名称 | 2.3芳香烃(教学课件)(共26张PPT)—2022-2023学年高二化学人教版(2019)选择性必修3 |

|
|
| 格式 | ppt | ||
| 文件大小 | 3.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-19 00:00:00 | ||
图片预览






文档简介
(共26张PPT)
第二章 烃
第三节 芳香烃
1、了解苯的同系物概念。
2、学习掌握苯及苯的同系物的结构和性质。
3、通过对苯环与甲基的相互影响了解苯与苯的同系物性质上的异同。
课程目标
教学重点
苯及苯的同系物的结构和化学性质。
教学难点
苯的同系物的结构和化学性质,基团间的相互影响。
苯
苯
1、芳香烃
分子中含有一个或多个 的 化合物。最简单的芳香烃是 。
苯环
烃类
苯
苯
2、苯的分子结构
(1)分子结构
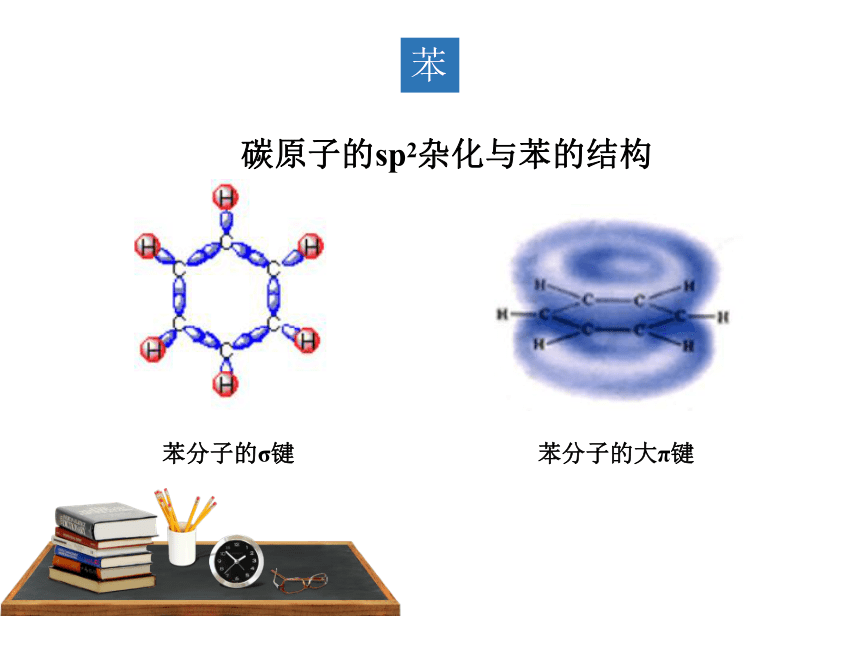
苯分子为平面 结构,分子中 个原子共平面,碳原子均采取 杂化,每个碳的杂化轨道分别与氢原子及相邻碳原子的 杂化轨道以σ键结合,键间夹角均为 ,连接成六元环状。每个碳原子余下的p轨道 碳、氢原子构成的平面,相互 形成 键,均匀地对称分布在苯环平面的上下两侧。
正六边形
12
sp2
sp2
120°
垂直于
平行重叠
大π
碳原子的sp2杂化与苯的结构
苯分子的大π键
苯分子的σ键
苯
(1) 分子式:
C6H6
C
C
C
C
C
C
H
H
H
H
H
H
(2)结构式:
或
(3)结构简式:
球棍模型
比例模型
(4)空间构型
苯是一个平面正六边形分子
在苯分子中不存在碳碳单键和双键的交替结构。
苯
分子组成和结构的不同表示方法
苯
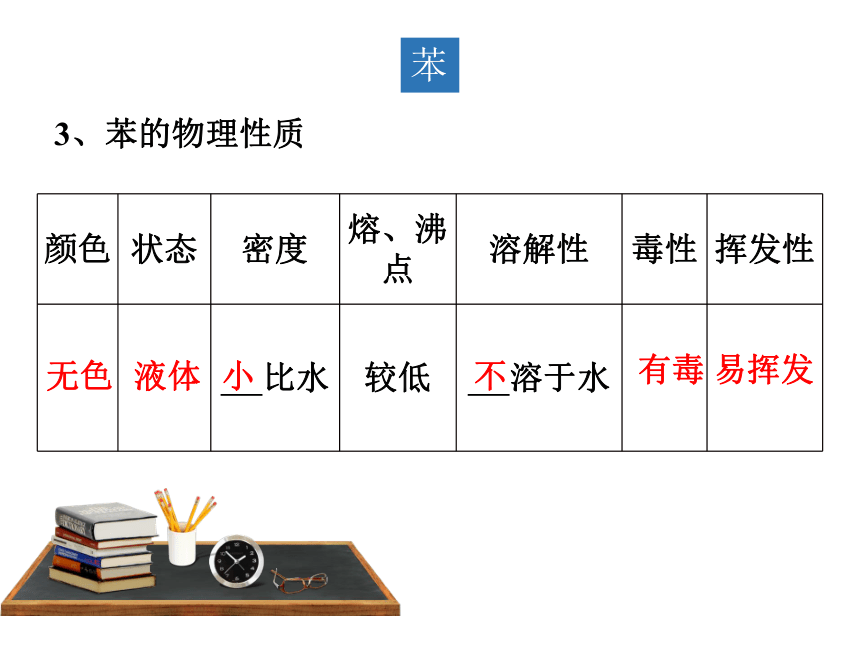
3、苯的物理性质
颜色 状态 密度 熔、沸点 溶解性 毒性 挥发性
比水 较低 溶于水
无色
液体
小
不
有毒
易挥发
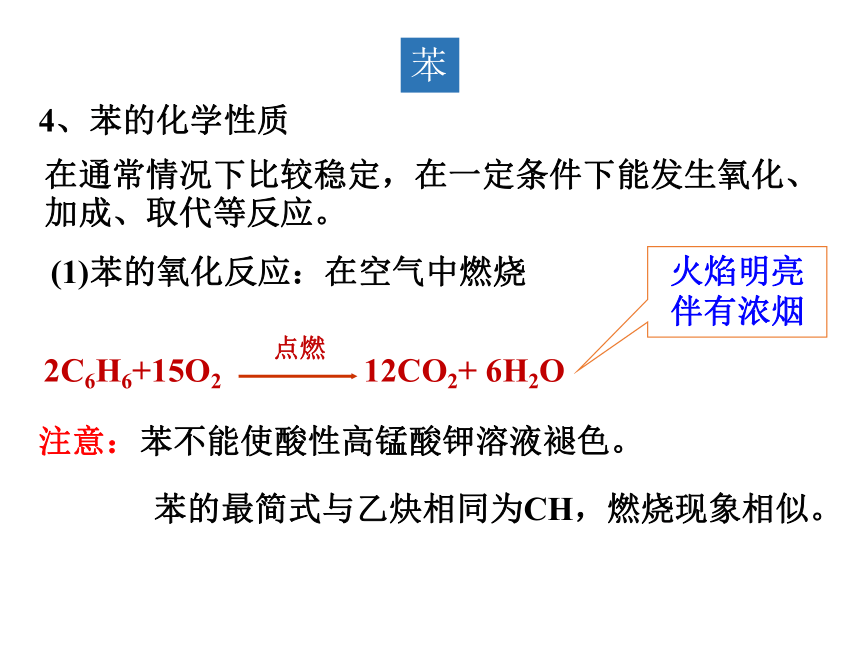
4、苯的化学性质
在通常情况下比较稳定,在一定条件下能发生氧化、加成、取代等反应。
(1)苯的氧化反应:在空气中燃烧
2C6H6+15O2 12CO2+ 6H2O
点燃
注意:苯不能使酸性高锰酸钾溶液褪色。
火焰明亮伴有浓烟
苯的最简式与乙炔相同为CH,燃烧现象相似。
苯
实验步骤:按左图连接好实验装置,并检验装置的气密性.把少量苯和液态溴放在烧瓶里.同时加入少量铁粉.在常温下,很快就会看到实验现象。
苯
(2)苯的取代反应(卤代、硝化、磺化)
+ Br2
Br
+ HBr
Fe
2. 溴苯是密度比水大的无色液体。
加热方式:水浴加热
注意:1.催化剂Fe与Br2反应生成FeBr3起催化剂作用,该反应是放热反应。
有白雾生成
苯
硝基苯为无色、具有苦杏仁味的油状液体,其密度大于水
+ HNO3(浓)
NO2
+ H2O
浓H2SO4
50~60℃
浓硫酸作用:催化剂、吸水剂
加热方式:水浴加热
硝基苯
苯
纯净的溴苯是无色液体,不溶于水,密度比水大,为什么所得溴苯为褐色?怎样得到纯净的溴苯?
提示:因为未反应的溴溶解在产物溴苯中;水洗,加NaOH溶液振荡,分液,再蒸馏。
实验步骤 : a.按图连接好装置,并检查装置的气密性; b.配制混合酸:先将1.5mL浓硝酸注入大试管中,再慢慢注入2mL浓硫酸,并及时摇匀和冷却; c.向冷却后的混合液中逐滴加入1mL苯,充分振荡,混合均匀; d.将大试管放在50~60℃的水浴中加热。
冷凝回流
注意:温度计应插入水面以下,水银球不能触及烧杯底部及烧杯壁。
(3)苯的加成反应
(环己烷)
+3 H2
催化剂
加热
磺化反应———浓硫酸是反应物
苯磺酸
苯
苯的同系物
1、组成和结构特点
(1)苯的同系物是苯环上的氢原子被 取代所得到的一系列产物。
(2)分子中只有一个 ,侧链都是 。
(3)通式为 (n≥7)。
烷基
苯环
烷基
CnH2n-6
苯的同系物
2、常见的苯的同系物
名 称 结构简式
甲苯
乙苯
苯的同系物
二甲苯 邻二甲苯
间二甲苯
对二甲苯
苯的同系物
3、物理性质
一般具有 的气味, 色液体,
溶于水, 溶于有机溶剂,密度比水的 。
类似苯
无
不
易
小
苯的同系物
4、化学性质
苯的同系物与苯都含有苯环,因此和苯具有相似的化学性质,能在一定条件下发生 、
和 反应,但由于 的相互影响,使苯的同系物的化学性质与苯和烷烃又有所不同。
溴代
硝化
催化加氢
苯环和烷基
苯的同系物
(1)氧化反应
①苯的同系物大多数能被酸性KMnO4溶液 而使其 。
②均能燃烧,燃烧的通式:
CnH2n-6+ O2 nCO2+(n-3)H2O
氧化
褪色
2mL苯
3滴高锰酸钾酸性溶液
用力振荡
2mL甲苯
3滴高锰酸钾酸性溶液
用力振荡
苯环影响侧链,使侧链能被强氧化剂氧化
实验结论:
苯不能被KMnO4酸性溶液氧化,甲苯能被KMnO4酸性溶液氧化
未褪色
褪色
苯的同系物
(2)取代反应
甲苯与浓硝酸和浓硫酸的混合物在加热条件下可以发生取代反应,生成一硝基取代物、二硝基取代物和三硝基取代物,硝基取代的位置均以甲基的邻对位为主。其中生成三硝基取代物的
化学方程式: ,有机产物名称
,又叫 ,用字母表示 。
(3)加成反应:
甲苯与氢气反应的化学方程式: 。
苯的同系物
2,4,6-三硝基甲苯
梯恩梯
TNT
苯 苯的同系物
相同点 结构组成 ①分子中都含有一个苯环②都符合分子通式CnH2n-6(n≥6)
化学性质 ①燃烧时现象相同,火焰明亮,伴有浓烟②都易发生苯环上的取代反应③都能发生加成反应,但都比较困难
苯与苯的同系物在分子组成、结构和性质上的异同
苯与苯的同系物在分子组成、结构和性质上的异同
苯 苯的同系物
不同点 取代反应 易发生取代反应,主要得到一元取代产物 更容易发生取代反应,常得到多元取代产物
氧化反应 难被氧化,不能使酸性KMnO4溶液褪色 易被氧化剂氧化,能使酸性KMnO4溶液褪色
差异原因 苯的同系物分子中,苯环与侧链相互影响。苯环影响侧链,使侧链烃基活化而易被氧化;侧链烃基影响苯环,使苯环上烃基邻、对位的氢原子活化而被取代
教学课件
感谢观看
第二章 烃
第三节 芳香烃
1、了解苯的同系物概念。
2、学习掌握苯及苯的同系物的结构和性质。
3、通过对苯环与甲基的相互影响了解苯与苯的同系物性质上的异同。
课程目标
教学重点
苯及苯的同系物的结构和化学性质。
教学难点
苯的同系物的结构和化学性质,基团间的相互影响。
苯
苯
1、芳香烃
分子中含有一个或多个 的 化合物。最简单的芳香烃是 。
苯环
烃类
苯
苯
2、苯的分子结构
(1)分子结构
苯分子为平面 结构,分子中 个原子共平面,碳原子均采取 杂化,每个碳的杂化轨道分别与氢原子及相邻碳原子的 杂化轨道以σ键结合,键间夹角均为 ,连接成六元环状。每个碳原子余下的p轨道 碳、氢原子构成的平面,相互 形成 键,均匀地对称分布在苯环平面的上下两侧。
正六边形
12
sp2
sp2
120°
垂直于
平行重叠
大π
碳原子的sp2杂化与苯的结构
苯分子的大π键
苯分子的σ键
苯
(1) 分子式:
C6H6
C
C
C
C
C
C
H
H
H
H
H
H
(2)结构式:
或
(3)结构简式:
球棍模型
比例模型
(4)空间构型
苯是一个平面正六边形分子
在苯分子中不存在碳碳单键和双键的交替结构。
苯
分子组成和结构的不同表示方法
苯
3、苯的物理性质
颜色 状态 密度 熔、沸点 溶解性 毒性 挥发性
比水 较低 溶于水
无色
液体
小
不
有毒
易挥发
4、苯的化学性质
在通常情况下比较稳定,在一定条件下能发生氧化、加成、取代等反应。
(1)苯的氧化反应:在空气中燃烧
2C6H6+15O2 12CO2+ 6H2O
点燃
注意:苯不能使酸性高锰酸钾溶液褪色。
火焰明亮伴有浓烟
苯的最简式与乙炔相同为CH,燃烧现象相似。
苯
实验步骤:按左图连接好实验装置,并检验装置的气密性.把少量苯和液态溴放在烧瓶里.同时加入少量铁粉.在常温下,很快就会看到实验现象。
苯
(2)苯的取代反应(卤代、硝化、磺化)
+ Br2
Br
+ HBr
Fe
2. 溴苯是密度比水大的无色液体。
加热方式:水浴加热
注意:1.催化剂Fe与Br2反应生成FeBr3起催化剂作用,该反应是放热反应。
有白雾生成
苯
硝基苯为无色、具有苦杏仁味的油状液体,其密度大于水
+ HNO3(浓)
NO2
+ H2O
浓H2SO4
50~60℃
浓硫酸作用:催化剂、吸水剂
加热方式:水浴加热
硝基苯
苯
纯净的溴苯是无色液体,不溶于水,密度比水大,为什么所得溴苯为褐色?怎样得到纯净的溴苯?
提示:因为未反应的溴溶解在产物溴苯中;水洗,加NaOH溶液振荡,分液,再蒸馏。
实验步骤 : a.按图连接好装置,并检查装置的气密性; b.配制混合酸:先将1.5mL浓硝酸注入大试管中,再慢慢注入2mL浓硫酸,并及时摇匀和冷却; c.向冷却后的混合液中逐滴加入1mL苯,充分振荡,混合均匀; d.将大试管放在50~60℃的水浴中加热。
冷凝回流
注意:温度计应插入水面以下,水银球不能触及烧杯底部及烧杯壁。
(3)苯的加成反应
(环己烷)
+3 H2
催化剂
加热
磺化反应———浓硫酸是反应物
苯磺酸
苯
苯的同系物
1、组成和结构特点
(1)苯的同系物是苯环上的氢原子被 取代所得到的一系列产物。
(2)分子中只有一个 ,侧链都是 。
(3)通式为 (n≥7)。
烷基
苯环
烷基
CnH2n-6
苯的同系物
2、常见的苯的同系物
名 称 结构简式
甲苯
乙苯
苯的同系物
二甲苯 邻二甲苯
间二甲苯
对二甲苯
苯的同系物
3、物理性质
一般具有 的气味, 色液体,
溶于水, 溶于有机溶剂,密度比水的 。
类似苯
无
不
易
小
苯的同系物
4、化学性质
苯的同系物与苯都含有苯环,因此和苯具有相似的化学性质,能在一定条件下发生 、
和 反应,但由于 的相互影响,使苯的同系物的化学性质与苯和烷烃又有所不同。
溴代
硝化
催化加氢
苯环和烷基
苯的同系物
(1)氧化反应
①苯的同系物大多数能被酸性KMnO4溶液 而使其 。
②均能燃烧,燃烧的通式:
CnH2n-6+ O2 nCO2+(n-3)H2O
氧化
褪色
2mL苯
3滴高锰酸钾酸性溶液
用力振荡
2mL甲苯
3滴高锰酸钾酸性溶液
用力振荡
苯环影响侧链,使侧链能被强氧化剂氧化
实验结论:
苯不能被KMnO4酸性溶液氧化,甲苯能被KMnO4酸性溶液氧化
未褪色
褪色
苯的同系物
(2)取代反应
甲苯与浓硝酸和浓硫酸的混合物在加热条件下可以发生取代反应,生成一硝基取代物、二硝基取代物和三硝基取代物,硝基取代的位置均以甲基的邻对位为主。其中生成三硝基取代物的
化学方程式: ,有机产物名称
,又叫 ,用字母表示 。
(3)加成反应:
甲苯与氢气反应的化学方程式: 。
苯的同系物
2,4,6-三硝基甲苯
梯恩梯
TNT
苯 苯的同系物
相同点 结构组成 ①分子中都含有一个苯环②都符合分子通式CnH2n-6(n≥6)
化学性质 ①燃烧时现象相同,火焰明亮,伴有浓烟②都易发生苯环上的取代反应③都能发生加成反应,但都比较困难
苯与苯的同系物在分子组成、结构和性质上的异同
苯与苯的同系物在分子组成、结构和性质上的异同
苯 苯的同系物
不同点 取代反应 易发生取代反应,主要得到一元取代产物 更容易发生取代反应,常得到多元取代产物
氧化反应 难被氧化,不能使酸性KMnO4溶液褪色 易被氧化剂氧化,能使酸性KMnO4溶液褪色
差异原因 苯的同系物分子中,苯环与侧链相互影响。苯环影响侧链,使侧链烃基活化而易被氧化;侧链烃基影响苯环,使苯环上烃基邻、对位的氢原子活化而被取代
教学课件
感谢观看
