第七单元常见的酸和碱测试题(含答案)---2022-2023学年九年级化学鲁教版下册
文档属性
| 名称 | 第七单元常见的酸和碱测试题(含答案)---2022-2023学年九年级化学鲁教版下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 162.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-18 00:00:00 | ||
图片预览



文档简介
第七单元《常见的酸和碱》测试题
一、单选题
1.在化学实验中必须注意安全操作。下列说法中正确的是( )
①在点燃H2、CO、CH4等易燃气体前,必须检验气体的纯度
②稀释浓硫酸时将浓硫酸沿器壁慢慢注入水中,并用玻璃棒搅拌
③浓硫酸不慎滴到皮肤上,应立即用大量水冲洗,再用3%﹣5%的 NaHCO3溶液涂上
④给试管中液体加热,液体一般不超过试管容积的1/3
⑤称量任何固体药品时,均要在天平的左右托盘上放等大的相同的纸片
A.③④⑤ B.②④⑤ C.①②③④ D.①③⑤
2.对于碱,下列说法正确的是
A.碱一定含有H元素
B.可使酚酞变红的都是碱溶液
C.所有非金属氧化物都可与碱溶液反应
D.酸与碱反应一定无现象
3.下列反应属于复分解反应的是( )
A.2KClO32KCl+3O2↑
B.CuSO4+2NaOH=Na2SO4+Cu(OH)2↓
C.Zn+H2SO4=ZnSO4+H2↑
D.3CO+Fe2O32Fe+3CO2
4.下列物质属于碱的是
A.H2O B.NH3·H2O C.CaCO3 D.H3BO3
5.钠(Na)是一种非常活泼的金属,常温下能与O2、H2O等物质反应,加热时能与CO2反应生成C、CO、Na2O和Na2CO3四种物质,其中Na2O是白色固体,遇水可生成NaOH。下列有关说法正确的是
A.钠应密封保存于水中
B.钠着火后应立即用二氧化碳灭火器熄灭
C.钠与CO2的反应需在通风橱中进行
D.钠与CO2反应生成的白色固体加水溶解后,滴加少量盐酸一定会产生气泡
6.下列有关实验现象的描述,正确的是
A.打开浓盐酸的瓶盖,瓶口冒白烟 B.向氢氧化钠溶液中滴加酚酞溶液,溶液变成蓝色
C.硫燃烧生成有刺激性气味的气体 D.铁丝伸入盛有氧气的集气瓶中剧烈燃烧
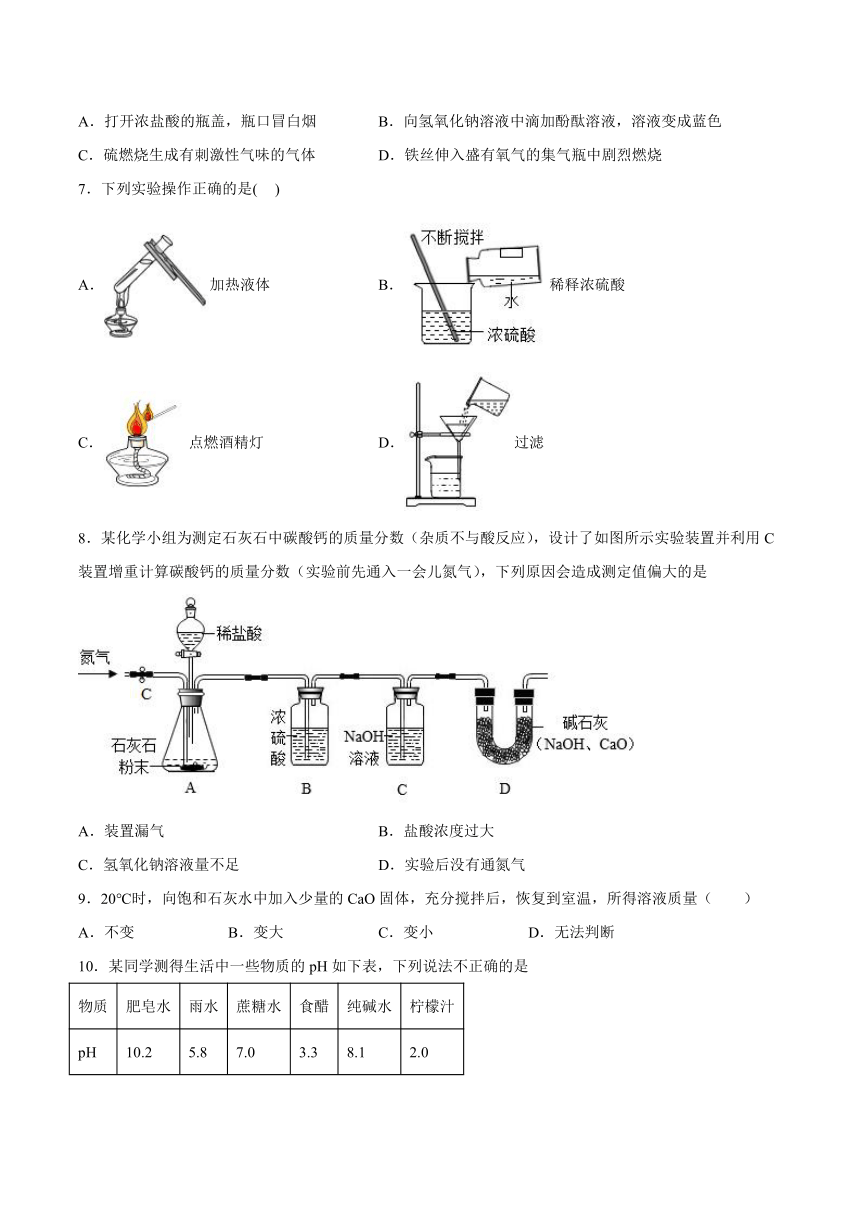
7.下列实验操作正确的是( )
A.加热液体 B.稀释浓硫酸
C.点燃酒精灯 D.过滤
8.某化学小组为测定石灰石中碳酸钙的质量分数(杂质不与酸反应),设计了如图所示实验装置并利用C装置增重计算碳酸钙的质量分数(实验前先通入一会儿氮气),下列原因会造成测定值偏大的是
A.装置漏气 B.盐酸浓度过大
C.氢氧化钠溶液量不足 D.实验后没有通氮气
9.20℃时,向饱和石灰水中加入少量的CaO固体,充分搅拌后,恢复到室温,所得溶液质量( )
A.不变 B.变大 C.变小 D.无法判断
10.某同学测得生活中一些物质的pH如下表,下列说法不正确的是
物质 肥皂水 雨水 蔗糖水 食醋 纯碱水 柠檬汁
pH 10.2 5.8 7.0 3.3 8.1 2.0
A.蔗糖水是中性的
B.肥皂水的碱性比纯碱水弱
C.柠檬汁的酸性比食醋强
D.雨水能使蓝色石蕊试纸变红
11.物质的性质决定用途,下列说法不正确的是
A.浓硫酸可以作食品干燥剂 B.干冰可以用于人工降雨
C.氩气可以做焊接金属时的保护气 D.氧气可以用于航天飞行时的助燃剂
12.下列物质的鉴别方法正确的是
A.用澄清石灰水鉴别氢气和一氧化碳
B.用无色酚酞试液鉴别澄清石灰水和氢氧化钠
C.用食盐水鉴别硬水和软水
D.用水鉴别硝酸铵固体和氢氧化钠固体
二、填空题
13.用化学符号填写:
(1)2个铵根离子________
(2)常见改良酸性土壤的碱是___________,
(3)溶于水能使溶液温度明显降低的___________
(4)氯化铁中铁元素的化合价___________________.
14.请用溶液的知识回答下列问题:
(1)净化水的操作有①过滤②蒸馏③静置沉淀等多种,其中净化程度最高的操作是_______(填序号);过滤时玻璃棒的作用是________;净水器中经常使用活性炭,主要利用活性炭的_______性。
(2)生活中常用________的方法降低水的硬度。
(3)A、B、C三种固体物质的溶解度曲线如图所示。
①t1℃时,A、B、C三种物质的溶解度由大到小的顺序是__________。
②A、B、C三种物质中,溶解度随温度升高而减小的是____________。
③t1℃时,相同质量的A、B饱和溶液中,A的饱和溶液中所含水的质量________B的饱和溶液中所含水的质量(填“大于”、“等于”或“小于”)。
(4)下图是某试剂瓶标签上的部分内容。请回答下列问题:
①该浓硫酸的溶质是________,溶液的质量是________g。
②稀释浓硫酸时,一定要把________沿烧杯壁慢慢注入盛_______的烧杯里,并用玻璃棒不断搅拌。
15.酸、碱是初中化学学习中重要的化合物。
(1)下列有关盐酸和硫酸的说法不正确的是______。
A 稀盐酸和稀硫酸都可用来除铁锈
B 打开浓盐酸或浓硫酸的试剂瓶瓶塞,瓶口都会产生白雾
C 稀盐酸和稀硫酸化学性质相似的原因是溶液中都有H+
D 将浓盐酸和浓硫酸敞口放置,溶液的溶质质量分数均减小
(2)如图所示,在白色点滴板1-5的孔穴中,分别滴加2滴稀盐酸。
有明显变化的孔穴有______(填孔穴序号)。
(3)实验小组用pH传感器探究稀盐酸和氢氧化钠溶液反应。实验操作和测定结果如图所示:
①盐酸和氢氧化钠反应的化学方程式为______。
②该实验中,甲溶液是______。
③能说明盐酸与氢氧化钠发生化学反应的依据是______。
④60s时,烧瓶内溶液中的溶质是______。
三、推断题
16.如图中的物质为初中化学常见物质,他们之间的反应关系如图所示(“→”表示转化关系,“一”表示相互能反应,部分反应物、生成物或反应条件已略去)。甲与A溶液反应得到浅绿色溶液;A、B发生中和反应,产物之一是厨房内常用的调味品;C常用于改良酸性土壤,且C的溶液与D的溶液反应可得到B;C的溶液与乙的溶液反应生成蓝色沉淀;乙与丙两种溶液反应生成两种不同颜色的沉淀。请回答
(1)D的化学式为______。
(2)乙在农业生产中的用途是_______。
(3)甲与乙反应的基本反应类型_____。
(4)欲通过一步实验证明A、B是否恰好完全反应,需要向A、B反应后的溶液中加入的试剂是__。
(5)乙与丙两溶液反应的化学方程式为______。
17.A~F 是初中化学常见的六种物质,化学兴趣小组同学设计了如下图所示的接龙游戏, 箭头表示一种物质可以转化成另一种物质。A是最常见的溶剂, B、C 为无色无味气体,A 转化成 E 为放热反应,且E、F 物质类别相同,D 与 E 反应可生成 F。
(1)写出下列物质的名称:
A_____ C_____。
(2)写出A 转化成B 的化学方程式:_____, 该反应属于_____(填基本反应类型)。
(3)D 与 E 反应生成 F 可观察到_____的现象。
四、实验题
18.某兴趣小组在探究碱的性质时进行下列图示的实验,请回答有关问题。
(1)通过分析实验1可知,氢氧化钠会吸收空气中的___________。
(2)实验2中观察到3个塑料瓶变瘪的程度为A>B>C,可证明能与、反应,其中C瓶在实验中起__________作用,A、B瓶变瘪程度差异的原因是__________。
(3)晓晓查阅资料了解到往溶液中滴加或通入图(2)中物质会产生如下现象:A中溶液显红色,B、C、D中均产生白色沉淀。
①写出D试管中反应的化学方程式:___________________。
②不同的碱溶液中都含有,所以碱有一些相似的化学性质。上述关于性质的实验不能体现碱的相似性质的是____________(填字母序号)。
五、计算题
19.水垢的主要成分是CaCO3,可以用白醋(主要成分是醋酸,用HA表示)浸泡除去。反应的化学方程式为,请计算:
(1)碳酸钙中钙元素的质量分数。
(2)若某水壶水垢中CaCO3的质量为10g,则完全除去时生成二氧化碳的质量是多少?
参考答案:
1.C 2.A 3.B 4.B 5.C 6.C 7.C 8.B 9.C 10.B 11.A 12.D
13. 2NH4+ Ca(OH)2 NH4NO3
14. ② 引流 吸附 煮沸 C>B>A(C、B、A) C 大于 硫酸(H2SO4) 920 浓硫酸 水
15. B 1、3、6 NaOH+HCl=NaCl+H2O 氢氧化钠溶液 溶液的pH不断增大且大于7 氢氧化钠和氯化钠(NaOH、NaCl)
16. Na2CO3 配制农药波尔多液等 置换反应 紫色石蕊溶液等
17. 水 二氧化碳 2H2O2H2↑+O2↑ 分解反应 有白色沉淀产生
18. 水 对比 易溶于水,其饱和溶液的浓度大,吸收的效果好,而微溶于水,其饱和溶液的浓度小,吸收的效果差 C
19.(1)碳酸钙中钙元素的质量分数为 ,
答:碳酸钙中钙元素的质量分数为40%。
(2)解:设完全除去时生成二氧化碳的质量是x
答:完全除去时生成二氧化碳的质量是4.4g
一、单选题
1.在化学实验中必须注意安全操作。下列说法中正确的是( )
①在点燃H2、CO、CH4等易燃气体前,必须检验气体的纯度
②稀释浓硫酸时将浓硫酸沿器壁慢慢注入水中,并用玻璃棒搅拌
③浓硫酸不慎滴到皮肤上,应立即用大量水冲洗,再用3%﹣5%的 NaHCO3溶液涂上
④给试管中液体加热,液体一般不超过试管容积的1/3
⑤称量任何固体药品时,均要在天平的左右托盘上放等大的相同的纸片
A.③④⑤ B.②④⑤ C.①②③④ D.①③⑤
2.对于碱,下列说法正确的是
A.碱一定含有H元素
B.可使酚酞变红的都是碱溶液
C.所有非金属氧化物都可与碱溶液反应
D.酸与碱反应一定无现象
3.下列反应属于复分解反应的是( )
A.2KClO32KCl+3O2↑
B.CuSO4+2NaOH=Na2SO4+Cu(OH)2↓
C.Zn+H2SO4=ZnSO4+H2↑
D.3CO+Fe2O32Fe+3CO2
4.下列物质属于碱的是
A.H2O B.NH3·H2O C.CaCO3 D.H3BO3
5.钠(Na)是一种非常活泼的金属,常温下能与O2、H2O等物质反应,加热时能与CO2反应生成C、CO、Na2O和Na2CO3四种物质,其中Na2O是白色固体,遇水可生成NaOH。下列有关说法正确的是
A.钠应密封保存于水中
B.钠着火后应立即用二氧化碳灭火器熄灭
C.钠与CO2的反应需在通风橱中进行
D.钠与CO2反应生成的白色固体加水溶解后,滴加少量盐酸一定会产生气泡
6.下列有关实验现象的描述,正确的是
A.打开浓盐酸的瓶盖,瓶口冒白烟 B.向氢氧化钠溶液中滴加酚酞溶液,溶液变成蓝色
C.硫燃烧生成有刺激性气味的气体 D.铁丝伸入盛有氧气的集气瓶中剧烈燃烧
7.下列实验操作正确的是( )
A.加热液体 B.稀释浓硫酸
C.点燃酒精灯 D.过滤
8.某化学小组为测定石灰石中碳酸钙的质量分数(杂质不与酸反应),设计了如图所示实验装置并利用C装置增重计算碳酸钙的质量分数(实验前先通入一会儿氮气),下列原因会造成测定值偏大的是
A.装置漏气 B.盐酸浓度过大
C.氢氧化钠溶液量不足 D.实验后没有通氮气
9.20℃时,向饱和石灰水中加入少量的CaO固体,充分搅拌后,恢复到室温,所得溶液质量( )
A.不变 B.变大 C.变小 D.无法判断
10.某同学测得生活中一些物质的pH如下表,下列说法不正确的是
物质 肥皂水 雨水 蔗糖水 食醋 纯碱水 柠檬汁
pH 10.2 5.8 7.0 3.3 8.1 2.0
A.蔗糖水是中性的
B.肥皂水的碱性比纯碱水弱
C.柠檬汁的酸性比食醋强
D.雨水能使蓝色石蕊试纸变红
11.物质的性质决定用途,下列说法不正确的是
A.浓硫酸可以作食品干燥剂 B.干冰可以用于人工降雨
C.氩气可以做焊接金属时的保护气 D.氧气可以用于航天飞行时的助燃剂
12.下列物质的鉴别方法正确的是
A.用澄清石灰水鉴别氢气和一氧化碳
B.用无色酚酞试液鉴别澄清石灰水和氢氧化钠
C.用食盐水鉴别硬水和软水
D.用水鉴别硝酸铵固体和氢氧化钠固体
二、填空题
13.用化学符号填写:
(1)2个铵根离子________
(2)常见改良酸性土壤的碱是___________,
(3)溶于水能使溶液温度明显降低的___________
(4)氯化铁中铁元素的化合价___________________.
14.请用溶液的知识回答下列问题:
(1)净化水的操作有①过滤②蒸馏③静置沉淀等多种,其中净化程度最高的操作是_______(填序号);过滤时玻璃棒的作用是________;净水器中经常使用活性炭,主要利用活性炭的_______性。
(2)生活中常用________的方法降低水的硬度。
(3)A、B、C三种固体物质的溶解度曲线如图所示。
①t1℃时,A、B、C三种物质的溶解度由大到小的顺序是__________。
②A、B、C三种物质中,溶解度随温度升高而减小的是____________。
③t1℃时,相同质量的A、B饱和溶液中,A的饱和溶液中所含水的质量________B的饱和溶液中所含水的质量(填“大于”、“等于”或“小于”)。
(4)下图是某试剂瓶标签上的部分内容。请回答下列问题:
①该浓硫酸的溶质是________,溶液的质量是________g。
②稀释浓硫酸时,一定要把________沿烧杯壁慢慢注入盛_______的烧杯里,并用玻璃棒不断搅拌。
15.酸、碱是初中化学学习中重要的化合物。
(1)下列有关盐酸和硫酸的说法不正确的是______。
A 稀盐酸和稀硫酸都可用来除铁锈
B 打开浓盐酸或浓硫酸的试剂瓶瓶塞,瓶口都会产生白雾
C 稀盐酸和稀硫酸化学性质相似的原因是溶液中都有H+
D 将浓盐酸和浓硫酸敞口放置,溶液的溶质质量分数均减小
(2)如图所示,在白色点滴板1-5的孔穴中,分别滴加2滴稀盐酸。
有明显变化的孔穴有______(填孔穴序号)。
(3)实验小组用pH传感器探究稀盐酸和氢氧化钠溶液反应。实验操作和测定结果如图所示:
①盐酸和氢氧化钠反应的化学方程式为______。
②该实验中,甲溶液是______。
③能说明盐酸与氢氧化钠发生化学反应的依据是______。
④60s时,烧瓶内溶液中的溶质是______。
三、推断题
16.如图中的物质为初中化学常见物质,他们之间的反应关系如图所示(“→”表示转化关系,“一”表示相互能反应,部分反应物、生成物或反应条件已略去)。甲与A溶液反应得到浅绿色溶液;A、B发生中和反应,产物之一是厨房内常用的调味品;C常用于改良酸性土壤,且C的溶液与D的溶液反应可得到B;C的溶液与乙的溶液反应生成蓝色沉淀;乙与丙两种溶液反应生成两种不同颜色的沉淀。请回答
(1)D的化学式为______。
(2)乙在农业生产中的用途是_______。
(3)甲与乙反应的基本反应类型_____。
(4)欲通过一步实验证明A、B是否恰好完全反应,需要向A、B反应后的溶液中加入的试剂是__。
(5)乙与丙两溶液反应的化学方程式为______。
17.A~F 是初中化学常见的六种物质,化学兴趣小组同学设计了如下图所示的接龙游戏, 箭头表示一种物质可以转化成另一种物质。A是最常见的溶剂, B、C 为无色无味气体,A 转化成 E 为放热反应,且E、F 物质类别相同,D 与 E 反应可生成 F。
(1)写出下列物质的名称:
A_____ C_____。
(2)写出A 转化成B 的化学方程式:_____, 该反应属于_____(填基本反应类型)。
(3)D 与 E 反应生成 F 可观察到_____的现象。
四、实验题
18.某兴趣小组在探究碱的性质时进行下列图示的实验,请回答有关问题。
(1)通过分析实验1可知,氢氧化钠会吸收空气中的___________。
(2)实验2中观察到3个塑料瓶变瘪的程度为A>B>C,可证明能与、反应,其中C瓶在实验中起__________作用,A、B瓶变瘪程度差异的原因是__________。
(3)晓晓查阅资料了解到往溶液中滴加或通入图(2)中物质会产生如下现象:A中溶液显红色,B、C、D中均产生白色沉淀。
①写出D试管中反应的化学方程式:___________________。
②不同的碱溶液中都含有,所以碱有一些相似的化学性质。上述关于性质的实验不能体现碱的相似性质的是____________(填字母序号)。
五、计算题
19.水垢的主要成分是CaCO3,可以用白醋(主要成分是醋酸,用HA表示)浸泡除去。反应的化学方程式为,请计算:
(1)碳酸钙中钙元素的质量分数。
(2)若某水壶水垢中CaCO3的质量为10g,则完全除去时生成二氧化碳的质量是多少?
参考答案:
1.C 2.A 3.B 4.B 5.C 6.C 7.C 8.B 9.C 10.B 11.A 12.D
13. 2NH4+ Ca(OH)2 NH4NO3
14. ② 引流 吸附 煮沸 C>B>A(C、B、A) C 大于 硫酸(H2SO4) 920 浓硫酸 水
15. B 1、3、6 NaOH+HCl=NaCl+H2O 氢氧化钠溶液 溶液的pH不断增大且大于7 氢氧化钠和氯化钠(NaOH、NaCl)
16. Na2CO3 配制农药波尔多液等 置换反应 紫色石蕊溶液等
17. 水 二氧化碳 2H2O2H2↑+O2↑ 分解反应 有白色沉淀产生
18. 水 对比 易溶于水,其饱和溶液的浓度大,吸收的效果好,而微溶于水,其饱和溶液的浓度小,吸收的效果差 C
19.(1)碳酸钙中钙元素的质量分数为 ,
答:碳酸钙中钙元素的质量分数为40%。
(2)解:设完全除去时生成二氧化碳的质量是x
答:完全除去时生成二氧化碳的质量是4.4g
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
