第七章溶液测试题--2022-2023学年九年级化学科粤版(2012)下册(含答案)
文档属性
| 名称 | 第七章溶液测试题--2022-2023学年九年级化学科粤版(2012)下册(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 268.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 其它版本 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-19 00:00:00 | ||
图片预览



文档简介
第七章《溶液》测试题
一、单选题
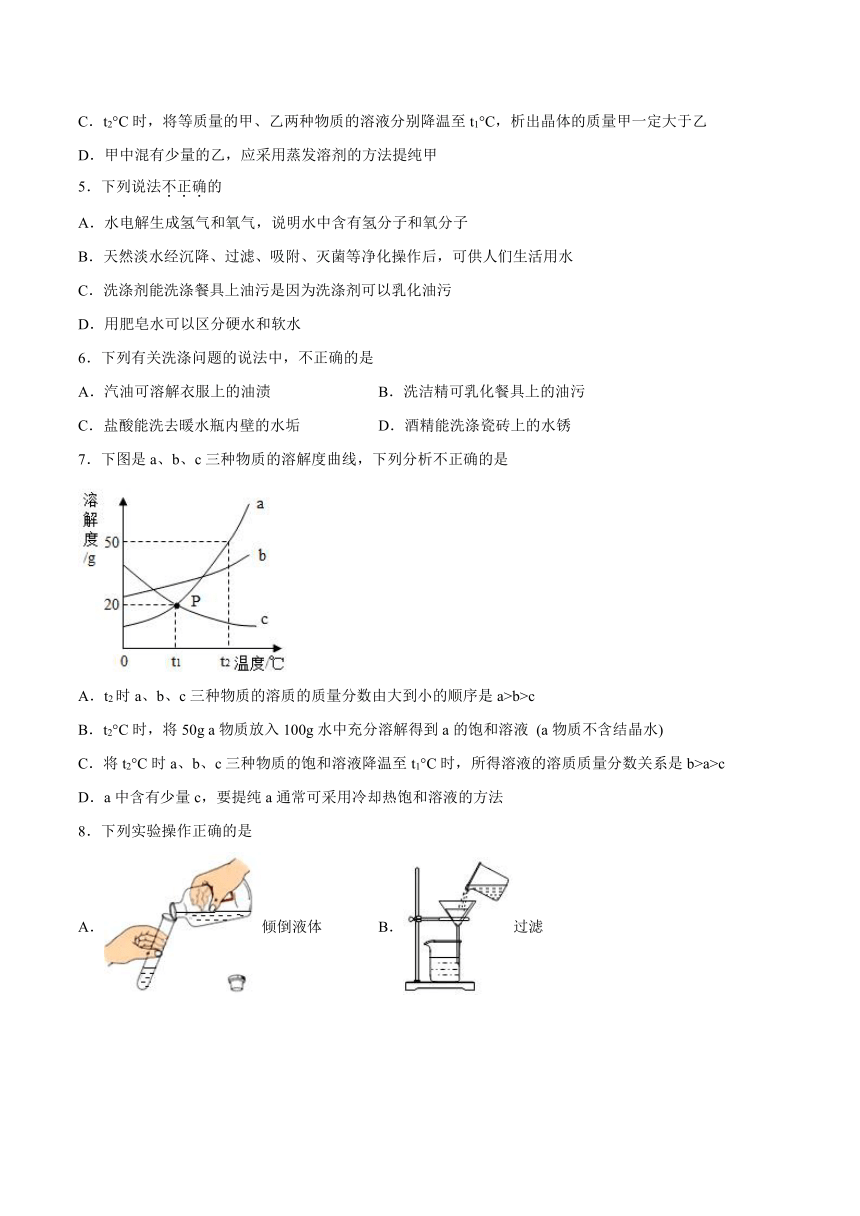
1.KNO3与NH4Cl的溶解度曲线如图。下列说法错误的是
A.常温下,NH4Cl易溶于水
B.t2℃时,两种溶液中溶质的质量分数一定相等
C.t3℃时,100g水中所能溶解的的KNO3的质量多于NH4Cl的质量
D.两种饱和溶液从t2℃降到t1℃时,均有晶体析出
2.水是重要的资源。下列关于水的说法不正确的是
A.通过氢气在氧气中燃烧生成水的实验,可证明水由氢、氧元素组成
B.自然界的水经过沉淀、过滤、吸附等操作,可得到纯净的水
C.生活中用肥皂水可鉴别硬水和软水
D.水是最常见的溶剂,高锰酸钾易溶于水,而碘几乎不溶于水
3.下列事实的解释不正确的是( )
A.水变成水蒸气体积增大--水分子变大 B.氮气用作保护气--氮气化学性质不活泼
C.洗洁精能除油污--洗洁精具有乳化作用 D.铁生锈--铁与氧气和水蒸气等发生反应
4.如图是甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法中正确的是
A.甲物质的溶解度大于乙物质的溶解度
B.t2°C时,甲饱和溶液中溶质的质量分数一定大于乙饱和溶液中溶质的质量分数
C.t2°C时,将等质量的甲、乙两种物质的溶液分别降温至t1°C,析出晶体的质量甲一定大于乙
D.甲中混有少量的乙,应采用蒸发溶剂的方法提纯甲
5.下列说法不正确的
A.水电解生成氢气和氧气,说明水中含有氢分子和氧分子
B.天然淡水经沉降、过滤、吸附、灭菌等净化操作后,可供人们生活用水
C.洗涤剂能洗涤餐具上油污是因为洗涤剂可以乳化油污
D.用肥皂水可以区分硬水和软水
6.下列有关洗涤问题的说法中,不正确的是
A.汽油可溶解衣服上的油渍 B.洗洁精可乳化餐具上的油污
C.盐酸能洗去暖水瓶内壁的水垢 D.酒精能洗涤瓷砖上的水锈
7.下图是a、b、c三种物质的溶解度曲线,下列分析不正确的是
A.t2时a、b、c三种物质的溶质的质量分数由大到小的顺序是a>b>c
B.t2°C时,将50g a物质放入100g水中充分溶解得到a的饱和溶液 (a物质不含结晶水)
C.将t2°C时a、b、c三种物质的饱和溶液降温至t1°C时,所得溶液的溶质质量分数关系是b>a>c
D.a中含有少量c,要提纯a通常可采用冷却热饱和溶液的方法
8.下列实验操作正确的是
A.倾倒液体 B.过滤
C.验满 D.给液体加热
9.下列实验操作正确的是( )
A.量取9.5mL液体 B.液体过滤
C.点燃酒精灯 D.制取蒸馏水
10.在蒸馏水中加入NaOH固体,不断搅拌,用温度传感器记录溶解过程的温度变化,如图a、c两点观察到溶液中有固体存在,b点固体完全消失。下列说法不正确的是
A.NaOH固体溶于水是放热过程
B.a、c两点时,NaOH溶解度相同
C.b点时,该溶液一定是不饱和溶液
D.d点时,该溶液一定是饱和溶液
11.下列实验方案能达到实验目的的是
A.探究物质溶解性与溶剂种类有关
B.区分硬水和软水
C.验证质量守恒定律
D.测定空气中氧气的含量
二、填空题
12.如图所示是a、b、c三种物质的溶解度曲线,根据图示回答:
Ⅰ.P点的含义是______________________。
Ⅱ.t2℃时,将30g a物质加入到50g水中不断搅拌,溶液质量为______________g。
Ⅲ.要把t1℃时C物质的不饱和溶液变为饱和溶液,有关说法正确的是__________。
A 可以采取升高温度的方法 B 溶剂的质量一定不变
C 溶质的质量分数一定变大 D 溶质的质量可能不变
Ⅳ.若a溶液中含有少量b,则提纯a的方法是_________________。
Ⅴ.t3℃时,将等质量的a、b、c三种物质饱和溶液降温到t1℃时,三种溶液的溶剂质量大小关系是_______________。
13.2020年“世界水日”的主题为“水与气候变化”。
(1)饮用硬度过大的水不利于人体健康,常用_______区分是硬水还是软水;生活中,将硬水软化并起到消毒杀菌作用的简单方法是_______。
(2)用加了洗涤剂的水能洗掉餐具的油污,这利用了洗涤剂的_______作用。
(3)如图为实验室电解水的装置,玻璃管a、b中收集到的气体体积比约为_______,反应的化学方程式为_______。
(4)下列关于水资源的说法不正确的是_______。(填序号)
①依法加强水资源监测和管理
②生活污水应集中处理排放
③地球上可供利用的淡水资源是丰富的
④农业上改大水漫灌为喷灌、滴灌可节约水资源
14.化学源于生活,服务于生活.
(1)食盐的主要成分是氯化钠(NaCl),其中氯元素的化合价为_______.
(2)餐具上的油污可用加洗涤剂的水洗掉,这是利用洗涤剂的_______作用.
(3)打开食醋的瓶子,闻到一股刺鼻的气味,原因是_______(从微观角度回答).
三、推断题
15.已知,A、B、C、D四种物质之间存在以下转化关系。其中C是单质,D是相对分子质量最小的氧化物。试回答:
(1)写出A、C、D三种物质的化学式:A ________ 、C ______ 、D __________ 。
(2)浅绿色溶液B中溶质的化学式 _______________ 。
(3)写出A→C的化学方程式: ______________________________ 。
16.已知,氧化铜与盐酸反应程成有色溶液,现有一包固体粉末,只可能含有氧化铜、碳、铝、铁、铜中的一种或几种。取适量样品进行分析,流程和实验现象如下图。请回答相关问题:
(1)操作a在名称是___________,操作时需要的玻璃仪器烧杯、玻璃棒和___________。
(2)向样品中加过量稀盐酸有气体产生,发生反应的化学方程式为___________。
(3)向固体A中加入硝酸银溶液,发生反应的化学方程式为____________。
(4)分析结果:这包固体粉末一定含有的物质是________(写化学式)。
四、实验题
17.根据如图回答有关问题。
(1)若要量取8mL稀盐酸,还缺少仪器是_____。
(2)利用上述仪器对浑浊的河水进行过滤,除了选择铁架台(带铁圈)外,还需选择图中的仪器是_____(填标号)。
(3)用加热高锰酸钾的方法制取氧气,反应的化学方程式是_____,选择以上仪器中的_____(填标号)来组装气体发生装置。
(4)利用“图甲”来制取CO2,该装置的优点是能控制反应随时开始和停止,为探究该优点的原因,在装置中连接压强传感器(如“图乙”),测定实验中试管内气体压强变化的情况如“图丙”所示。下列说法正确的是_____(填序号)。
①ab段试管中液面逐渐上升
②bc段石灰石与稀盐酸脱离接触
③c点的对应操作是打开弹簧夹
18.水是重要的自然资源,在化学实验中起重要作用.
(1)请根据以下实验回答问题:
①从微观角度分析,下图所示实验1和实验2的本质区别是_______________________________.
②分析实验2的结论是:水是由____________________组成的
(2)水是很好的溶剂.如图所示是a、b两种固体物质在水中溶解度曲线,根据图回答:
①30℃时,50g水中加入25g物质a,充分搅拌所得溶液的质量为______ ,属于______溶液(填“饱和”或“不饱和”)。
②如图所示,试管1、2中分别盛有20℃时等质量的a、b物质饱和溶液,底部有等质量的a、b固体剩余,向烧杯的水中加入硝酸铵固体,下列判断正确的是__(不考虑溶剂的蒸发,析出的固体不含水)。
A a物质溶液由饱和溶液变成不饱和溶液 B 试管2底部的b物质固体增多
C 变化后溶液中溶质质量分数:a>b D a、b物质的溶液中溶剂质量相等
五、计算题
19.硅酸钠(Na2SiO3)是我国优先发展的精细化工产品。现以125t石英砂(其中SiO2质量分数为96%)为原料,与足量的NaOH溶液恰好完全反应,得到硅酸钠溶液的质量为610t。已知:工业制备硅酸钠的反应为:2NaOH+ SiO2 Na2SiO3 + H2O;
试计算:
(1)125t石英砂中SiO2的质量。__
(2)所得硅酸钠溶液中溶质的质量分数(石英砂中杂质不溶于水)。__
参考答案:
1.B 2.B 3.A 4.B 5.A 6.D 7.A 8.D 9.C 10.C 11.B
12. t1℃,a和c的溶解度相等,都为20g/100g水 75 AD 蒸发浓缩、降温结晶 c>b>a
13.(1) 肥皂水 加热煮沸
(2)乳化
(3) 2:1
(4)③
14. ﹣1 乳化 分子是不断运动的
15.(1) Fe H2 H2O
(2)FeSO4
(3)
16. 过滤 漏斗 2Al+6HCl=2AlCl3+3H2↑ Cu+2AgNO3=Cu(NO3)2+2Ag Al、Cu、C
17.(1)胶头滴管
(2)ABF
(3)
CDGH
(4)②③
18. 水分子是否改变 氢、氧元素 70g 饱和 D
19. 解:125t石英砂中SiO2的质量为:125t ×96%=120t 设设所得Na2SiO3的质量为x。
所得硅酸钠溶液中溶质的质量分数为
答:(1)125t石英砂中SiO2的质量是120t,(2)所得硅酸钠溶液中溶质质量分数为40%
一、单选题
1.KNO3与NH4Cl的溶解度曲线如图。下列说法错误的是
A.常温下,NH4Cl易溶于水
B.t2℃时,两种溶液中溶质的质量分数一定相等
C.t3℃时,100g水中所能溶解的的KNO3的质量多于NH4Cl的质量
D.两种饱和溶液从t2℃降到t1℃时,均有晶体析出
2.水是重要的资源。下列关于水的说法不正确的是
A.通过氢气在氧气中燃烧生成水的实验,可证明水由氢、氧元素组成
B.自然界的水经过沉淀、过滤、吸附等操作,可得到纯净的水
C.生活中用肥皂水可鉴别硬水和软水
D.水是最常见的溶剂,高锰酸钾易溶于水,而碘几乎不溶于水
3.下列事实的解释不正确的是( )
A.水变成水蒸气体积增大--水分子变大 B.氮气用作保护气--氮气化学性质不活泼
C.洗洁精能除油污--洗洁精具有乳化作用 D.铁生锈--铁与氧气和水蒸气等发生反应
4.如图是甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法中正确的是
A.甲物质的溶解度大于乙物质的溶解度
B.t2°C时,甲饱和溶液中溶质的质量分数一定大于乙饱和溶液中溶质的质量分数
C.t2°C时,将等质量的甲、乙两种物质的溶液分别降温至t1°C,析出晶体的质量甲一定大于乙
D.甲中混有少量的乙,应采用蒸发溶剂的方法提纯甲
5.下列说法不正确的
A.水电解生成氢气和氧气,说明水中含有氢分子和氧分子
B.天然淡水经沉降、过滤、吸附、灭菌等净化操作后,可供人们生活用水
C.洗涤剂能洗涤餐具上油污是因为洗涤剂可以乳化油污
D.用肥皂水可以区分硬水和软水
6.下列有关洗涤问题的说法中,不正确的是
A.汽油可溶解衣服上的油渍 B.洗洁精可乳化餐具上的油污
C.盐酸能洗去暖水瓶内壁的水垢 D.酒精能洗涤瓷砖上的水锈
7.下图是a、b、c三种物质的溶解度曲线,下列分析不正确的是
A.t2时a、b、c三种物质的溶质的质量分数由大到小的顺序是a>b>c
B.t2°C时,将50g a物质放入100g水中充分溶解得到a的饱和溶液 (a物质不含结晶水)
C.将t2°C时a、b、c三种物质的饱和溶液降温至t1°C时,所得溶液的溶质质量分数关系是b>a>c
D.a中含有少量c,要提纯a通常可采用冷却热饱和溶液的方法
8.下列实验操作正确的是
A.倾倒液体 B.过滤
C.验满 D.给液体加热
9.下列实验操作正确的是( )
A.量取9.5mL液体 B.液体过滤
C.点燃酒精灯 D.制取蒸馏水
10.在蒸馏水中加入NaOH固体,不断搅拌,用温度传感器记录溶解过程的温度变化,如图a、c两点观察到溶液中有固体存在,b点固体完全消失。下列说法不正确的是
A.NaOH固体溶于水是放热过程
B.a、c两点时,NaOH溶解度相同
C.b点时,该溶液一定是不饱和溶液
D.d点时,该溶液一定是饱和溶液
11.下列实验方案能达到实验目的的是
A.探究物质溶解性与溶剂种类有关
B.区分硬水和软水
C.验证质量守恒定律
D.测定空气中氧气的含量
二、填空题
12.如图所示是a、b、c三种物质的溶解度曲线,根据图示回答:
Ⅰ.P点的含义是______________________。
Ⅱ.t2℃时,将30g a物质加入到50g水中不断搅拌,溶液质量为______________g。
Ⅲ.要把t1℃时C物质的不饱和溶液变为饱和溶液,有关说法正确的是__________。
A 可以采取升高温度的方法 B 溶剂的质量一定不变
C 溶质的质量分数一定变大 D 溶质的质量可能不变
Ⅳ.若a溶液中含有少量b,则提纯a的方法是_________________。
Ⅴ.t3℃时,将等质量的a、b、c三种物质饱和溶液降温到t1℃时,三种溶液的溶剂质量大小关系是_______________。
13.2020年“世界水日”的主题为“水与气候变化”。
(1)饮用硬度过大的水不利于人体健康,常用_______区分是硬水还是软水;生活中,将硬水软化并起到消毒杀菌作用的简单方法是_______。
(2)用加了洗涤剂的水能洗掉餐具的油污,这利用了洗涤剂的_______作用。
(3)如图为实验室电解水的装置,玻璃管a、b中收集到的气体体积比约为_______,反应的化学方程式为_______。
(4)下列关于水资源的说法不正确的是_______。(填序号)
①依法加强水资源监测和管理
②生活污水应集中处理排放
③地球上可供利用的淡水资源是丰富的
④农业上改大水漫灌为喷灌、滴灌可节约水资源
14.化学源于生活,服务于生活.
(1)食盐的主要成分是氯化钠(NaCl),其中氯元素的化合价为_______.
(2)餐具上的油污可用加洗涤剂的水洗掉,这是利用洗涤剂的_______作用.
(3)打开食醋的瓶子,闻到一股刺鼻的气味,原因是_______(从微观角度回答).
三、推断题
15.已知,A、B、C、D四种物质之间存在以下转化关系。其中C是单质,D是相对分子质量最小的氧化物。试回答:
(1)写出A、C、D三种物质的化学式:A ________ 、C ______ 、D __________ 。
(2)浅绿色溶液B中溶质的化学式 _______________ 。
(3)写出A→C的化学方程式: ______________________________ 。
16.已知,氧化铜与盐酸反应程成有色溶液,现有一包固体粉末,只可能含有氧化铜、碳、铝、铁、铜中的一种或几种。取适量样品进行分析,流程和实验现象如下图。请回答相关问题:
(1)操作a在名称是___________,操作时需要的玻璃仪器烧杯、玻璃棒和___________。
(2)向样品中加过量稀盐酸有气体产生,发生反应的化学方程式为___________。
(3)向固体A中加入硝酸银溶液,发生反应的化学方程式为____________。
(4)分析结果:这包固体粉末一定含有的物质是________(写化学式)。
四、实验题
17.根据如图回答有关问题。
(1)若要量取8mL稀盐酸,还缺少仪器是_____。
(2)利用上述仪器对浑浊的河水进行过滤,除了选择铁架台(带铁圈)外,还需选择图中的仪器是_____(填标号)。
(3)用加热高锰酸钾的方法制取氧气,反应的化学方程式是_____,选择以上仪器中的_____(填标号)来组装气体发生装置。
(4)利用“图甲”来制取CO2,该装置的优点是能控制反应随时开始和停止,为探究该优点的原因,在装置中连接压强传感器(如“图乙”),测定实验中试管内气体压强变化的情况如“图丙”所示。下列说法正确的是_____(填序号)。
①ab段试管中液面逐渐上升
②bc段石灰石与稀盐酸脱离接触
③c点的对应操作是打开弹簧夹
18.水是重要的自然资源,在化学实验中起重要作用.
(1)请根据以下实验回答问题:
①从微观角度分析,下图所示实验1和实验2的本质区别是_______________________________.
②分析实验2的结论是:水是由____________________组成的
(2)水是很好的溶剂.如图所示是a、b两种固体物质在水中溶解度曲线,根据图回答:
①30℃时,50g水中加入25g物质a,充分搅拌所得溶液的质量为______ ,属于______溶液(填“饱和”或“不饱和”)。
②如图所示,试管1、2中分别盛有20℃时等质量的a、b物质饱和溶液,底部有等质量的a、b固体剩余,向烧杯的水中加入硝酸铵固体,下列判断正确的是__(不考虑溶剂的蒸发,析出的固体不含水)。
A a物质溶液由饱和溶液变成不饱和溶液 B 试管2底部的b物质固体增多
C 变化后溶液中溶质质量分数:a>b D a、b物质的溶液中溶剂质量相等
五、计算题
19.硅酸钠(Na2SiO3)是我国优先发展的精细化工产品。现以125t石英砂(其中SiO2质量分数为96%)为原料,与足量的NaOH溶液恰好完全反应,得到硅酸钠溶液的质量为610t。已知:工业制备硅酸钠的反应为:2NaOH+ SiO2 Na2SiO3 + H2O;
试计算:
(1)125t石英砂中SiO2的质量。__
(2)所得硅酸钠溶液中溶质的质量分数(石英砂中杂质不溶于水)。__
参考答案:
1.B 2.B 3.A 4.B 5.A 6.D 7.A 8.D 9.C 10.C 11.B
12. t1℃,a和c的溶解度相等,都为20g/100g水 75 AD 蒸发浓缩、降温结晶 c>b>a
13.(1) 肥皂水 加热煮沸
(2)乳化
(3) 2:1
(4)③
14. ﹣1 乳化 分子是不断运动的
15.(1) Fe H2 H2O
(2)FeSO4
(3)
16. 过滤 漏斗 2Al+6HCl=2AlCl3+3H2↑ Cu+2AgNO3=Cu(NO3)2+2Ag Al、Cu、C
17.(1)胶头滴管
(2)ABF
(3)
CDGH
(4)②③
18. 水分子是否改变 氢、氧元素 70g 饱和 D
19. 解:125t石英砂中SiO2的质量为:125t ×96%=120t 设设所得Na2SiO3的质量为x。
所得硅酸钠溶液中溶质的质量分数为
答:(1)125t石英砂中SiO2的质量是120t,(2)所得硅酸钠溶液中溶质质量分数为40%
同课章节目录
