专题8 有机化合物的获得与应用 检测题(含解析) 2022-2023学年下学期高一化学苏教版(2019)必修第二册
文档属性
| 名称 | 专题8 有机化合物的获得与应用 检测题(含解析) 2022-2023学年下学期高一化学苏教版(2019)必修第二册 |

|
|
| 格式 | docx | ||
| 文件大小 | 174.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-20 00:00:00 | ||
图片预览




文档简介
专题8 有机化合物的获得与应用 检测题
一、单选题
1.下列说法正确的是
A.相对分子质量相等的两种有机物必定是同分异构体
B.乙烯、聚乙烯的结构简式相同,均可发生加成反应
C.经测定,间二甲苯只有一种结构可证明苯分子中单双键交替结构
D.化学性质相似的有机物不一定是同系物
2.下列关于常见有机化合物的说法中,正确的是
A.苯不能因反应而使溴水褪色但能使酸性高锰酸钾溶液褪色
B.甲烷的一氯代物只有一种可证明甲烷为正四面体结构而不是平面形
C.可用溴水鉴别四氯化碳和己烷这两种无色液体
D.乙烯和聚乙烯都能与溴的四氯化碳溶液发生加成反应
3.下列关于烃的说法正确的是
A.丙烯与溴水发生加成反应的产物是
B.通式为一定是烷烃,通式为一定是烯烃
C.用溴水或酸性溶液都可以除去乙烷中混有的乙烯
D.乙烯和苯分子中的所有原子均在同一平面内
4.下列说法错误的是
A.CH3—CH=CH2和CH2=CH2的最简式相同
B.苯、甲苯、苯酚均能发生取代反应
C.乙烯使酸性高锰酸钾溶液及溴的四氯化碳溶液褪色原理相同
D.常压下,正戊烷、异戊烷、新戊烷的沸点依次降低
5.页岩气是指赋存于富有机质泥页岩及其夹层中,以吸附和游离状态为主要存在方式的非常规天然气,成分以甲烷为主,是一种清洁、高效的能源资源和化工原料。世界能源研究所的最新研究表明,中国页岩气储量高达30万亿立方米以上,居世界第一,几乎是美国的两倍。下列关于页岩气主要成分甲烷的描述不正确的是
A.甲烷完全燃烧只生成CO2和H2O,可推测出甲烷仅由碳、氢两种元素组成
B.甲烷分子中,碳元素的质量分数为75%
C.甲烷分子和氨气分子所含的电子总数相等
D.鉴别H2、CO和CH4三种无色气体的方法是比较三种气体燃烧后的产物
6.用表示阿伏伽德罗常数的值,下列说法正确的是
A.18g重水中所含质子数为
B.0.1mol的与足量反应,生成的分子数为
C.标准状况下,22.4L己烷中含有的分子数为
D.16g甲烷中所含C-H数目为
7.据报道科研人员应用计算机模拟出结构类似C60的物质N60;4H是主要来源于宇宙射线的初级粒子,人类在月球上发现了储量丰富的3H。下列说法正确的是
A.N60与C60互为同素异形体 B.3H2与4H2互为同位素
C.C2H4和C3H6可能互为同系物 D.3H2O与4H2O互为同分异构体
8.下列说法中,不正确的是( )
A.乙醇与金属钠反应时,是乙醇分子中羟基中的O—H键断裂
B.检验乙醇中是否含有水,可加入少量无水硫酸铜,若变蓝则含水
C.乙醇在一定条件下可氧化成CH3COOH
D.甲烷、乙烯、苯、乙醇都是无色不溶于水的有机化合物
9.判断下列方程式正确的是
A.乙酸与碳酸钠溶液的反应:2H++CO32-=H2O+CO2
B.苯酚钠中通入少量的二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO32-
C.往乙醇中加入重铬酸钾溶液:16H++3C2H5OH+2Cr2O72-→ 3CH3COOH+4Cr3++11H2O
D.萘和氢气发生加成:
10.设为阿伏伽德罗常数的值,下列说法正确的是
A.0.1mol/L 溶液中含有0.2mol
B.标准状况下,11.2L苯含有的分子数为0.5
C.常温常压下,63g 含有的原子总数为5
D.2.8g铁粉与足量盐酸反应转移电子的数目为0.15
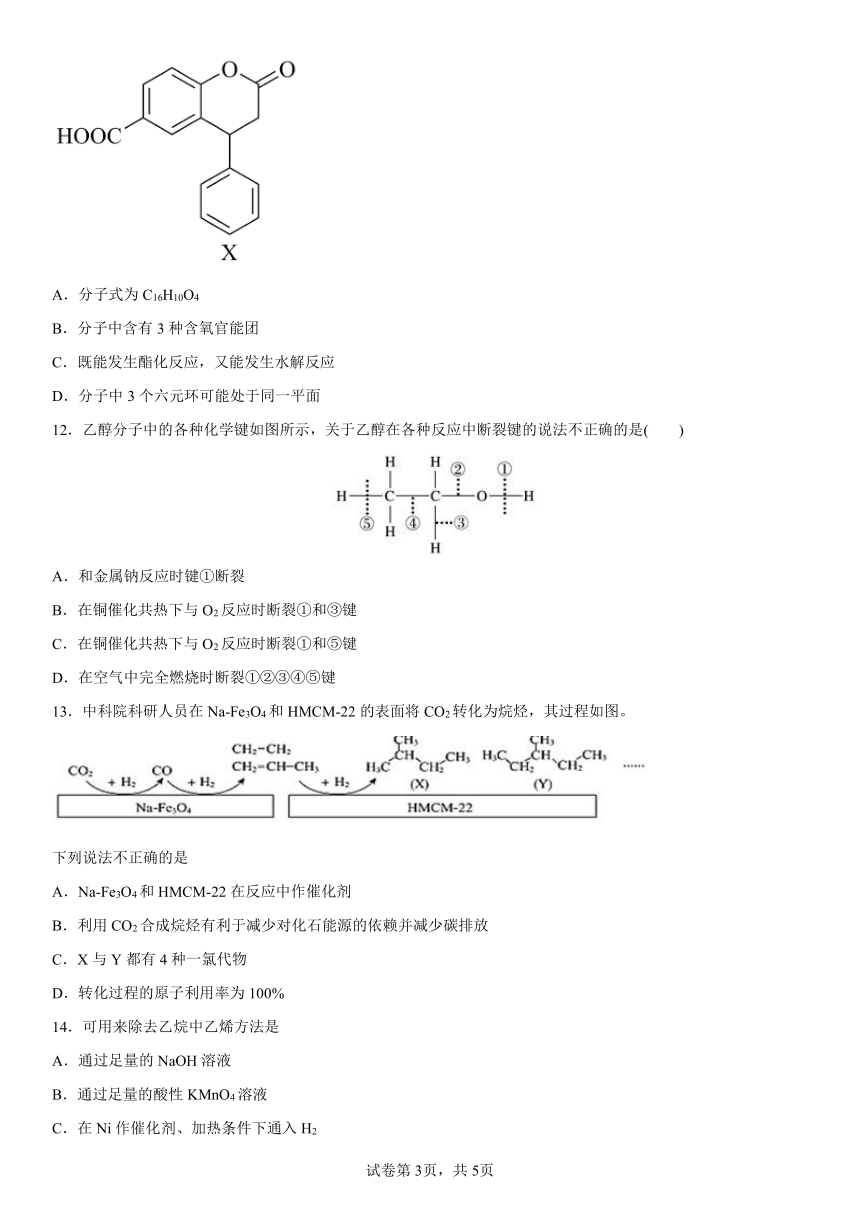
11.某种医药中间体X,其结构简式如图所示。下列有关该化合物的说法正确的是
A.分子式为C16H10O4
B.分子中含有3种含氧官能团
C.既能发生酯化反应,又能发生水解反应
D.分子中3个六元环可能处于同一平面
12.乙醇分子中的各种化学键如图所示,关于乙醇在各种反应中断裂键的说法不正确的是( )
A.和金属钠反应时键①断裂
B.在铜催化共热下与O2反应时断裂①和③键
C.在铜催化共热下与O2反应时断裂①和⑤键
D.在空气中完全燃烧时断裂①②③④⑤键
13.中科院科研人员在Na-Fe3O4和HMCM-22的表面将CO2转化为烷烃,其过程如图。
下列说法不正确的是
A.Na-Fe3O4和HMCM-22在反应中作催化剂
B.利用CO2合成烷烃有利于减少对化石能源的依赖并减少碳排放
C.X与Y都有4种一氯代物
D.转化过程的原子利用率为100%
14.可用来除去乙烷中乙烯方法是
A.通过足量的NaOH溶液
B.通过足量的酸性KMnO4溶液
C.在Ni作催化剂、加热条件下通入H2
D.通过足量的溴水
二、填空题
15.染发剂中普遍含有对苯二胺(其化学式为C6H8N2)会使易过敏的人引起发痒、水肿、气喘、胃炎和贫血等症状,另外它还具有致癌作用。因此,科学界告诫我们:慎用染发剂,少染发为好。
(1)一个对苯二胺分子中碳氢元素质量比_____。
(2)在对苯二胺中,所含元素的质量分数最大的元素是_____(填元素名称)。
16.苯的物理性质
颜色状态 密度、溶解性 毒性 熔、沸点 挥发性
___色___体 ___溶于水且密度比水___ ___毒 较低 易挥发
17.填空。
(1)①的俗称为_______;
②甲烷分子的空间结构为_______。
(2)①工业制漂白粉的化学方程式_______。
②与NaOH溶液反应的离子方程式_______。
18.乙烯的产量可以用来衡量一个国家的石油化工发展水平。请回答下列问题:
(1)若将乙烯气体通入溴的四氯化碳溶液中,反应的化学方程式为_______。
(2)可以用来除去乙烷中混有的少量乙烯的试剂是_______(填序号)。
①水 ②氢气 ③溴水 ④酸性KMnO4溶液
(3)下列化学反应原理相同的一组是_______(填序号)。
①乙烯使溴的四氯化碳溶液和酸性KMnO4溶液褪色
②SO2使溴水和酸性KMnO4溶液褪色
③SO2使品红溶液和滴有酚酞的NaOH溶液褪色
④乙烯与溴水的反应和苯与液溴在催化剂作用下的反应
19.油脂的组成
(1)油脂的成分主要是高级脂肪酸与甘油形成的酯。
(R、R′、R″代表高级脂肪酸的烃基)
高级脂肪酸的种类很多,如饱和的____C17H35COOH)、不饱和的____(C17H33COOH)等。
(2)状态
常温下呈液态的油脂称为____,如花生油、芝麻油、大豆油等____油,含较多不饱和高级脂肪酸的甘油酯。
常温下呈固态的油脂称为____,如牛油、羊油等____油脂,含较多饱和高级脂肪酸的甘油酯。
20.回答下列问题
(1)用作消化系统X射线检查的内服药剂物质的化学式___________
(2)请写出氟原子核外电子排布___________
(3)是离子化合物,各原子均满足2电子或8电子稳定结构,的电子式___________
(4)写出乙烷的结构式___________
21.写出甲烷的空间构型为_______,分子式为_______,电子式为_______,结构式为_______,结构简式为_______。
22.现有乙醇、乙酸乙酯、甲醛、苯、四种有机物:
(1)具有水果香味的物质是_______。
(2)医疗消毒常用75%的_______溶液。
(3)居室装修完,通常要开窗通风一段时间后才能入住,原因是装修材料散发出有毒的_______和_______。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
【详解】A.相对分子质量相等的两种有机物不一定是同分异构体,如丙三醇和甲苯的相对分子质量为92,但分子式不同,故A错误;
B.聚乙烯中不存在碳碳双键,不能发生加成反应,故B错误;
C.无论苯分子是否为单双键交替结构,间二甲苯都只有一种结构,故C错误;
D.化学性质相似的有机物不一定是同系物,可能是同分异构体,如正丁烷和异丁烷,故D正确;
故选D。
2.C
【详解】A.苯不能使溴水、酸性高锰酸钾溶液褪色,故A错误;
B.如果甲烷空间构型为正方形,其一氯甲烷也有一种,因此甲烷的一氯代物只有一种不可证明甲烷为正四面体结构而不是平面形,可从二氯甲烷只有一种可证明甲烷为正四面体而不是平面形,故B错误;
C.四氯化碳、己烷难溶于水,溴单质易溶于四氯化碳和己烷,四氯化碳的密度大于水,溴的四氯化碳溶液在下层,己烷的密度小于水,溴的己烷溶液在上层,可用溴水鉴别四氯化碳和己烷,故C正确;
D.乙烯的结构简式为CH2=CH2,含有碳碳双键,能与溴单质发生加成反应,而使溴的四氯化碳溶液褪色,聚乙烯不含碳碳双键,不能使溴的四氯化碳溶液褪色,故D错误;
答案为C。
3.D
【详解】A.丙烯分子与溴水发生加成反应的产物是,A错误;
B.通式为一定是链状烷烃,环状烷烃不符合,通式为不一定是烯烃,也可能是环烷烃,B错误;
C.酸性高锰酸钾溶液能把乙烯氧化为CO2,引入新杂质,可以用溴水除去乙烷中混有的乙烯,不能用酸性溶液,C错误;
D.乙烯和苯分子均是平面形结构,其中所有原子均在同一平面内,D正确;
答案选D。
4.C
【详解】A、CH3-CH=CH2和CH2=CH2的分子式分别为C3H6、C2H4,最简式都是CnH2n,故A正确;
B.苯环上的H可取代,如溴苯的制备,甲苯中苯环上的H易取代,如2,4,6-三硝基甲苯的制备,苯酚能够与溴反应生成三溴苯酚沉淀,则苯、甲苯、苯酚在一定条件下均能发生取代反应,故B正确;
C.乙烯使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色,分别发生氧化反应、加成反应,褪色原理不同,故C错误;
D.烷烃同分异构体中支链越多,沸点越低,则正戊烷、异戊烷、新戊烷的沸点依次降低,故D正确;
答案选C。
5.A
【详解】A.甲烷完全燃烧只生成CO2和H2O,O元素可以来自于O2,C和H元素只能来自与甲烷,因此甲烷中一定还有C、H两种元素,但是也可能存在O元素,A错误;
B.甲烷分子中,碳元素的质量分数为=75%,B正确;
C.每个CH4分子和每个NH3分子均含有10个电子,C正确;
D.H2燃烧后只生成H2O,CO燃烧后只生成CO2,CH4燃烧后生成H2O和CO2,因此可以通过燃烧后的产物鉴别三种物质,D正确;
故选A。
6.D
【详解】A.18g重水的物质的量是18g÷20g/mol=0.9mol,其中所含质子数为,A错误;
B.0.1mol的与足量反应,由于是可逆反应,因此生成的分子数小于,B错误;
C.标准状况下己烷不是气态,22.4L己烷中含有的分子数不是,C错误;
D.16g甲烷的物质的量是16g÷16g/mol=1.0mol,其中所含C-H数目为,D正确;
答案选D。
7.C
【详解】A.N60与C60是由不同元素组成的单质,不是同素异形体,A错误;
B.3H与4H是质子数相同、中子数不同的原子,互为同位素,但是3H2与4H2为单质,B错误;
C.C2H4为烯烃,C3H6可能为烯烃或环烷烃,若均为单烯烃,二者为同系物 ,C正确;
D.3H2O与4H2O是氢元素的不同核素和氧原子构成的水分子,不是同分异构体,故D错误;
故选C。
8.D
【详解】A、乙醇与金属钠反应生成乙醇钠,是乙醇分子中羟基中的O—H键断裂,选项A正确;
B、检验乙醇中是否含有水可用无水硫酸铜作检验试剂,若变蓝则表明乙醇中含水,选项B正确;
C、乙醇在酸性KMnO4溶液中可被氧化成乙酸,选项C正确;
D、甲烷、乙烯、苯都不溶于水,但乙醇却能与水以任意比例混溶,选项D不正确。
答案选D。
9.C
【详解】A. 乙酸是弱酸,在离子方程式中不能用H+表示,A不正确;B. 苯酚钠中通入二氧化碳,不论二氧化碳是否足量,都生成HCO3-,B不正确; C. 往乙醇中加入重铬酸钾溶液,发生反应的离子方程式为16H++3C2H5OH+2Cr2O72-→ 3CH3COOH+4Cr3++11H2O,C正确;D. 萘和氢气发生加成反应,1个萘分子只能消耗5个氢气分子,D不正确。本题选C。
10.C
【详解】A.缺溶液的体积,无法计算0.1mol/L氯化镁溶液中含有的氯离子物质的量,故A错误;
B.标准状况下,苯为液态,无法计算11.2L苯的物质的量和含有的分子数,故B错误;
C.63g硝酸含有的原子个数为×5×NAmol—1=5NA,故C正确;
D.铁与盐酸反应生成氯化亚铁和氢气,则2.8g铁粉与足量盐酸反应转移电子的数目为×2×NAmol—1=NA,故D错误;
故选C。
11.C
【详解】A.根据结构简式可知,该有机物的分子式为:C16H12O4,A错误;
B.分子中含羧基和酯基两种含氧官能团,B错误;
C.分子中含羧基和酯基,故可发生酯化反应和水解反应,C正确;
D.分子中含两个苯环,可能共平面,但和另一个六元环一定不共平面,D错误;
答案选C。
12.C
【详解】A. 乙醇与钠反应生成乙醇钠,是羟基中的O—H键断裂,A项正确;
B. 乙醇催化氧化成乙醛时,断裂①和③化学键,B项正确,
C. 乙醇催化氧化成乙醛时,断裂①和③化学键,C项错误;
D. 乙醇完全燃烧时,化学键①②③④⑤全部断裂,D项正确;
答案选C。
13.D
【详解】A.根据图示,在Na-Fe3O4和HMCM-22的表面将CO2转化为烷烃,Na-Fe3O4和HMCM-22在反应中作催化剂,故A正确;
B.利用CO2合成烷烃,实现碳的循环利用,有利于减少对化石能源的依赖并减少碳排放,故B正确;
C. 2-甲基丁烷、3-甲基戊烷都有4种等效氢,所以都有 4 种一氯代物,故C正确;
D.根据元素守恒,转化过程中有水生成,原子利用率小于100%,故D错误;
故答案为:D
14.D
【详解】A.NaOH溶液不和乙烯反应,故A不选;
B.乙烯被酸性KMnO4溶液氧化为二氧化碳,引入新杂质,故B不选;
C.乙烯和氢气反应能生成乙烷,但通入氢气的量不好控制,且反应不一定完全,所以不可行,故C不选;
D.乙烯和溴加成生成液态的1,2-二溴乙烷,乙烷和溴不反应,所以通过足量的溴水可以除去乙烷中的乙烯,故D选;
故选D。
15.(1)9:1
(2)碳
【详解】(1)一个对苯二胺分子中碳氢元素质量比为(6×12):(8×1)=9:1;
故答案为:9:1。
(2)在对苯二胺中,碳氢氮三种元素质量比为(6×12):(8×1)(2×14)=18:2:7,故质量分数最大的是碳元素;
故答案为:碳。
16. 无 液 不 小 有
【解析】略
17.(1) 小苏打 正四面体形
(2)
【详解】(1)水溶液碱性没有碳酸钠强,俗称小苏打;甲烷分子式为CH4,空间结构为正四面体形,碳原子位于正四面体体心;
(2)工业制漂白粉是氯气和石灰乳反应生成氯化钙和次氯酸钙,即;与NaOH溶液反应生成偏铝酸钠和水,即离子方程式为。
18. ③ ②
【详解】(1)若将乙烯气体通入溴的四氯化碳溶液中,发生加成反应,生成1,2-二溴乙烷,反应的化学方程式为。故答案为:;
(2)①乙烯在水中溶解度小,故不选; ②氢气与乙烯加成反应不完全,同时无法控制所加氢气的量,故不选; ③溴水与乙烯发生加成反应,生成1,2-二溴乙烷,故选; ④酸性KMnO4溶液与乙烯反应生成二氧化碳,引入新的杂质,故不选;故答案为:③;
(3)①乙烯使溴的四氯化碳溶液和酸性KMnO4溶液褪色,前者为加成反应,后者为氧化反应,化学反应原理不相同,故不选;
②SO2使溴水和酸性KMnO4溶液褪色,二氧化硫均作还原剂,被氧化,化学反应原理相同,故选;
③SO2使品红溶液和滴有酚酞的NaOH溶液褪色,前者为漂白,后者由于二氧化硫是酸性氧化物,化学反应原理不相同,故不选;
④乙烯与溴水的反应和苯与液溴在催化剂作用下的反应,前者发生加成反应,后者发生取代反应,化学反应原理不相同,故不选;
故答案为:②。
19.(1) 硬脂酸 油酸
(2) 油 植物 脂肪 动物
【解析】略
20.(1)
(2)
(3)
(4)
【解析】(1)
医疗上用作消化系统X射线检查的内服药剂,俗称钡餐的物质是硫酸钡,化学式为:。
(2)
F的原子序数为9,氟原子核外有9个电子,其原子的结构示意图为:,氟原子核外电子排布为:。
(3)
是离子化合物,各原子均满足2电子或8电子稳定结构,的化学式为,其电子式是:。
(4)
乙烷的分子式为C2H6,结构简式为CH3CH3,其结构式为:。
21. 正四面体 CH4 CH4
【详解】甲烷的空间构型为正四面体,分子式为CH4,电子式为,结构式为,结构简式为CH4。
22. 乙酸乙酯 乙醇 甲醛 苯
【分析】低级酯一般具有香味;乙醇可使蛋白质变性,常用于杀菌消毒;装修材料中含有大量的甲醛、苯等有害物质。
【详解】(1)乙酸乙酯具有水果香味,故答案为:乙酸乙酯;
(2)75%乙醇具有使蛋白质变性而起到杀菌消毒的作用,故答案为:乙醇;
(3)装修材料中含有大量的甲醛、苯等有害物质,如不通风就直接入住会给人体带来较大危害,故答案为:甲醛和苯。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列说法正确的是
A.相对分子质量相等的两种有机物必定是同分异构体
B.乙烯、聚乙烯的结构简式相同,均可发生加成反应
C.经测定,间二甲苯只有一种结构可证明苯分子中单双键交替结构
D.化学性质相似的有机物不一定是同系物
2.下列关于常见有机化合物的说法中,正确的是
A.苯不能因反应而使溴水褪色但能使酸性高锰酸钾溶液褪色
B.甲烷的一氯代物只有一种可证明甲烷为正四面体结构而不是平面形
C.可用溴水鉴别四氯化碳和己烷这两种无色液体
D.乙烯和聚乙烯都能与溴的四氯化碳溶液发生加成反应
3.下列关于烃的说法正确的是
A.丙烯与溴水发生加成反应的产物是
B.通式为一定是烷烃,通式为一定是烯烃
C.用溴水或酸性溶液都可以除去乙烷中混有的乙烯
D.乙烯和苯分子中的所有原子均在同一平面内
4.下列说法错误的是
A.CH3—CH=CH2和CH2=CH2的最简式相同
B.苯、甲苯、苯酚均能发生取代反应
C.乙烯使酸性高锰酸钾溶液及溴的四氯化碳溶液褪色原理相同
D.常压下,正戊烷、异戊烷、新戊烷的沸点依次降低
5.页岩气是指赋存于富有机质泥页岩及其夹层中,以吸附和游离状态为主要存在方式的非常规天然气,成分以甲烷为主,是一种清洁、高效的能源资源和化工原料。世界能源研究所的最新研究表明,中国页岩气储量高达30万亿立方米以上,居世界第一,几乎是美国的两倍。下列关于页岩气主要成分甲烷的描述不正确的是
A.甲烷完全燃烧只生成CO2和H2O,可推测出甲烷仅由碳、氢两种元素组成
B.甲烷分子中,碳元素的质量分数为75%
C.甲烷分子和氨气分子所含的电子总数相等
D.鉴别H2、CO和CH4三种无色气体的方法是比较三种气体燃烧后的产物
6.用表示阿伏伽德罗常数的值,下列说法正确的是
A.18g重水中所含质子数为
B.0.1mol的与足量反应,生成的分子数为
C.标准状况下,22.4L己烷中含有的分子数为
D.16g甲烷中所含C-H数目为
7.据报道科研人员应用计算机模拟出结构类似C60的物质N60;4H是主要来源于宇宙射线的初级粒子,人类在月球上发现了储量丰富的3H。下列说法正确的是
A.N60与C60互为同素异形体 B.3H2与4H2互为同位素
C.C2H4和C3H6可能互为同系物 D.3H2O与4H2O互为同分异构体
8.下列说法中,不正确的是( )
A.乙醇与金属钠反应时,是乙醇分子中羟基中的O—H键断裂
B.检验乙醇中是否含有水,可加入少量无水硫酸铜,若变蓝则含水
C.乙醇在一定条件下可氧化成CH3COOH
D.甲烷、乙烯、苯、乙醇都是无色不溶于水的有机化合物
9.判断下列方程式正确的是
A.乙酸与碳酸钠溶液的反应:2H++CO32-=H2O+CO2
B.苯酚钠中通入少量的二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO32-
C.往乙醇中加入重铬酸钾溶液:16H++3C2H5OH+2Cr2O72-→ 3CH3COOH+4Cr3++11H2O
D.萘和氢气发生加成:
10.设为阿伏伽德罗常数的值,下列说法正确的是
A.0.1mol/L 溶液中含有0.2mol
B.标准状况下,11.2L苯含有的分子数为0.5
C.常温常压下,63g 含有的原子总数为5
D.2.8g铁粉与足量盐酸反应转移电子的数目为0.15
11.某种医药中间体X,其结构简式如图所示。下列有关该化合物的说法正确的是
A.分子式为C16H10O4
B.分子中含有3种含氧官能团
C.既能发生酯化反应,又能发生水解反应
D.分子中3个六元环可能处于同一平面
12.乙醇分子中的各种化学键如图所示,关于乙醇在各种反应中断裂键的说法不正确的是( )
A.和金属钠反应时键①断裂
B.在铜催化共热下与O2反应时断裂①和③键
C.在铜催化共热下与O2反应时断裂①和⑤键
D.在空气中完全燃烧时断裂①②③④⑤键
13.中科院科研人员在Na-Fe3O4和HMCM-22的表面将CO2转化为烷烃,其过程如图。
下列说法不正确的是
A.Na-Fe3O4和HMCM-22在反应中作催化剂
B.利用CO2合成烷烃有利于减少对化石能源的依赖并减少碳排放
C.X与Y都有4种一氯代物
D.转化过程的原子利用率为100%
14.可用来除去乙烷中乙烯方法是
A.通过足量的NaOH溶液
B.通过足量的酸性KMnO4溶液
C.在Ni作催化剂、加热条件下通入H2
D.通过足量的溴水
二、填空题
15.染发剂中普遍含有对苯二胺(其化学式为C6H8N2)会使易过敏的人引起发痒、水肿、气喘、胃炎和贫血等症状,另外它还具有致癌作用。因此,科学界告诫我们:慎用染发剂,少染发为好。
(1)一个对苯二胺分子中碳氢元素质量比_____。
(2)在对苯二胺中,所含元素的质量分数最大的元素是_____(填元素名称)。
16.苯的物理性质
颜色状态 密度、溶解性 毒性 熔、沸点 挥发性
___色___体 ___溶于水且密度比水___ ___毒 较低 易挥发
17.填空。
(1)①的俗称为_______;
②甲烷分子的空间结构为_______。
(2)①工业制漂白粉的化学方程式_______。
②与NaOH溶液反应的离子方程式_______。
18.乙烯的产量可以用来衡量一个国家的石油化工发展水平。请回答下列问题:
(1)若将乙烯气体通入溴的四氯化碳溶液中,反应的化学方程式为_______。
(2)可以用来除去乙烷中混有的少量乙烯的试剂是_______(填序号)。
①水 ②氢气 ③溴水 ④酸性KMnO4溶液
(3)下列化学反应原理相同的一组是_______(填序号)。
①乙烯使溴的四氯化碳溶液和酸性KMnO4溶液褪色
②SO2使溴水和酸性KMnO4溶液褪色
③SO2使品红溶液和滴有酚酞的NaOH溶液褪色
④乙烯与溴水的反应和苯与液溴在催化剂作用下的反应
19.油脂的组成
(1)油脂的成分主要是高级脂肪酸与甘油形成的酯。
(R、R′、R″代表高级脂肪酸的烃基)
高级脂肪酸的种类很多,如饱和的____C17H35COOH)、不饱和的____(C17H33COOH)等。
(2)状态
常温下呈液态的油脂称为____,如花生油、芝麻油、大豆油等____油,含较多不饱和高级脂肪酸的甘油酯。
常温下呈固态的油脂称为____,如牛油、羊油等____油脂,含较多饱和高级脂肪酸的甘油酯。
20.回答下列问题
(1)用作消化系统X射线检查的内服药剂物质的化学式___________
(2)请写出氟原子核外电子排布___________
(3)是离子化合物,各原子均满足2电子或8电子稳定结构,的电子式___________
(4)写出乙烷的结构式___________
21.写出甲烷的空间构型为_______,分子式为_______,电子式为_______,结构式为_______,结构简式为_______。
22.现有乙醇、乙酸乙酯、甲醛、苯、四种有机物:
(1)具有水果香味的物质是_______。
(2)医疗消毒常用75%的_______溶液。
(3)居室装修完,通常要开窗通风一段时间后才能入住,原因是装修材料散发出有毒的_______和_______。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
【详解】A.相对分子质量相等的两种有机物不一定是同分异构体,如丙三醇和甲苯的相对分子质量为92,但分子式不同,故A错误;
B.聚乙烯中不存在碳碳双键,不能发生加成反应,故B错误;
C.无论苯分子是否为单双键交替结构,间二甲苯都只有一种结构,故C错误;
D.化学性质相似的有机物不一定是同系物,可能是同分异构体,如正丁烷和异丁烷,故D正确;
故选D。
2.C
【详解】A.苯不能使溴水、酸性高锰酸钾溶液褪色,故A错误;
B.如果甲烷空间构型为正方形,其一氯甲烷也有一种,因此甲烷的一氯代物只有一种不可证明甲烷为正四面体结构而不是平面形,可从二氯甲烷只有一种可证明甲烷为正四面体而不是平面形,故B错误;
C.四氯化碳、己烷难溶于水,溴单质易溶于四氯化碳和己烷,四氯化碳的密度大于水,溴的四氯化碳溶液在下层,己烷的密度小于水,溴的己烷溶液在上层,可用溴水鉴别四氯化碳和己烷,故C正确;
D.乙烯的结构简式为CH2=CH2,含有碳碳双键,能与溴单质发生加成反应,而使溴的四氯化碳溶液褪色,聚乙烯不含碳碳双键,不能使溴的四氯化碳溶液褪色,故D错误;
答案为C。
3.D
【详解】A.丙烯分子与溴水发生加成反应的产物是,A错误;
B.通式为一定是链状烷烃,环状烷烃不符合,通式为不一定是烯烃,也可能是环烷烃,B错误;
C.酸性高锰酸钾溶液能把乙烯氧化为CO2,引入新杂质,可以用溴水除去乙烷中混有的乙烯,不能用酸性溶液,C错误;
D.乙烯和苯分子均是平面形结构,其中所有原子均在同一平面内,D正确;
答案选D。
4.C
【详解】A、CH3-CH=CH2和CH2=CH2的分子式分别为C3H6、C2H4,最简式都是CnH2n,故A正确;
B.苯环上的H可取代,如溴苯的制备,甲苯中苯环上的H易取代,如2,4,6-三硝基甲苯的制备,苯酚能够与溴反应生成三溴苯酚沉淀,则苯、甲苯、苯酚在一定条件下均能发生取代反应,故B正确;
C.乙烯使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色,分别发生氧化反应、加成反应,褪色原理不同,故C错误;
D.烷烃同分异构体中支链越多,沸点越低,则正戊烷、异戊烷、新戊烷的沸点依次降低,故D正确;
答案选C。
5.A
【详解】A.甲烷完全燃烧只生成CO2和H2O,O元素可以来自于O2,C和H元素只能来自与甲烷,因此甲烷中一定还有C、H两种元素,但是也可能存在O元素,A错误;
B.甲烷分子中,碳元素的质量分数为=75%,B正确;
C.每个CH4分子和每个NH3分子均含有10个电子,C正确;
D.H2燃烧后只生成H2O,CO燃烧后只生成CO2,CH4燃烧后生成H2O和CO2,因此可以通过燃烧后的产物鉴别三种物质,D正确;
故选A。
6.D
【详解】A.18g重水的物质的量是18g÷20g/mol=0.9mol,其中所含质子数为,A错误;
B.0.1mol的与足量反应,由于是可逆反应,因此生成的分子数小于,B错误;
C.标准状况下己烷不是气态,22.4L己烷中含有的分子数不是,C错误;
D.16g甲烷的物质的量是16g÷16g/mol=1.0mol,其中所含C-H数目为,D正确;
答案选D。
7.C
【详解】A.N60与C60是由不同元素组成的单质,不是同素异形体,A错误;
B.3H与4H是质子数相同、中子数不同的原子,互为同位素,但是3H2与4H2为单质,B错误;
C.C2H4为烯烃,C3H6可能为烯烃或环烷烃,若均为单烯烃,二者为同系物 ,C正确;
D.3H2O与4H2O是氢元素的不同核素和氧原子构成的水分子,不是同分异构体,故D错误;
故选C。
8.D
【详解】A、乙醇与金属钠反应生成乙醇钠,是乙醇分子中羟基中的O—H键断裂,选项A正确;
B、检验乙醇中是否含有水可用无水硫酸铜作检验试剂,若变蓝则表明乙醇中含水,选项B正确;
C、乙醇在酸性KMnO4溶液中可被氧化成乙酸,选项C正确;
D、甲烷、乙烯、苯都不溶于水,但乙醇却能与水以任意比例混溶,选项D不正确。
答案选D。
9.C
【详解】A. 乙酸是弱酸,在离子方程式中不能用H+表示,A不正确;B. 苯酚钠中通入二氧化碳,不论二氧化碳是否足量,都生成HCO3-,B不正确; C. 往乙醇中加入重铬酸钾溶液,发生反应的离子方程式为16H++3C2H5OH+2Cr2O72-→ 3CH3COOH+4Cr3++11H2O,C正确;D. 萘和氢气发生加成反应,1个萘分子只能消耗5个氢气分子,D不正确。本题选C。
10.C
【详解】A.缺溶液的体积,无法计算0.1mol/L氯化镁溶液中含有的氯离子物质的量,故A错误;
B.标准状况下,苯为液态,无法计算11.2L苯的物质的量和含有的分子数,故B错误;
C.63g硝酸含有的原子个数为×5×NAmol—1=5NA,故C正确;
D.铁与盐酸反应生成氯化亚铁和氢气,则2.8g铁粉与足量盐酸反应转移电子的数目为×2×NAmol—1=NA,故D错误;
故选C。
11.C
【详解】A.根据结构简式可知,该有机物的分子式为:C16H12O4,A错误;
B.分子中含羧基和酯基两种含氧官能团,B错误;
C.分子中含羧基和酯基,故可发生酯化反应和水解反应,C正确;
D.分子中含两个苯环,可能共平面,但和另一个六元环一定不共平面,D错误;
答案选C。
12.C
【详解】A. 乙醇与钠反应生成乙醇钠,是羟基中的O—H键断裂,A项正确;
B. 乙醇催化氧化成乙醛时,断裂①和③化学键,B项正确,
C. 乙醇催化氧化成乙醛时,断裂①和③化学键,C项错误;
D. 乙醇完全燃烧时,化学键①②③④⑤全部断裂,D项正确;
答案选C。
13.D
【详解】A.根据图示,在Na-Fe3O4和HMCM-22的表面将CO2转化为烷烃,Na-Fe3O4和HMCM-22在反应中作催化剂,故A正确;
B.利用CO2合成烷烃,实现碳的循环利用,有利于减少对化石能源的依赖并减少碳排放,故B正确;
C. 2-甲基丁烷、3-甲基戊烷都有4种等效氢,所以都有 4 种一氯代物,故C正确;
D.根据元素守恒,转化过程中有水生成,原子利用率小于100%,故D错误;
故答案为:D
14.D
【详解】A.NaOH溶液不和乙烯反应,故A不选;
B.乙烯被酸性KMnO4溶液氧化为二氧化碳,引入新杂质,故B不选;
C.乙烯和氢气反应能生成乙烷,但通入氢气的量不好控制,且反应不一定完全,所以不可行,故C不选;
D.乙烯和溴加成生成液态的1,2-二溴乙烷,乙烷和溴不反应,所以通过足量的溴水可以除去乙烷中的乙烯,故D选;
故选D。
15.(1)9:1
(2)碳
【详解】(1)一个对苯二胺分子中碳氢元素质量比为(6×12):(8×1)=9:1;
故答案为:9:1。
(2)在对苯二胺中,碳氢氮三种元素质量比为(6×12):(8×1)(2×14)=18:2:7,故质量分数最大的是碳元素;
故答案为:碳。
16. 无 液 不 小 有
【解析】略
17.(1) 小苏打 正四面体形
(2)
【详解】(1)水溶液碱性没有碳酸钠强,俗称小苏打;甲烷分子式为CH4,空间结构为正四面体形,碳原子位于正四面体体心;
(2)工业制漂白粉是氯气和石灰乳反应生成氯化钙和次氯酸钙,即;与NaOH溶液反应生成偏铝酸钠和水,即离子方程式为。
18. ③ ②
【详解】(1)若将乙烯气体通入溴的四氯化碳溶液中,发生加成反应,生成1,2-二溴乙烷,反应的化学方程式为。故答案为:;
(2)①乙烯在水中溶解度小,故不选; ②氢气与乙烯加成反应不完全,同时无法控制所加氢气的量,故不选; ③溴水与乙烯发生加成反应,生成1,2-二溴乙烷,故选; ④酸性KMnO4溶液与乙烯反应生成二氧化碳,引入新的杂质,故不选;故答案为:③;
(3)①乙烯使溴的四氯化碳溶液和酸性KMnO4溶液褪色,前者为加成反应,后者为氧化反应,化学反应原理不相同,故不选;
②SO2使溴水和酸性KMnO4溶液褪色,二氧化硫均作还原剂,被氧化,化学反应原理相同,故选;
③SO2使品红溶液和滴有酚酞的NaOH溶液褪色,前者为漂白,后者由于二氧化硫是酸性氧化物,化学反应原理不相同,故不选;
④乙烯与溴水的反应和苯与液溴在催化剂作用下的反应,前者发生加成反应,后者发生取代反应,化学反应原理不相同,故不选;
故答案为:②。
19.(1) 硬脂酸 油酸
(2) 油 植物 脂肪 动物
【解析】略
20.(1)
(2)
(3)
(4)
【解析】(1)
医疗上用作消化系统X射线检查的内服药剂,俗称钡餐的物质是硫酸钡,化学式为:。
(2)
F的原子序数为9,氟原子核外有9个电子,其原子的结构示意图为:,氟原子核外电子排布为:。
(3)
是离子化合物,各原子均满足2电子或8电子稳定结构,的化学式为,其电子式是:。
(4)
乙烷的分子式为C2H6,结构简式为CH3CH3,其结构式为:。
21. 正四面体 CH4 CH4
【详解】甲烷的空间构型为正四面体,分子式为CH4,电子式为,结构式为,结构简式为CH4。
22. 乙酸乙酯 乙醇 甲醛 苯
【分析】低级酯一般具有香味;乙醇可使蛋白质变性,常用于杀菌消毒;装修材料中含有大量的甲醛、苯等有害物质。
【详解】(1)乙酸乙酯具有水果香味,故答案为:乙酸乙酯;
(2)75%乙醇具有使蛋白质变性而起到杀菌消毒的作用,故答案为:乙醇;
(3)装修材料中含有大量的甲醛、苯等有害物质,如不通风就直接入住会给人体带来较大危害,故答案为:甲醛和苯。
答案第1页,共2页
答案第1页,共2页
