5.1.2 硫酸 学案(第二课时) 2022-2023学年高一化学人教版(2019)必修第二册
文档属性
| 名称 | 5.1.2 硫酸 学案(第二课时) 2022-2023学年高一化学人教版(2019)必修第二册 |
|
|
| 格式 | doc | ||
| 文件大小 | 497.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-21 00:00:00 | ||
图片预览


文档简介
人教版(2019)必修第二册 第五章 化工生产中的重要非金属元素
第一节课时2 硫酸
学习目标
1.了解硫酸的工业制备原理与用途。
2.通过实验探究,认识浓硫酸的吸水性和脱水性及其区别。
3.通过浓硫酸与铜反应的实验探究,掌握浓硫酸的强氧化性,提升实验探究能力与创新意识。
自主预习
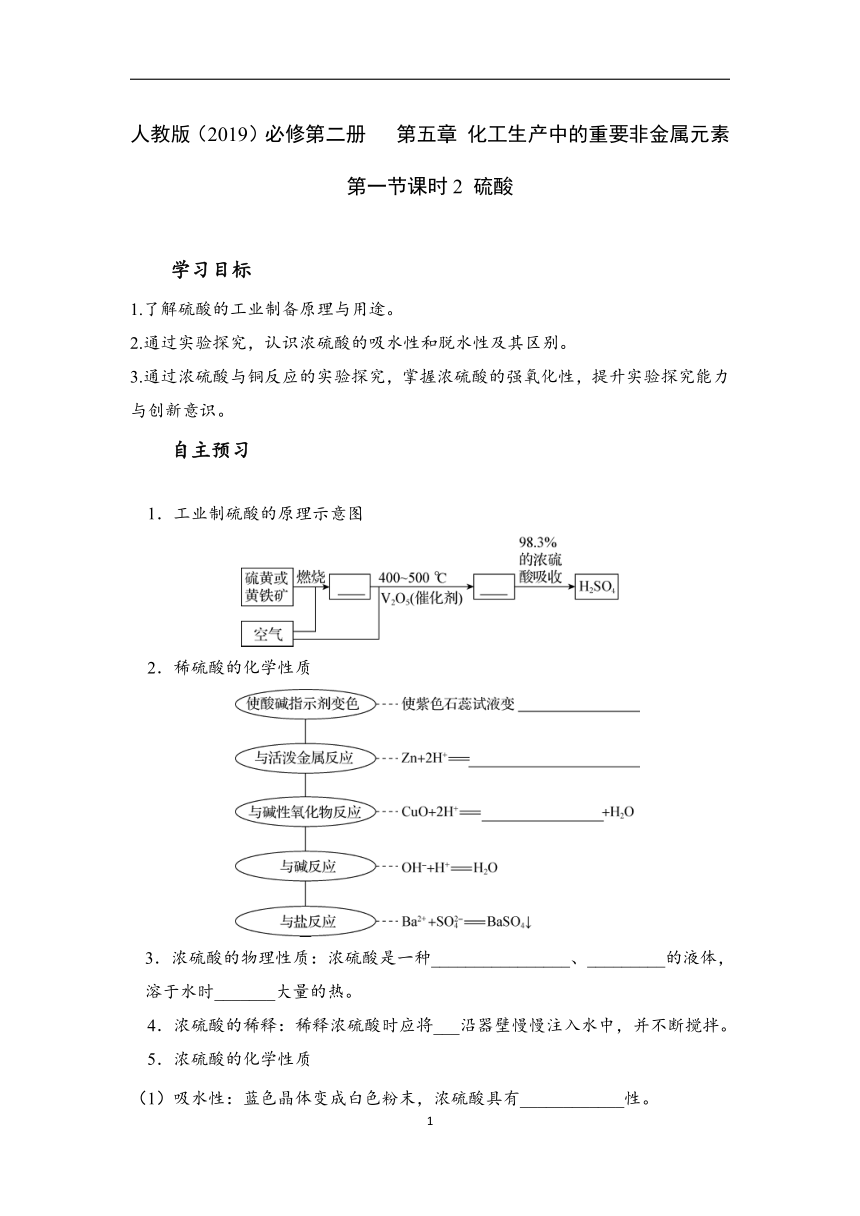
1.工业制硫酸的原理示意图
2.稀硫酸的化学性质
3.浓硫酸的物理性质:浓硫酸是一种________________、_________的液体,溶于水时_______大量的热。
4.浓硫酸的稀释:稀释浓硫酸时应将___沿器壁慢慢注入水中,并不断搅拌。
5.浓硫酸的化学性质
(1)吸水性:蓝色晶体变成白色粉末,浓硫酸具有____________性。
(2)脱水性
实验操作
实验现象 ①蔗糖逐渐变黑②蔗糖体积膨胀,形成黑色疏松多孔的海绵状的炭,并放出有刺激性气味的气体
实验结论 ①浓硫酸具有__________,能将蔗糖炭化②浓硫酸具有_________,能将炭氧化成CO2,自身被还原为SO2
(3)强氧化性:能氧化大多数金属单质和部分非金属单质。
①与金属的反应。
实验操作
实验现象 a试管中铜丝表面______________;b试管中的品红溶液逐渐变为____________;c试管中的石蕊溶液逐渐变为___________;将a试管里的溶液冷却后慢慢倒入水中,溶液变为__________
化学方程式 _____________________________________________
②与非金属的反应。
在加热时,浓硫酸与木炭发生反应:
_______________________________________________。
【思考讨论1】所有金属单质与浓硫酸都能反应吗?
_______________________________________________。
【思考讨论2】浓硫酸不能用来干燥哪些气体?
_______________________________________________。
课堂练习
1.下列事实与原因对应关系正确的是( )
A. 在空气中敞口久置的浓硫酸,溶液质量增大——浓硫酸具有难挥发性
B. 浓滴在纸上,使纸变黑——浓硫酸具有脱水性
C. 浓硫酸与蔗糖作用有海绵状的炭生成——浓硫酸具有吸水性
D. 浓硫酸可与铜反应——只显示浓硫酸的强氧化性
2.储存浓的铁罐外口常会出现严重的腐蚀现象,这体现了( )
A. 浓的吸水性和酸性
B. 浓的脱水性和吸水性
C. 浓的强氧化性和吸水性
D. 浓的吸水性和稀的通性(酸性)
3.通常情况下,以下气体不能用浓硫酸干燥的是( )
A.SO2 B.Cl2 C.HCl D.H2S
4.下列叙述正确的是( )
A. 浓硫酸是一种干燥剂,能够干燥氢气、氧气、氨气等,但不能干燥有较强还原性的HI、等
B. 浓硫酸与单质硫反应的化学方程式为,在此反应中,浓硫酸既表现了强氧化性又表现了酸性
C. 把足量铜粉投入含2 mol的浓硫酸中,反应后得到的气体在标准状况下的体积为22.4 L
D. 常温下能够用铁、铝质容器盛放浓硫酸,是因为浓硫酸的强氧化性使其钝化
5.在化学课上围绕浓硫酸的化学性质进行了如下实验探究,将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀,然后加入浓硫酸,生成黑色物质。
请回答下列问题:
(1)生成的黑色物质(单质)是______(填化学式)。
(2)这种黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激性气味,是大气的主要污染物之一,这种刺激性气味的气体成分是________(填化学式),反应的化学方程式为____________________。
(3)将(2)中产生的有刺激性气味的气体通入品红溶液中,可以看到品红溶液________,说明这种气体具有________性;将(2)中产生的有刺激性气味的气体通入水中可生成一种不稳定、易分解的酸,请写出该反应的化学方程式:_______________________________。
(4)能否用澄清石灰水鉴别这两种气体?________(填“能”或“不能”)。若不能,请填写两种能鉴别的试剂:______________。
6.为了验证木炭可被浓氧化成,选用如图所示仪器(内含物质)组装成实验装置。
(1)如按气流由左向右流向,连接上述装置的正确顺序是________接________,________接________,________接________。(填各接口字母)
(2)仪器乙、丙应有怎样的实验现象才表明已检验出:仪器乙中_________;仪器丙中________________。
(3)丁中酸性溶液的作用是________________________。
(4)写出甲中反应的化学方程式:____________________。
2
第一节课时2 硫酸
学习目标
1.了解硫酸的工业制备原理与用途。
2.通过实验探究,认识浓硫酸的吸水性和脱水性及其区别。
3.通过浓硫酸与铜反应的实验探究,掌握浓硫酸的强氧化性,提升实验探究能力与创新意识。
自主预习
1.工业制硫酸的原理示意图
2.稀硫酸的化学性质
3.浓硫酸的物理性质:浓硫酸是一种________________、_________的液体,溶于水时_______大量的热。
4.浓硫酸的稀释:稀释浓硫酸时应将___沿器壁慢慢注入水中,并不断搅拌。
5.浓硫酸的化学性质
(1)吸水性:蓝色晶体变成白色粉末,浓硫酸具有____________性。
(2)脱水性
实验操作
实验现象 ①蔗糖逐渐变黑②蔗糖体积膨胀,形成黑色疏松多孔的海绵状的炭,并放出有刺激性气味的气体
实验结论 ①浓硫酸具有__________,能将蔗糖炭化②浓硫酸具有_________,能将炭氧化成CO2,自身被还原为SO2
(3)强氧化性:能氧化大多数金属单质和部分非金属单质。
①与金属的反应。
实验操作
实验现象 a试管中铜丝表面______________;b试管中的品红溶液逐渐变为____________;c试管中的石蕊溶液逐渐变为___________;将a试管里的溶液冷却后慢慢倒入水中,溶液变为__________
化学方程式 _____________________________________________
②与非金属的反应。
在加热时,浓硫酸与木炭发生反应:
_______________________________________________。
【思考讨论1】所有金属单质与浓硫酸都能反应吗?
_______________________________________________。
【思考讨论2】浓硫酸不能用来干燥哪些气体?
_______________________________________________。
课堂练习
1.下列事实与原因对应关系正确的是( )
A. 在空气中敞口久置的浓硫酸,溶液质量增大——浓硫酸具有难挥发性
B. 浓滴在纸上,使纸变黑——浓硫酸具有脱水性
C. 浓硫酸与蔗糖作用有海绵状的炭生成——浓硫酸具有吸水性
D. 浓硫酸可与铜反应——只显示浓硫酸的强氧化性
2.储存浓的铁罐外口常会出现严重的腐蚀现象,这体现了( )
A. 浓的吸水性和酸性
B. 浓的脱水性和吸水性
C. 浓的强氧化性和吸水性
D. 浓的吸水性和稀的通性(酸性)
3.通常情况下,以下气体不能用浓硫酸干燥的是( )
A.SO2 B.Cl2 C.HCl D.H2S
4.下列叙述正确的是( )
A. 浓硫酸是一种干燥剂,能够干燥氢气、氧气、氨气等,但不能干燥有较强还原性的HI、等
B. 浓硫酸与单质硫反应的化学方程式为,在此反应中,浓硫酸既表现了强氧化性又表现了酸性
C. 把足量铜粉投入含2 mol的浓硫酸中,反应后得到的气体在标准状况下的体积为22.4 L
D. 常温下能够用铁、铝质容器盛放浓硫酸,是因为浓硫酸的强氧化性使其钝化
5.在化学课上围绕浓硫酸的化学性质进行了如下实验探究,将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀,然后加入浓硫酸,生成黑色物质。
请回答下列问题:
(1)生成的黑色物质(单质)是______(填化学式)。
(2)这种黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激性气味,是大气的主要污染物之一,这种刺激性气味的气体成分是________(填化学式),反应的化学方程式为____________________。
(3)将(2)中产生的有刺激性气味的气体通入品红溶液中,可以看到品红溶液________,说明这种气体具有________性;将(2)中产生的有刺激性气味的气体通入水中可生成一种不稳定、易分解的酸,请写出该反应的化学方程式:_______________________________。
(4)能否用澄清石灰水鉴别这两种气体?________(填“能”或“不能”)。若不能,请填写两种能鉴别的试剂:______________。
6.为了验证木炭可被浓氧化成,选用如图所示仪器(内含物质)组装成实验装置。
(1)如按气流由左向右流向,连接上述装置的正确顺序是________接________,________接________,________接________。(填各接口字母)
(2)仪器乙、丙应有怎样的实验现象才表明已检验出:仪器乙中_________;仪器丙中________________。
(3)丁中酸性溶液的作用是________________________。
(4)写出甲中反应的化学方程式:____________________。
2
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
