专题7初识酸、碱和盐检测题(含答案) --2022-2023学年九年级化学仁爱版下册
文档属性
| 名称 | 专题7初识酸、碱和盐检测题(含答案) --2022-2023学年九年级化学仁爱版下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 124.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 仁爱科普版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-19 00:00:00 | ||
图片预览


文档简介
专题7《初识酸、碱和盐》检测题
一、单选题
1.下列实验操作能达到实验目的的是
实验目的 实验操作
A.除去CaCl2中的CaCO3 加入过量的稀盐酸
B.干燥氨气 洗气,通过浓硫酸
C.鉴别硝酸铵和磷矿粉 ①看外观②加熟石灰
D.配制10%的硫酸溶液 计算、称量、量取、溶解
A.A B.B C.C D.D
2.运用分类思想认识物质是化学上常用的方法。下列说法正确的是
A.柠檬酸、碳酸均属于酸,它们都能使石蕊溶液变红
B.氮气、氢气都属于非金属单质,它们都能在氧气中燃烧
C.氧化镁、氧化铝均属于金属氧化物,它们都易溶解于水
D.硝酸铵、氯化铵均属于铵盐,它们都能跟碱性肥料混合使用
3.实验室有许多药品需要密封保存。对下列药品密封保存的原因解释不正确的是
A.浓硫酸﹣﹣﹣防止吸水
B.浓盐酸﹣﹣﹣防止挥发
C.生石灰﹣﹣﹣防止氧化
D.氢氧化钠﹣﹣﹣防止潮解和变质
4.下列实验现象描述正确的是
A.二氧化碳能使干燥的紫色石蕊纸花变红
B.氢气在氧气中燃烧时,火焰呈黄色,放出大量的热
C.在装有少量干燥生石灰的试管中加入少量水,试管外壁温度会降低
D.细铁丝与氧气剧烈燃烧,火星四射,放出大量的热,生成黑色固体物质
5.下图为xx泡打粉的标签如图所示,下列说法错误的是
A.碳酸氢钠俗称小苏打 B.泡打粉可以随意放置
C.加入泡打粉制作的蛋糕更松软 D.碳酸钙可做补钙剂
6.下列实验现象的描述不正确的是
A.把二氧化碳通入石蕊溶液,溶液变红
B.硫在空气中燃烧生成二氧化硫
C.硝酸铵固体溶于水时吸收热量
D.打开浓盐酸的瓶盖,瓶口出现大量白雾
7.下列对化学基本观念的认知正确的是( )
A.价值观:补充微量元素无需适可而止
B.能量观:酒精燃烧吸收大量的热
C.分类观:纯碱和烧碱从组成上都属于碱
D.守恒观:电解水反应前后,元素种类和原子数目均不变
8.紫甘蓝汁呈紫色,茶花汁呈浅黄色。用分光光度计测不同颜色的溶液,其可见光吸收峰波长范围不同。现用分光光度计测量以上两种汁液在不同酸碱度条件下的吸收峰波长,其关系如图所示。下列说法正确的是
A.将茶花汁滴入白醋,溶液显蓝色
B.茶花汁可用于检验雨水是否为酸雨
C.在pH为0~14范围内,可见光吸收峰波长变化越大的汁液越适合作酸碱指示剂
D.往滴有紫甘蓝汁的盐酸中逐滴加入NaOH溶液至过量较多时,溶液由红紫色变为绿色
9.某溶液能使紫色石蕊溶液变红,下列各组离子在该溶液中能大量共存的是( )
A.Ag+、Na+、 Cl﹣、NO3﹣ B.Na+、K+、OH﹣、SO42﹣
C.K+、Na+、CO32﹣、 Cl﹣ D.Ba2+、Mg2+、NO3﹣、Cl﹣
10.实验现象是我们得出结论的重要依据。下列实验现象与结论叙述不符的是
A.KMnO4 溶于水形成的紫色溶液能导电,说明 KMnO4 溶液中存在离子
B.向无色溶液中滴入酚酞溶液,溶液变成红色,该溶液一定是碱溶液
C.50mL 水与 50mL 酒精混合后体积小于 100mL,说明分子间有间隙
D.向鸡蛋白溶液中加入BaCl2溶液产生白色沉淀,说明重金属盐能使蛋白质变性
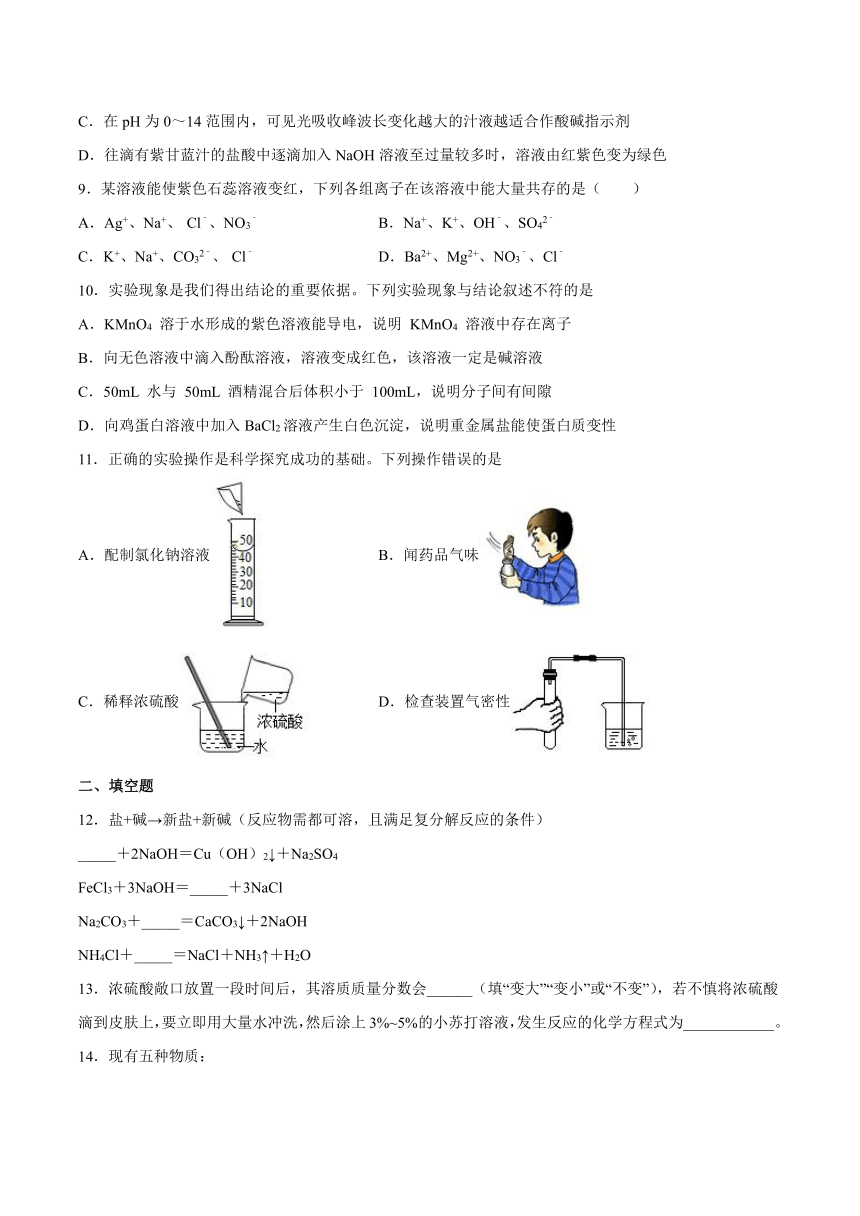
11.正确的实验操作是科学探究成功的基础。下列操作错误的是
A.配制氯化钠溶液 B.闻药品气味
C.稀释浓硫酸 D.检查装置气密性
二、填空题
12.盐+碱→新盐+新碱(反应物需都可溶,且满足复分解反应的条件)
_____+2NaOH=Cu(OH)2↓+Na2SO4
FeCl3+3NaOH=_____+3NaCl
Na2CO3+_____=CaCO3↓+2NaOH
NH4Cl+_____=NaCl+NH3↑+H2O
13.浓硫酸敞口放置一段时间后,其溶质质量分数会______(填“变大”“变小”或“不变”),若不慎将浓硫酸滴到皮肤上,要立即用大量水冲洗,然后涂上3%~5%的小苏打溶液,发生反应的化学方程式为____________。
14.现有五种物质:
A.磁铁矿 B.水 C.干冰 D.纯碱 E.氮气
请用相应物质的序号填空:
(1)实验室中最常用的溶剂是_____;
(2)可用于高炉炼铁的原料的是____;
(3)可用于人工降雨的是_______;
(4)可用作生产烧碱原料的是___。
三、推断题
15.2012年奥运会将在英国伦敦举行。奥运五环代表五大洲人们手拉手和睦相处。如图,A、B、C、D、E各代表铁、水、二氧化碳、硫酸铜溶液、氢氧化钙溶液中的一种物质。常温下,相连环物质间能发生反应,不相连环物质间不能发生反应,且B的相对分子质量大于D.请填空:
(1)写出下列物质的化学式:B______,D______;
(2)写出B与C发生反应的化学方程式:______,C与D发生反应的化学方程式:______;
(3)相连环物质间发生的反应,没有涉及的基本反应类型是______。
16.A、B、C、D、E五种物质都含有一种相同的元素,相互之间存在如图所示的转化关系(部分反应及条件已省略)。“—”表示物质间可以发生化学反应,“→”表示物质间存在相应的转化关系。若A、B是组成元素相同的无色液体,C、D是两种常见的无色气体,E是一种白色固体,受热可以生成A、D和一种有刺激性气味的气体。试回答下列问题:
(1)上述五种物质中所含的相同元素是 _____(填元素符号);E物质的化学式为 _____;
(2)B物质名称为 _____;
(3)上述五种物质中有 _____种属于氧化物;
(4)自然界中,通过 _____(填变化名称)可将D转化为C;
(5)写出由C→A的一个反应方程式 _____。
四、实验题
17.根据初中所学的知识并结合下列仪器回答问题:
(1)写出仪器的名称:j_____________。
(2)实验室选取d、e、i、j、k五种仪器制取并收集氧气时,反应的化学方程式为__________________,其中还缺少的仪器是_______________。
(3)实验室制取氢气的化学方程式____________________________。
(4)小明同学在组装实验室制取二氧化碳的发生装置时,除了选用了仪器b、g 外还需选择上述仪器中的_________(填写序号)。反应的化学方程式是________________________。
(5)小琪同学用浓盐酸与大理石在上述装置中反应,制取CO2并检验其有关性质。小琪同学将二氧化碳通入盛有澄清石灰水的烧杯中,观察到烧杯中澄清石灰水溶液不变浑浊。造成这一现象的可能原因是_______________________。
(6)某学生想要通过碳酸氢铵分解产生的氨气来探究氨水具有碱性,而氨气不具有碱性。按下图所示进行实验:(滤纸条用酚酞试液浸泡并晾干)
[资料] NH4HCO3NH3↑+H2O+CO2↑ 2NH3+H2SO4 ====(NH4)2 SO4
试分析:A装置中加入浓硫酸的作用是_______,B中氢氧化钠固体的作用是:Ⅰ.干燥气体;Ⅱ._______________(用化学方程式表示),该同学看到_________________________现象,得出了正确的结论。
18.小明在“探究盐酸和氢氧化钙能否发生化学反应”时,设计了如图所示的对照实验:
他设想在室温下,先取少量氢氧化钙粉末分别放入两只烧杯中,在Ⅱ烧杯中加入一定量的蒸馏水,在I烧杯中加入含等量蒸馏水的浓盐酸,充分搅拌,一段时间后,观察现象。根据上述情况,请回答以下问题:
(1)你认为要得到可靠的实验结论,需要保证实验I、Ⅱ中______完全相同。预测通过观察______的现象,说明盐酸和氢氧化钙发生了化学反应;
(2)设计对照实验Ⅱ的目的是______:
(3)如果不采用对照实验,请你设计一个简单实验证明盐酸和氢氧化钙能够发生化学反应:______。
五、计算题
19.现有碳酸钠和氯化钠的固体混合物20g,全部溶解在100g水中,再向其中加入一定质量的稀盐酸,恰好完全反应,放出4.4g气体,同时得到10%的氯化钠溶液。试计算:
(1)固体混合物中碳酸钠的质量分数______
(2)加入稀盐酸的质量______
参考答案:
1.C 2.A 3.C 4.D 5.B 6.B 7.D 8.D 9.D 10.B 11.A
12. CuSO4 Fe(OH)3 ↓ Ca(OH)2 NaOH
13. 变小
14. B A C D
15. CuSO4 CO2 CuSO4+Ca(OH)2=CaSO4+Cu(OH)2↓ Ca(OH)2+CO2=CaCO3↓+H2O 分解反应
16.(1) O NH4HCO3
(2)过氧化氢
(3)3
(4)光合作用
(5)2H2+O22H2O
17. 水槽 2KClO3 2KCl+3O2↑ 铁架台 Zn+ H2SO4==ZnSO4+H2↑ f CaCO3 + 2HCl == CaCl2 + H2O + CO2↑ 制得的二氧化碳中混有氯化氢气体 利用浓硫酸溶于水放出的大量热使NH4HCO3分解 吸收二氧化碳 C瓶中干燥的滤纸条不变红,D瓶中湿润的滤纸条变红
18.(1) 氢氧化钙粉末的质量 实验I中白色粉末消失成为无色溶液或(实验I中的浑浊程度比实验Ⅱ中小)
(2)排除氢氧化钙粉末溶于水的因素,以证实氢氧化钙粉末与盐酸发生化学反应
(3)在一定量的氢氧化钙粉末中加入适量的水,再滴加2--3滴酚酞试液,浑浊液变红,然后加入适量盐酸至红色消失,变为无色液体,说明盐酸与氢氧化钙能够发生化学反应
19.(1)53%;(2)95.4g
一、单选题
1.下列实验操作能达到实验目的的是
实验目的 实验操作
A.除去CaCl2中的CaCO3 加入过量的稀盐酸
B.干燥氨气 洗气,通过浓硫酸
C.鉴别硝酸铵和磷矿粉 ①看外观②加熟石灰
D.配制10%的硫酸溶液 计算、称量、量取、溶解
A.A B.B C.C D.D
2.运用分类思想认识物质是化学上常用的方法。下列说法正确的是
A.柠檬酸、碳酸均属于酸,它们都能使石蕊溶液变红
B.氮气、氢气都属于非金属单质,它们都能在氧气中燃烧
C.氧化镁、氧化铝均属于金属氧化物,它们都易溶解于水
D.硝酸铵、氯化铵均属于铵盐,它们都能跟碱性肥料混合使用
3.实验室有许多药品需要密封保存。对下列药品密封保存的原因解释不正确的是
A.浓硫酸﹣﹣﹣防止吸水
B.浓盐酸﹣﹣﹣防止挥发
C.生石灰﹣﹣﹣防止氧化
D.氢氧化钠﹣﹣﹣防止潮解和变质
4.下列实验现象描述正确的是
A.二氧化碳能使干燥的紫色石蕊纸花变红
B.氢气在氧气中燃烧时,火焰呈黄色,放出大量的热
C.在装有少量干燥生石灰的试管中加入少量水,试管外壁温度会降低
D.细铁丝与氧气剧烈燃烧,火星四射,放出大量的热,生成黑色固体物质
5.下图为xx泡打粉的标签如图所示,下列说法错误的是
A.碳酸氢钠俗称小苏打 B.泡打粉可以随意放置
C.加入泡打粉制作的蛋糕更松软 D.碳酸钙可做补钙剂
6.下列实验现象的描述不正确的是
A.把二氧化碳通入石蕊溶液,溶液变红
B.硫在空气中燃烧生成二氧化硫
C.硝酸铵固体溶于水时吸收热量
D.打开浓盐酸的瓶盖,瓶口出现大量白雾
7.下列对化学基本观念的认知正确的是( )
A.价值观:补充微量元素无需适可而止
B.能量观:酒精燃烧吸收大量的热
C.分类观:纯碱和烧碱从组成上都属于碱
D.守恒观:电解水反应前后,元素种类和原子数目均不变
8.紫甘蓝汁呈紫色,茶花汁呈浅黄色。用分光光度计测不同颜色的溶液,其可见光吸收峰波长范围不同。现用分光光度计测量以上两种汁液在不同酸碱度条件下的吸收峰波长,其关系如图所示。下列说法正确的是
A.将茶花汁滴入白醋,溶液显蓝色
B.茶花汁可用于检验雨水是否为酸雨
C.在pH为0~14范围内,可见光吸收峰波长变化越大的汁液越适合作酸碱指示剂
D.往滴有紫甘蓝汁的盐酸中逐滴加入NaOH溶液至过量较多时,溶液由红紫色变为绿色
9.某溶液能使紫色石蕊溶液变红,下列各组离子在该溶液中能大量共存的是( )
A.Ag+、Na+、 Cl﹣、NO3﹣ B.Na+、K+、OH﹣、SO42﹣
C.K+、Na+、CO32﹣、 Cl﹣ D.Ba2+、Mg2+、NO3﹣、Cl﹣
10.实验现象是我们得出结论的重要依据。下列实验现象与结论叙述不符的是
A.KMnO4 溶于水形成的紫色溶液能导电,说明 KMnO4 溶液中存在离子
B.向无色溶液中滴入酚酞溶液,溶液变成红色,该溶液一定是碱溶液
C.50mL 水与 50mL 酒精混合后体积小于 100mL,说明分子间有间隙
D.向鸡蛋白溶液中加入BaCl2溶液产生白色沉淀,说明重金属盐能使蛋白质变性
11.正确的实验操作是科学探究成功的基础。下列操作错误的是
A.配制氯化钠溶液 B.闻药品气味
C.稀释浓硫酸 D.检查装置气密性
二、填空题
12.盐+碱→新盐+新碱(反应物需都可溶,且满足复分解反应的条件)
_____+2NaOH=Cu(OH)2↓+Na2SO4
FeCl3+3NaOH=_____+3NaCl
Na2CO3+_____=CaCO3↓+2NaOH
NH4Cl+_____=NaCl+NH3↑+H2O
13.浓硫酸敞口放置一段时间后,其溶质质量分数会______(填“变大”“变小”或“不变”),若不慎将浓硫酸滴到皮肤上,要立即用大量水冲洗,然后涂上3%~5%的小苏打溶液,发生反应的化学方程式为____________。
14.现有五种物质:
A.磁铁矿 B.水 C.干冰 D.纯碱 E.氮气
请用相应物质的序号填空:
(1)实验室中最常用的溶剂是_____;
(2)可用于高炉炼铁的原料的是____;
(3)可用于人工降雨的是_______;
(4)可用作生产烧碱原料的是___。
三、推断题
15.2012年奥运会将在英国伦敦举行。奥运五环代表五大洲人们手拉手和睦相处。如图,A、B、C、D、E各代表铁、水、二氧化碳、硫酸铜溶液、氢氧化钙溶液中的一种物质。常温下,相连环物质间能发生反应,不相连环物质间不能发生反应,且B的相对分子质量大于D.请填空:
(1)写出下列物质的化学式:B______,D______;
(2)写出B与C发生反应的化学方程式:______,C与D发生反应的化学方程式:______;
(3)相连环物质间发生的反应,没有涉及的基本反应类型是______。
16.A、B、C、D、E五种物质都含有一种相同的元素,相互之间存在如图所示的转化关系(部分反应及条件已省略)。“—”表示物质间可以发生化学反应,“→”表示物质间存在相应的转化关系。若A、B是组成元素相同的无色液体,C、D是两种常见的无色气体,E是一种白色固体,受热可以生成A、D和一种有刺激性气味的气体。试回答下列问题:
(1)上述五种物质中所含的相同元素是 _____(填元素符号);E物质的化学式为 _____;
(2)B物质名称为 _____;
(3)上述五种物质中有 _____种属于氧化物;
(4)自然界中,通过 _____(填变化名称)可将D转化为C;
(5)写出由C→A的一个反应方程式 _____。
四、实验题
17.根据初中所学的知识并结合下列仪器回答问题:
(1)写出仪器的名称:j_____________。
(2)实验室选取d、e、i、j、k五种仪器制取并收集氧气时,反应的化学方程式为__________________,其中还缺少的仪器是_______________。
(3)实验室制取氢气的化学方程式____________________________。
(4)小明同学在组装实验室制取二氧化碳的发生装置时,除了选用了仪器b、g 外还需选择上述仪器中的_________(填写序号)。反应的化学方程式是________________________。
(5)小琪同学用浓盐酸与大理石在上述装置中反应,制取CO2并检验其有关性质。小琪同学将二氧化碳通入盛有澄清石灰水的烧杯中,观察到烧杯中澄清石灰水溶液不变浑浊。造成这一现象的可能原因是_______________________。
(6)某学生想要通过碳酸氢铵分解产生的氨气来探究氨水具有碱性,而氨气不具有碱性。按下图所示进行实验:(滤纸条用酚酞试液浸泡并晾干)
[资料] NH4HCO3NH3↑+H2O+CO2↑ 2NH3+H2SO4 ====(NH4)2 SO4
试分析:A装置中加入浓硫酸的作用是_______,B中氢氧化钠固体的作用是:Ⅰ.干燥气体;Ⅱ._______________(用化学方程式表示),该同学看到_________________________现象,得出了正确的结论。
18.小明在“探究盐酸和氢氧化钙能否发生化学反应”时,设计了如图所示的对照实验:
他设想在室温下,先取少量氢氧化钙粉末分别放入两只烧杯中,在Ⅱ烧杯中加入一定量的蒸馏水,在I烧杯中加入含等量蒸馏水的浓盐酸,充分搅拌,一段时间后,观察现象。根据上述情况,请回答以下问题:
(1)你认为要得到可靠的实验结论,需要保证实验I、Ⅱ中______完全相同。预测通过观察______的现象,说明盐酸和氢氧化钙发生了化学反应;
(2)设计对照实验Ⅱ的目的是______:
(3)如果不采用对照实验,请你设计一个简单实验证明盐酸和氢氧化钙能够发生化学反应:______。
五、计算题
19.现有碳酸钠和氯化钠的固体混合物20g,全部溶解在100g水中,再向其中加入一定质量的稀盐酸,恰好完全反应,放出4.4g气体,同时得到10%的氯化钠溶液。试计算:
(1)固体混合物中碳酸钠的质量分数______
(2)加入稀盐酸的质量______
参考答案:
1.C 2.A 3.C 4.D 5.B 6.B 7.D 8.D 9.D 10.B 11.A
12. CuSO4 Fe(OH)3 ↓ Ca(OH)2 NaOH
13. 变小
14. B A C D
15. CuSO4 CO2 CuSO4+Ca(OH)2=CaSO4+Cu(OH)2↓ Ca(OH)2+CO2=CaCO3↓+H2O 分解反应
16.(1) O NH4HCO3
(2)过氧化氢
(3)3
(4)光合作用
(5)2H2+O22H2O
17. 水槽 2KClO3 2KCl+3O2↑ 铁架台 Zn+ H2SO4==ZnSO4+H2↑ f CaCO3 + 2HCl == CaCl2 + H2O + CO2↑ 制得的二氧化碳中混有氯化氢气体 利用浓硫酸溶于水放出的大量热使NH4HCO3分解 吸收二氧化碳 C瓶中干燥的滤纸条不变红,D瓶中湿润的滤纸条变红
18.(1) 氢氧化钙粉末的质量 实验I中白色粉末消失成为无色溶液或(实验I中的浑浊程度比实验Ⅱ中小)
(2)排除氢氧化钙粉末溶于水的因素,以证实氢氧化钙粉末与盐酸发生化学反应
(3)在一定量的氢氧化钙粉末中加入适量的水,再滴加2--3滴酚酞试液,浑浊液变红,然后加入适量盐酸至红色消失,变为无色液体,说明盐酸与氢氧化钙能够发生化学反应
19.(1)53%;(2)95.4g
