第11章酸与碱检测题(含答案) --2022-2023学年九年级化学京改版(2013)下册
文档属性
| 名称 | 第11章酸与碱检测题(含答案) --2022-2023学年九年级化学京改版(2013)下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 83.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-19 00:00:00 | ||
图片预览


文档简介
第11章《酸与碱》检测题
一、单选题
1.下表是一些食物的pH,其中最不适宜胃酸过多的人食用的是
物质 玉米粥 牛奶 鸡蛋清 番茄
pH 7.0~8.0 6.3~6.6 7.6~8.0 4.0~4.4
A.玉米粥 B.番茄
C.鸡蛋清 D.牛奶
2.生产、生活中会用到不同的“洗涤”,下列“洗涤”方法不能达到目的是
A.在水中加入洗涤剂清洗餐盘
B.用汽油清洗油漆
C.用氢氧化钠溶液清洗排油烟机
D.用食盐水清洗金属表面的铁锈
3.下列物质的用途,利用其物理性质的是
A.液氮做制冷剂 B.稀盐酸做除锈剂
C.高锰酸钾做制氧剂 D.CO用于冶炼金属做还原剂
4.分类是认识物质的常用方法,下列分类错误的是
A.化合物:氧化铝 干冰 B.混合物:氯酸钾 乙醇
C.酸:盐酸 硫酸 D.碱:氢氧化钠 氨水
5.下列物质用途主要由其化学性质决定的是
A.稀有气体做电光源 B.生石灰用于食品加热
C.液氮制造低温环境 D.浓硫酸可作某些气体的干燥剂
6.根据下图实验,说法正确的是
A.品红的扩散速度相同
B.浓氨水变红
C.浓氨水有很强的挥发性
D.分子运动速率与温度无关
7.下列关于混合物提纯的方法正确的是
A.除去CO2中CO—— 通入氧气点燃
B.除去N2中的O2 ——通过灼热铜网
C.除去生石灰中混有的少量碳酸钙——将混合物溶于水后过滤
D.除去铁粉中混有的少量铜——加入适量稀盐酸充分反应后过滤
8.某课外活动小组测得某化工厂排放的废水的为4,为了将该废水的调到7,该小组提出的治理方案是向废水中加入适量的下列物质,该物质是
A.稀盐酸 B.生石灰
C.废铜屑 D.水
9.醋是家庭中不可缺少的调味品之一,同时,醋还具有较强的杀灭细菌、抑制病毒的作用。另外,醋可使胃中酸性增强,促进食欲,帮助消化,对于胃酸较少的人更是一剂良药。醋中的主要成分是醋酸,其化学式为CH3COOH。下列有关叙述中错误的是
A.醋酸的水溶液呈酸性,其pH大于7,滴入紫色石蕊试液显蓝色
B.醋酸能与氢氧化钠溶液反应生成醋酸钠和水,该反应为中和反应
C.用醋可以洗净铝制品的污垢,还可除去暖壶、水壶中的水垢
D.醋酸是由三种元素组成的化合物,一个醋酸分子由8个原子构成
10.逻辑推理是化学学习中常用的思维方法。下列推理正确的是
A.中和反应生成盐和水,则生成盐和水的反应一定是中和反应
B.化合物是由不同种元素组成的,所以由不同种元素组成的纯净物一定是化合物
C.单质中只含有一种元素,所以只含有一种元素的物质一定是单质
D.活泼金属能与稀盐酸反应放出气体,则能与稀盐酸反应放出气体的物质一定是活泼金属
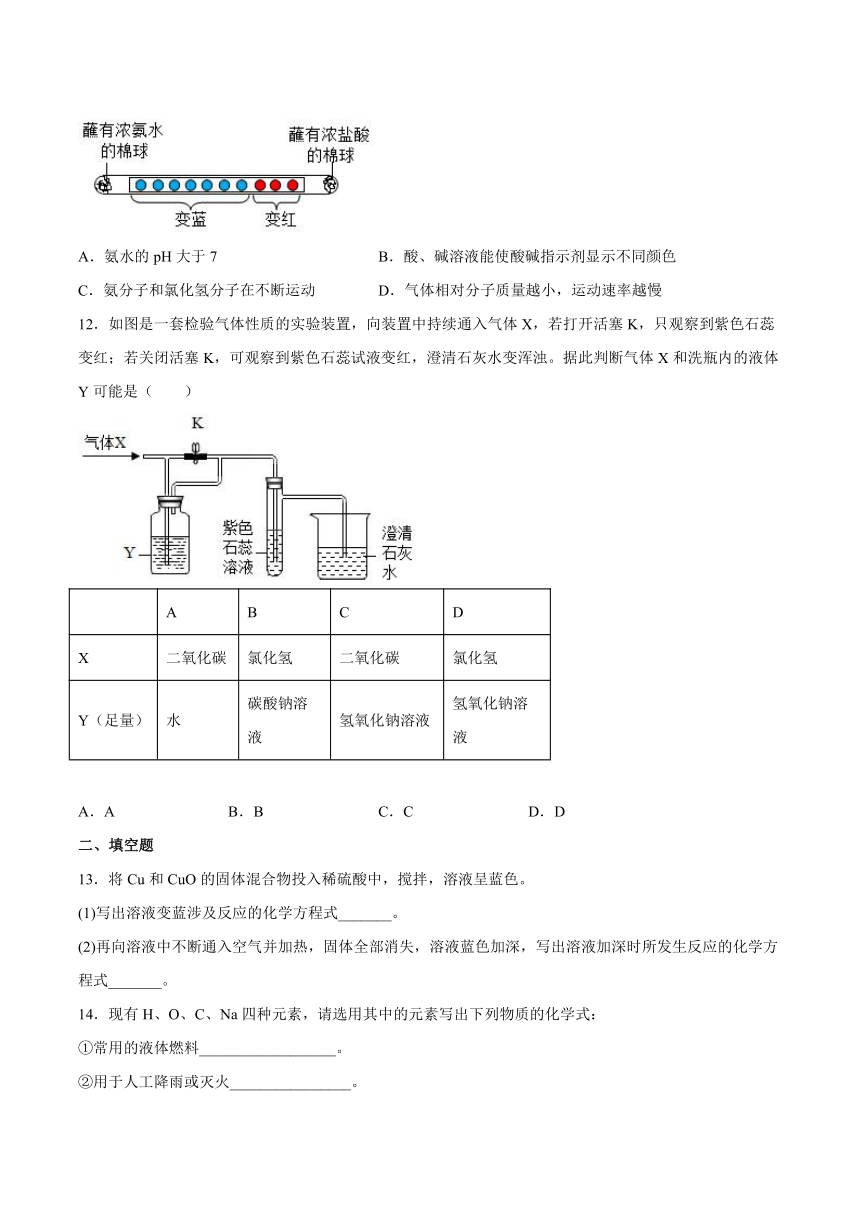
11.取一滤纸条,等间距滴10滴紫色石蕊试液,然后装入玻璃管中(如图),两端管口同时放入分别蘸有浓氨水和浓盐酸的棉球,几秒后观察到图示现象。下列结论不正确的是
A.氨水的pH大于7 B.酸、碱溶液能使酸碱指示剂显示不同颜色
C.氨分子和氯化氢分子在不断运动 D.气体相对分子质量越小,运动速率越慢
12.如图是一套检验气体性质的实验装置,向装置中持续通入气体X,若打开活塞K,只观察到紫色石蕊变红;若关闭活塞K,可观察到紫色石蕊试液变红,澄清石灰水变浑浊。据此判断气体X和洗瓶内的液体Y可能是( )
A B C D
X 二氧化碳 氯化氢 二氧化碳 氯化氢
Y(足量) 水 碳酸钠溶液 氢氧化钠溶液 氢氧化钠溶液
A.A B.B C.C D.D
二、填空题
13.将Cu和CuO的固体混合物投入稀硫酸中,搅拌,溶液呈蓝色。
(1)写出溶液变蓝涉及反应的化学方程式_______。
(2)再向溶液中不断通入空气并加热,固体全部消失,溶液蓝色加深,写出溶液加深时所发生反应的化学方程式_______。
14.现有H、O、C、Na四种元素,请选用其中的元素写出下列物质的化学式:
①常用的液体燃料__________________。
②用于人工降雨或灭火________________。
③制肥皂的碱________________。
三、推断题
15.A、B、C、D、E、F是初中化学常见的物质,已知A是一种单质,B为红棕色固体,D常用于改良酸性土壤,F与B属于同类物质,其相互反应情况如图所示(短线“-”相连的物质碱能反应,箭头“→”表示能生成)。
(1)A的化学式为______;D的名称为______。
(2)B与C反应的化学方程式为__________,实验时无色溶液变成_______色;D转化为E的化学方程式为_____________________。A与C的反应属于______反应(填基本反应类型)。
(3)写出F的一种用途:__________________。
16.如图A-E是初中化学常见的物质,各物质的转化关系如图所示。已知E可以用来改良酸性土壤。C和E物质类别相同,且C、E相对分子质量之比为20:37。B和D所属物质类别不同,且B中只含两种元素。其中图中的“一”表示相连两物质之间能发生反应,“→”表示一种物质能一步转化成另一种物质(部分反应物、生成物、反应条件已略去)。下列说法正确的是
A.D→B的反应类型属于置换反应
B.A可以与油脂发生反应
C.D一定是盐酸
D.A、C反应的实质是氢离子和氢氧根离子反应生成水分子
四、实验题
17.根据下图所示, 回答有关问题:
(1)写出图中标有字母的仪器名称:a__________。
(2)实验室用高锰酸钾制取氧气,应选用的发生装置是________(填字母),实验时该装置试管口应放一团棉花,其目的是_______________;反应的化学方程式为_____________________。
(3)实验室制取二氧化碳气体,若要获得干燥的二氧化碳,除发生装置外,还应选用D装置,装置中的液体是______________________(填写试剂名称)。如果用E装置收集该气体,则气体应从____________端进入(填b或c)。通常用澄清石灰水来检验二氧化碳,反应的化学方程式为________________________。
(4)下图是以锌粒和稀硫酸反应制备H2,并用排水法收集.请把图补画完整_____。
五、计算题
18.实验室测定一瓶变质的熟石灰中氢氧化钙的含量,取样品10g于锥形瓶中,向锥形瓶中滴加稀盐酸,充分反应后,测得加入稀盐酸的质量与反应生成气体的质量关系如图所示。请计算样品中氢氧化钙的质量分数。
参考答案:
1.B 2.D 3.A 4.B 5.B 6.C 7.B 8.B 9.A 10.B 11.D 12.B
13.(1)
(2)、
14. C2H5OH CO2 NaOH
15. Fe 熟石灰 Fe2O3 + 6HCl==2FeCl3 + 3H2O 黄 CO2+Ca(OH)2=CaCO3↓+H2O 置换反应 干燥剂
16.D
17. 长颈漏斗 A 加热时,防止固体药品随氧气流进入导管或造成堵塞 2KMnO4 K2MnO4+ MnO2 + O2↑ 浓硫酸 b CO2 +Ca(OH)2 = CaCO3↓+H2O
18.解:设样品中氢氧化钙的质量分数为x
x=0.5=50%
答:样品中氢氧化钙的质量分数为50%
一、单选题
1.下表是一些食物的pH,其中最不适宜胃酸过多的人食用的是
物质 玉米粥 牛奶 鸡蛋清 番茄
pH 7.0~8.0 6.3~6.6 7.6~8.0 4.0~4.4
A.玉米粥 B.番茄
C.鸡蛋清 D.牛奶
2.生产、生活中会用到不同的“洗涤”,下列“洗涤”方法不能达到目的是
A.在水中加入洗涤剂清洗餐盘
B.用汽油清洗油漆
C.用氢氧化钠溶液清洗排油烟机
D.用食盐水清洗金属表面的铁锈
3.下列物质的用途,利用其物理性质的是
A.液氮做制冷剂 B.稀盐酸做除锈剂
C.高锰酸钾做制氧剂 D.CO用于冶炼金属做还原剂
4.分类是认识物质的常用方法,下列分类错误的是
A.化合物:氧化铝 干冰 B.混合物:氯酸钾 乙醇
C.酸:盐酸 硫酸 D.碱:氢氧化钠 氨水
5.下列物质用途主要由其化学性质决定的是
A.稀有气体做电光源 B.生石灰用于食品加热
C.液氮制造低温环境 D.浓硫酸可作某些气体的干燥剂
6.根据下图实验,说法正确的是
A.品红的扩散速度相同
B.浓氨水变红
C.浓氨水有很强的挥发性
D.分子运动速率与温度无关
7.下列关于混合物提纯的方法正确的是
A.除去CO2中CO—— 通入氧气点燃
B.除去N2中的O2 ——通过灼热铜网
C.除去生石灰中混有的少量碳酸钙——将混合物溶于水后过滤
D.除去铁粉中混有的少量铜——加入适量稀盐酸充分反应后过滤
8.某课外活动小组测得某化工厂排放的废水的为4,为了将该废水的调到7,该小组提出的治理方案是向废水中加入适量的下列物质,该物质是
A.稀盐酸 B.生石灰
C.废铜屑 D.水
9.醋是家庭中不可缺少的调味品之一,同时,醋还具有较强的杀灭细菌、抑制病毒的作用。另外,醋可使胃中酸性增强,促进食欲,帮助消化,对于胃酸较少的人更是一剂良药。醋中的主要成分是醋酸,其化学式为CH3COOH。下列有关叙述中错误的是
A.醋酸的水溶液呈酸性,其pH大于7,滴入紫色石蕊试液显蓝色
B.醋酸能与氢氧化钠溶液反应生成醋酸钠和水,该反应为中和反应
C.用醋可以洗净铝制品的污垢,还可除去暖壶、水壶中的水垢
D.醋酸是由三种元素组成的化合物,一个醋酸分子由8个原子构成
10.逻辑推理是化学学习中常用的思维方法。下列推理正确的是
A.中和反应生成盐和水,则生成盐和水的反应一定是中和反应
B.化合物是由不同种元素组成的,所以由不同种元素组成的纯净物一定是化合物
C.单质中只含有一种元素,所以只含有一种元素的物质一定是单质
D.活泼金属能与稀盐酸反应放出气体,则能与稀盐酸反应放出气体的物质一定是活泼金属
11.取一滤纸条,等间距滴10滴紫色石蕊试液,然后装入玻璃管中(如图),两端管口同时放入分别蘸有浓氨水和浓盐酸的棉球,几秒后观察到图示现象。下列结论不正确的是
A.氨水的pH大于7 B.酸、碱溶液能使酸碱指示剂显示不同颜色
C.氨分子和氯化氢分子在不断运动 D.气体相对分子质量越小,运动速率越慢
12.如图是一套检验气体性质的实验装置,向装置中持续通入气体X,若打开活塞K,只观察到紫色石蕊变红;若关闭活塞K,可观察到紫色石蕊试液变红,澄清石灰水变浑浊。据此判断气体X和洗瓶内的液体Y可能是( )
A B C D
X 二氧化碳 氯化氢 二氧化碳 氯化氢
Y(足量) 水 碳酸钠溶液 氢氧化钠溶液 氢氧化钠溶液
A.A B.B C.C D.D
二、填空题
13.将Cu和CuO的固体混合物投入稀硫酸中,搅拌,溶液呈蓝色。
(1)写出溶液变蓝涉及反应的化学方程式_______。
(2)再向溶液中不断通入空气并加热,固体全部消失,溶液蓝色加深,写出溶液加深时所发生反应的化学方程式_______。
14.现有H、O、C、Na四种元素,请选用其中的元素写出下列物质的化学式:
①常用的液体燃料__________________。
②用于人工降雨或灭火________________。
③制肥皂的碱________________。
三、推断题
15.A、B、C、D、E、F是初中化学常见的物质,已知A是一种单质,B为红棕色固体,D常用于改良酸性土壤,F与B属于同类物质,其相互反应情况如图所示(短线“-”相连的物质碱能反应,箭头“→”表示能生成)。
(1)A的化学式为______;D的名称为______。
(2)B与C反应的化学方程式为__________,实验时无色溶液变成_______色;D转化为E的化学方程式为_____________________。A与C的反应属于______反应(填基本反应类型)。
(3)写出F的一种用途:__________________。
16.如图A-E是初中化学常见的物质,各物质的转化关系如图所示。已知E可以用来改良酸性土壤。C和E物质类别相同,且C、E相对分子质量之比为20:37。B和D所属物质类别不同,且B中只含两种元素。其中图中的“一”表示相连两物质之间能发生反应,“→”表示一种物质能一步转化成另一种物质(部分反应物、生成物、反应条件已略去)。下列说法正确的是
A.D→B的反应类型属于置换反应
B.A可以与油脂发生反应
C.D一定是盐酸
D.A、C反应的实质是氢离子和氢氧根离子反应生成水分子
四、实验题
17.根据下图所示, 回答有关问题:
(1)写出图中标有字母的仪器名称:a__________。
(2)实验室用高锰酸钾制取氧气,应选用的发生装置是________(填字母),实验时该装置试管口应放一团棉花,其目的是_______________;反应的化学方程式为_____________________。
(3)实验室制取二氧化碳气体,若要获得干燥的二氧化碳,除发生装置外,还应选用D装置,装置中的液体是______________________(填写试剂名称)。如果用E装置收集该气体,则气体应从____________端进入(填b或c)。通常用澄清石灰水来检验二氧化碳,反应的化学方程式为________________________。
(4)下图是以锌粒和稀硫酸反应制备H2,并用排水法收集.请把图补画完整_____。
五、计算题
18.实验室测定一瓶变质的熟石灰中氢氧化钙的含量,取样品10g于锥形瓶中,向锥形瓶中滴加稀盐酸,充分反应后,测得加入稀盐酸的质量与反应生成气体的质量关系如图所示。请计算样品中氢氧化钙的质量分数。
参考答案:
1.B 2.D 3.A 4.B 5.B 6.C 7.B 8.B 9.A 10.B 11.D 12.B
13.(1)
(2)、
14. C2H5OH CO2 NaOH
15. Fe 熟石灰 Fe2O3 + 6HCl==2FeCl3 + 3H2O 黄 CO2+Ca(OH)2=CaCO3↓+H2O 置换反应 干燥剂
16.D
17. 长颈漏斗 A 加热时,防止固体药品随氧气流进入导管或造成堵塞 2KMnO4 K2MnO4+ MnO2 + O2↑ 浓硫酸 b CO2 +Ca(OH)2 = CaCO3↓+H2O
18.解:设样品中氢氧化钙的质量分数为x
x=0.5=50%
答:样品中氢氧化钙的质量分数为50%
