第八单元海水中的化学测试题(含答案) --2022-2023学年九年级化学鲁教版下册
文档属性
| 名称 | 第八单元海水中的化学测试题(含答案) --2022-2023学年九年级化学鲁教版下册 |
|
|
| 格式 | docx | ||
| 文件大小 | 146.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-19 00:00:00 | ||
图片预览



文档简介
第八单元《海水中的化学》测试题
一、单选题
1.下列依据实验目的设计的实验方案中,正确的是
序号 实验目的 实验方案
A 除去CaCO3中的KCl 溶解、过滤、洗涤、干燥
B 除去ZnSO4溶液中的H2SO4 加入足量氧化铁粉末,过滤
C 除去NaCl溶液中的MgCl2 加入过量NaOH溶液,过滤
D 除去CO2中的水蒸气 将气体通过装有生石灰的干燥管
A.A B.B C.C D.D
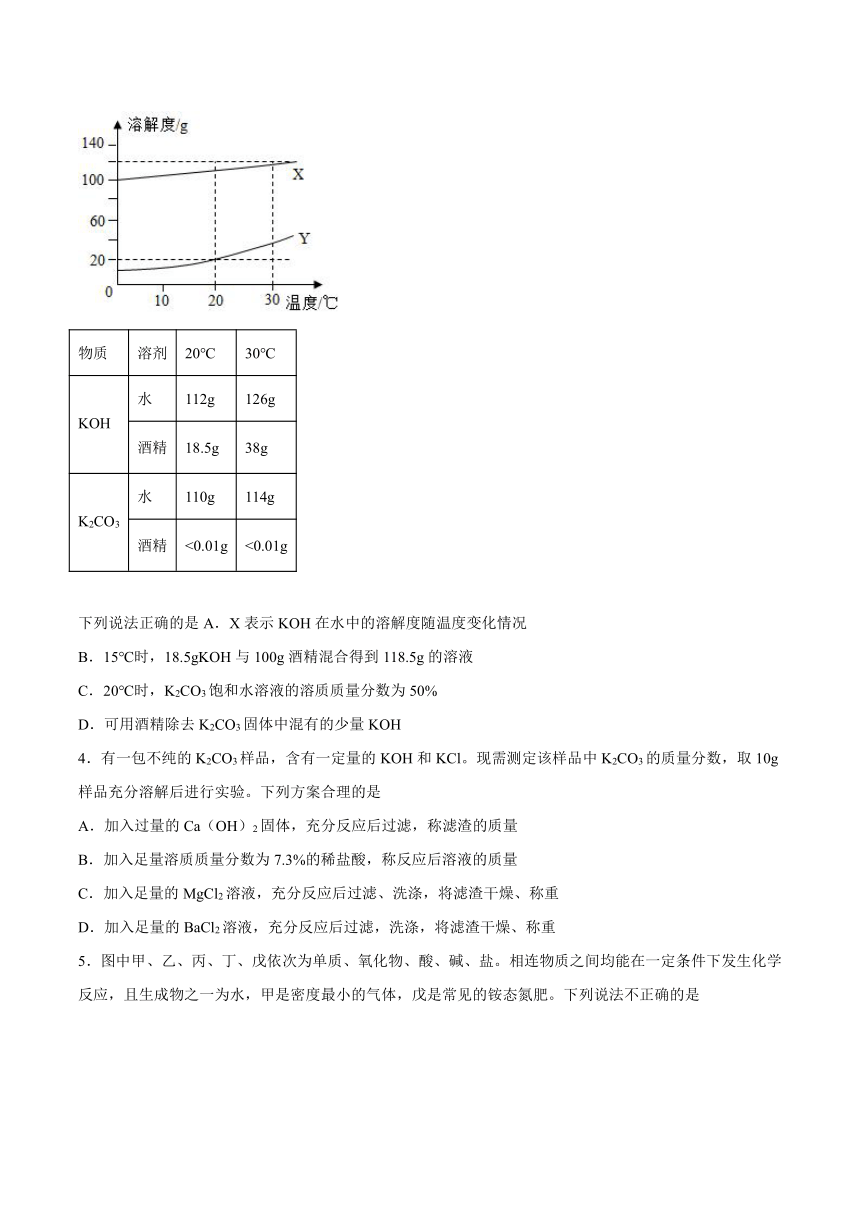
2.如图为甲、乙两种固体物质的溶解度曲线,据此判断以下叙述正确的是( )
A.甲的溶解度比乙的溶解度大
B.乙的溶解度受温度变化影响较大
C.要从乙的饱和溶液中得到乙,通常采用蒸发溶剂的方法
D.20℃时,甲、乙两种饱和溶液中溶质的质量相等
3.不同温度下,KOH、K2CO3分别在水和酒精中的溶解度如下表。下图中X、Y分别表示两种物质在水或酒精中的溶解度随温度变化曲线。
物质 溶剂 20℃ 30℃
KOH 水 112g 126g
酒精 18.5g 38g
K2CO3 水 110g 114g
酒精 <0.01g <0.01g
下列说法正确的是A.X表示KOH在水中的溶解度随温度变化情况
B.15℃时,18.5gKOH与100g酒精混合得到118.5g的溶液
C.20℃时,K2CO3饱和水溶液的溶质质量分数为50%
D.可用酒精除去K2CO3固体中混有的少量KOH
4.有一包不纯的K2CO3样品,含有一定量的KOH和KCl。现需测定该样品中K2CO3的质量分数,取10g样品充分溶解后进行实验。下列方案合理的是
A.加入过量的Ca(OH)2固体,充分反应后过滤,称滤渣的质量
B.加入足量溶质质量分数为7.3%的稀盐酸,称反应后溶液的质量
C.加入足量的MgCl2溶液,充分反应后过滤、洗涤,将滤渣干燥、称重
D.加入足量的BaCl2溶液,充分反应后过滤,洗涤,将滤渣干燥、称重
5.图中甲、乙、丙、丁、戊依次为单质、氧化物、酸、碱、盐。相连物质之间均能在一定条件下发生化学反应,且生成物之一为水,甲是密度最小的气体,戊是常见的铵态氮肥。下列说法不正确的是
A.乙和丙反应后溶液可能为黄色
B.丙和丁发生的反应一定属于中和反应
C.甲和乙的反应中一定有元素化合价的变化
D.若丁和戊反应生成气体,则该气体能使紫色石蕊溶液变红
6.除去下列物质中的少量杂质,所用的试剂和操作方法都正确的是
选项 物质 杂质 试剂 操作方法
A MgCl2溶液 HCl Mg(OH)2 加过量的Mg(OH)2固体,过滤
B KNO3溶液 K2SO4 硝酸钡 加入过量的硝酸钡溶液,过滤
C CuO 木炭粉 稀硫酸 加入足量的稀硫酸,洗涤,干燥
D MnO2 KCl 蒸馏水 加入适量的蒸馏水溶解,过滤,将滤液蒸干
A.A B.B C.C D.D
7.下列根据证据得出的结论,错误的是
选项 证据 结论
A 碳酸氢钠溶液能使酚酞溶液变红 碳酸氢钠溶液呈碱性
B 电解水得到氢气和氧气 分子可以再分
C 取水样加入肥皂水,振荡,出现较多泡沫 水样为软水
D 往溶液中滴加BaCl2溶液,产生白色沉淀 溶液中含有或
A.A B.B C.C D.D
8.在“P+Q→盐+水”的反应中,物质P和Q可能是
A.HCl,Ca(OH)2
B.SO2,Na2O
C.BaCl2,H2SO4
D.H2SO4,ZnCl2
9.下列实验现象描述正确的是
A.硫在空气中燃烧:淡黄色固体燃烧,发出蓝紫色火焰,放热
B.将氢气通入灼热的氧化铜:紫红色粉末逐渐变为黑色
C.镁在空气中燃烧:银白色固体燃烧,发出耀眼白光,放热,生成白色固体
D.碳酸钠粉末与足量盐酸反应:白色固体表面有气泡产生,固体减少
10.某矿物质水标签上的部分内容如图所示,若要检验其中含MgSO4,需要的试剂之一是
品 名:××饮用矿物质水 配料表:水、食品添加剂(氯化钾、硫酸镁)
A.稀硫酸 B.AgNO3溶液 C.BaCl2溶液 D.金属镁
11.下列教材课外实验中,发生化学变化的是( )
A.石墨导电实验 B.自制汽水
C.自制白糖晶体 D.简易净水器
12.下列推理正确的是( )
A.原子核由质子和中子构成,则原子中都有质子和中子
B.单质只含一种元素,则只含一种元素的物质一定是单质
C.碱溶液能使酚酞溶液变红,所以能使酚酞溶液变红的溶液一定呈碱性
D.碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
二、填空题
13.请用“>”“<”或“=”填空:
(1)质子数:O______O2-;
(2)氯元素化合价:Ca(ClO)2______KCl;
(3)溶液体积:酒精与水混合前______混合后;
(4)水中溶氧量:夏天______冬天(不考虑其他影响因素)。
14.通过晾晒海水可以得到粗盐,去除粗盐中难溶性杂质经过的溶解、过滤、蒸发等步骤中,都用到的玻璃仪器是______,蒸发中这种仪器的作用是______,在提纯的盐溶液中滴加适量______溶液,即可除去盐溶液中含有的硫酸钠。
三、推断题
15.A、B、C、D、E是初中常见的五种不同类别的物质。图中“→”表示一种物质能转化为另一种物质,“一”表示两种物质能发生反应。其中A是一种红棕色的金属氧化物,D可以制肥皂,而且是炉具清洁剂的成分,胃液中含有E。
(1)写出下列物质的化学式;A______。B______。
(2)写出A与E反应的化学方程式______。
(3)写出足量E与固体C反应的实验现象______。
(4)下图是工业生产E溶液的流程。其中“?”代表的物质是上图中的______。(填字母)
16.碳酸钾广泛应用于玻璃、纺织印染和肥皂生产等领域,制取碳酸钾的工艺流程示意图如图:
温度/℃ 0 10 20 30 40 60 80 100
K2CO3的溶解度/g 107.0 109.0 111.0 114.0 117.0 126.0 139.0 156.0
KCl的溶解度/g 28 31 34 37 40 45 51 56
根据如图图表信息,回答下列问题:
(1)生成碳酸钾的化学方程式为______。
(2)上述流程中可循环使用的物质是______,NH4Cl在农业上可用作______。
(3)得到K2CO3晶浆的结晶方法是______。
(4)上述流程中洗涤K2CO3晶体应选用______(填序号)。
①NH4Cl溶液 ②热水 ③饱和K2CO3溶液
(5)往40℃700g氯化钾饱和溶液中,不断通入氨气和二氧化碳,控制温度在60~80℃之间,充分吸收混合。在有机萃取后,冷却至20℃时,理论上能得到K2CO3晶体______g。(忽略实验过程中的水分蒸发,结果保留整数)
(6)某CaCl2中混有KCl杂质,简述提纯该CaCl2的实验操作:______。
四、实验题
17.化学晚会上,小明表演了一个小魔术——“矿泉水”变成“牛奶”、“雪碧”和“红酒”。回答下列问题:
(1) “矿泉水”实际是石灰水,加入液体A后出现白色浑浊,形似牛奶,该过程发生反应的化学方程式为__________。
(2)“牛奶”中加入B,有大量气泡产生,变成雪碧,则B物质是________,该过程发生的化学反应最多有________个。
(3)C是一种紫色的溶液,滴入“雪碧”中变为红色,则雪碧的组成是________。
18.(1)如图是氧气的制取与性质实验装置图
回答下列问题:
①装置B的作用是 _________________ ,装置C中硫粉燃烧的现象是 __________________ ,装置D的作用是 ___________
②装置A中发生反应的化学方程式为 __________________________ ,装置D中发生反应的化学方程式为 ______________
(2)已知某固体混合物A中含有CuSO4、FeCl3、NaNO3、BaCl2、CaCO3五种物质中的两种或多种,按下述步骤进行实验探究,观察实验现象,并加以分析推理(设过程中所有发生的反应都恰好完全反应)
Ⅰ、取一定质量的该固体混合物A放入一洁净烧杯中,向其中加入适量NaOH溶液,搅拌,待烧杯中物质充分反应后,过滤,得红褐色沉淀B和滤液C
Ⅱ、另取一定质量的该固体混合物A放入另一洁净烧杯中,向其中加入适量H2SO4溶液,搅拌,待烧杯中物质充分反应后,过滤,得白色沉淀D和滤液E
Ⅲ、将所得溶液C和溶液E充分混合,再向混合后的溶液中加入适量AgNO3溶液,待充分反应后,过滤,得白色沉淀F和滤液G
Ⅳ、根据上述实验过程和发生的现象做出相应的推理,填写以下空白:
①在固体混合物A里,上述五种物质中肯定存在的物质是(写化学式) _______________________
②写出步骤Ⅲ中生成白色沉淀F的1个化学方程式: _______________________
③在滤液G中,含有的金属阳离子共有 ___________ 种,该滤液中肯定存在的酸根离子是 ___________
④在混合物A里,上述五种物质中肯定不存在的物质是(写化学式) _________________ ,得出此结论的理由是 _________________
五、计算题
19.某造纸厂排放的废水中含有一定量的氢氧化钠,为测定氢氧化钠的浓度,取100.0g沉淀后的澄清废水,逐滴滴入溶质质量分数为9.8%的稀硫酸恰好完全反应时用去稀硫酸的质量是20.0g(假设废水中不含其它与硫酸反应的物质)。
(1)计算废水中氢氧化钠的溶质质量分数。
(2)为掌握该反应恰好完全反应的时机,在滴入稀硫酸前应该进行的操作是_____。
参考答案:
1.A 2.C 3.D 4.D 5.D 6.A 7.D 8.A 9.C 10.C 11.B 12.C
13.(1)=
(2)>
(3)>
(4)<
14. 玻璃棒 搅拌,防止因局部温度过高,造成液滴飞溅 BaCl2
15. Fe2O3 Fe 白色固体逐渐减少至消失,有气泡产生 D
16.(1)
(2) 有机萃剂 氮肥
(3)蒸发结晶
(4)③
(5)185
(6)加入足量的碳酸钾,过滤、洗涤,往滤渣中加入适量的稀盐酸,蒸发结晶的氯化钙
17. Ca(OH)2+Na2CO3= CaCO3↓+2NaOH HCl 3 NaCl、CaCl2、HCl、H2O
18. 除去水蒸气(干燥气体或吸收水分) 产生蓝紫色火焰 吸收二氧化硫,防止污染空气 2H2O22H2O+O2↑ SO2+2NaOH=Na2SO3+H2O FeCl3、BaCl2 NaCl+AgNO3=AgCl↓+NaNO3 3 ##硝酸根##硝酸根离子
CuSO4、CaCO3 Ⅰ中只有红褐色沉淀
19.(1)1.6%;(2)给废水样品中滴入几滴酚酞溶液
一、单选题
1.下列依据实验目的设计的实验方案中,正确的是
序号 实验目的 实验方案
A 除去CaCO3中的KCl 溶解、过滤、洗涤、干燥
B 除去ZnSO4溶液中的H2SO4 加入足量氧化铁粉末,过滤
C 除去NaCl溶液中的MgCl2 加入过量NaOH溶液,过滤
D 除去CO2中的水蒸气 将气体通过装有生石灰的干燥管
A.A B.B C.C D.D
2.如图为甲、乙两种固体物质的溶解度曲线,据此判断以下叙述正确的是( )
A.甲的溶解度比乙的溶解度大
B.乙的溶解度受温度变化影响较大
C.要从乙的饱和溶液中得到乙,通常采用蒸发溶剂的方法
D.20℃时,甲、乙两种饱和溶液中溶质的质量相等
3.不同温度下,KOH、K2CO3分别在水和酒精中的溶解度如下表。下图中X、Y分别表示两种物质在水或酒精中的溶解度随温度变化曲线。
物质 溶剂 20℃ 30℃
KOH 水 112g 126g
酒精 18.5g 38g
K2CO3 水 110g 114g
酒精 <0.01g <0.01g
下列说法正确的是A.X表示KOH在水中的溶解度随温度变化情况
B.15℃时,18.5gKOH与100g酒精混合得到118.5g的溶液
C.20℃时,K2CO3饱和水溶液的溶质质量分数为50%
D.可用酒精除去K2CO3固体中混有的少量KOH
4.有一包不纯的K2CO3样品,含有一定量的KOH和KCl。现需测定该样品中K2CO3的质量分数,取10g样品充分溶解后进行实验。下列方案合理的是
A.加入过量的Ca(OH)2固体,充分反应后过滤,称滤渣的质量
B.加入足量溶质质量分数为7.3%的稀盐酸,称反应后溶液的质量
C.加入足量的MgCl2溶液,充分反应后过滤、洗涤,将滤渣干燥、称重
D.加入足量的BaCl2溶液,充分反应后过滤,洗涤,将滤渣干燥、称重
5.图中甲、乙、丙、丁、戊依次为单质、氧化物、酸、碱、盐。相连物质之间均能在一定条件下发生化学反应,且生成物之一为水,甲是密度最小的气体,戊是常见的铵态氮肥。下列说法不正确的是
A.乙和丙反应后溶液可能为黄色
B.丙和丁发生的反应一定属于中和反应
C.甲和乙的反应中一定有元素化合价的变化
D.若丁和戊反应生成气体,则该气体能使紫色石蕊溶液变红
6.除去下列物质中的少量杂质,所用的试剂和操作方法都正确的是
选项 物质 杂质 试剂 操作方法
A MgCl2溶液 HCl Mg(OH)2 加过量的Mg(OH)2固体,过滤
B KNO3溶液 K2SO4 硝酸钡 加入过量的硝酸钡溶液,过滤
C CuO 木炭粉 稀硫酸 加入足量的稀硫酸,洗涤,干燥
D MnO2 KCl 蒸馏水 加入适量的蒸馏水溶解,过滤,将滤液蒸干
A.A B.B C.C D.D
7.下列根据证据得出的结论,错误的是
选项 证据 结论
A 碳酸氢钠溶液能使酚酞溶液变红 碳酸氢钠溶液呈碱性
B 电解水得到氢气和氧气 分子可以再分
C 取水样加入肥皂水,振荡,出现较多泡沫 水样为软水
D 往溶液中滴加BaCl2溶液,产生白色沉淀 溶液中含有或
A.A B.B C.C D.D
8.在“P+Q→盐+水”的反应中,物质P和Q可能是
A.HCl,Ca(OH)2
B.SO2,Na2O
C.BaCl2,H2SO4
D.H2SO4,ZnCl2
9.下列实验现象描述正确的是
A.硫在空气中燃烧:淡黄色固体燃烧,发出蓝紫色火焰,放热
B.将氢气通入灼热的氧化铜:紫红色粉末逐渐变为黑色
C.镁在空气中燃烧:银白色固体燃烧,发出耀眼白光,放热,生成白色固体
D.碳酸钠粉末与足量盐酸反应:白色固体表面有气泡产生,固体减少
10.某矿物质水标签上的部分内容如图所示,若要检验其中含MgSO4,需要的试剂之一是
品 名:××饮用矿物质水 配料表:水、食品添加剂(氯化钾、硫酸镁)
A.稀硫酸 B.AgNO3溶液 C.BaCl2溶液 D.金属镁
11.下列教材课外实验中,发生化学变化的是( )
A.石墨导电实验 B.自制汽水
C.自制白糖晶体 D.简易净水器
12.下列推理正确的是( )
A.原子核由质子和中子构成,则原子中都有质子和中子
B.单质只含一种元素,则只含一种元素的物质一定是单质
C.碱溶液能使酚酞溶液变红,所以能使酚酞溶液变红的溶液一定呈碱性
D.碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
二、填空题
13.请用“>”“<”或“=”填空:
(1)质子数:O______O2-;
(2)氯元素化合价:Ca(ClO)2______KCl;
(3)溶液体积:酒精与水混合前______混合后;
(4)水中溶氧量:夏天______冬天(不考虑其他影响因素)。
14.通过晾晒海水可以得到粗盐,去除粗盐中难溶性杂质经过的溶解、过滤、蒸发等步骤中,都用到的玻璃仪器是______,蒸发中这种仪器的作用是______,在提纯的盐溶液中滴加适量______溶液,即可除去盐溶液中含有的硫酸钠。
三、推断题
15.A、B、C、D、E是初中常见的五种不同类别的物质。图中“→”表示一种物质能转化为另一种物质,“一”表示两种物质能发生反应。其中A是一种红棕色的金属氧化物,D可以制肥皂,而且是炉具清洁剂的成分,胃液中含有E。
(1)写出下列物质的化学式;A______。B______。
(2)写出A与E反应的化学方程式______。
(3)写出足量E与固体C反应的实验现象______。
(4)下图是工业生产E溶液的流程。其中“?”代表的物质是上图中的______。(填字母)
16.碳酸钾广泛应用于玻璃、纺织印染和肥皂生产等领域,制取碳酸钾的工艺流程示意图如图:
温度/℃ 0 10 20 30 40 60 80 100
K2CO3的溶解度/g 107.0 109.0 111.0 114.0 117.0 126.0 139.0 156.0
KCl的溶解度/g 28 31 34 37 40 45 51 56
根据如图图表信息,回答下列问题:
(1)生成碳酸钾的化学方程式为______。
(2)上述流程中可循环使用的物质是______,NH4Cl在农业上可用作______。
(3)得到K2CO3晶浆的结晶方法是______。
(4)上述流程中洗涤K2CO3晶体应选用______(填序号)。
①NH4Cl溶液 ②热水 ③饱和K2CO3溶液
(5)往40℃700g氯化钾饱和溶液中,不断通入氨气和二氧化碳,控制温度在60~80℃之间,充分吸收混合。在有机萃取后,冷却至20℃时,理论上能得到K2CO3晶体______g。(忽略实验过程中的水分蒸发,结果保留整数)
(6)某CaCl2中混有KCl杂质,简述提纯该CaCl2的实验操作:______。
四、实验题
17.化学晚会上,小明表演了一个小魔术——“矿泉水”变成“牛奶”、“雪碧”和“红酒”。回答下列问题:
(1) “矿泉水”实际是石灰水,加入液体A后出现白色浑浊,形似牛奶,该过程发生反应的化学方程式为__________。
(2)“牛奶”中加入B,有大量气泡产生,变成雪碧,则B物质是________,该过程发生的化学反应最多有________个。
(3)C是一种紫色的溶液,滴入“雪碧”中变为红色,则雪碧的组成是________。
18.(1)如图是氧气的制取与性质实验装置图
回答下列问题:
①装置B的作用是 _________________ ,装置C中硫粉燃烧的现象是 __________________ ,装置D的作用是 ___________
②装置A中发生反应的化学方程式为 __________________________ ,装置D中发生反应的化学方程式为 ______________
(2)已知某固体混合物A中含有CuSO4、FeCl3、NaNO3、BaCl2、CaCO3五种物质中的两种或多种,按下述步骤进行实验探究,观察实验现象,并加以分析推理(设过程中所有发生的反应都恰好完全反应)
Ⅰ、取一定质量的该固体混合物A放入一洁净烧杯中,向其中加入适量NaOH溶液,搅拌,待烧杯中物质充分反应后,过滤,得红褐色沉淀B和滤液C
Ⅱ、另取一定质量的该固体混合物A放入另一洁净烧杯中,向其中加入适量H2SO4溶液,搅拌,待烧杯中物质充分反应后,过滤,得白色沉淀D和滤液E
Ⅲ、将所得溶液C和溶液E充分混合,再向混合后的溶液中加入适量AgNO3溶液,待充分反应后,过滤,得白色沉淀F和滤液G
Ⅳ、根据上述实验过程和发生的现象做出相应的推理,填写以下空白:
①在固体混合物A里,上述五种物质中肯定存在的物质是(写化学式) _______________________
②写出步骤Ⅲ中生成白色沉淀F的1个化学方程式: _______________________
③在滤液G中,含有的金属阳离子共有 ___________ 种,该滤液中肯定存在的酸根离子是 ___________
④在混合物A里,上述五种物质中肯定不存在的物质是(写化学式) _________________ ,得出此结论的理由是 _________________
五、计算题
19.某造纸厂排放的废水中含有一定量的氢氧化钠,为测定氢氧化钠的浓度,取100.0g沉淀后的澄清废水,逐滴滴入溶质质量分数为9.8%的稀硫酸恰好完全反应时用去稀硫酸的质量是20.0g(假设废水中不含其它与硫酸反应的物质)。
(1)计算废水中氢氧化钠的溶质质量分数。
(2)为掌握该反应恰好完全反应的时机,在滴入稀硫酸前应该进行的操作是_____。
参考答案:
1.A 2.C 3.D 4.D 5.D 6.A 7.D 8.A 9.C 10.C 11.B 12.C
13.(1)=
(2)>
(3)>
(4)<
14. 玻璃棒 搅拌,防止因局部温度过高,造成液滴飞溅 BaCl2
15. Fe2O3 Fe 白色固体逐渐减少至消失,有气泡产生 D
16.(1)
(2) 有机萃剂 氮肥
(3)蒸发结晶
(4)③
(5)185
(6)加入足量的碳酸钾,过滤、洗涤,往滤渣中加入适量的稀盐酸,蒸发结晶的氯化钙
17. Ca(OH)2+Na2CO3= CaCO3↓+2NaOH HCl 3 NaCl、CaCl2、HCl、H2O
18. 除去水蒸气(干燥气体或吸收水分) 产生蓝紫色火焰 吸收二氧化硫,防止污染空气 2H2O22H2O+O2↑ SO2+2NaOH=Na2SO3+H2O FeCl3、BaCl2 NaCl+AgNO3=AgCl↓+NaNO3 3 ##硝酸根##硝酸根离子
CuSO4、CaCO3 Ⅰ中只有红褐色沉淀
19.(1)1.6%;(2)给废水样品中滴入几滴酚酞溶液
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
