5.2.2氮的氧化物溶于水的计算 课件(共14张PPT)2022-2023学年高一下学期化学人教版(2019)必修第二册
文档属性
| 名称 | 5.2.2氮的氧化物溶于水的计算 课件(共14张PPT)2022-2023学年高一下学期化学人教版(2019)必修第二册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 782.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-21 00:00:00 | ||
图片预览





文档简介
(共14张PPT)
第二节 氮及其化合物
第二课时 氮的氧化物溶于水的计算
第五章 化工生产中的重要非金属元素
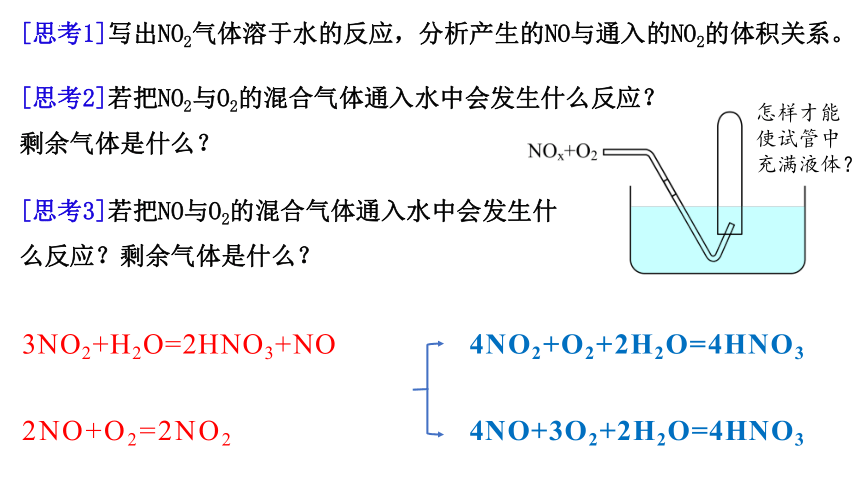
[思考1]写出NO2气体溶于水的反应,分析产生的NO与通入的NO2的体积关系。
[思考2]若把NO2与O2的混合气体通入水中会发生什么反应?
剩余气体是什么?
[思考3]若把NO与O2的混合气体通入水中会发生什么反应?剩余气体是什么?
怎样才能使试管中充满液体?
3NO2+H2O=2HNO3+NO
2NO+O2=2NO2
4NO2+O2+2H2O=4HNO3
4NO+3O2+2H2O=4HNO3
例1.向盛有15mLNO2气体,倒立于水槽的试管A中通入O2,充分反应后,试管中还剩余气体3mL,则通入的O2体积可能是多少?
气体剩余只能是NO或O2,不可能是NO2。
剩余气体3mL
①NO2过量→3mLNO
②3mLO2
1
6mL 1.5mL
1
15mL 3.75mL
4NO2+O2+2H2O==4HNO3
3NO2+H2O==2HNO3+NO
3 1
9mL 3mL
4NO2+O2+2H2O==4HNO3
例2.向盛有15mLNO气体,倒立于水槽的试管A中通入O2,充分反应后,试管中还剩余气体3mL,则通入的O2体积可能是多少?
气体剩余只能是NO或O2,不可能是NO2。
剩余气体3mL
①3mLNO
②3mLO2
4NO+3O2+2H2O==4HNO3
3
12mL 9mL
4NO+3O2+2H2O==4HNO3
3
15mL 11.25mL
例3.将V mL NO和NO2的混合气通过水吸收后,得得a mL无色气体A,将此无色气体A与等体积O2混合,再通过水充分吸收后,收集到5 mL无色气体B。试回答:
(1)A气体是_____,B气体是_____;(2)A气体的体积是____。
【解析】 (1)NO2溶于水生成NO,故A为NO,NO与O2通入水中发生反应4NO+3O2+2H2O=4HNO3,二者等体积时,O2过量,故B为O2;
(2)4NO + 3O2+2H2O=4HNO3
a mL 3a/4mL 依题意:a-3a/4=5,a=20
NO O2 20 mL
提炼归纳
氮的氧化物溶于水的计算
1.反应原理
3NO2+H2O=2HNO3+NO ①
2NO+O2=2NO2 ②
反应①×2+② 4NO2+O2+2H2O=4HNO3 ③
反应①×2+②×3 4NO+3O2+2H2O=4HNO3 ④
2.计算类型
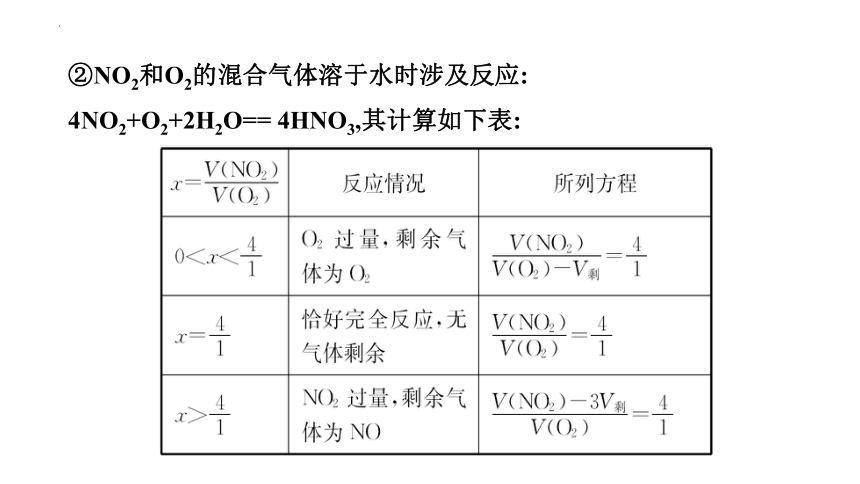
②NO2和O2的混合气体溶于水时涉及反应:
4NO2+O2+2H2O== 4HNO3,其计算如下表:
③NO和O2的混合气体溶于水时涉及反应:
4NO+3O2+2H2O===4HNO3,其计算如下表:
1. 如图所示的试管中装有12 mL NO,然后间歇缓慢地通入8 mLO2。有关最终状态的描述:①试管内气体呈红棕色,②试管内气体呈无色,③试管内液面不变,④试管内液面上升,⑤试管内气体是O2,⑥试管内气体是NO 。其中正确的是( )
C
A. ①③ B. ②④⑤
C. ②④⑥ D. ②③⑤
学习评价
2. 同温同压下,在3支相同体积的试管中分别充有等体积混合的两种气体,它们是①NO和NO2,②NO2和O2,③NO和N2。现将3支试管均倒置于水槽中,充分反应后,试管中剩余气体的体积分别为V1、V2、V3,则下列关系正确的是( )
D
A.V1>V2>V3 B.V1>V3>V2
C.V2>V3>V1 D.V3>V1>V2
学习评价
3. 在容积为672 mL的烧瓶中充满NO和NO2的混合气体,将其倒立在水槽里,去塞后再通入280 mL氧气,恰好完全反应,且液体充满烧瓶(气体体积都已折合为标准状况下的体积),下列有关叙述正确的是( )
B
A. 总反应为NO+NO2+O2+H2O === 2HNO3
B. 总反应为4NO+8NO2+5O2+6H2O === 12HNO3
C. 生成硝酸的物质的量浓度均为0.030 mol·L-1
D. 生成硝酸的物质的量浓度约为0.060 mol·L-1
学习评价
试管中气体(标况)倒立在水槽中探究
类别 气体 上升高度 C(B)(mol/L)
Ⅰ ①一满试管HCl
②试管中HCl、 空气各一半
Ⅱ ③一满试管NO2
Ⅲ ④一满试管NO2、 O2(4:1)混合气体
充满
1/2
2/3
1/22.4
1/22.4
1/22.4
4
5
×
1
22.4
充满
V(aq)
CB=
nB
V
=
V/22.4
= mol/L
1
22.4
形成溶液的体积=所消耗的气体体积
计算的关键:
拓展延伸
学习评价
4.在一定条件下,将m体积NO与n体积O2先后通入倒立在水中且盛满水的容器中,充分反应后,容器内残留体积的气体,该气体与空气接触后变为红棕色,则m与n的比值为______
5.将20mL充满NO和NO2的混合气体的试管倒立于盛水的水槽中,充分反应后,剩余气体10mL,求原混合气体中NO和NO2的体积。
解:设混合气体气体中V(NO2) = x , V(NO) = y
解得:x=15,y=5
x + y = 20
(1/3)x + y = 10
3NO2 + H2O == 2HNO3 + NO
答:混合气体气体中NO为5mL,NO2为15mL
x
(1/3)x
学习评价
第二节 氮及其化合物
第二课时 氮的氧化物溶于水的计算
第五章 化工生产中的重要非金属元素
[思考1]写出NO2气体溶于水的反应,分析产生的NO与通入的NO2的体积关系。
[思考2]若把NO2与O2的混合气体通入水中会发生什么反应?
剩余气体是什么?
[思考3]若把NO与O2的混合气体通入水中会发生什么反应?剩余气体是什么?
怎样才能使试管中充满液体?
3NO2+H2O=2HNO3+NO
2NO+O2=2NO2
4NO2+O2+2H2O=4HNO3
4NO+3O2+2H2O=4HNO3
例1.向盛有15mLNO2气体,倒立于水槽的试管A中通入O2,充分反应后,试管中还剩余气体3mL,则通入的O2体积可能是多少?
气体剩余只能是NO或O2,不可能是NO2。
剩余气体3mL
①NO2过量→3mLNO
②3mLO2
1
6mL 1.5mL
1
15mL 3.75mL
4NO2+O2+2H2O==4HNO3
3NO2+H2O==2HNO3+NO
3 1
9mL 3mL
4NO2+O2+2H2O==4HNO3
例2.向盛有15mLNO气体,倒立于水槽的试管A中通入O2,充分反应后,试管中还剩余气体3mL,则通入的O2体积可能是多少?
气体剩余只能是NO或O2,不可能是NO2。
剩余气体3mL
①3mLNO
②3mLO2
4NO+3O2+2H2O==4HNO3
3
12mL 9mL
4NO+3O2+2H2O==4HNO3
3
15mL 11.25mL
例3.将V mL NO和NO2的混合气通过水吸收后,得得a mL无色气体A,将此无色气体A与等体积O2混合,再通过水充分吸收后,收集到5 mL无色气体B。试回答:
(1)A气体是_____,B气体是_____;(2)A气体的体积是____。
【解析】 (1)NO2溶于水生成NO,故A为NO,NO与O2通入水中发生反应4NO+3O2+2H2O=4HNO3,二者等体积时,O2过量,故B为O2;
(2)4NO + 3O2+2H2O=4HNO3
a mL 3a/4mL 依题意:a-3a/4=5,a=20
NO O2 20 mL
提炼归纳
氮的氧化物溶于水的计算
1.反应原理
3NO2+H2O=2HNO3+NO ①
2NO+O2=2NO2 ②
反应①×2+② 4NO2+O2+2H2O=4HNO3 ③
反应①×2+②×3 4NO+3O2+2H2O=4HNO3 ④
2.计算类型
②NO2和O2的混合气体溶于水时涉及反应:
4NO2+O2+2H2O== 4HNO3,其计算如下表:
③NO和O2的混合气体溶于水时涉及反应:
4NO+3O2+2H2O===4HNO3,其计算如下表:
1. 如图所示的试管中装有12 mL NO,然后间歇缓慢地通入8 mLO2。有关最终状态的描述:①试管内气体呈红棕色,②试管内气体呈无色,③试管内液面不变,④试管内液面上升,⑤试管内气体是O2,⑥试管内气体是NO 。其中正确的是( )
C
A. ①③ B. ②④⑤
C. ②④⑥ D. ②③⑤
学习评价
2. 同温同压下,在3支相同体积的试管中分别充有等体积混合的两种气体,它们是①NO和NO2,②NO2和O2,③NO和N2。现将3支试管均倒置于水槽中,充分反应后,试管中剩余气体的体积分别为V1、V2、V3,则下列关系正确的是( )
D
A.V1>V2>V3 B.V1>V3>V2
C.V2>V3>V1 D.V3>V1>V2
学习评价
3. 在容积为672 mL的烧瓶中充满NO和NO2的混合气体,将其倒立在水槽里,去塞后再通入280 mL氧气,恰好完全反应,且液体充满烧瓶(气体体积都已折合为标准状况下的体积),下列有关叙述正确的是( )
B
A. 总反应为NO+NO2+O2+H2O === 2HNO3
B. 总反应为4NO+8NO2+5O2+6H2O === 12HNO3
C. 生成硝酸的物质的量浓度均为0.030 mol·L-1
D. 生成硝酸的物质的量浓度约为0.060 mol·L-1
学习评价
试管中气体(标况)倒立在水槽中探究
类别 气体 上升高度 C(B)(mol/L)
Ⅰ ①一满试管HCl
②试管中HCl、 空气各一半
Ⅱ ③一满试管NO2
Ⅲ ④一满试管NO2、 O2(4:1)混合气体
充满
1/2
2/3
1/22.4
1/22.4
1/22.4
4
5
×
1
22.4
充满
V(aq)
CB=
nB
V
=
V/22.4
= mol/L
1
22.4
形成溶液的体积=所消耗的气体体积
计算的关键:
拓展延伸
学习评价
4.在一定条件下,将m体积NO与n体积O2先后通入倒立在水中且盛满水的容器中,充分反应后,容器内残留体积的气体,该气体与空气接触后变为红棕色,则m与n的比值为______
5.将20mL充满NO和NO2的混合气体的试管倒立于盛水的水槽中,充分反应后,剩余气体10mL,求原混合气体中NO和NO2的体积。
解:设混合气体气体中V(NO2) = x , V(NO) = y
解得:x=15,y=5
x + y = 20
(1/3)x + y = 10
3NO2 + H2O == 2HNO3 + NO
答:混合气体气体中NO为5mL,NO2为15mL
x
(1/3)x
学习评价
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
