2022-2023学年高一化学 苏教版2019 必修第二册 教学课件 6-3-2 化学电源(共25张PPT)
文档属性
| 名称 | 2022-2023学年高一化学 苏教版2019 必修第二册 教学课件 6-3-2 化学电源(共25张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 7.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-21 00:00:00 | ||
图片预览






文档简介
(共25张PPT)
1.3.2 化学电源
学习目标
1. 知道常见的化学电源的种类。
2.掌握简单原电池的电极反应。
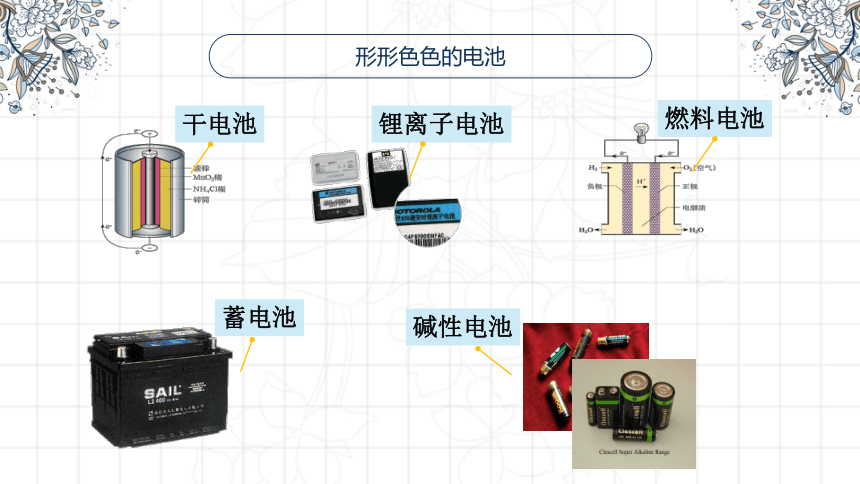
形形色色的电池
干电池
蓄电池
锂离子电池
燃料电池
碱性电池
简易电池无法长久稳定地使用,于是人们发明并制造了多种多样的能够较长时间稳定持续供电的化学电源。化学电源的能量转化率比燃料燃烧高得多。
化学
电池
一次性电池:干电池
二次电池(充电电池):铅蓄电池
燃料电池:氢氧燃料电池
常见一次电池
锌锰干电池
1、结构:锌筒为 极,石墨棒为 极,在石墨棒周围填充糊状的MnO2和NH4Cl作 。
负
正
电解质
2、原理
总反应为: Zn+2MnO2+2NH4Cl==Zn(NH3)2Cl2 + 2MnO(OH)
负极:Zn-2e- + 2NH4+ = [Zn(NH3)2]2+ + 2H+
正极:2MnO2 + 2H+ + 2e - =2MnO(OH)
缺陷
锌锰干电池电量小,而且在放电过程中容易发生气胀或漏液,会导致电器设备的腐蚀。
改进
①在外壳套上防腐金属筒或塑料筒制成防漏电池;
②将电池内的电解质NH4Cl换成湿的KOH,并在构造上进行改进,
制成碱性锌锰电池。
二次电池
1、结构:银锌电池是一种纽扣式大容量电池,Zn作 极,Ag2O作 极,电解质溶液为KOH溶液。
(1)银锌纽扣电池
2、原理:
总反应为:Zn +Ag2O + H2O 2Ag + Zn(OH)2
负
正
银锌扣电池
负极:Zn-2e-+ 2OH-==Zn(OH)2
正极:Ag2O + H2O +2e-==2Ag + 2OH-
二次电池
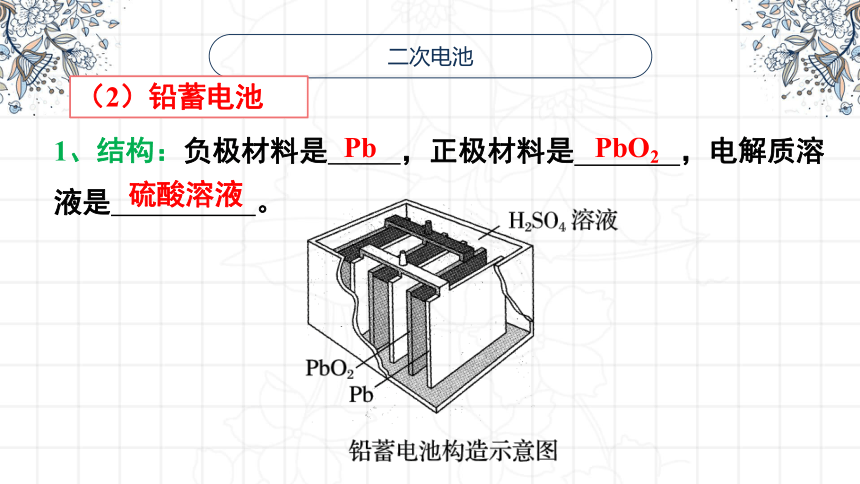
1、结构:负极材料是 ,正极材料是 ,电解质溶液是 。
(2)铅蓄电池
Pb
PbO2
硫酸溶液
二次电池
负极: Pb- 2e-+ SO4 2 - =PbSO4
正极: PbO2+4H++SO42- + 2e- = PbSO4 +2H2O
2、原理:
放电:
总反应:
充电:
PbSO4 =Pb+ SO42-
PbSO4 +2H2O = PbO2 + 4H++ SO42-
阴极: 与外接电源负极相连
阳极: 与外接电源正极相连
+2e-
-2e-
二次电池
(3)镍氢电池
放电过程
负极:
正极:
MH-e- +OH-=M+H2O
MH
NiO(OH)
KOH溶液
电解质:
NiO(OH)+e- =NiO+OH-
总反应: NiO(OH)+MH NiO +M+H2O
燃料电池
工作原理:燃料燃烧
氢氧燃料电池结构
2H2 + O2 == 2H2O
4e-
反应原理:
⑴氢氧燃料电池
电极: Pt或石墨制作的惰性电极
电解质溶液: 硫酸溶液
负极: 2H2 - 4e- = 4H+
正极: O2+ 4H++ 4e- = 2H2O
总反应:2H2 + O2 = 2H2O
思考2:电池工作一段时间后,上述溶液的pH如何变化?
酸性减弱,pH变大。
燃料电池
1.如果电解质溶液换成氢氧化钾呢?
负极:2H2+4OH--4e-===4H2O
正极:O2+2H2O+4e-===4OH-
氢氧燃料电池
以KOH(aq)为电解质溶液 以稀硫酸为电解质溶液
总反应 2H2+O2===2H2O
正极 O2+2H2O+4e-=4OH-
负极 2H2+4OH--4e-=4H2O
2H2+O2===2H2O
2H2-4e-===4H+
O2+4H++4e-===2H2O
甲醇燃料电池
(2)甲醇燃料电池
总反应:2CH3OH+3O2+4OH_===2CO32-+6H2O
碱性:
负极:CH3OH - 6e- + 8OH- =CO32- + 6H2O
正极:O2 + 4e-+ 2H20 = 4OH-
3.简易燃料电池的制备
原理:
构成了氢氧燃料电池,先电解水生成了H2和O2,
H2在负极,
电极反应:2H2-4e-===4H+,
O2在正极,
电极反应:O2+2H2O+4e-===4OH-
电解池
三、电解池
将电能转化为化学能的装置
利用电解我们可以获得普通化学方法难以制备的物质
应用:
二次电池的充电,冶炼活泼金属钠、镁、铝等
应用:
电解水制得氢气和氧气;电解饱和食盐水制备烧碱、氯气和氢气。
电解
电解池
资料卡片
电解在物质制备中的应用
可以将电解运用于制备钠、镁、铝、钙等活泼金属单质。
例如电解熔融的氧化铝得到单质铝。
学以致用
1.锌锰碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌锰碱性电池以KOH溶液为电解液,电池反应为Zn+2MnO2+H2O== Zn(OH)2+Mn2O3。下列有关说法错误的是( )
A.电池工作时,锌失去电子被氧化
B.电池工作时,电解液中的OH-向锌极移动
C.电池工作时,电子由正极通过外电路流向负极
D.当外电路中每通过0.2 mol电子时,锌的质量理论上减小6.5 g
C
学以致用
2.锂海水电池常用在海上浮标等助航设备中,其示意图如图所示。电池反应为2Li+2H2O==2LiOH+H2↑。电池工作时,下列说法错误的是( )
A.金属锂作负极
B.电子从锂电极经导线流向镍电极
C.海水作为电解质溶液
D.可将电能转化为化学能
D
学以致用
3.(2021·广东卷,9)火星大气中含有大量CO2,一种有CO2参加反应的新型全固态电池有望为火星探测器供电。该电池以金属钠为负极,碳纳米管为正极,放电时( )
A.负极上发生还原反应
B.CO2在正极上得电子
C.阳离子由正极移向负极
D.将电能转化为化学能
B
学以致用
4.如图是氢氧燃料电池构造示意图。下列说法不正确的是( )
A.a极是正极
B.电子由b通过溶液流向a
C.该电池总反应是2H2+O2 2H2O
D.氢氧燃料电池是环保电池
AB
学以致用
5.下列描述中,不符合生产实际的是( )
A.电解熔融的氯化铝制取金属铝
B.电解熔融的氯化钠制取金属钠,阴极反应式为Na++e- Na
C.电解饱和食盐水制烧碱
D.电解熔融的氯化镁制取金属镁
A
作业布置
1.写《课时作业》P114~115页
观
看
谢
谢
1.3.2 化学电源
学习目标
1. 知道常见的化学电源的种类。
2.掌握简单原电池的电极反应。
形形色色的电池
干电池
蓄电池
锂离子电池
燃料电池
碱性电池
简易电池无法长久稳定地使用,于是人们发明并制造了多种多样的能够较长时间稳定持续供电的化学电源。化学电源的能量转化率比燃料燃烧高得多。
化学
电池
一次性电池:干电池
二次电池(充电电池):铅蓄电池
燃料电池:氢氧燃料电池
常见一次电池
锌锰干电池
1、结构:锌筒为 极,石墨棒为 极,在石墨棒周围填充糊状的MnO2和NH4Cl作 。
负
正
电解质
2、原理
总反应为: Zn+2MnO2+2NH4Cl==Zn(NH3)2Cl2 + 2MnO(OH)
负极:Zn-2e- + 2NH4+ = [Zn(NH3)2]2+ + 2H+
正极:2MnO2 + 2H+ + 2e - =2MnO(OH)
缺陷
锌锰干电池电量小,而且在放电过程中容易发生气胀或漏液,会导致电器设备的腐蚀。
改进
①在外壳套上防腐金属筒或塑料筒制成防漏电池;
②将电池内的电解质NH4Cl换成湿的KOH,并在构造上进行改进,
制成碱性锌锰电池。
二次电池
1、结构:银锌电池是一种纽扣式大容量电池,Zn作 极,Ag2O作 极,电解质溶液为KOH溶液。
(1)银锌纽扣电池
2、原理:
总反应为:Zn +Ag2O + H2O 2Ag + Zn(OH)2
负
正
银锌扣电池
负极:Zn-2e-+ 2OH-==Zn(OH)2
正极:Ag2O + H2O +2e-==2Ag + 2OH-
二次电池
1、结构:负极材料是 ,正极材料是 ,电解质溶液是 。
(2)铅蓄电池
Pb
PbO2
硫酸溶液
二次电池
负极: Pb- 2e-+ SO4 2 - =PbSO4
正极: PbO2+4H++SO42- + 2e- = PbSO4 +2H2O
2、原理:
放电:
总反应:
充电:
PbSO4 =Pb+ SO42-
PbSO4 +2H2O = PbO2 + 4H++ SO42-
阴极: 与外接电源负极相连
阳极: 与外接电源正极相连
+2e-
-2e-
二次电池
(3)镍氢电池
放电过程
负极:
正极:
MH-e- +OH-=M+H2O
MH
NiO(OH)
KOH溶液
电解质:
NiO(OH)+e- =NiO+OH-
总反应: NiO(OH)+MH NiO +M+H2O
燃料电池
工作原理:燃料燃烧
氢氧燃料电池结构
2H2 + O2 == 2H2O
4e-
反应原理:
⑴氢氧燃料电池
电极: Pt或石墨制作的惰性电极
电解质溶液: 硫酸溶液
负极: 2H2 - 4e- = 4H+
正极: O2+ 4H++ 4e- = 2H2O
总反应:2H2 + O2 = 2H2O
思考2:电池工作一段时间后,上述溶液的pH如何变化?
酸性减弱,pH变大。
燃料电池
1.如果电解质溶液换成氢氧化钾呢?
负极:2H2+4OH--4e-===4H2O
正极:O2+2H2O+4e-===4OH-
氢氧燃料电池
以KOH(aq)为电解质溶液 以稀硫酸为电解质溶液
总反应 2H2+O2===2H2O
正极 O2+2H2O+4e-=4OH-
负极 2H2+4OH--4e-=4H2O
2H2+O2===2H2O
2H2-4e-===4H+
O2+4H++4e-===2H2O
甲醇燃料电池
(2)甲醇燃料电池
总反应:2CH3OH+3O2+4OH_===2CO32-+6H2O
碱性:
负极:CH3OH - 6e- + 8OH- =CO32- + 6H2O
正极:O2 + 4e-+ 2H20 = 4OH-
3.简易燃料电池的制备
原理:
构成了氢氧燃料电池,先电解水生成了H2和O2,
H2在负极,
电极反应:2H2-4e-===4H+,
O2在正极,
电极反应:O2+2H2O+4e-===4OH-
电解池
三、电解池
将电能转化为化学能的装置
利用电解我们可以获得普通化学方法难以制备的物质
应用:
二次电池的充电,冶炼活泼金属钠、镁、铝等
应用:
电解水制得氢气和氧气;电解饱和食盐水制备烧碱、氯气和氢气。
电解
电解池
资料卡片
电解在物质制备中的应用
可以将电解运用于制备钠、镁、铝、钙等活泼金属单质。
例如电解熔融的氧化铝得到单质铝。
学以致用
1.锌锰碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌锰碱性电池以KOH溶液为电解液,电池反应为Zn+2MnO2+H2O== Zn(OH)2+Mn2O3。下列有关说法错误的是( )
A.电池工作时,锌失去电子被氧化
B.电池工作时,电解液中的OH-向锌极移动
C.电池工作时,电子由正极通过外电路流向负极
D.当外电路中每通过0.2 mol电子时,锌的质量理论上减小6.5 g
C
学以致用
2.锂海水电池常用在海上浮标等助航设备中,其示意图如图所示。电池反应为2Li+2H2O==2LiOH+H2↑。电池工作时,下列说法错误的是( )
A.金属锂作负极
B.电子从锂电极经导线流向镍电极
C.海水作为电解质溶液
D.可将电能转化为化学能
D
学以致用
3.(2021·广东卷,9)火星大气中含有大量CO2,一种有CO2参加反应的新型全固态电池有望为火星探测器供电。该电池以金属钠为负极,碳纳米管为正极,放电时( )
A.负极上发生还原反应
B.CO2在正极上得电子
C.阳离子由正极移向负极
D.将电能转化为化学能
B
学以致用
4.如图是氢氧燃料电池构造示意图。下列说法不正确的是( )
A.a极是正极
B.电子由b通过溶液流向a
C.该电池总反应是2H2+O2 2H2O
D.氢氧燃料电池是环保电池
AB
学以致用
5.下列描述中,不符合生产实际的是( )
A.电解熔融的氯化铝制取金属铝
B.电解熔融的氯化钠制取金属钠,阴极反应式为Na++e- Na
C.电解饱和食盐水制烧碱
D.电解熔融的氯化镁制取金属镁
A
作业布置
1.写《课时作业》P114~115页
观
看
谢
谢
