8.1.2 石油炼制 乙烯 课件(共36张PPT含视频) 2022-2023学年高一化学 苏教版(2019)必修第二册
文档属性
| 名称 | 8.1.2 石油炼制 乙烯 课件(共36张PPT含视频) 2022-2023学年高一化学 苏教版(2019)必修第二册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 22.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-21 00:00:00 | ||
图片预览









文档简介
(共36张PPT)
8.1.2 石油炼制 乙烯
学习目标
1.了解石油的炼制。
2.掌握乙烯的结构与性质
3.认识加成反应
一、石油炼制
1.石油的组成
石油是一种重要的化石燃料,其组成元素主要是 ,同时还含有少量的 等元素。石油中含多种液态烃,并溶有少量的气态和固态烃。
碳和氢
硫、氧、氮
石油是一种黑褐色的粘稠状物质,有特殊气味,比水轻,不溶于水,没有固定沸点。
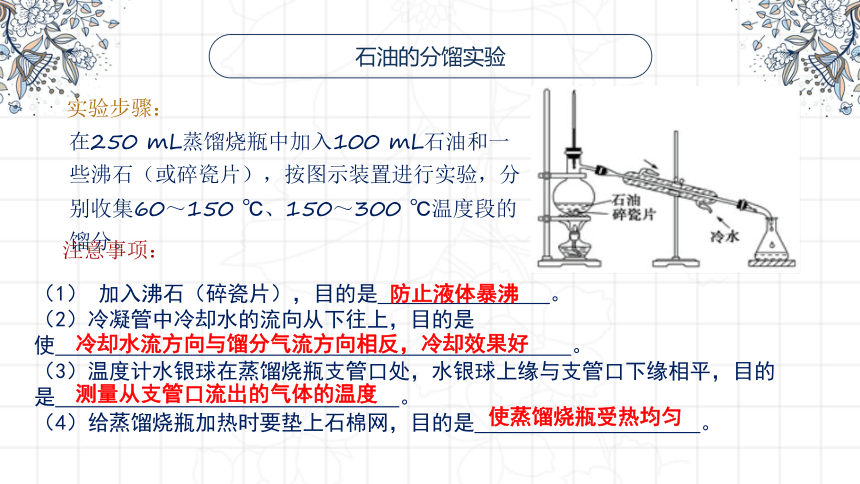
石油的分馏实验
实验步骤:
注意事项:
在250 mL蒸馏烧瓶中加入100 mL石油和一些沸石(或碎瓷片),按图示装置进行实验,分别收集60~150 ℃、150~300 ℃温度段的馏分。
(1) 加入沸石(碎瓷片),目的是 。
(2)冷凝管中冷却水的流向从下往上,目的是使 。
(3)温度计水银球在蒸馏烧瓶支管口处,水银球上缘与支管口下缘相平,目的是 。
(4)给蒸馏烧瓶加热时要垫上石棉网,目的是 。
防止液体暴沸
冷却水流方向与馏分气流方向相反,冷却效果好
测量从支管口流出的气体的温度
使蒸馏烧瓶受热均匀
一、石油炼制
2.石油的应用
分馏 ①原理:利用原油中各组分 的不同进行分离
②产物:获得汽油、煤油、柴油等含碳原子少的轻质油(直馏汽油)
裂化 ①原理:将含碳原子数较多、沸点较高的烃 为碳原子数较少、 沸点较低的烃的过程。
如C16H34 C8H18+C8H16
②产物: 。
裂解 ①原理:裂解就是 ,得到碳原子数更小的烃类。
C8H18 C4H10+C4H8
C4H10 CH4+C3H6
C4H10 C2H6+C2H4
②产物: 。
沸点
断裂
碳原子数较少、沸点较低的烃
深度裂化
短链不饱和烃,如乙烯
二、乙烯的性质
颜色 气味 状态 溶解度 密度
稍有气味
无色
气体
难溶于水
比空气略小
用排水法收集乙烯
(一)物理性质
二、乙烯的性质
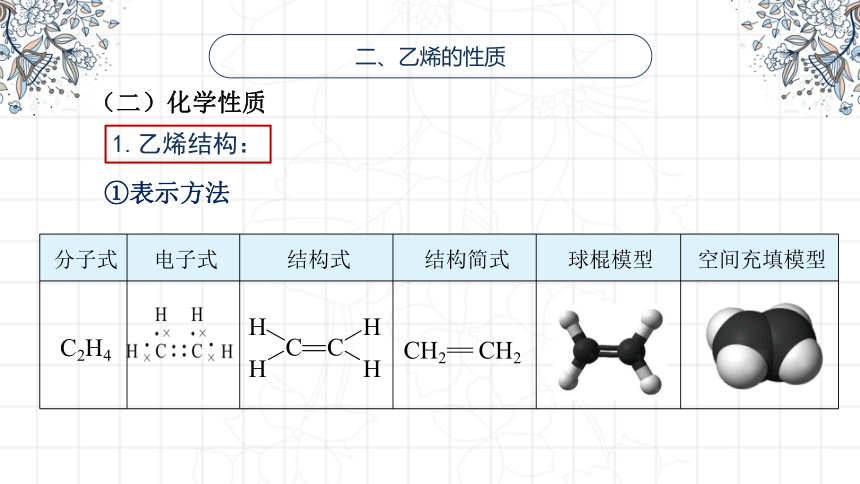
1.乙烯结构:
(二)化学性质
分子式 电子式 结构式 结构简式 球棍模型 空间充填模型
C2H4
CH2== CH2
①表示方法
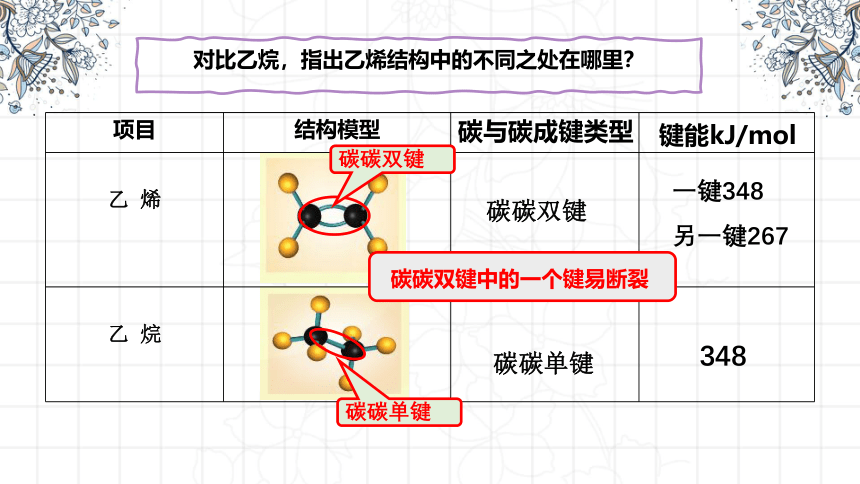
项目 结构模型
乙 烯
乙 烷
碳碳单键
碳碳双键
碳碳双键
碳与碳成键类型
碳碳单键
键能kJ/mol
一键348
另一键267
348
碳碳双键中的一个键易断裂
对比乙烷,指出乙烯结构中的不同之处在哪里?
二、乙烯的性质
1.乙烯结构:
(二)化学性质
②结构特点
a.乙烯为 结构,2个碳原子和4个氢原子 。
平面
共面
b.乙烯分子中的碳碳双键中两个碳碳键不完全相同,其中 ,发生化学反应时易断裂,因此乙烯的化学性质 。
一个键不稳定
较活泼
二、乙烯的性质
2.氧化反应:
(二)化学性质
①在氧气中燃烧
现象:
在空气中燃烧,火焰明亮且伴有黑烟
反应方程式:
二、乙烯的性质
2.氧化反应:
(二)化学性质
②与酸性高锰酸钾溶液反应
现象:
酸性高锰酸钾溶液褪色
反应方程式:
5C2H4+ 12KMnO4 + 18H2SO4= 12MnSO4+10CO2+28H2O+6K2SO4
应用:
鉴别乙烯(与烷烃比)
思考
能不能用酸性高锰酸钾除去乙烷中的乙烯?
不能,乙烯被酸性高锰酸钾氧化成CO2,引入了新的杂质
二、乙烯的性质
3.加成反应:
(二)化学性质
将乙烯通入溴的四氯化碳溶液
现象:
乙烯使溴的四氯化碳溶液褪色
反应方程式:
二、乙烯的性质
3.加成反应:
(二)化学性质
有机物分子中双键(或三键)连接的碳原子与其他原子或原子团直接结合生成新化合物的反应叫加成反应。
CH2 == CH2 + Br2 CH2BrCH2Br
加成反应机理
我是
溴分子
加成反应机理
加成反应机理
加成反应机理
二、乙烯的性质
乙烯不仅可以与溴发生加成反应,在一定条件下,还可以与氯气、氢气、氯化氢和水等物质发生加成反应。
CH2=CH2 + H—OH
CH3CH2OH(乙醇)
催化剂
CH2=CH2 + H—H
CH3CH3 (乙烷)
催化剂
CH2=CH2 + H—Cl
CH3CH2Cl (氯乙烷)
催化剂
工业上制取酒精的原理
取代反应与加成反应的比较
CH2=CH2 + H—Cl
CH3CH2Cl (氯乙烷)
催化剂
CH3CH3 + Cl2
CH3CH2Cl (氯乙烷)+HCI
光照
加成反应
取代反应
类型 取代反应 加成反应
反应物的结构特征 含有易被取代的原子或原子团,如烷烃中的氢原子
生成物种类
化学键变化情况
通常为含碳碳双键(或三键)的有机化合物
两种
一种
双键变单键,三键变双键(或者单键)
无单键、双键、三键之间的变化
思考探究
思考1
制取氯乙烷应用乙烯和HCl的加成反应还是用乙烷与Cl2的取代反应?
制取氯乙烷应用乙烯和HCl的加成反应而不能用乙烷与Cl2的取代反应。因为乙烯与HCl的加成产物只有一种,而乙烷与Cl2的取代产物是多种氯代烃的混合物。
思考探究
思考2
结合今天学习的乙烯的性质,如何区分甲烷和乙烯?
(1)鉴别甲烷和乙烯的方法:
①通入溴水中,褪色的为乙烯;
②通入酸性KMnO4溶液中,褪色的为乙烯;
③点燃时,火焰明亮并伴有黑烟的为乙烯。
(2)除去甲烷中混有的乙烯的方法:
使用溴水或溴的四氯化碳溶液,不能使用酸性KMnO4溶液。
二、乙烯的性质
4.加聚反应:
相对分子质量小的化合物相互加成聚合成相对分子质量大的聚合物
单体:聚合成高分子化合物的小分子化合物,如CH2=CH2;
链节:高分子化合物中的最小重复单元,如 — CH2 — CH2 —;
聚合度:高分子化合物中的链节数,如聚乙烯中的n。
三、乙烯的用途
1.植物生长调节剂,催熟剂等
2.乙烯是基本的化工原料;
合成乙醇、乙醛、合成塑料等……
乙烯的产量可以用来衡量一个国家的石油化工的发展水平。
课堂小结
课堂练习
1.如图是石油分馏塔的示意图。下列说法正确的是 ( )
A.a、b、c中a的沸点最高
B.a、b、c中b的熔点最低
C.a、b、c中c的平均相对分子质量最大
D.每一种馏分都是纯净物
C
石油分馏时,沸点低的馏分先汽化,冷凝后流出,沸点高的馏分后汽化,冷凝后流出。
石油中有些成分的沸点很接近,因此馏出的馏分仍为混合物。
课堂练习
2.请回答实验室石油分馏的有关问题。
(1)如图是实验室石油分馏的装置图,试指出有关仪器的名称:A ;B 。
(2)图中有 处错误。
(3)实验室石油分馏的正确操作顺序是E→ →
→A→ → →G。
A.连接接液管
B.装入碎瓷片和石油,塞上带温度计的塞子
C.检查装置气密性
D.连接冷凝管及进出水管
E.在铁架台上放酒精灯,固定好铁圈,放上石棉网
F.固定好蒸馏烧瓶
G.加热
蒸馏烧瓶
冷凝管
3
F
C
D
B
课堂练习
3.下列说法不正确的是( )
A.石油的裂化、裂解都是从长链烃变成短链烃
B.裂化的目的是获得轻质液体燃料,裂解的目的是获得乙烯、丙烯等小分子烃
C.石油经过分馏及裂化等工序炼制后即能得到纯净物
D.裂化、裂解是化学变化
C
课堂练习
4.下列说法正确的是( )
A.乙烯分子的电子式为
B.乙烯分子的球棍模型为
C.乙烯分子是平面结构
D.乙烯分子的结构简式为CH2CH2
C
课堂练习
2.下列关于乙烯用途、性质、结构的叙述正确的是( )
①乙烯通入水中即可转化为乙醇 ②乙烯可作香蕉等水果的催熟剂
③乙烯容易与溴水发生反应,1 mol乙烯发生加成反应消耗1 mol溴单质,
说明一个乙烯分子中含有一个碳碳双键
④乙烯能够被酸性KMnO4溶液所氧化,说明乙烯结构中含有一个碳碳双键
⑤乙烯分子中所有原子在同一个平面上
A.①②④ B.②④⑤
C.②③⑤ D.①④⑤
C
课堂练习
AC
作业布置
1.预习乙炔
2.写课时作业P125~127页 合格考题组及等级考题组
第13、14题
观
看
谢
谢
8.1.2 石油炼制 乙烯
学习目标
1.了解石油的炼制。
2.掌握乙烯的结构与性质
3.认识加成反应
一、石油炼制
1.石油的组成
石油是一种重要的化石燃料,其组成元素主要是 ,同时还含有少量的 等元素。石油中含多种液态烃,并溶有少量的气态和固态烃。
碳和氢
硫、氧、氮
石油是一种黑褐色的粘稠状物质,有特殊气味,比水轻,不溶于水,没有固定沸点。
石油的分馏实验
实验步骤:
注意事项:
在250 mL蒸馏烧瓶中加入100 mL石油和一些沸石(或碎瓷片),按图示装置进行实验,分别收集60~150 ℃、150~300 ℃温度段的馏分。
(1) 加入沸石(碎瓷片),目的是 。
(2)冷凝管中冷却水的流向从下往上,目的是使 。
(3)温度计水银球在蒸馏烧瓶支管口处,水银球上缘与支管口下缘相平,目的是 。
(4)给蒸馏烧瓶加热时要垫上石棉网,目的是 。
防止液体暴沸
冷却水流方向与馏分气流方向相反,冷却效果好
测量从支管口流出的气体的温度
使蒸馏烧瓶受热均匀
一、石油炼制
2.石油的应用
分馏 ①原理:利用原油中各组分 的不同进行分离
②产物:获得汽油、煤油、柴油等含碳原子少的轻质油(直馏汽油)
裂化 ①原理:将含碳原子数较多、沸点较高的烃 为碳原子数较少、 沸点较低的烃的过程。
如C16H34 C8H18+C8H16
②产物: 。
裂解 ①原理:裂解就是 ,得到碳原子数更小的烃类。
C8H18 C4H10+C4H8
C4H10 CH4+C3H6
C4H10 C2H6+C2H4
②产物: 。
沸点
断裂
碳原子数较少、沸点较低的烃
深度裂化
短链不饱和烃,如乙烯
二、乙烯的性质
颜色 气味 状态 溶解度 密度
稍有气味
无色
气体
难溶于水
比空气略小
用排水法收集乙烯
(一)物理性质
二、乙烯的性质
1.乙烯结构:
(二)化学性质
分子式 电子式 结构式 结构简式 球棍模型 空间充填模型
C2H4
CH2== CH2
①表示方法
项目 结构模型
乙 烯
乙 烷
碳碳单键
碳碳双键
碳碳双键
碳与碳成键类型
碳碳单键
键能kJ/mol
一键348
另一键267
348
碳碳双键中的一个键易断裂
对比乙烷,指出乙烯结构中的不同之处在哪里?
二、乙烯的性质
1.乙烯结构:
(二)化学性质
②结构特点
a.乙烯为 结构,2个碳原子和4个氢原子 。
平面
共面
b.乙烯分子中的碳碳双键中两个碳碳键不完全相同,其中 ,发生化学反应时易断裂,因此乙烯的化学性质 。
一个键不稳定
较活泼
二、乙烯的性质
2.氧化反应:
(二)化学性质
①在氧气中燃烧
现象:
在空气中燃烧,火焰明亮且伴有黑烟
反应方程式:
二、乙烯的性质
2.氧化反应:
(二)化学性质
②与酸性高锰酸钾溶液反应
现象:
酸性高锰酸钾溶液褪色
反应方程式:
5C2H4+ 12KMnO4 + 18H2SO4= 12MnSO4+10CO2+28H2O+6K2SO4
应用:
鉴别乙烯(与烷烃比)
思考
能不能用酸性高锰酸钾除去乙烷中的乙烯?
不能,乙烯被酸性高锰酸钾氧化成CO2,引入了新的杂质
二、乙烯的性质
3.加成反应:
(二)化学性质
将乙烯通入溴的四氯化碳溶液
现象:
乙烯使溴的四氯化碳溶液褪色
反应方程式:
二、乙烯的性质
3.加成反应:
(二)化学性质
有机物分子中双键(或三键)连接的碳原子与其他原子或原子团直接结合生成新化合物的反应叫加成反应。
CH2 == CH2 + Br2 CH2BrCH2Br
加成反应机理
我是
溴分子
加成反应机理
加成反应机理
加成反应机理
二、乙烯的性质
乙烯不仅可以与溴发生加成反应,在一定条件下,还可以与氯气、氢气、氯化氢和水等物质发生加成反应。
CH2=CH2 + H—OH
CH3CH2OH(乙醇)
催化剂
CH2=CH2 + H—H
CH3CH3 (乙烷)
催化剂
CH2=CH2 + H—Cl
CH3CH2Cl (氯乙烷)
催化剂
工业上制取酒精的原理
取代反应与加成反应的比较
CH2=CH2 + H—Cl
CH3CH2Cl (氯乙烷)
催化剂
CH3CH3 + Cl2
CH3CH2Cl (氯乙烷)+HCI
光照
加成反应
取代反应
类型 取代反应 加成反应
反应物的结构特征 含有易被取代的原子或原子团,如烷烃中的氢原子
生成物种类
化学键变化情况
通常为含碳碳双键(或三键)的有机化合物
两种
一种
双键变单键,三键变双键(或者单键)
无单键、双键、三键之间的变化
思考探究
思考1
制取氯乙烷应用乙烯和HCl的加成反应还是用乙烷与Cl2的取代反应?
制取氯乙烷应用乙烯和HCl的加成反应而不能用乙烷与Cl2的取代反应。因为乙烯与HCl的加成产物只有一种,而乙烷与Cl2的取代产物是多种氯代烃的混合物。
思考探究
思考2
结合今天学习的乙烯的性质,如何区分甲烷和乙烯?
(1)鉴别甲烷和乙烯的方法:
①通入溴水中,褪色的为乙烯;
②通入酸性KMnO4溶液中,褪色的为乙烯;
③点燃时,火焰明亮并伴有黑烟的为乙烯。
(2)除去甲烷中混有的乙烯的方法:
使用溴水或溴的四氯化碳溶液,不能使用酸性KMnO4溶液。
二、乙烯的性质
4.加聚反应:
相对分子质量小的化合物相互加成聚合成相对分子质量大的聚合物
单体:聚合成高分子化合物的小分子化合物,如CH2=CH2;
链节:高分子化合物中的最小重复单元,如 — CH2 — CH2 —;
聚合度:高分子化合物中的链节数,如聚乙烯中的n。
三、乙烯的用途
1.植物生长调节剂,催熟剂等
2.乙烯是基本的化工原料;
合成乙醇、乙醛、合成塑料等……
乙烯的产量可以用来衡量一个国家的石油化工的发展水平。
课堂小结
课堂练习
1.如图是石油分馏塔的示意图。下列说法正确的是 ( )
A.a、b、c中a的沸点最高
B.a、b、c中b的熔点最低
C.a、b、c中c的平均相对分子质量最大
D.每一种馏分都是纯净物
C
石油分馏时,沸点低的馏分先汽化,冷凝后流出,沸点高的馏分后汽化,冷凝后流出。
石油中有些成分的沸点很接近,因此馏出的馏分仍为混合物。
课堂练习
2.请回答实验室石油分馏的有关问题。
(1)如图是实验室石油分馏的装置图,试指出有关仪器的名称:A ;B 。
(2)图中有 处错误。
(3)实验室石油分馏的正确操作顺序是E→ →
→A→ → →G。
A.连接接液管
B.装入碎瓷片和石油,塞上带温度计的塞子
C.检查装置气密性
D.连接冷凝管及进出水管
E.在铁架台上放酒精灯,固定好铁圈,放上石棉网
F.固定好蒸馏烧瓶
G.加热
蒸馏烧瓶
冷凝管
3
F
C
D
B
课堂练习
3.下列说法不正确的是( )
A.石油的裂化、裂解都是从长链烃变成短链烃
B.裂化的目的是获得轻质液体燃料,裂解的目的是获得乙烯、丙烯等小分子烃
C.石油经过分馏及裂化等工序炼制后即能得到纯净物
D.裂化、裂解是化学变化
C
课堂练习
4.下列说法正确的是( )
A.乙烯分子的电子式为
B.乙烯分子的球棍模型为
C.乙烯分子是平面结构
D.乙烯分子的结构简式为CH2CH2
C
课堂练习
2.下列关于乙烯用途、性质、结构的叙述正确的是( )
①乙烯通入水中即可转化为乙醇 ②乙烯可作香蕉等水果的催熟剂
③乙烯容易与溴水发生反应,1 mol乙烯发生加成反应消耗1 mol溴单质,
说明一个乙烯分子中含有一个碳碳双键
④乙烯能够被酸性KMnO4溶液所氧化,说明乙烯结构中含有一个碳碳双键
⑤乙烯分子中所有原子在同一个平面上
A.①②④ B.②④⑤
C.②③⑤ D.①④⑤
C
课堂练习
AC
作业布置
1.预习乙炔
2.写课时作业P125~127页 合格考题组及等级考题组
第13、14题
观
看
谢
谢
