2022-2023学年高一化学 苏教版2019 必修第二册 教学课件 8-2-4 糖类(共17张PPT)
文档属性
| 名称 | 2022-2023学年高一化学 苏教版2019 必修第二册 教学课件 8-2-4 糖类(共17张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 33.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-21 00:00:00 | ||
图片预览




文档简介
(共17张PPT)
8.2.4 糖类
学习目标
1.认识糖类的分类
2.认识葡萄糖的特征反应
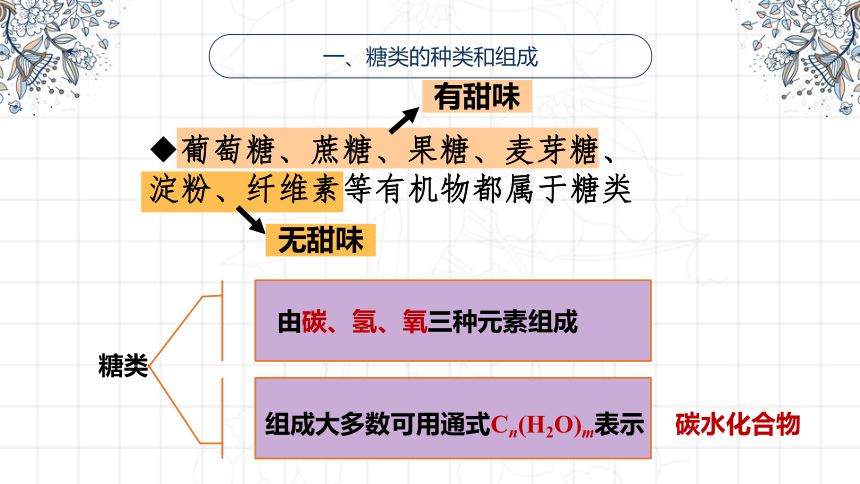
一、糖类的种类和组成
葡萄糖、蔗糖、果糖、麦芽糖、淀粉、纤维素等有机物都属于糖类
有甜味
无甜味
糖类
碳水化合物
组成大多数可用通式Cn(H2O)m表示
由碳、氢、氧三种元素组成
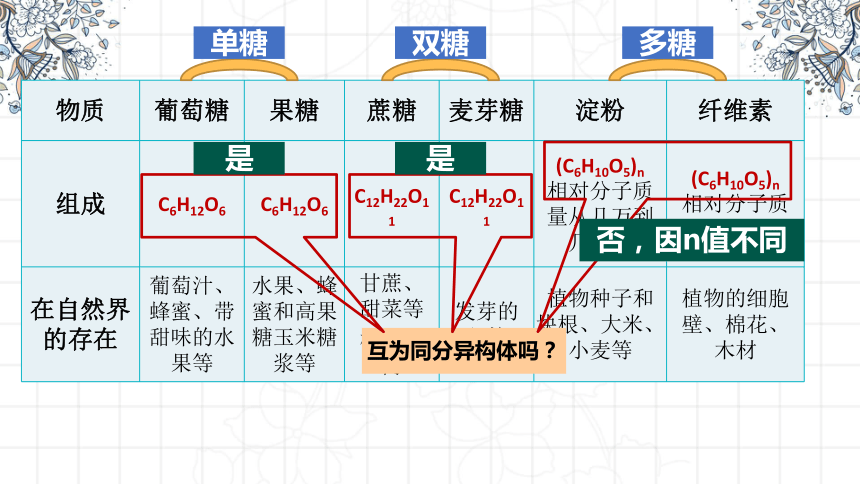
物质 葡萄糖 果糖 蔗糖 麦芽糖 淀粉 纤维素
组成 C6H12O6 C6H12O6 C12H22O11 C12H22O11 (C6H10O5)n
相对分子质量从几万到几十万 (C6H10O5)n
相对分子质量200万以上
在自然界的存在 葡萄汁、蜂蜜、带甜味的水果等 水果、蜂蜜和高果糖玉米糖浆等 甘蔗、甜菜等 植物体内 发芽的谷粒 植物种子和块根、大米、小麦等 植物的细胞壁、棉花、木材
互为同分异构体吗?
是
是
否,因n值不同
单糖
双糖
多糖
二、常见糖类的物理性质
葡萄糖 蔗糖 淀粉 纤维素
颜色、状态 无色晶体 白色晶体 白色粉末 白色固体
水溶性 能溶于水 极易溶于水 难溶于冷水,可溶于热水 不溶于水
三、常见糖类的化学性质
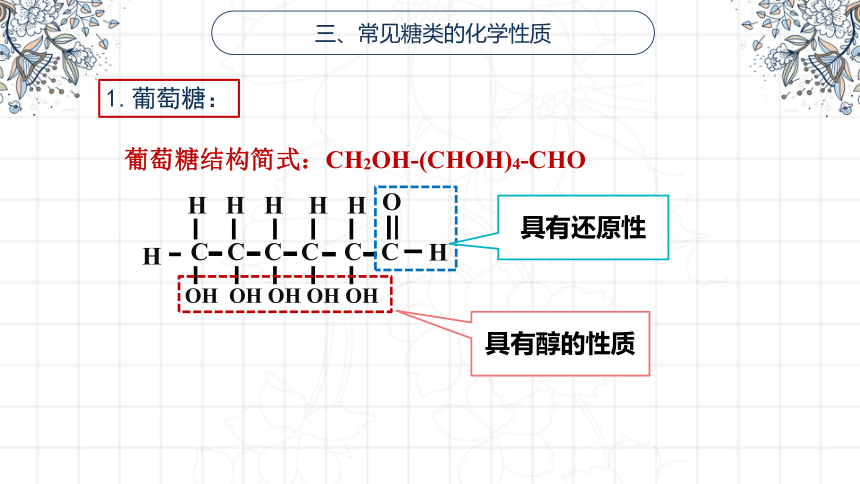
1.葡萄糖:
葡萄糖结构简式:CH2OH-(CHOH)4-CHO
C C C C C C
O
H
OH OH OH OH OH
H
H H H H H
具有醇的性质
具有还原性
三、常见糖类的化学性质
1.葡萄糖:
①氧化反应-呼吸作用
C6H12O6(s)+6O2(g)===6CO2(g)+6H2O(l) ΔH=-2 803 kJ·mol-1
应用:提供生命活动所需要的能量
②氧化反应-银镜反应(实验2)
向AgNO3溶液加入稀氨水,沉淀消失后再滴加1 mL 10%葡萄糖,水浴加热,在试管壁上生成银白色光亮的银镜。
实验现象
银镜反应实验
葡萄糖具有还原性,能被弱氧化剂如银氨溶液氧化,生成光亮的银镜
注意事项
实验结论
单质银
葡萄糖检验方法一
①银氨溶液的配制方法:将稀氨水逐滴加到稀AgNO3溶液中,边滴加边振荡,至析出的沉淀恰好溶解为止。
②实验成功的条件:水浴加热,碱性环境,试管要洁净,不能搅拌。
③清洗银镜的方法:先用稀HNO3溶解,再用清水冲洗。
三、常见糖类的化学性质
1.葡萄糖:
③氧化反应-和新制的Cu(OH)2反应(实验3)
实验现象
试管中有砖红色沉淀生成。
葡萄糖具有还原性,能被新制的Cu(OH)2碱性悬浊液氧化为砖红色的Cu2O沉淀。
实验结论
葡萄糖检验方法二
检验糖尿病
三、常见糖类的化学性质
2.淀粉:
①遇碘变蓝
②水解反应
用于检验淀粉
(C6H10O5)n+nH2O
淀粉
n C6H12O6
葡萄糖
稀硫酸
△
猜想
溶液呈蓝色
未产生银镜
未水解
部分水解
完全水解
溶液呈蓝色
产生银镜
溶液不变蓝
产生银镜
思考:淀粉水解程度如何检验?
滴加NaOH溶液目的是什么?
淀粉水解反应是用硫酸作催化剂,而与新制的Cu(OH)2碱性悬浊液反应的溶液必须呈碱性,所以应先中和再检验。
三、常见糖类的化学性质
2.淀粉:
③分解反应
应用1:富含淀粉的谷物酿酒
C6H12O6 2C2H5OH+2CO2↑
酒化酶
应用2:富含纤维素的植物秸秆制造工业酒精
淀粉、纤维素在一定条件下能水解成葡萄糖。
课堂练习
1.大米、小麦、玉米等谷类食物中所含的营养物质主要是( )
A.淀粉 B.油脂
C.纤维素 D.水
A
课堂练习
2.下列物质中属于糖类的是 (填序号)。
①蔗糖 ②乙醇 ③乙酸乙酯 ④纤维素 ⑤淀粉 ⑥乙酸
①④⑤
课堂练习
3.葡萄糖(C6H12O6)是一种重要的营养物质,下列关于葡萄糖的说法中正确的是( )
A.葡萄糖是一种单糖
B.葡萄糖分子中有6个碳原子、6个水分子
C.常温下,葡萄糖可与新制的氢氧化铜碱性悬浊液反应
D.1 mol葡萄糖完全燃烧需要9 mol氧气
A
课堂练习
5.鉴别乙酸与葡萄糖溶液,下列试剂不合理的是 ( )
A.氢氧化钠溶液
B.银氨溶液
C.乙醇
D.新制的Cu(OH)2碱性悬浊液
AC
观
看
谢
谢
8.2.4 糖类
学习目标
1.认识糖类的分类
2.认识葡萄糖的特征反应
一、糖类的种类和组成
葡萄糖、蔗糖、果糖、麦芽糖、淀粉、纤维素等有机物都属于糖类
有甜味
无甜味
糖类
碳水化合物
组成大多数可用通式Cn(H2O)m表示
由碳、氢、氧三种元素组成
物质 葡萄糖 果糖 蔗糖 麦芽糖 淀粉 纤维素
组成 C6H12O6 C6H12O6 C12H22O11 C12H22O11 (C6H10O5)n
相对分子质量从几万到几十万 (C6H10O5)n
相对分子质量200万以上
在自然界的存在 葡萄汁、蜂蜜、带甜味的水果等 水果、蜂蜜和高果糖玉米糖浆等 甘蔗、甜菜等 植物体内 发芽的谷粒 植物种子和块根、大米、小麦等 植物的细胞壁、棉花、木材
互为同分异构体吗?
是
是
否,因n值不同
单糖
双糖
多糖
二、常见糖类的物理性质
葡萄糖 蔗糖 淀粉 纤维素
颜色、状态 无色晶体 白色晶体 白色粉末 白色固体
水溶性 能溶于水 极易溶于水 难溶于冷水,可溶于热水 不溶于水
三、常见糖类的化学性质
1.葡萄糖:
葡萄糖结构简式:CH2OH-(CHOH)4-CHO
C C C C C C
O
H
OH OH OH OH OH
H
H H H H H
具有醇的性质
具有还原性
三、常见糖类的化学性质
1.葡萄糖:
①氧化反应-呼吸作用
C6H12O6(s)+6O2(g)===6CO2(g)+6H2O(l) ΔH=-2 803 kJ·mol-1
应用:提供生命活动所需要的能量
②氧化反应-银镜反应(实验2)
向AgNO3溶液加入稀氨水,沉淀消失后再滴加1 mL 10%葡萄糖,水浴加热,在试管壁上生成银白色光亮的银镜。
实验现象
银镜反应实验
葡萄糖具有还原性,能被弱氧化剂如银氨溶液氧化,生成光亮的银镜
注意事项
实验结论
单质银
葡萄糖检验方法一
①银氨溶液的配制方法:将稀氨水逐滴加到稀AgNO3溶液中,边滴加边振荡,至析出的沉淀恰好溶解为止。
②实验成功的条件:水浴加热,碱性环境,试管要洁净,不能搅拌。
③清洗银镜的方法:先用稀HNO3溶解,再用清水冲洗。
三、常见糖类的化学性质
1.葡萄糖:
③氧化反应-和新制的Cu(OH)2反应(实验3)
实验现象
试管中有砖红色沉淀生成。
葡萄糖具有还原性,能被新制的Cu(OH)2碱性悬浊液氧化为砖红色的Cu2O沉淀。
实验结论
葡萄糖检验方法二
检验糖尿病
三、常见糖类的化学性质
2.淀粉:
①遇碘变蓝
②水解反应
用于检验淀粉
(C6H10O5)n+nH2O
淀粉
n C6H12O6
葡萄糖
稀硫酸
△
猜想
溶液呈蓝色
未产生银镜
未水解
部分水解
完全水解
溶液呈蓝色
产生银镜
溶液不变蓝
产生银镜
思考:淀粉水解程度如何检验?
滴加NaOH溶液目的是什么?
淀粉水解反应是用硫酸作催化剂,而与新制的Cu(OH)2碱性悬浊液反应的溶液必须呈碱性,所以应先中和再检验。
三、常见糖类的化学性质
2.淀粉:
③分解反应
应用1:富含淀粉的谷物酿酒
C6H12O6 2C2H5OH+2CO2↑
酒化酶
应用2:富含纤维素的植物秸秆制造工业酒精
淀粉、纤维素在一定条件下能水解成葡萄糖。
课堂练习
1.大米、小麦、玉米等谷类食物中所含的营养物质主要是( )
A.淀粉 B.油脂
C.纤维素 D.水
A
课堂练习
2.下列物质中属于糖类的是 (填序号)。
①蔗糖 ②乙醇 ③乙酸乙酯 ④纤维素 ⑤淀粉 ⑥乙酸
①④⑤
课堂练习
3.葡萄糖(C6H12O6)是一种重要的营养物质,下列关于葡萄糖的说法中正确的是( )
A.葡萄糖是一种单糖
B.葡萄糖分子中有6个碳原子、6个水分子
C.常温下,葡萄糖可与新制的氢氧化铜碱性悬浊液反应
D.1 mol葡萄糖完全燃烧需要9 mol氧气
A
课堂练习
5.鉴别乙酸与葡萄糖溶液,下列试剂不合理的是 ( )
A.氢氧化钠溶液
B.银氨溶液
C.乙醇
D.新制的Cu(OH)2碱性悬浊液
AC
观
看
谢
谢
