人教版(2019)高中化学必修第二册 《7.1.2 烷烃》名师教学设计
文档属性
| 名称 | 人教版(2019)高中化学必修第二册 《7.1.2 烷烃》名师教学设计 |

|
|
| 格式 | docx | ||
| 文件大小 | 306.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-21 21:20:28 | ||
图片预览


文档简介
第七章 有机化合物
第一节 认识有机化合物
第二课时 《烷烃》教学设计
——基于“教、学、评”一体化思路学习“有机物中碳原子的成键特点”
教材分析
“烷烃”是《新课标》中必修课程主题4“简单的有机化合物及其应用”中二级标题“典型有机化合物的性质”的内容。本节课的内容是在学生通过碳原子的成键特点对有机物结构特别是甲烷的结构有了一定认识,并学习了烷烃、同系物和同分异构体的概念之后,进一步以甲烷为模型学习烷烃的物理、化学性质,其中,取代反应作为新的有机反应类型,是这节课的重点与难点。教材从生活中常见的烷烃:天然气、凡士林、石蜡等入手,让学生体会烷烃的物理性质,加强化学与生活的联系;再基于对甲烷的认识,引出烷烃的稳定性、可燃性等化学性质;最后重点介绍取代反应,通过比较甲烷与氯气的混合气体分别在黑暗和光照条件下的变化,让学生通过观察实验现象、讨论分析原因认识光照条件下甲烷与氯气发生取代反应。
本节课位于人教版新教材(2019年)必修第二册第七章“有机化合物”的第一节“认识有机化合物”。旧人教版在有机化合物这一章节中,先学习最简单的有机物——甲烷,通过学习甲烷的结构已经性质,对有机物有了初步认识之后,再引出烷烃、同系物、同分异构体的概念。与旧人教版相比,新人教版则是以“有机物种类繁多”为切入点,先着重介绍碳原子的成键特点,并通过资料卡片介绍实验模型研究物质结构的方法,让学生认识有机物的结构,接着先从结构角度,介绍了烷烃的概念,并引出“同系物”、“同分异构体”的概念,再介绍烷烃的性质,这样可以让学生建立研究有机物要从结构入手的观念,也深化了“结构决定性质”这一化学观念。
二、学情分析
学生在初中化学学习中,已经学习了甲烷的物理性质和甲烷能燃烧的化学性质,在学习这一章有机化合物之前,又较系统地学习了无机化合物,初步了解了学习元素化合物的一般方法,初步建立物质性质和用途间的关系,也对“结构决定性质”有了一定认识,为学习有机化合物奠定了一定基础。在上一节课中,学生认识了有机物,并通过碳原子的成键特点认识了基本有机物的结构,对烷烃的概念、元素组成以及结构也有了一定了解。但是对于有机物的性质还没有涉及,还不知道有机物特有的反应类型。
素养目标
【教学目标】
知道甲烷的物理性质和甲烷具有可燃性、稳定性和高温分解性,能建立性质与用途之间的联系
通过实验探究,从宏观上认识甲烷与氯气的取代反应;能从化学键角度,于微观层面认识取代反应的本质
能通过学习甲烷的性质为模型,认识烷烃的物理和化学性质。
【评价目标】
1.通过对甲烷的性质探讨,诊断并发展学生对常见有机物的认知模型的构建和符号表征的理解。
2.通过对甲烷在生活生产中应用的讨论,诊断并发展学生对化学学科价值的认识以及“性质决定用途”观念。
3.通过类比甲烷的性质,推出烷烃性质,诊断并发展学生分析推理能力和概念归纳运用能力。
四、教学重点、难点
1.教学重点:从宏观和微观角度知道甲烷和烷烃的物理、化学性质
2.教学难点:甲烷和氯气发生取代反应的实验探究和反应实质的微观探究
五、教学方法
1.情境探究,阅读素材,进行信息提取与分析
2.实验探究(取代反应概念的引出)
3.类比推理(以甲烷为模型推理出烷烃的性质)
六、教学设计思路
在上一节课,学生通过学习碳原子的成键特点认识了基本有机物的结构,并知道了烷烃的定义,本节课先以甲烷在自然界的存在为问题引入新课,设置学习情境,接着让学生通过阅读材料,提取并分析信息,得出甲烷的物理性质和具有可燃性、稳定性和高温分解性,其中甲烷的可燃性和稳定性是与它可以作为燃料息息相关,培养学生“性质决定用途”的化学观念。取代反应是有机物中的反应类型,学生在之前的学习中没有接触过,在本节课中,以探究甲烷与氯气反应为基础,引导学生观察现象并认识到氯气参与反应生成了氯化氢和难溶于水的混合物质,再从化学键的角度,让学生从微观层面认识到取代反应的本质,并可以将取代反应和无机化学中的复分解反应、置换反应做比较,旧知联系新知,帮助学生理解新概念。接着,以甲烷的性质为模型,类比推理出烷烃也具有类似的性质,培养学生分析推理能力。
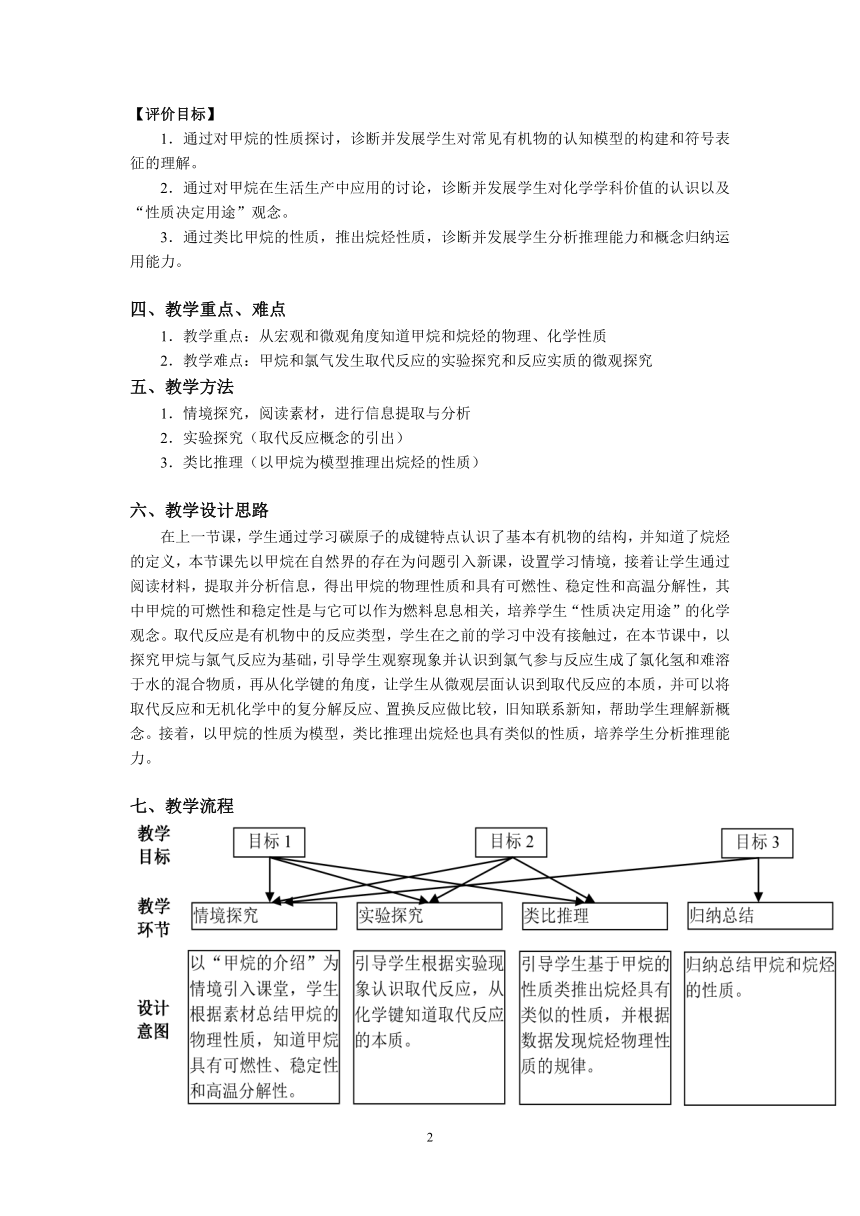
七、教学流程
八、教学过程
环节 教师活动 学生活动
环节一: 情境探究,认识甲烷基本性质 通过问题:同学们,你们知道甲烷在自然界主要存在于哪里吗?它有什么用处?从生活中常见的天然气和学生较陌生的物质可燃冰为引入,将学生带入甲烷的学习课堂,引发学生的兴趣。 思考,并回答自然界中甲烷的存在与用途。
【任务1】根据介绍甲烷的材料,总结出甲烷的性质,并说出甲烷的哪些性质令它可以作燃料? 思考1:家用天然气为什么要添加人工气味? 解析原因,强调甲烷是无色无味的气体。 思考2:实验室为什么用向下排空气法和排水法收集甲烷? 引导学生得出甲烷密度比空气小,难溶于水的结论。 阅读材料,通过思考问题,结合材料,提炼出甲烷的物理性质:无色无味的气体,密度比空气小,难溶于水。 并通过与实际生活中的现象和实验室收集气体的方法联系,加强物质的性质决定用途这一观念。
回顾上节课学习的内容, 带领学生复习甲烷的结构和并加强其用符号表征有机物的能力,详细介绍“球棍模型”和“空间充填模型”,加强学生对不同模型的特点和作用的理解。 写出甲烷的分子式、电子式、结构式、结构简式。 进一步认识甲烷的空间构型,并深入学习“球棍模型”和“空间充填模型”的特点。
从材料中“甲烷中的碳氢共价单键很稳定”,引出甲烷的化学性质也很稳定,展示甲烷通入酸性KMnO4溶液和溴水溶液的实验现象,带领学生得出结论,将抽象的稳定性转化为具体的与不同试剂的反应现象。 从化学键的性质认识甲烷的稳定性,并通过观察实验现象,得出甲烷不与酸性KMnO4溶液和溴水溶液反应的结论,将甲烷的稳定性具象化,与实际联系。
引导学生根据材料提示,写出甲烷在高温下分解的反应方程式,介绍甲烷高温分解产物炭黑在生产中的应用,加强化学与生活的联系。 通过材料提示,写出甲烷高温分解的反应方程式,加强根据反应物和部分生成物写出陌生反应的方程式的能力,取新知:甲烷的分解反应。
环节二: 实验探究,认识甲烷的取代反应 【任务2】根据甲烷和氯气反应的实验探究取代反应。 播放实验视频,引导学生观察实验现象并思考原因。 介绍实验用到的药品,并解释用途,引导学生从“固、液、气”的角度描述反应现象,并逐一解释出现该现象的原因。 观看实验视频,描述现象,并思考出现这些现象的原因。 在老师的引导下,从宏观角度认识甲烷和氯气发生反应的条件和现象。
先从化学键角度介绍甲烷与氯气发生的取代反应中断裂和新生成的化学键,再从物质的角度,分析反应生成了一氯甲烷和氯化氢。从甲烷中的氢原子被氯原子所取代,引出“取代反应”的概念。 根据反应后溶液呈酸性和生成难溶于水的混合物的提示,思考甲烷与氯气反应的实质。 初步认识甲烷的氯代反应,体会其过程的复杂性。能够运用结构式表达取代反应的过程。
进一步讲解甲烷与氯气反应的历程,引导学生认识甲烷中四个氢原子等效,都可以发生取代反应,并加强学生用结构式表示有机物反应的能力。 通过思考题:“取代反应的产物有哪些?那种产物最多?”,加强学生对取代反应产物的认识 以甲烷与氯气反应生成一氯甲烷为例,写出生成二氯甲烷、三氯甲烷、四氯化碳的反应方程式,进一步认识和体会取代反应的特点:连锁反应、产物复杂。 并通过思考题深刻认识甲烷与氯气反应的产物是4种有机物和1种无机物的混合物,并知道反应物和生成物的数量关系。
归纳甲烷的性质,强调学生较为陌生的高温分解反应和取代反应。 在老师的带领下,对甲烷的性质进行归纳,有一个总体的认识。
环节三: 根据甲烷的性质,类比推出烷烃的性质 【任务3】根据甲烷的性质,类比推理出烷烃的性质。 引导学生根据不同烷烃的熔沸点、密度的数据,得出烷烃的物理性质和其变化规律。 通过甲烷的物理性质的学习,以及烷烃的熔沸点、密度的书籍,类比推出烷烃有物理性质,学会分析数据,得出规律。
引导学生根据甲烷的化学性质,推理出烷烃的化学性质。 向学生介绍液化石油气的主要成分为丙烷,并根据甲烷、丙烷燃烧的反应方程式和烷烃的通式,引导学生对烷烃燃烧的反应通式进行配平。 联系生活,向学生介绍烷烃高温分解反应在生产中的应用。 根据甲烷的化学性质,推理烷烃的化学性质。 通过写出丙烷燃烧的反应方程式,归纳出烷烃燃烧的通式。 初步认识烷烃高温分解的产物,并与生活联系,体会化学在生活中的应用
重点解释烷烃的取代反应,以乙烷、丙烷和氯气反应生成一氯取代物为例,加强学生书写有机反应方程式的能力。通过分析丙烷和氯气反应生成一氯取代物有两种可能,令学生体会取代反应的产物复杂,复习、深入理解同分异构体的概念。 通过思考题:“1mol乙烷最多可与多少mol氯气反应?”,令学生理解取代反应中反应物的数量关系。 写出乙烷、丙烷和氯气反应生成一氯取代物的反应方程式。 通过丙烷和氯气的反应,复习“同分异构体”的概念,并通过实例,体会取代反应产物复杂的特点。 通过思考题,掌握取代反应中反应物的数量关系与有机物中可被取代的原子数量有关。
环节四: 总结归纳 通过甲烷的性质,对比并总结烷烃的物理、化学性质,特别强调不同之处:烷烃分解反应生成较短碳链的烷烃和烯烃;烷烃的取代反应产物更加复杂,会有同分异构体产生。 强调本节课学习的重点:取代反应。 在老师的引导下,总结归纳甲烷和烷烃的性质
板书设计
十、课堂测评
1.下列反应属于取代反应的是( )
A.CH4C+2H2 B.2HI+Cl22HCl+I2
C.CH4+2O2CO2+2H2O D.CH4+Cl2CH3Cl+HCl
2.室温下,下列关于甲烷与Cl2的取代反应所得产物的说法正确的是( )
A.都是有机物
B.都不溶于水
C.有一种气态物质,其余均是液体
D.除一种外,其余分子均是四面体结构
3.下列有关甲烷的取代反应的叙述正确的是( )
A.甲烷与氯气的物质的量之比为1∶1,混合发生取代反应只生成CH3Cl
B.甲烷与氯气的取代反应,生成的产物中CH3Cl最多
C.甲烷与氯气的取代反应生成的产物为混合物
D.1 mol甲烷生成CCl4最多消耗2 mol氯气
4.关于烷烃的叙述不正确的是( )
A.分子式符合CnH2n+2的烃一定是烷烃
B.烷烃均能与氯水发生取代反应
C.正戊烷的熔点、沸点比异戊烷的高
D.烷烃不能被酸性高锰酸钾溶液等强氧化剂氧化
5.常温下,1 mol某烷烃在光照条件下与氯气发生取代反应,若在适当的条件下,完全取代需要消耗6 mol Cl2,则下列判断正确的是( )
A.该烷烃的分子式为C5H12
B.反应所生成的有机产物能直接使AgNO3溶液褪色
C.该烷烃的四氯代物有2种
D.反应容器中,一氯代物所占的物质的量分数最大
题号 答案 1 (D) 2 (D) 3 (C) 4 (B) 5 (C)
质量 水平 L1 L2 L2 L3 L2 L2 L3 L1 L4 L2 L2 L1 L4 L2 L2 L3 L4 L3 L3 L2
SOLO M M R U U M M R E M M R M M R U E R R M
1
第一节 认识有机化合物
第二课时 《烷烃》教学设计
——基于“教、学、评”一体化思路学习“有机物中碳原子的成键特点”
教材分析
“烷烃”是《新课标》中必修课程主题4“简单的有机化合物及其应用”中二级标题“典型有机化合物的性质”的内容。本节课的内容是在学生通过碳原子的成键特点对有机物结构特别是甲烷的结构有了一定认识,并学习了烷烃、同系物和同分异构体的概念之后,进一步以甲烷为模型学习烷烃的物理、化学性质,其中,取代反应作为新的有机反应类型,是这节课的重点与难点。教材从生活中常见的烷烃:天然气、凡士林、石蜡等入手,让学生体会烷烃的物理性质,加强化学与生活的联系;再基于对甲烷的认识,引出烷烃的稳定性、可燃性等化学性质;最后重点介绍取代反应,通过比较甲烷与氯气的混合气体分别在黑暗和光照条件下的变化,让学生通过观察实验现象、讨论分析原因认识光照条件下甲烷与氯气发生取代反应。
本节课位于人教版新教材(2019年)必修第二册第七章“有机化合物”的第一节“认识有机化合物”。旧人教版在有机化合物这一章节中,先学习最简单的有机物——甲烷,通过学习甲烷的结构已经性质,对有机物有了初步认识之后,再引出烷烃、同系物、同分异构体的概念。与旧人教版相比,新人教版则是以“有机物种类繁多”为切入点,先着重介绍碳原子的成键特点,并通过资料卡片介绍实验模型研究物质结构的方法,让学生认识有机物的结构,接着先从结构角度,介绍了烷烃的概念,并引出“同系物”、“同分异构体”的概念,再介绍烷烃的性质,这样可以让学生建立研究有机物要从结构入手的观念,也深化了“结构决定性质”这一化学观念。
二、学情分析
学生在初中化学学习中,已经学习了甲烷的物理性质和甲烷能燃烧的化学性质,在学习这一章有机化合物之前,又较系统地学习了无机化合物,初步了解了学习元素化合物的一般方法,初步建立物质性质和用途间的关系,也对“结构决定性质”有了一定认识,为学习有机化合物奠定了一定基础。在上一节课中,学生认识了有机物,并通过碳原子的成键特点认识了基本有机物的结构,对烷烃的概念、元素组成以及结构也有了一定了解。但是对于有机物的性质还没有涉及,还不知道有机物特有的反应类型。
素养目标
【教学目标】
知道甲烷的物理性质和甲烷具有可燃性、稳定性和高温分解性,能建立性质与用途之间的联系
通过实验探究,从宏观上认识甲烷与氯气的取代反应;能从化学键角度,于微观层面认识取代反应的本质
能通过学习甲烷的性质为模型,认识烷烃的物理和化学性质。
【评价目标】
1.通过对甲烷的性质探讨,诊断并发展学生对常见有机物的认知模型的构建和符号表征的理解。
2.通过对甲烷在生活生产中应用的讨论,诊断并发展学生对化学学科价值的认识以及“性质决定用途”观念。
3.通过类比甲烷的性质,推出烷烃性质,诊断并发展学生分析推理能力和概念归纳运用能力。
四、教学重点、难点
1.教学重点:从宏观和微观角度知道甲烷和烷烃的物理、化学性质
2.教学难点:甲烷和氯气发生取代反应的实验探究和反应实质的微观探究
五、教学方法
1.情境探究,阅读素材,进行信息提取与分析
2.实验探究(取代反应概念的引出)
3.类比推理(以甲烷为模型推理出烷烃的性质)
六、教学设计思路
在上一节课,学生通过学习碳原子的成键特点认识了基本有机物的结构,并知道了烷烃的定义,本节课先以甲烷在自然界的存在为问题引入新课,设置学习情境,接着让学生通过阅读材料,提取并分析信息,得出甲烷的物理性质和具有可燃性、稳定性和高温分解性,其中甲烷的可燃性和稳定性是与它可以作为燃料息息相关,培养学生“性质决定用途”的化学观念。取代反应是有机物中的反应类型,学生在之前的学习中没有接触过,在本节课中,以探究甲烷与氯气反应为基础,引导学生观察现象并认识到氯气参与反应生成了氯化氢和难溶于水的混合物质,再从化学键的角度,让学生从微观层面认识到取代反应的本质,并可以将取代反应和无机化学中的复分解反应、置换反应做比较,旧知联系新知,帮助学生理解新概念。接着,以甲烷的性质为模型,类比推理出烷烃也具有类似的性质,培养学生分析推理能力。
七、教学流程
八、教学过程
环节 教师活动 学生活动
环节一: 情境探究,认识甲烷基本性质 通过问题:同学们,你们知道甲烷在自然界主要存在于哪里吗?它有什么用处?从生活中常见的天然气和学生较陌生的物质可燃冰为引入,将学生带入甲烷的学习课堂,引发学生的兴趣。 思考,并回答自然界中甲烷的存在与用途。
【任务1】根据介绍甲烷的材料,总结出甲烷的性质,并说出甲烷的哪些性质令它可以作燃料? 思考1:家用天然气为什么要添加人工气味? 解析原因,强调甲烷是无色无味的气体。 思考2:实验室为什么用向下排空气法和排水法收集甲烷? 引导学生得出甲烷密度比空气小,难溶于水的结论。 阅读材料,通过思考问题,结合材料,提炼出甲烷的物理性质:无色无味的气体,密度比空气小,难溶于水。 并通过与实际生活中的现象和实验室收集气体的方法联系,加强物质的性质决定用途这一观念。
回顾上节课学习的内容, 带领学生复习甲烷的结构和并加强其用符号表征有机物的能力,详细介绍“球棍模型”和“空间充填模型”,加强学生对不同模型的特点和作用的理解。 写出甲烷的分子式、电子式、结构式、结构简式。 进一步认识甲烷的空间构型,并深入学习“球棍模型”和“空间充填模型”的特点。
从材料中“甲烷中的碳氢共价单键很稳定”,引出甲烷的化学性质也很稳定,展示甲烷通入酸性KMnO4溶液和溴水溶液的实验现象,带领学生得出结论,将抽象的稳定性转化为具体的与不同试剂的反应现象。 从化学键的性质认识甲烷的稳定性,并通过观察实验现象,得出甲烷不与酸性KMnO4溶液和溴水溶液反应的结论,将甲烷的稳定性具象化,与实际联系。
引导学生根据材料提示,写出甲烷在高温下分解的反应方程式,介绍甲烷高温分解产物炭黑在生产中的应用,加强化学与生活的联系。 通过材料提示,写出甲烷高温分解的反应方程式,加强根据反应物和部分生成物写出陌生反应的方程式的能力,取新知:甲烷的分解反应。
环节二: 实验探究,认识甲烷的取代反应 【任务2】根据甲烷和氯气反应的实验探究取代反应。 播放实验视频,引导学生观察实验现象并思考原因。 介绍实验用到的药品,并解释用途,引导学生从“固、液、气”的角度描述反应现象,并逐一解释出现该现象的原因。 观看实验视频,描述现象,并思考出现这些现象的原因。 在老师的引导下,从宏观角度认识甲烷和氯气发生反应的条件和现象。
先从化学键角度介绍甲烷与氯气发生的取代反应中断裂和新生成的化学键,再从物质的角度,分析反应生成了一氯甲烷和氯化氢。从甲烷中的氢原子被氯原子所取代,引出“取代反应”的概念。 根据反应后溶液呈酸性和生成难溶于水的混合物的提示,思考甲烷与氯气反应的实质。 初步认识甲烷的氯代反应,体会其过程的复杂性。能够运用结构式表达取代反应的过程。
进一步讲解甲烷与氯气反应的历程,引导学生认识甲烷中四个氢原子等效,都可以发生取代反应,并加强学生用结构式表示有机物反应的能力。 通过思考题:“取代反应的产物有哪些?那种产物最多?”,加强学生对取代反应产物的认识 以甲烷与氯气反应生成一氯甲烷为例,写出生成二氯甲烷、三氯甲烷、四氯化碳的反应方程式,进一步认识和体会取代反应的特点:连锁反应、产物复杂。 并通过思考题深刻认识甲烷与氯气反应的产物是4种有机物和1种无机物的混合物,并知道反应物和生成物的数量关系。
归纳甲烷的性质,强调学生较为陌生的高温分解反应和取代反应。 在老师的带领下,对甲烷的性质进行归纳,有一个总体的认识。
环节三: 根据甲烷的性质,类比推出烷烃的性质 【任务3】根据甲烷的性质,类比推理出烷烃的性质。 引导学生根据不同烷烃的熔沸点、密度的数据,得出烷烃的物理性质和其变化规律。 通过甲烷的物理性质的学习,以及烷烃的熔沸点、密度的书籍,类比推出烷烃有物理性质,学会分析数据,得出规律。
引导学生根据甲烷的化学性质,推理出烷烃的化学性质。 向学生介绍液化石油气的主要成分为丙烷,并根据甲烷、丙烷燃烧的反应方程式和烷烃的通式,引导学生对烷烃燃烧的反应通式进行配平。 联系生活,向学生介绍烷烃高温分解反应在生产中的应用。 根据甲烷的化学性质,推理烷烃的化学性质。 通过写出丙烷燃烧的反应方程式,归纳出烷烃燃烧的通式。 初步认识烷烃高温分解的产物,并与生活联系,体会化学在生活中的应用
重点解释烷烃的取代反应,以乙烷、丙烷和氯气反应生成一氯取代物为例,加强学生书写有机反应方程式的能力。通过分析丙烷和氯气反应生成一氯取代物有两种可能,令学生体会取代反应的产物复杂,复习、深入理解同分异构体的概念。 通过思考题:“1mol乙烷最多可与多少mol氯气反应?”,令学生理解取代反应中反应物的数量关系。 写出乙烷、丙烷和氯气反应生成一氯取代物的反应方程式。 通过丙烷和氯气的反应,复习“同分异构体”的概念,并通过实例,体会取代反应产物复杂的特点。 通过思考题,掌握取代反应中反应物的数量关系与有机物中可被取代的原子数量有关。
环节四: 总结归纳 通过甲烷的性质,对比并总结烷烃的物理、化学性质,特别强调不同之处:烷烃分解反应生成较短碳链的烷烃和烯烃;烷烃的取代反应产物更加复杂,会有同分异构体产生。 强调本节课学习的重点:取代反应。 在老师的引导下,总结归纳甲烷和烷烃的性质
板书设计
十、课堂测评
1.下列反应属于取代反应的是( )
A.CH4C+2H2 B.2HI+Cl22HCl+I2
C.CH4+2O2CO2+2H2O D.CH4+Cl2CH3Cl+HCl
2.室温下,下列关于甲烷与Cl2的取代反应所得产物的说法正确的是( )
A.都是有机物
B.都不溶于水
C.有一种气态物质,其余均是液体
D.除一种外,其余分子均是四面体结构
3.下列有关甲烷的取代反应的叙述正确的是( )
A.甲烷与氯气的物质的量之比为1∶1,混合发生取代反应只生成CH3Cl
B.甲烷与氯气的取代反应,生成的产物中CH3Cl最多
C.甲烷与氯气的取代反应生成的产物为混合物
D.1 mol甲烷生成CCl4最多消耗2 mol氯气
4.关于烷烃的叙述不正确的是( )
A.分子式符合CnH2n+2的烃一定是烷烃
B.烷烃均能与氯水发生取代反应
C.正戊烷的熔点、沸点比异戊烷的高
D.烷烃不能被酸性高锰酸钾溶液等强氧化剂氧化
5.常温下,1 mol某烷烃在光照条件下与氯气发生取代反应,若在适当的条件下,完全取代需要消耗6 mol Cl2,则下列判断正确的是( )
A.该烷烃的分子式为C5H12
B.反应所生成的有机产物能直接使AgNO3溶液褪色
C.该烷烃的四氯代物有2种
D.反应容器中,一氯代物所占的物质的量分数最大
题号 答案 1 (D) 2 (D) 3 (C) 4 (B) 5 (C)
质量 水平 L1 L2 L2 L3 L2 L2 L3 L1 L4 L2 L2 L1 L4 L2 L2 L3 L4 L3 L3 L2
SOLO M M R U U M M R E M M R M M R U E R R M
1
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
