3.5 有机合成 周测(含解析) 高中化学人教版(2019)选择性必修3
文档属性
| 名称 | 3.5 有机合成 周测(含解析) 高中化学人教版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-23 00:00:00 | ||
图片预览



文档简介
有机合成周测
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列物质中含少量杂质(括号内为杂质),选用除杂试剂和方法均正确的是
A.:酸性溶液,洗气
B.己烷(己烯):溴水,分液
C.硝基苯:溶液,分液
D.:溶液,蒸馏
2.下列各组混合物能用分液漏斗分离的是
A.苯酚和苯 B.乙醛和水 C.乙酸乙酯和水 D.苯酚和水
3.下列有关有机物的说法正确的是
A.油脂在溶液中会稳定存在
B.丙酸和乙酸乙酯所含的官能团相同
C.苯和裂化汽油都可以作碘水中的萃取剂
D.与丙烷在光照下反应,液态产物为混合物
4.现有环状化合物结构如图。有关说法正确的是
A.a、b、c均可与钠反应
B.a、b、c互为同分异构体
C.a、b、c均可发生氧化反应和加成反应
D.等物质的量的a和b消耗NaOH的物质的量之比为2:1
5.有机物X的结构简式如图所示,下列有关X的说法不正确的是
A.X分子中所有原子不可能共面 B.1molX最多能与发生加成反应
C.X能使酸性高锰酸钾溶液褪色 D.X在空气中完全燃烧生成水和二氧化碳
6.紫草主要用于治疗烧伤、湿疹、丹毒等,其主要成分紫草素的结构简式如图,下列关于紫草素的说法正确的是
A.该物质能与NaOH反应,且1mol紫草素能消耗3molNaOH
B.紫草素的同分异构体中可能含有两个苯环
C.紫草素能使溴水、酸性KMnO4溶液褪色,且反应原理相同
D.紫草素与苯酚互为同系物
7.下列说法正确的是
A.棉花和蚕丝的主要成分都是纤维素
B.蛋白质在一定条件下发生水解反应生成葡萄糖
C.乙二醇的水溶液凝固点很低,可作汽车发动机的抗冻剂
D.氨基酸以两性离子的形态存在时,在水中溶解度最大
8.下列反应的方程式书写正确的是
A.用碳酸氢钠溶液检验水杨酸中的羧基:+2→ +2H2O+2CO2↑
B.1-溴丙烷与氢氧化钾的乙醇溶液共热:CH3CH2CH2Br+KOHCH3CH2CH2OH+KBr
C.用溴水检验丙烯醛中的碳碳双键:CH2=CHCHO+Br2CH2BrCHBrCHO
D.n +n+(2n-1)H2O
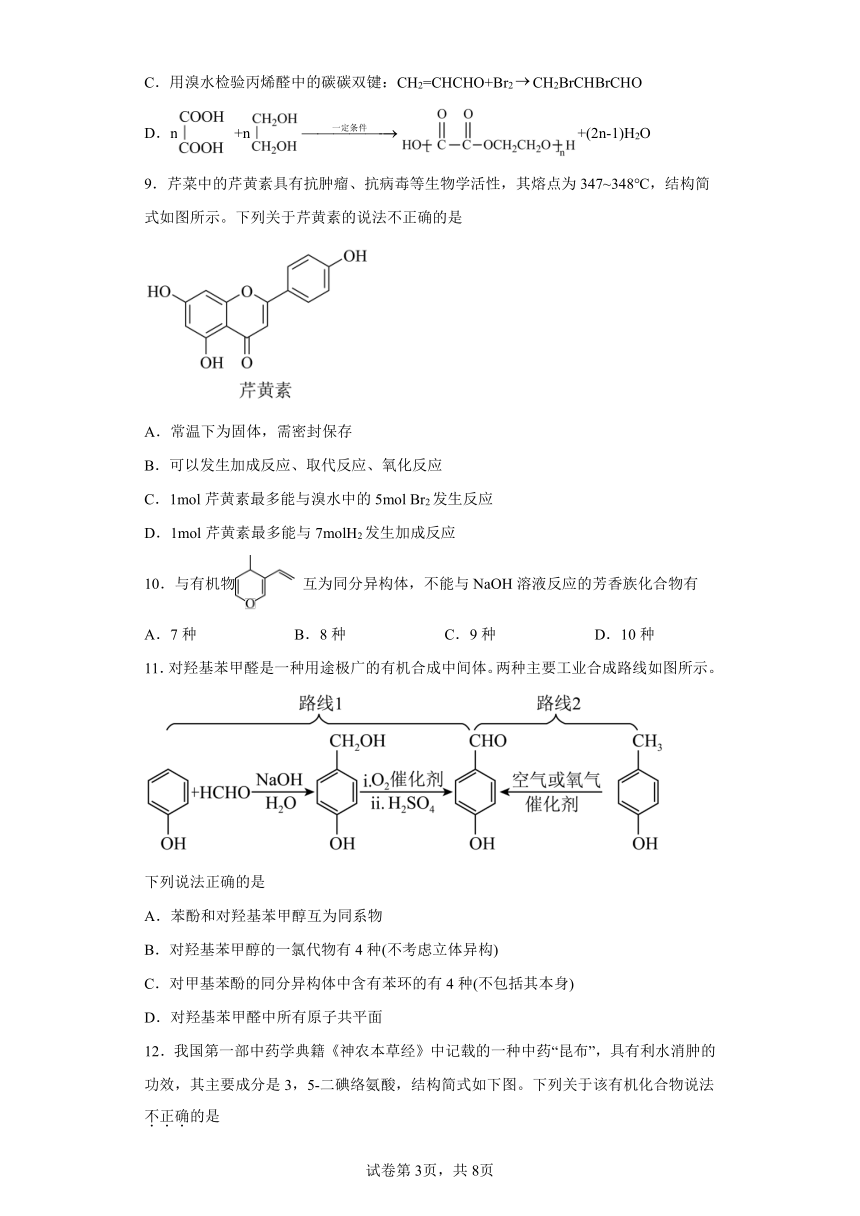
9.芹菜中的芹黄素具有抗肿瘤、抗病毒等生物学活性,其熔点为347~348℃,结构简式如图所示。下列关于芹黄素的说法不正确的是
A.常温下为固体,需密封保存
B.可以发生加成反应、取代反应、氧化反应
C.1mol芹黄素最多能与溴水中的5mol Br2发生反应
D.1mol芹黄素最多能与7molH2发生加成反应
10.与有机物 互为同分异构体,不能与NaOH溶液反应的芳香族化合物有
A.7种 B.8种 C.9种 D.10种
11.对羟基苯甲醛是一种用途极广的有机合成中间体。两种主要工业合成路线如图所示。
下列说法正确的是
A.苯酚和对羟基苯甲醇互为同系物
B.对羟基苯甲醇的一氯代物有4种(不考虑立体异构)
C.对甲基苯酚的同分异构体中含有苯环的有4种(不包括其本身)
D.对羟基苯甲醛中所有原子共平面
12.我国第一部中药学典籍《神农本草经》中记载的一种中药“昆布”,具有利水消肿的功效,其主要成分是3,5-二碘络氨酸,结构简式如下图。下列关于该有机化合物说法不正确的是
A.分子中含有手性碳原子
B.能与发生取代反应
C.既能与酸反应,也能与碱反应
D.理论上1mol该物质与足量反应可生成
二、填空题
13.按要求回答下列问题:
(1)的系统命名为______________;
(2)3—甲基—2一戊烯的结构简式为______________;
(3)的分子式为______________;
(4)某烃的分子式为C4H4,它是合成橡胶的中间体,它有多种同分异构体
①试写出它的一种链式结构的同分异构体的结构简式______________.
②它有一种同分异构体,每个碳原子均达饱和,且碳与碳的夹角相同,该分子中碳原子形成的空间构型为______________形
14.有机物A 的结构简式为,它可通过不同化学反应分别制得B、C、D和E四种物质。
请回答下列问题:
(1)在A~E五种物质中,互为同分异构体的是______(填字母代号)。
(2)写出由A生成B的化学方程式:________________。
(3)已知HCHO分子中所有原子在同一平面内,则上述分子中所有的原子有可能都在同一平面内的是______(填字母代号)。
(4)C能形成高聚物,该高聚物的结构简式为________。
三、实验题
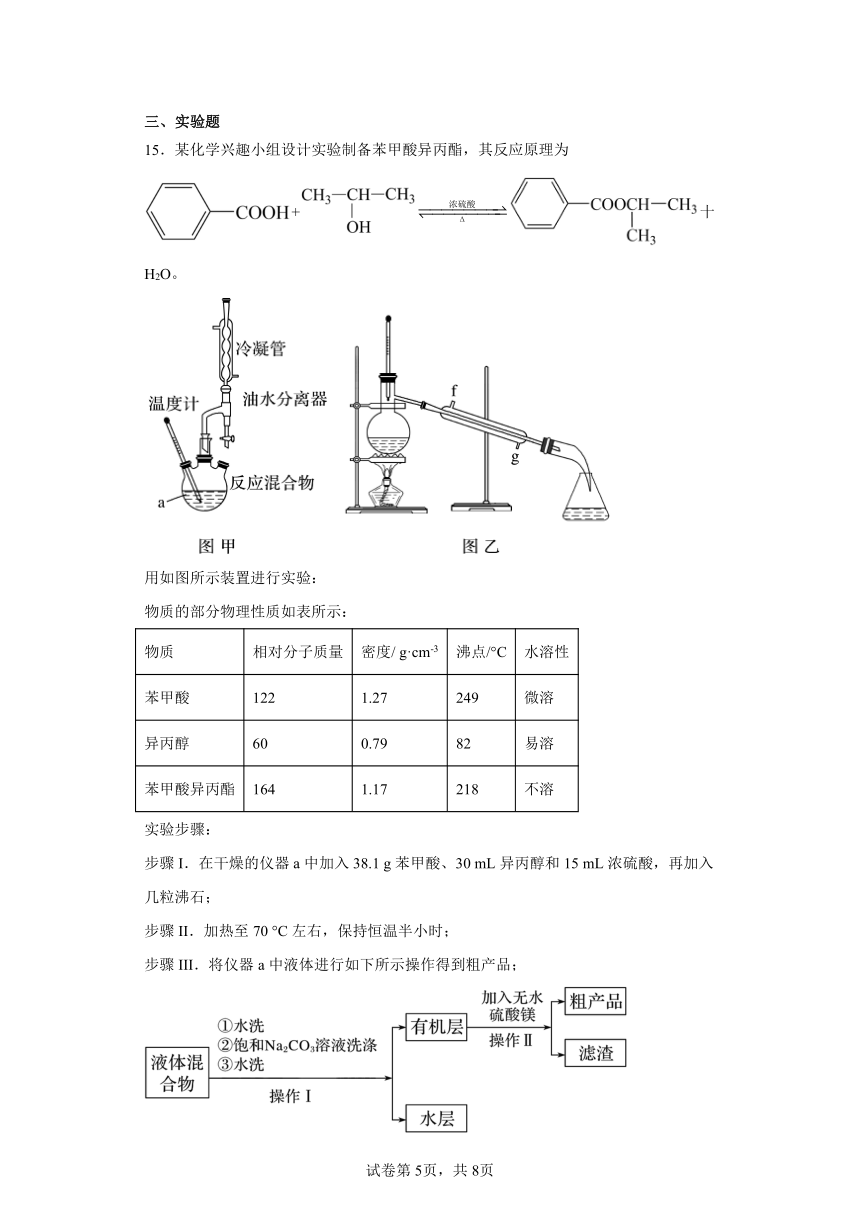
15.某化学兴趣小组设计实验制备苯甲酸异丙酯,其反应原理为
+十H2O。
用如图所示装置进行实验:
物质的部分物理性质如表所示:
物质 相对分子质量 密度/ g·cm-3 沸点/°C 水溶性
苯甲酸 122 1.27 249 微溶
异丙醇 60 0.79 82 易溶
苯甲酸异丙酯 164 1.17 218 不溶
实验步骤:
步骤I.在干燥的仪器a中加入38.1 g苯甲酸、30 mL异丙醇和15 mL浓硫酸,再加入几粒沸石;
步骤II.加热至70 °C左右,保持恒温半小时;
步骤III.将仪器a中液体进行如下所示操作得到粗产品;
步骤IV.将粗产品用图乙所示装置进行精制。
试回答下列问题:
(1)步骤I中加入三种试剂的先后顺序一定错误的是_ (填字母)。
A.异丙醇、苯甲酸、浓硫酸
B.异丙醇、浓硫酸、苯甲酸
C.浓硫酸、异丙醇、苯甲酸
(2)图乙中仪器b的名称为_。 加入的苯甲酸和异丙醇中,需过量的是异丙醇,目的是___________。
(3)本实验一般采用的加热方式为___________,因为温度过高会影响产率。
(4)操作I的分离方法名称为___________,其中第二次水洗的目的是___________,操作II中加入无水硫酸镁的作用为___________。
(5)如果得到的苯甲酸异丙酯的质量为38.360g,则该实验的产率为___________%(结果保留2位有效数字)。
16.Ⅰ、某班在实验室进行制取乙酸乙酯的分组实验,主要步骤如下:
①按右图连接好装置,并检查装置的气密性。
②在试管甲中加入3mL乙醇,然后边振荡试管边慢慢加入2mL浓硫酸和2mL乙酸,再加入沸石。然后用酒精灯缓慢加热。
③待试管乙(装有少量饱和碳酸钠溶液)中收集到一定量产物后停止加热,撤出试管B,振荡后静置。
已知:
相对分子质量 密度/(g.cm-3) 熔点/℃ 沸点/℃ 水中溶解性
乙醇 46 0.789 -117.3 78.5 以任意比互溶
乙酸 60 1.050 16.6 117.9 易溶
乙酸乙酯 88 0.897 -84 77 难溶
回答下列问题:
(1)试管甲中主要反应的化学方程式为___________。
(2)两组同学想要比较所制得的乙酸乙酯的产量,简便的方法是___________。
(3)该反应为可逆反应,要提高乙酸乙酯的产率,该实验中采取的措施有___________。
(4)现对全班同学试管乙中的液体集中处理,得到乙酸乙酯的粗产品并回收乙醇。假设全班共做10组实验,得到乙酸乙酯共20.4g,请计算乙酸乙酯的产率为___________(保留两位有效数字)。
Ⅱ、实验小组用下列装置进行实验。
(5)该实验的目的是___________,请写出总反应化学方程式___________。
(6)若想检验试管a中收集的液体成分含有乙醛,请分别写出两种检验方法的主要化学方程式:
①___________
②___________
17.乙酰水杨酸(阿司匹林)是一种白色晶体,在临床上被广泛用于发热、肌肉痛、神经痛、头痛、风湿热、急性风湿性关节炎等的治疗。乙酰水杨酸的合成原理和装置如下:
请回答下列问题:
(1)实验中水浴加热的优点_______,是直导管的作用是_______。
(2)根据阿司匹林的结构分析,其不可能发生的反应是_______。
A.加成反应 B.氧化反应 C.酯化反应 D.水解反应 E.银镜反应
(3)阿司匹林也可通过水杨酸和乙酸反应制取,写出该反应方程式:_______。
(4)乙酰水杨酸粗产品中常含有少量水杨酸杂质,该产品提纯方法与苯甲酸类似,采用_______法。提纯后,请设计实验方案验证水杨酸是否完全除去_______。
四、有机推断题
18.用石油产品A(C3H6)为主要原料,合成具有广泛用途的有机玻璃PMMA。流程如下(部分产物和条件省略)
试回答下列问题:
(1)B的名称________;X试剂为_______(化学式);D中官能团名称_________。
(2)E→G的化学方程式为________________________________________,反应类型是_________。
(3)T是G的同分异构体,1molT与足量新制Cu(OH)2悬浊液反应最多生成2molCu2O沉淀,T的结构有________种(不含立体结构)。
(4)若高分子化合物PMMA的相对分子质量为1.5×106,其聚合度为_______。
(5)参照上述流程,以为原料合成 (其它原料自选)。设计合成路线:________________________。
试卷第2页,共2页
试卷第1页,共1页
参考答案:
1.C
【详解】A.乙烯含有碳碳双键能和酸性高锰酸钾反应生成二氧化碳气体,引入新杂质气体,A错误;
B.己烯和溴加成的生成物和己烷互溶,不能分液分离,B错误;
C.氢氧化钠和二氧化氮反应生成盐溶液,盐溶液与硝基苯互不相溶,可以分液分离,C正确;
D.和氢氧化钠溶液加热会发生取代反应生成乙醇,D错误;
故选C。
2.C
【详解】A.苯酚易溶于苯,苯酚和苯形成溶液,不能用分液漏斗分离,故A不合题意;
B.乙醛和水相互溶解,不能用分液漏斗分离,故B符合题意;
C.乙酸乙酯和水不互溶,乙酸乙酯在上层,水在下层,能用分液漏斗分离,故C不合题意;
D.通常苯酚微溶于水,上层为溶有少量苯酚的水溶液,下层为溶有水的苯酚溶液,所以不能用分液漏斗彻底分离,故D不合题意;
故答案为C。
3.D
【详解】A. 油脂在等强碱溶液中会发生水解反应,即皂化反应,A项错误;
B. 丙酸含有羧基,乙酸乙酯含有酯基,二者的官能团不同,B项错误;
C. 裂化汽油含有不饱和烃,与发生加成反应,C项错误;
D. 丙烷与氯气在光照下发生取代反应,液态产物为多氯代物,如一氯丙烷、二氯丙烷、三氯丙烷等,故液态产物为混合物,D项正确。
答案选D。
4.B
【分析】a分子中含有酯基,b分子含有羧基,c中含有羟基,三种环状化合物的分子式均为C5H8O2,根据官能团的性质分析解答。
【详解】A.酯基不和钠发生反应,A错误;
B.三种环状化合物的分子式均为C5H8O2,结构不同,互为同分异构体,B正确;
C.a、b、c含有的官能团不能发生加成反应,C错误;
D.1mol a分子中含有1mol酯基,1mol b分子含有1mol羧基,等物质的量的a和b消耗NaOH的物质的量之比为1:1,D错误;
故选B。
5.B
【详解】A.分子中含有饱和碳原子,与饱和碳原子相连的四个原子一定不在同一平面上,A项正确;
B.分子中的苯环、碳碳双键能与氢气发生加成反应,所以最多能与发生加成反应,B项错误;
C.分子中的碳碳双键能使酸性高锰酸钾溶液褪色,C项正确;
D.X由C、H、O三种元素组成,在空气中完全燃烧时生成水和二氧化碳,D项正确;
答案选B。
6.B
【详解】A.紫草素中含有酚羟基能与反应,且紫草素含有2mol酚羟基能消耗,A错误;
B.紫草素有9个不饱和度,所以同分异构体中可能含有两个苯环,B正确;
C.紫草素能使溴水褪色是发生加成和取代反应、使酸性溶液褪色是发生氧化反应,反应原理不相同,C错误;
D.紫草素与苯酚不互为同系物,D错误。
故选B。
7.C
【详解】A.棉花的主要成分是纤维素,蚕丝的主要成分是蛋白质,选项A错误;
B.蛋白质在一定条件下发生水解最终生成氨基酸,选项B错误;
C.乙二醇的水溶液凝固点很低,可作内燃机的抗冻剂,选项C正确;
D.氨基酸处于等电状态时,主要是以.两性离子形式存在,此时它的溶解度最小,选项D错误;
答案选C。
8.D
【详解】A.酚羟基的酸性比碳酸弱,故酚羟基与碳酸氢根不反应,方程式为:,A错误;
B.1-溴丙烷在氢氧化钾的乙醇溶液中应该发生消去反应生成丙烯,B错误;
C.醛基也能跟溴水反应,故不能用溴水检验碳碳双键,C错误;
D.乙二酸和乙二醇的发生缩聚反应,脱去2n-1个水,D正确;
故选D。
9.D
【详解】A.熔点为347℃~348℃,则常温下为固体,含有酚羟基,易被氧化,应密封保存,故A正确;
B.由可知,苯环、羰基和碳碳双键可发生加成反应,苯环上可发生取代反应,含有酚羟基,易被氧化,可发生氧化反应,故B正确;
C.由可知,与溴水能发生取代反应的位置只能是酚羟基的邻对位,如,与溴水能发生加成反应的有碳碳双键,则1mol芹黄素最多能与溴水中的5mol Br2发生反应,故C正确;
D.由可知,苯环、羰基和碳碳双键均可与H2发生加成反应,有二个苯环,一个羰基,一个碳碳双键,则1mol芹黄素最多能与8molH2发生加成反应,故D错误;
答案为D。
10.D
【详解】从有机物的结构简式可知,其不饱和度为4,总共有8个碳原子,1个氧原子,则其分子式为C8H10O,其同分异构体是不能与NaOH溶液反应的芳香族化合物,则说明其同分异构体中含有一个苯环,且苯环上不能有酚羟基,则满足条件的同分异构体有、两种、 的邻、间、对三种,的邻、间、对三种,和两种,总共10种,故答案为D。
11.C
【详解】A.由题图知,苯酚的分子式为,对羟基苯甲醇的分子式为,同系物是指结构相似,分子组成上相差一个或若干个原子团,则二者不互为同系物,A错误;
B.采用等效氢法进行分析,对羟基苯甲醇中等效氢原子有5种(),氯原子取代C上的氢,则其一氯代物有3种,B错误;
C.利用口诀分析苯环上的取代情况,若苯环上有1个取代基,则取代基为或,有2种;若苯环上有2个取代基,取代基为和,除去本身,有“邻、间”2种,则共有4种,C正确;
D.对羟基苯甲醛中单键可以旋转,则该物质分子中所有原子不一定共平面,D错误;
故答案选C。
12.D
【详解】A.手性碳原子是指与四个各不相同原子或基团相连的碳原子,该有机物有1个手性碳原子,A正确;
B.该有机物含有C-H键,光照下能与Br2发生取代反应,B正确;
C.该有机物含有酚羟基、羧基和氨基,具有弱酸性和弱碱性,既能与酸反应,也能与碱反应,C正确;
D.该有机物有1个羧基,因此理论上1mol该物质与足量反应可生成,即44g CO2,D错误;
故答案为:D。
【点睛】判断一个碳原子是否是手性碳原子,首先要观察该碳原子是否有双键或三键连接,如果有则必然不属于手性碳原子,即不饱和碳一定不是手性碳。
13.(1)2,3二甲基丁烷
(2)
(3)C4H8O
(4) CH2CH-CCH 正四面体
【详解】(1)有机物主链有4个C原子,母体是丁烷,支链有2、3号为甲基取代基,名称为2,3-二甲基丁烷;
(2)按照烯烃的命名,3—甲基—2一戊烯的主链有5个碳原子,2、3号碳之间有碳碳双键,3号碳上有取代基甲基,此有机物的结构简式为;
(3)键线式中交点、拐点、端点都是碳原子,有机物中碳原子有4个化学键,因此有机物的分子式为C4H8O;
(4)①4个碳原子的饱和链烃分子式为C4H10,与C4H4对比,C4H4比饱和链烃少了6个H,即C4H4中有3个碳碳双键或1个碳碳双键和1个叁键,有机物中碳原子不能同时连有2个碳碳双键,即结构简式为CH2CH-CCH ;
②每个碳原子均达饱和,且碳与碳的夹角相同,空间构型为正四面体。
14. C和E C
【详解】(1)A发生催化氧化生成B,A发生消去反应生成C,A与甲酸发生酯化反应生成D,为取代反应,A发生分子内酯化反应生成E,也属于取代反应,C、E均比A少H2O,四种物质中只有C、E的分子式相同,但结构不同,则C与E互为同分异构体;
故答案为:C和E;
(2)A发生催化氧化生成B,由A生成B的化学方程式为;
故答案为:;
(3)已知HCHO分子中所有原子在同一平面内,表明羰基是平面结构。ABDE中均含有亚甲基,是空间四面体结构,只有C中含有苯环和碳碳双键,都是平面结构,分子中所有的原子有可能都在同一平面内;
故答案为:C;
(4)C中含有C=C官能团,可发生加聚反应,该高聚物的结构简式为,反应的方程式为n;
故答案为:。
15.(1)C
(2) 蒸馏烧瓶 有利于酯化反应向正反应方向进行,提高苯甲酸的转化率
(3)水浴加热
(4) 分液 除去残留的碳酸钠 除去残留的水
(5)75
【分析】三口烧瓶中加入苯甲酸、异丙醇和浓硫酸,再加入几粒沸石,水浴加热至70 °C左右,冷凝回流,保持恒温半小时,反应生成苯甲酸异丙酯,将a中的液体混合物洗涤、分液,有机层加无水硫酸钠干燥除水得苯甲酸异丙酯粗品;
(1)
浓硫酸和异丙醇、苯甲酸混合放热,浓硫酸密度大,为防止液体飞溅,不能最先加浓硫酸,故选C。
(2)
根据装置图,图乙中仪器b的名称为蒸馏烧瓶。酯化反应可逆,加过量异丙醇,有利于酯化反应向正反应方向进行,提高苯甲酸的转化率。
(3)
本实验加热至70 °C左右反应,为控制反应温度,一般采用的加热方式为水浴加热。
(4)
根据流程图,操作I把有几层和水层分开,用分液法分离互不相容的液体;第二步加入饱和碳酸钠溶液洗涤,液体中有碳酸钠残留,所以第二次水洗的目的是除去残留的碳酸钠;无水硫酸镁易吸水,操作II中加入无水硫酸镁的作用为除去残留的水。
(5)
加入38.1 g苯甲酸,苯甲酸的物质的量是,理论上生成苯甲酸异丙酯的物质的量为0.3123mol,如果得到的苯甲酸异丙酯的质量为38.360g,则该实验的产率为。
16.(1)CH3COOH+C2H5OH CH3COOCH2CH3+H2O
(2)使用相同规格的试管,比较乙中两支试管中上层液体的高度
(3)从反应体系中不断的蒸出乙酸乙酯、使用过量的乙醇、用浓硫酸吸收生成物H2O等都可以使平衡正向移动,从而提高乙酸乙酯的产率
(4)66.23%
(5) 验证乙醇的催化氧化 2 C2H5OH +O2 2CH3CHO+2H2O
(6) ①CH3CHO+2Ag ( NH3 ) 2OH CH3COONH4 +2Ag↓+3NH3+H2O ②CH3CHO+NaOH+2Cu (OH ) 2Cu2O↓+CH3COONa+ 3H2O
【分析】I、(1)试管甲中主要反应为乙酸和乙醇在浓硫酸加热的条件下反应生成乙酸乙酯,根据原子守恒即可写出反应的方程式;
(2)两组同学想要比较所制得的乙酸乙酯的产量,简便的方法比较生成液体的多少即可;
(3)可逆反应,增大反应物浓度或减小生成物浓度均可以使平衡正向移动;
(4)3mL乙醇质量为: 3mL×0.789g/cm3=2.367g, 2mL乙酸质量为: 2mL×1.05g/cm3=2.10g,乙酸完全反应需要的乙醇的质量为g=1.61g<2.367g,乙醇过量,乙酸完全反应,根据乙酸的量计算出理论上生成乙酸乙酯的质量为3.08g,全班共做10组实验,理论上可以得到: 3.08g×10=30.8g乙酸乙酯,实际得到乙酸乙酯共20.4g,即可计算出乙酸乙酯的产率;
I、
(1)由图可知;该实验的目的是验证乙醇的催化氧化;根据原子守恒即可写出反应的化学方程式;
(2)乙醛可以与新制的银氨溶液或氢氧化铜悬浊液反应生成银镜或生成砖红色的沉,故可以用新制的银氨溶液或氢氧化铜悬浊液来检验生成的乙醛,根据原子守恒即可写出反应的方程式。
(1)
根据题意可知,试管甲中主要反应为乙酸和乙醇在浓硫酸加热的条件下反应生成乙酸乙酯CH3COOH+C2H5OH CH3COOCH2CH3+H2O;
(2)
两组同学想要比较所制得的乙酸乙酯的产量,简便的方法是使用相同规格的试管,比较乙中两支试管中上层液体的高度。
(3)
该反应为可逆反应,从反应体系中不断的蒸出乙酸乙酯、使用过量的乙醇、用浓硫酸吸收生成物H2O等都可以使平衡正向移动,从而提高乙酸乙酯的产率,
(4)
3mL乙醇质量为: 3mL×0.789g/cm3=2.367g,2mL乙酸质量为: 2mL×1.05g/cm3=2.10g,乙酸完全反应需要的乙醇的质量为 =1.61g<2.367g,乙醇过量,乙酸完全反应,根据乙酸的量计算出理论上生成乙酸乙酯的质量为3.08g,全班共做10组实验,理论上可以得到: 3.08g×10=30.8g乙酸乙酯,实际得到乙酸乙酯共20.4g,即可计算出乙酸乙酯的产率为 =66.23%;
(5)
由图可知,该实验的目的是验证乙醇的催化氧化,总反应化学方程式为: 2 C2H5OH +O2 2CH3CHO+2H2O;
(6)
乙醛可以与新制的银氨溶液或氢氧化铜悬浊液反应生成银镜或生成砖红色的沉淀,故可以用新制的银氨溶液或氢氧化铜悬浊液来检验生成的乙醛,根据原子守恒写出反应的方程式分别如下:
①CH3CHO+2Ag ( NH3 ) 2OH CH3COONH4 +2Ag↓+3NH3+H2O ;
②CH3CHO+NaOH+2Cu (OH ) 2Cu2O↓+CH3COONa+ 3H2O。
17. 使反应体系受热均匀,容易控制温度 冷凝、回流,减少水杨酸和乙酸酐挥发造成的损失 E ; 重结晶 滴加氯化铁溶液鉴别没有紫色溶液出现,说明水杨酸完全除去
【分析】本题是制备类型的题,根据制备原理选择制备的仪器,根据水杨酸的结构判断其可能具有的性质,另外在制备过程中,分析可能引入的杂志,分析提纯方法。
【详解】(1)水浴加热可以使反应物受热均匀,并且温度容易控制,故答案为使反应体系受热均匀,容易控制温度,直导管可以促进生成物冷凝、回流,减少水杨酸和乙酸酐挥发造成的损失他,故答案为冷凝、回流,减少水杨酸和乙酸酐挥发造成的损失;
(2)含有酯基,能发生水解反应,含有羧基,能发生酯化反应,含有苯环,能发生加成反应,有机物可以燃烧,但是没有醛基,不能发生银镜反应故选E;
(3)水杨酸和乙酸反应属于酯化反应,其反应方程式:;
(4)该产品提纯方法与粗苯甲酸的提纯是重结晶,然后采用趁热过滤冷却结晶就可以,所以乙酰水杨酸粗产品的提纯方法也是重结晶,降温结晶,水杨酸具有酚羟基,可以通过滴加氯化铁溶液鉴别没有紫色溶液出现,说明水杨酸完全除去。
18. 2-丙醇(或异丙醇) H2O 羧基、羟基 酯化反应(或取代反应) 4 1.5×104
【详解】流程中C为丙酮(),B催化氧化(与O2、Cu、加热)生成丙酮,则B为;又因为A分子式为C3H6,A与X在催化剂条件下反应生成B,所以A为丙烯(CH2=CH-CH3)、X是H2O;G一定条件下发生加聚反应生成PMMA,由PMMA的结构可推出G为:;D为,D生成E,E和F在浓硫酸加热条件下生成G,所以E为、F为甲醇,E和F发生酯化反应生成G。
(1)B为,名称为:2—丙醇(或异丙醇);X是H2O;D为,含有的官能团名称为:羧基和羟基。
(2)E和F在浓硫酸加热条件下发生酯化反应(取代反应)生成G,化学方程式为:+CH3OH+H2O。
(3)T是G()的同分异构体,1molT与足量新制Cu(OH)2悬浊液反应最多生成2molCu2O沉淀,则T中含有2个醛基,可能的结构有:OHC(CH2)3CHO、OHCCH2CH(CH3)CHO、OHCC(CH3)2CHO、OHCCH(CH2CH3)CHO共4种。
(4)由PMMA的结构可得其分子式为(C5H8O2)n,所以相对分子质量为:100n=1.5×106,解得n=1.5×104,即其聚合度为1.5×104。
(5)由流程中C→D的转化,要合成,需要合成,以为原料,可以先水解生成,催化氧化生成,故合成路线为:。
【点睛】本题通过有机玻璃PMMA的合成工艺流程为载体,考查有机化学的核心知识,涉及常见有机物官能团的结构、性质及相互转化关系,涉及有机物结构简式的确定、反应类型的判断、化学方程式的书写、同分异构体的识别和书写、合成路线的选择等知识。能够通过题给情境,运用所学知识进行分析是完成此类题目的关键。本题首先应该分析流程,借助题给信息和流程中已知的物质,推出未知物质,可从C开始逆推确定B、A和X,然后从PMMA逆推同时结合D正推,确定E、F和G;判断同分异构体的种数是该题的难点,针对不同的物质类别,抓住书写同分异构体的一般规律,首先判断该物质中含有的官能团种类、取代基的个数及种类,注意书写过程中的不重不漏;物质制备合成路线的选择,需要根据物质之间结构的异同,利用所学化学知识和题给信息,选择合适的条件和试剂,可采用逆合成分析法。
答案第1页,共2页
答案第1页,共2页
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列物质中含少量杂质(括号内为杂质),选用除杂试剂和方法均正确的是
A.:酸性溶液,洗气
B.己烷(己烯):溴水,分液
C.硝基苯:溶液,分液
D.:溶液,蒸馏
2.下列各组混合物能用分液漏斗分离的是
A.苯酚和苯 B.乙醛和水 C.乙酸乙酯和水 D.苯酚和水
3.下列有关有机物的说法正确的是
A.油脂在溶液中会稳定存在
B.丙酸和乙酸乙酯所含的官能团相同
C.苯和裂化汽油都可以作碘水中的萃取剂
D.与丙烷在光照下反应,液态产物为混合物
4.现有环状化合物结构如图。有关说法正确的是
A.a、b、c均可与钠反应
B.a、b、c互为同分异构体
C.a、b、c均可发生氧化反应和加成反应
D.等物质的量的a和b消耗NaOH的物质的量之比为2:1
5.有机物X的结构简式如图所示,下列有关X的说法不正确的是
A.X分子中所有原子不可能共面 B.1molX最多能与发生加成反应
C.X能使酸性高锰酸钾溶液褪色 D.X在空气中完全燃烧生成水和二氧化碳
6.紫草主要用于治疗烧伤、湿疹、丹毒等,其主要成分紫草素的结构简式如图,下列关于紫草素的说法正确的是
A.该物质能与NaOH反应,且1mol紫草素能消耗3molNaOH
B.紫草素的同分异构体中可能含有两个苯环
C.紫草素能使溴水、酸性KMnO4溶液褪色,且反应原理相同
D.紫草素与苯酚互为同系物
7.下列说法正确的是
A.棉花和蚕丝的主要成分都是纤维素
B.蛋白质在一定条件下发生水解反应生成葡萄糖
C.乙二醇的水溶液凝固点很低,可作汽车发动机的抗冻剂
D.氨基酸以两性离子的形态存在时,在水中溶解度最大
8.下列反应的方程式书写正确的是
A.用碳酸氢钠溶液检验水杨酸中的羧基:+2→ +2H2O+2CO2↑
B.1-溴丙烷与氢氧化钾的乙醇溶液共热:CH3CH2CH2Br+KOHCH3CH2CH2OH+KBr
C.用溴水检验丙烯醛中的碳碳双键:CH2=CHCHO+Br2CH2BrCHBrCHO
D.n +n+(2n-1)H2O
9.芹菜中的芹黄素具有抗肿瘤、抗病毒等生物学活性,其熔点为347~348℃,结构简式如图所示。下列关于芹黄素的说法不正确的是
A.常温下为固体,需密封保存
B.可以发生加成反应、取代反应、氧化反应
C.1mol芹黄素最多能与溴水中的5mol Br2发生反应
D.1mol芹黄素最多能与7molH2发生加成反应
10.与有机物 互为同分异构体,不能与NaOH溶液反应的芳香族化合物有
A.7种 B.8种 C.9种 D.10种
11.对羟基苯甲醛是一种用途极广的有机合成中间体。两种主要工业合成路线如图所示。
下列说法正确的是
A.苯酚和对羟基苯甲醇互为同系物
B.对羟基苯甲醇的一氯代物有4种(不考虑立体异构)
C.对甲基苯酚的同分异构体中含有苯环的有4种(不包括其本身)
D.对羟基苯甲醛中所有原子共平面
12.我国第一部中药学典籍《神农本草经》中记载的一种中药“昆布”,具有利水消肿的功效,其主要成分是3,5-二碘络氨酸,结构简式如下图。下列关于该有机化合物说法不正确的是
A.分子中含有手性碳原子
B.能与发生取代反应
C.既能与酸反应,也能与碱反应
D.理论上1mol该物质与足量反应可生成
二、填空题
13.按要求回答下列问题:
(1)的系统命名为______________;
(2)3—甲基—2一戊烯的结构简式为______________;
(3)的分子式为______________;
(4)某烃的分子式为C4H4,它是合成橡胶的中间体,它有多种同分异构体
①试写出它的一种链式结构的同分异构体的结构简式______________.
②它有一种同分异构体,每个碳原子均达饱和,且碳与碳的夹角相同,该分子中碳原子形成的空间构型为______________形
14.有机物A 的结构简式为,它可通过不同化学反应分别制得B、C、D和E四种物质。
请回答下列问题:
(1)在A~E五种物质中,互为同分异构体的是______(填字母代号)。
(2)写出由A生成B的化学方程式:________________。
(3)已知HCHO分子中所有原子在同一平面内,则上述分子中所有的原子有可能都在同一平面内的是______(填字母代号)。
(4)C能形成高聚物,该高聚物的结构简式为________。
三、实验题
15.某化学兴趣小组设计实验制备苯甲酸异丙酯,其反应原理为
+十H2O。
用如图所示装置进行实验:
物质的部分物理性质如表所示:
物质 相对分子质量 密度/ g·cm-3 沸点/°C 水溶性
苯甲酸 122 1.27 249 微溶
异丙醇 60 0.79 82 易溶
苯甲酸异丙酯 164 1.17 218 不溶
实验步骤:
步骤I.在干燥的仪器a中加入38.1 g苯甲酸、30 mL异丙醇和15 mL浓硫酸,再加入几粒沸石;
步骤II.加热至70 °C左右,保持恒温半小时;
步骤III.将仪器a中液体进行如下所示操作得到粗产品;
步骤IV.将粗产品用图乙所示装置进行精制。
试回答下列问题:
(1)步骤I中加入三种试剂的先后顺序一定错误的是_ (填字母)。
A.异丙醇、苯甲酸、浓硫酸
B.异丙醇、浓硫酸、苯甲酸
C.浓硫酸、异丙醇、苯甲酸
(2)图乙中仪器b的名称为_。 加入的苯甲酸和异丙醇中,需过量的是异丙醇,目的是___________。
(3)本实验一般采用的加热方式为___________,因为温度过高会影响产率。
(4)操作I的分离方法名称为___________,其中第二次水洗的目的是___________,操作II中加入无水硫酸镁的作用为___________。
(5)如果得到的苯甲酸异丙酯的质量为38.360g,则该实验的产率为___________%(结果保留2位有效数字)。
16.Ⅰ、某班在实验室进行制取乙酸乙酯的分组实验,主要步骤如下:
①按右图连接好装置,并检查装置的气密性。
②在试管甲中加入3mL乙醇,然后边振荡试管边慢慢加入2mL浓硫酸和2mL乙酸,再加入沸石。然后用酒精灯缓慢加热。
③待试管乙(装有少量饱和碳酸钠溶液)中收集到一定量产物后停止加热,撤出试管B,振荡后静置。
已知:
相对分子质量 密度/(g.cm-3) 熔点/℃ 沸点/℃ 水中溶解性
乙醇 46 0.789 -117.3 78.5 以任意比互溶
乙酸 60 1.050 16.6 117.9 易溶
乙酸乙酯 88 0.897 -84 77 难溶
回答下列问题:
(1)试管甲中主要反应的化学方程式为___________。
(2)两组同学想要比较所制得的乙酸乙酯的产量,简便的方法是___________。
(3)该反应为可逆反应,要提高乙酸乙酯的产率,该实验中采取的措施有___________。
(4)现对全班同学试管乙中的液体集中处理,得到乙酸乙酯的粗产品并回收乙醇。假设全班共做10组实验,得到乙酸乙酯共20.4g,请计算乙酸乙酯的产率为___________(保留两位有效数字)。
Ⅱ、实验小组用下列装置进行实验。
(5)该实验的目的是___________,请写出总反应化学方程式___________。
(6)若想检验试管a中收集的液体成分含有乙醛,请分别写出两种检验方法的主要化学方程式:
①___________
②___________
17.乙酰水杨酸(阿司匹林)是一种白色晶体,在临床上被广泛用于发热、肌肉痛、神经痛、头痛、风湿热、急性风湿性关节炎等的治疗。乙酰水杨酸的合成原理和装置如下:
请回答下列问题:
(1)实验中水浴加热的优点_______,是直导管的作用是_______。
(2)根据阿司匹林的结构分析,其不可能发生的反应是_______。
A.加成反应 B.氧化反应 C.酯化反应 D.水解反应 E.银镜反应
(3)阿司匹林也可通过水杨酸和乙酸反应制取,写出该反应方程式:_______。
(4)乙酰水杨酸粗产品中常含有少量水杨酸杂质,该产品提纯方法与苯甲酸类似,采用_______法。提纯后,请设计实验方案验证水杨酸是否完全除去_______。
四、有机推断题
18.用石油产品A(C3H6)为主要原料,合成具有广泛用途的有机玻璃PMMA。流程如下(部分产物和条件省略)
试回答下列问题:
(1)B的名称________;X试剂为_______(化学式);D中官能团名称_________。
(2)E→G的化学方程式为________________________________________,反应类型是_________。
(3)T是G的同分异构体,1molT与足量新制Cu(OH)2悬浊液反应最多生成2molCu2O沉淀,T的结构有________种(不含立体结构)。
(4)若高分子化合物PMMA的相对分子质量为1.5×106,其聚合度为_______。
(5)参照上述流程,以为原料合成 (其它原料自选)。设计合成路线:________________________。
试卷第2页,共2页
试卷第1页,共1页
参考答案:
1.C
【详解】A.乙烯含有碳碳双键能和酸性高锰酸钾反应生成二氧化碳气体,引入新杂质气体,A错误;
B.己烯和溴加成的生成物和己烷互溶,不能分液分离,B错误;
C.氢氧化钠和二氧化氮反应生成盐溶液,盐溶液与硝基苯互不相溶,可以分液分离,C正确;
D.和氢氧化钠溶液加热会发生取代反应生成乙醇,D错误;
故选C。
2.C
【详解】A.苯酚易溶于苯,苯酚和苯形成溶液,不能用分液漏斗分离,故A不合题意;
B.乙醛和水相互溶解,不能用分液漏斗分离,故B符合题意;
C.乙酸乙酯和水不互溶,乙酸乙酯在上层,水在下层,能用分液漏斗分离,故C不合题意;
D.通常苯酚微溶于水,上层为溶有少量苯酚的水溶液,下层为溶有水的苯酚溶液,所以不能用分液漏斗彻底分离,故D不合题意;
故答案为C。
3.D
【详解】A. 油脂在等强碱溶液中会发生水解反应,即皂化反应,A项错误;
B. 丙酸含有羧基,乙酸乙酯含有酯基,二者的官能团不同,B项错误;
C. 裂化汽油含有不饱和烃,与发生加成反应,C项错误;
D. 丙烷与氯气在光照下发生取代反应,液态产物为多氯代物,如一氯丙烷、二氯丙烷、三氯丙烷等,故液态产物为混合物,D项正确。
答案选D。
4.B
【分析】a分子中含有酯基,b分子含有羧基,c中含有羟基,三种环状化合物的分子式均为C5H8O2,根据官能团的性质分析解答。
【详解】A.酯基不和钠发生反应,A错误;
B.三种环状化合物的分子式均为C5H8O2,结构不同,互为同分异构体,B正确;
C.a、b、c含有的官能团不能发生加成反应,C错误;
D.1mol a分子中含有1mol酯基,1mol b分子含有1mol羧基,等物质的量的a和b消耗NaOH的物质的量之比为1:1,D错误;
故选B。
5.B
【详解】A.分子中含有饱和碳原子,与饱和碳原子相连的四个原子一定不在同一平面上,A项正确;
B.分子中的苯环、碳碳双键能与氢气发生加成反应,所以最多能与发生加成反应,B项错误;
C.分子中的碳碳双键能使酸性高锰酸钾溶液褪色,C项正确;
D.X由C、H、O三种元素组成,在空气中完全燃烧时生成水和二氧化碳,D项正确;
答案选B。
6.B
【详解】A.紫草素中含有酚羟基能与反应,且紫草素含有2mol酚羟基能消耗,A错误;
B.紫草素有9个不饱和度,所以同分异构体中可能含有两个苯环,B正确;
C.紫草素能使溴水褪色是发生加成和取代反应、使酸性溶液褪色是发生氧化反应,反应原理不相同,C错误;
D.紫草素与苯酚不互为同系物,D错误。
故选B。
7.C
【详解】A.棉花的主要成分是纤维素,蚕丝的主要成分是蛋白质,选项A错误;
B.蛋白质在一定条件下发生水解最终生成氨基酸,选项B错误;
C.乙二醇的水溶液凝固点很低,可作内燃机的抗冻剂,选项C正确;
D.氨基酸处于等电状态时,主要是以.两性离子形式存在,此时它的溶解度最小,选项D错误;
答案选C。
8.D
【详解】A.酚羟基的酸性比碳酸弱,故酚羟基与碳酸氢根不反应,方程式为:,A错误;
B.1-溴丙烷在氢氧化钾的乙醇溶液中应该发生消去反应生成丙烯,B错误;
C.醛基也能跟溴水反应,故不能用溴水检验碳碳双键,C错误;
D.乙二酸和乙二醇的发生缩聚反应,脱去2n-1个水,D正确;
故选D。
9.D
【详解】A.熔点为347℃~348℃,则常温下为固体,含有酚羟基,易被氧化,应密封保存,故A正确;
B.由可知,苯环、羰基和碳碳双键可发生加成反应,苯环上可发生取代反应,含有酚羟基,易被氧化,可发生氧化反应,故B正确;
C.由可知,与溴水能发生取代反应的位置只能是酚羟基的邻对位,如,与溴水能发生加成反应的有碳碳双键,则1mol芹黄素最多能与溴水中的5mol Br2发生反应,故C正确;
D.由可知,苯环、羰基和碳碳双键均可与H2发生加成反应,有二个苯环,一个羰基,一个碳碳双键,则1mol芹黄素最多能与8molH2发生加成反应,故D错误;
答案为D。
10.D
【详解】从有机物的结构简式可知,其不饱和度为4,总共有8个碳原子,1个氧原子,则其分子式为C8H10O,其同分异构体是不能与NaOH溶液反应的芳香族化合物,则说明其同分异构体中含有一个苯环,且苯环上不能有酚羟基,则满足条件的同分异构体有、两种、 的邻、间、对三种,的邻、间、对三种,和两种,总共10种,故答案为D。
11.C
【详解】A.由题图知,苯酚的分子式为,对羟基苯甲醇的分子式为,同系物是指结构相似,分子组成上相差一个或若干个原子团,则二者不互为同系物,A错误;
B.采用等效氢法进行分析,对羟基苯甲醇中等效氢原子有5种(),氯原子取代C上的氢,则其一氯代物有3种,B错误;
C.利用口诀分析苯环上的取代情况,若苯环上有1个取代基,则取代基为或,有2种;若苯环上有2个取代基,取代基为和,除去本身,有“邻、间”2种,则共有4种,C正确;
D.对羟基苯甲醛中单键可以旋转,则该物质分子中所有原子不一定共平面,D错误;
故答案选C。
12.D
【详解】A.手性碳原子是指与四个各不相同原子或基团相连的碳原子,该有机物有1个手性碳原子,A正确;
B.该有机物含有C-H键,光照下能与Br2发生取代反应,B正确;
C.该有机物含有酚羟基、羧基和氨基,具有弱酸性和弱碱性,既能与酸反应,也能与碱反应,C正确;
D.该有机物有1个羧基,因此理论上1mol该物质与足量反应可生成,即44g CO2,D错误;
故答案为:D。
【点睛】判断一个碳原子是否是手性碳原子,首先要观察该碳原子是否有双键或三键连接,如果有则必然不属于手性碳原子,即不饱和碳一定不是手性碳。
13.(1)2,3二甲基丁烷
(2)
(3)C4H8O
(4) CH2CH-CCH 正四面体
【详解】(1)有机物主链有4个C原子,母体是丁烷,支链有2、3号为甲基取代基,名称为2,3-二甲基丁烷;
(2)按照烯烃的命名,3—甲基—2一戊烯的主链有5个碳原子,2、3号碳之间有碳碳双键,3号碳上有取代基甲基,此有机物的结构简式为;
(3)键线式中交点、拐点、端点都是碳原子,有机物中碳原子有4个化学键,因此有机物的分子式为C4H8O;
(4)①4个碳原子的饱和链烃分子式为C4H10,与C4H4对比,C4H4比饱和链烃少了6个H,即C4H4中有3个碳碳双键或1个碳碳双键和1个叁键,有机物中碳原子不能同时连有2个碳碳双键,即结构简式为CH2CH-CCH ;
②每个碳原子均达饱和,且碳与碳的夹角相同,空间构型为正四面体。
14. C和E C
【详解】(1)A发生催化氧化生成B,A发生消去反应生成C,A与甲酸发生酯化反应生成D,为取代反应,A发生分子内酯化反应生成E,也属于取代反应,C、E均比A少H2O,四种物质中只有C、E的分子式相同,但结构不同,则C与E互为同分异构体;
故答案为:C和E;
(2)A发生催化氧化生成B,由A生成B的化学方程式为;
故答案为:;
(3)已知HCHO分子中所有原子在同一平面内,表明羰基是平面结构。ABDE中均含有亚甲基,是空间四面体结构,只有C中含有苯环和碳碳双键,都是平面结构,分子中所有的原子有可能都在同一平面内;
故答案为:C;
(4)C中含有C=C官能团,可发生加聚反应,该高聚物的结构简式为,反应的方程式为n;
故答案为:。
15.(1)C
(2) 蒸馏烧瓶 有利于酯化反应向正反应方向进行,提高苯甲酸的转化率
(3)水浴加热
(4) 分液 除去残留的碳酸钠 除去残留的水
(5)75
【分析】三口烧瓶中加入苯甲酸、异丙醇和浓硫酸,再加入几粒沸石,水浴加热至70 °C左右,冷凝回流,保持恒温半小时,反应生成苯甲酸异丙酯,将a中的液体混合物洗涤、分液,有机层加无水硫酸钠干燥除水得苯甲酸异丙酯粗品;
(1)
浓硫酸和异丙醇、苯甲酸混合放热,浓硫酸密度大,为防止液体飞溅,不能最先加浓硫酸,故选C。
(2)
根据装置图,图乙中仪器b的名称为蒸馏烧瓶。酯化反应可逆,加过量异丙醇,有利于酯化反应向正反应方向进行,提高苯甲酸的转化率。
(3)
本实验加热至70 °C左右反应,为控制反应温度,一般采用的加热方式为水浴加热。
(4)
根据流程图,操作I把有几层和水层分开,用分液法分离互不相容的液体;第二步加入饱和碳酸钠溶液洗涤,液体中有碳酸钠残留,所以第二次水洗的目的是除去残留的碳酸钠;无水硫酸镁易吸水,操作II中加入无水硫酸镁的作用为除去残留的水。
(5)
加入38.1 g苯甲酸,苯甲酸的物质的量是,理论上生成苯甲酸异丙酯的物质的量为0.3123mol,如果得到的苯甲酸异丙酯的质量为38.360g,则该实验的产率为。
16.(1)CH3COOH+C2H5OH CH3COOCH2CH3+H2O
(2)使用相同规格的试管,比较乙中两支试管中上层液体的高度
(3)从反应体系中不断的蒸出乙酸乙酯、使用过量的乙醇、用浓硫酸吸收生成物H2O等都可以使平衡正向移动,从而提高乙酸乙酯的产率
(4)66.23%
(5) 验证乙醇的催化氧化 2 C2H5OH +O2 2CH3CHO+2H2O
(6) ①CH3CHO+2Ag ( NH3 ) 2OH CH3COONH4 +2Ag↓+3NH3+H2O ②CH3CHO+NaOH+2Cu (OH ) 2Cu2O↓+CH3COONa+ 3H2O
【分析】I、(1)试管甲中主要反应为乙酸和乙醇在浓硫酸加热的条件下反应生成乙酸乙酯,根据原子守恒即可写出反应的方程式;
(2)两组同学想要比较所制得的乙酸乙酯的产量,简便的方法比较生成液体的多少即可;
(3)可逆反应,增大反应物浓度或减小生成物浓度均可以使平衡正向移动;
(4)3mL乙醇质量为: 3mL×0.789g/cm3=2.367g, 2mL乙酸质量为: 2mL×1.05g/cm3=2.10g,乙酸完全反应需要的乙醇的质量为g=1.61g<2.367g,乙醇过量,乙酸完全反应,根据乙酸的量计算出理论上生成乙酸乙酯的质量为3.08g,全班共做10组实验,理论上可以得到: 3.08g×10=30.8g乙酸乙酯,实际得到乙酸乙酯共20.4g,即可计算出乙酸乙酯的产率;
I、
(1)由图可知;该实验的目的是验证乙醇的催化氧化;根据原子守恒即可写出反应的化学方程式;
(2)乙醛可以与新制的银氨溶液或氢氧化铜悬浊液反应生成银镜或生成砖红色的沉,故可以用新制的银氨溶液或氢氧化铜悬浊液来检验生成的乙醛,根据原子守恒即可写出反应的方程式。
(1)
根据题意可知,试管甲中主要反应为乙酸和乙醇在浓硫酸加热的条件下反应生成乙酸乙酯CH3COOH+C2H5OH CH3COOCH2CH3+H2O;
(2)
两组同学想要比较所制得的乙酸乙酯的产量,简便的方法是使用相同规格的试管,比较乙中两支试管中上层液体的高度。
(3)
该反应为可逆反应,从反应体系中不断的蒸出乙酸乙酯、使用过量的乙醇、用浓硫酸吸收生成物H2O等都可以使平衡正向移动,从而提高乙酸乙酯的产率,
(4)
3mL乙醇质量为: 3mL×0.789g/cm3=2.367g,2mL乙酸质量为: 2mL×1.05g/cm3=2.10g,乙酸完全反应需要的乙醇的质量为 =1.61g<2.367g,乙醇过量,乙酸完全反应,根据乙酸的量计算出理论上生成乙酸乙酯的质量为3.08g,全班共做10组实验,理论上可以得到: 3.08g×10=30.8g乙酸乙酯,实际得到乙酸乙酯共20.4g,即可计算出乙酸乙酯的产率为 =66.23%;
(5)
由图可知,该实验的目的是验证乙醇的催化氧化,总反应化学方程式为: 2 C2H5OH +O2 2CH3CHO+2H2O;
(6)
乙醛可以与新制的银氨溶液或氢氧化铜悬浊液反应生成银镜或生成砖红色的沉淀,故可以用新制的银氨溶液或氢氧化铜悬浊液来检验生成的乙醛,根据原子守恒写出反应的方程式分别如下:
①CH3CHO+2Ag ( NH3 ) 2OH CH3COONH4 +2Ag↓+3NH3+H2O ;
②CH3CHO+NaOH+2Cu (OH ) 2Cu2O↓+CH3COONa+ 3H2O。
17. 使反应体系受热均匀,容易控制温度 冷凝、回流,减少水杨酸和乙酸酐挥发造成的损失 E ; 重结晶 滴加氯化铁溶液鉴别没有紫色溶液出现,说明水杨酸完全除去
【分析】本题是制备类型的题,根据制备原理选择制备的仪器,根据水杨酸的结构判断其可能具有的性质,另外在制备过程中,分析可能引入的杂志,分析提纯方法。
【详解】(1)水浴加热可以使反应物受热均匀,并且温度容易控制,故答案为使反应体系受热均匀,容易控制温度,直导管可以促进生成物冷凝、回流,减少水杨酸和乙酸酐挥发造成的损失他,故答案为冷凝、回流,减少水杨酸和乙酸酐挥发造成的损失;
(2)含有酯基,能发生水解反应,含有羧基,能发生酯化反应,含有苯环,能发生加成反应,有机物可以燃烧,但是没有醛基,不能发生银镜反应故选E;
(3)水杨酸和乙酸反应属于酯化反应,其反应方程式:;
(4)该产品提纯方法与粗苯甲酸的提纯是重结晶,然后采用趁热过滤冷却结晶就可以,所以乙酰水杨酸粗产品的提纯方法也是重结晶,降温结晶,水杨酸具有酚羟基,可以通过滴加氯化铁溶液鉴别没有紫色溶液出现,说明水杨酸完全除去。
18. 2-丙醇(或异丙醇) H2O 羧基、羟基 酯化反应(或取代反应) 4 1.5×104
【详解】流程中C为丙酮(),B催化氧化(与O2、Cu、加热)生成丙酮,则B为;又因为A分子式为C3H6,A与X在催化剂条件下反应生成B,所以A为丙烯(CH2=CH-CH3)、X是H2O;G一定条件下发生加聚反应生成PMMA,由PMMA的结构可推出G为:;D为,D生成E,E和F在浓硫酸加热条件下生成G,所以E为、F为甲醇,E和F发生酯化反应生成G。
(1)B为,名称为:2—丙醇(或异丙醇);X是H2O;D为,含有的官能团名称为:羧基和羟基。
(2)E和F在浓硫酸加热条件下发生酯化反应(取代反应)生成G,化学方程式为:+CH3OH+H2O。
(3)T是G()的同分异构体,1molT与足量新制Cu(OH)2悬浊液反应最多生成2molCu2O沉淀,则T中含有2个醛基,可能的结构有:OHC(CH2)3CHO、OHCCH2CH(CH3)CHO、OHCC(CH3)2CHO、OHCCH(CH2CH3)CHO共4种。
(4)由PMMA的结构可得其分子式为(C5H8O2)n,所以相对分子质量为:100n=1.5×106,解得n=1.5×104,即其聚合度为1.5×104。
(5)由流程中C→D的转化,要合成,需要合成,以为原料,可以先水解生成,催化氧化生成,故合成路线为:。
【点睛】本题通过有机玻璃PMMA的合成工艺流程为载体,考查有机化学的核心知识,涉及常见有机物官能团的结构、性质及相互转化关系,涉及有机物结构简式的确定、反应类型的判断、化学方程式的书写、同分异构体的识别和书写、合成路线的选择等知识。能够通过题给情境,运用所学知识进行分析是完成此类题目的关键。本题首先应该分析流程,借助题给信息和流程中已知的物质,推出未知物质,可从C开始逆推确定B、A和X,然后从PMMA逆推同时结合D正推,确定E、F和G;判断同分异构体的种数是该题的难点,针对不同的物质类别,抓住书写同分异构体的一般规律,首先判断该物质中含有的官能团种类、取代基的个数及种类,注意书写过程中的不重不漏;物质制备合成路线的选择,需要根据物质之间结构的异同,利用所学化学知识和题给信息,选择合适的条件和试剂,可采用逆合成分析法。
答案第1页,共2页
答案第1页,共2页
