2.2 烯烃 炔烃 同步练习(含解析)
文档属性
| 名称 | 2.2 烯烃 炔烃 同步练习(含解析) |  | |
| 格式 | docx | ||
| 文件大小 | 620.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-23 08:14:50 | ||
图片预览


文档简介
2.2 烯烃
1.下列反应属于加成反应的是
A.乙醇与钠反应生成乙醇钠和氢气 B.乙烯与溴单质反应生成1,2-二溴乙烷
C.乙酸与乙醇反应生成乙酸乙酯和水 D.甲烷与氯气反应生成一氯甲烷和氯化氢
2.兴趣小组用乙醇和浓硫酸制取乙烯,并验证乙烯气体的生成,所用实验装置如图所示。下列说法正确的是
A.装置A烧瓶中应加入浓硫酸、再沿烧瓶内壁缓慢加入乙醇
B.反应时应迅速升温到170℃,并控制温度保持不变
C.为除去乙烯中混有的SO2杂质,装置B洗气瓶中应装入酸性KMnO4溶液
D.实验中有少量副产物乙醚生成,分离乙醇和乙醚的混合物可以采用分液的方法
3.下列说法正确的是
A.除去苯中含有的少量苯酚,可向其中加入溴水,然后分液
B.向丙烯醛中加入溴水,溴水褪色,证明丙烯醛中含有碳碳双键
C.将铁锈溶于浓盐酸,滴入溶液,紫色褪去,证明铁锈中含有二价铁
D.向盛有2mL0.1mol/LNaCl溶液的试管中,滴加2滴0.1mol/L溶液,振荡,然后继续滴加4滴0.1mol/LKI溶液,观察到白色沉淀转化为黄色,说明(AgCl)>(AgI)
4.已知1,3-丁二烯可发生反应:CH2=CH-CH=CH2+Br2→BrCH2-CH=CH-CH2Br。有机物能使溴水褪色,它与溴发生等物质的量加成反应时生成物不可能是
A. B.
C. D.
5.下列化学用语表达正确的是( )
A.乙烯的电子式: B.丙烷分子的比例模型:
C.CO2分子球棍模型: D.乙醇的分子式:C2H6O
6.下列化学用语或模型表示正确的是( )
A.H2O2分子结构式:H-O-O-H
B.氮气的电子式:
C.比例模型:可以表示甲烷分子,也可以表示四氯化碳分子
D.C2H4分子比例模型:
7.用NA表示阿伏加德罗常数的值。下列与有机物的结构、性质有关的叙述正确的是
A.28g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA
B.在密闭容器中加入1.5mol H2和0.5molN2,充分反应后可得到NH3分子数为NA
C.4.6g有机物C2H6O的分子中含有的C-H键数目一定为0.5NA
D.甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应
8.下列说法正确的是
A. 的一溴代物和的一溴代物都有4种(不考虑立体异构)
B.分子中的4个碳原子在同一直线上,且存在顺反异构体
C.按系统命名法,化合物的名称是2,3,4-三甲基-2-乙基戊烷
D.由单烯烃和氢气加成制得,则对应的单烯烃有5种
9.已知有机物a和b的结构简式分别为和。下列说法正确的是(不考虑立体异构)
A.a分子中含有6个键,2个键 B.a与苯互为同分异构体
C.b可使溴水褪色,反应时键断裂 D.b的一氯代物有5种
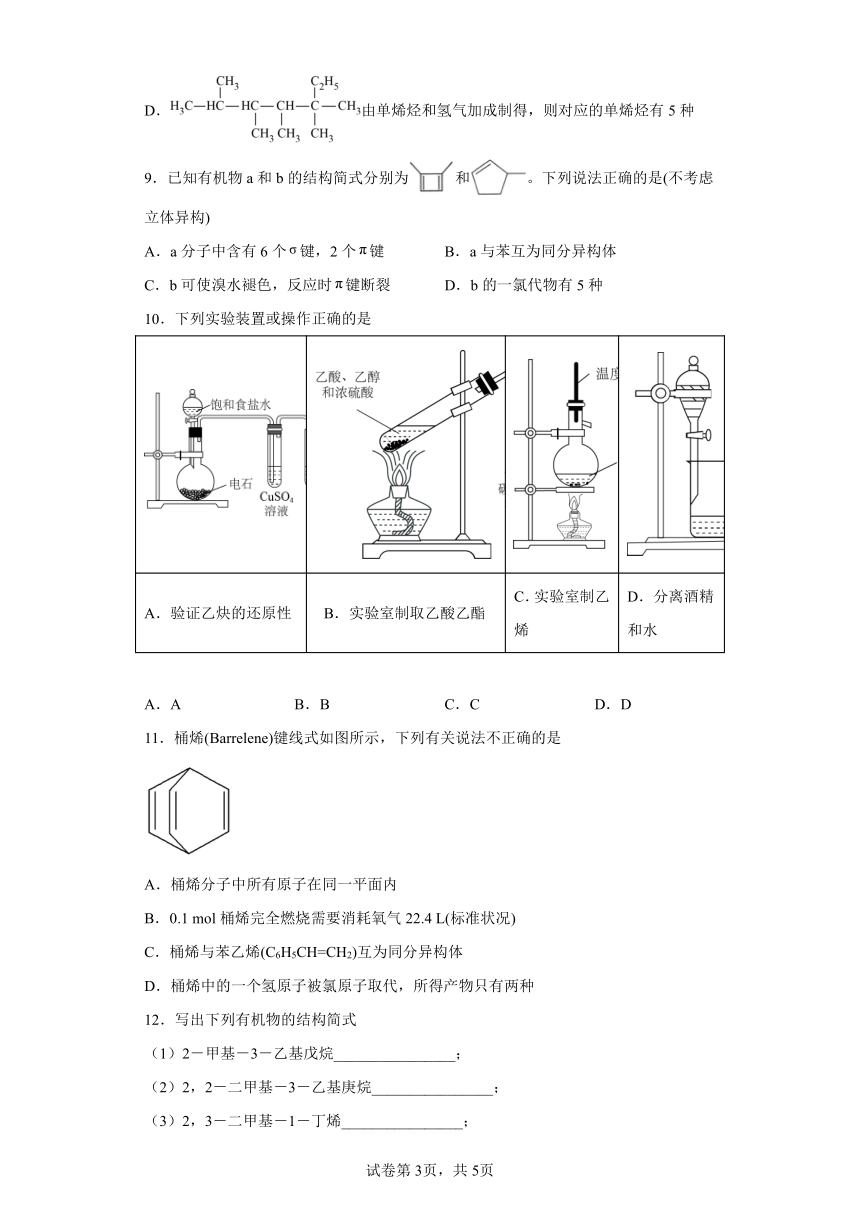
10.下列实验装置或操作正确的是
A.验证乙炔的还原性 B.实验室制取乙酸乙酯 C.实验室制乙烯 D.分离酒精和水
A.A B.B C.C D.D
11.桶烯(Barrelene)键线式如图所示,下列有关说法不正确的是
A.桶烯分子中所有原子在同一平面内
B.0.1 mol桶烯完全燃烧需要消耗氧气22.4 L(标准状况)
C.桶烯与苯乙烯(C6H5CH=CH2)互为同分异构体
D.桶烯中的一个氢原子被氯原子取代,所得产物只有两种
12.写出下列有机物的结构简式
(1)2-甲基-3-乙基戊烷________________;
(2)2,2-二甲基-3-乙基庚烷________________;
(3)2,3-二甲基-1-丁烯________________;
(4)2,4,6-三硝基甲苯________________;
(5)聚乙烯________________;
(6)聚2-甲基-1,3-丁二烯________________。
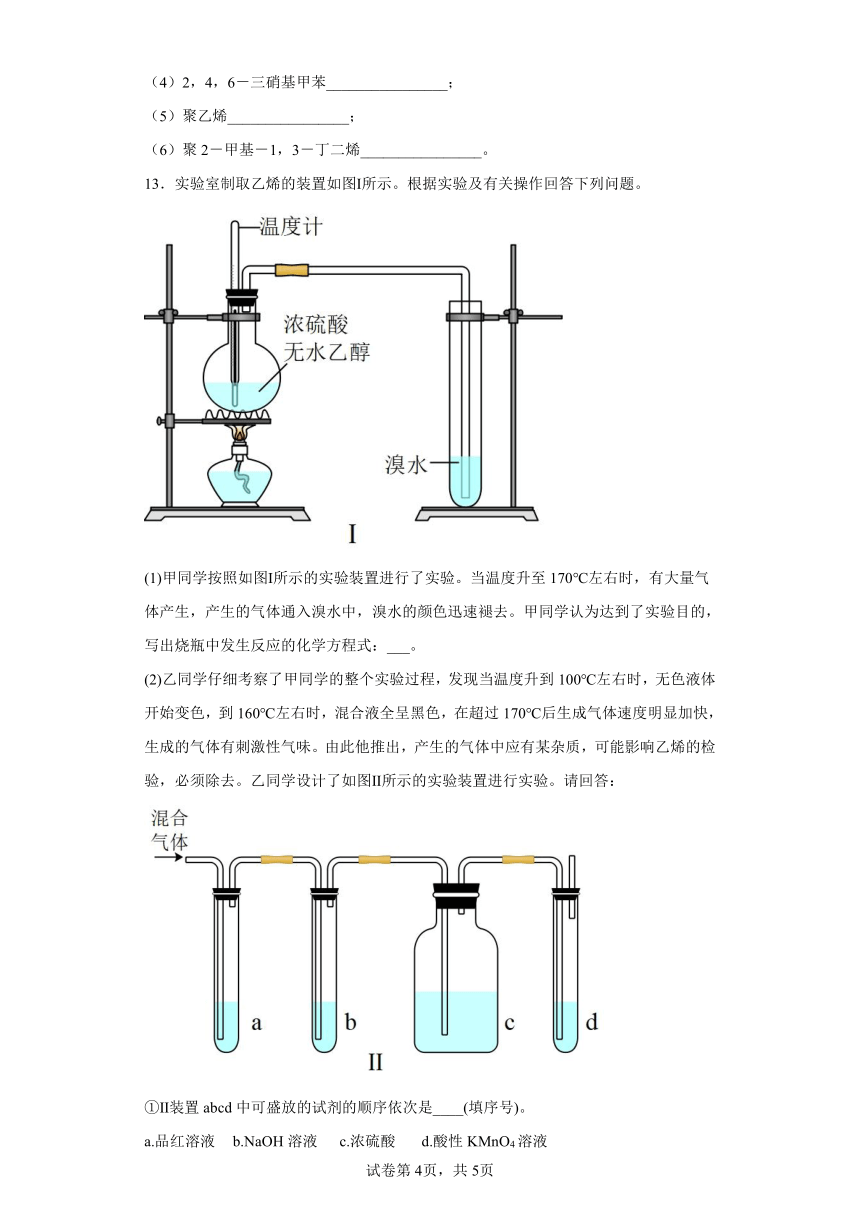
13.实验室制取乙烯的装置如图Ⅰ所示。根据实验及有关操作回答下列问题。
(1)甲同学按照如图Ⅰ所示的实验装置进行了实验。当温度升至170℃左右时,有大量气体产生,产生的气体通入溴水中,溴水的颜色迅速褪去。甲同学认为达到了实验目的,写出烧瓶中发生反应的化学方程式:___。
(2)乙同学仔细考察了甲同学的整个实验过程,发现当温度升到100℃左右时,无色液体开始变色,到160℃左右时,混合液全呈黑色,在超过170℃后生成气体速度明显加快,生成的气体有刺激性气味。由此他推出,产生的气体中应有某杂质,可能影响乙烯的检验,必须除去。乙同学设计了如图Ⅱ所示的实验装置进行实验。请回答:
①Ⅱ装置abcd中可盛放的试剂的顺序依次是____(填序号)。
a.品红溶液 b.NaOH溶液 c.浓硫酸 d.酸性KMnO4溶液
②乙设计的实验中能确定生成了乙烯的现象是____。
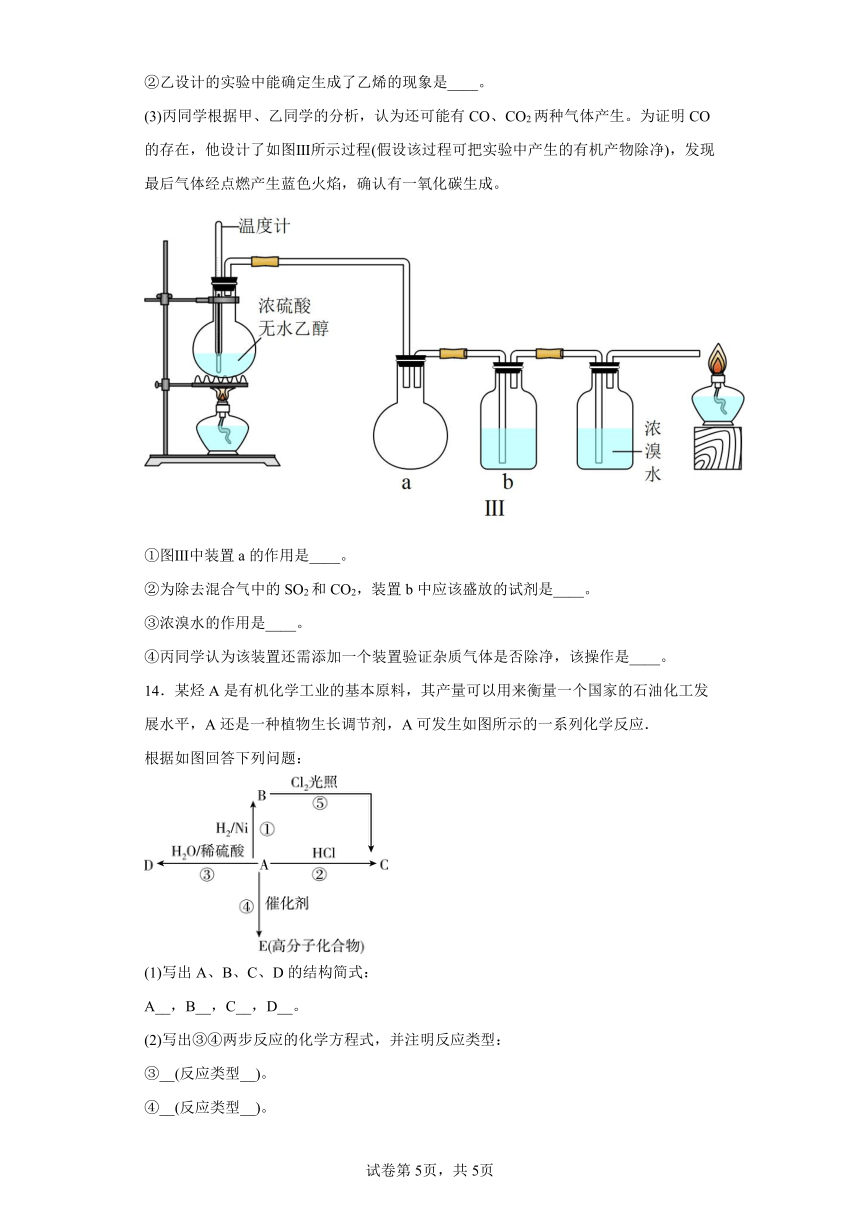
(3)丙同学根据甲、乙同学的分析,认为还可能有CO、CO2两种气体产生。为证明CO的存在,他设计了如图Ⅲ所示过程(假设该过程可把实验中产生的有机产物除净),发现最后气体经点燃产生蓝色火焰,确认有一氧化碳生成。
①图Ⅲ中装置a的作用是____。
②为除去混合气中的SO2和CO2,装置b中应该盛放的试剂是____。
③浓溴水的作用是____。
④丙同学认为该装置还需添加一个装置验证杂质气体是否除净,该操作是____。
14.某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应.
根据如图回答下列问题:
(1)写出A、B、C、D的结构简式:
A__,B__,C__,D__。
(2)写出③④两步反应的化学方程式,并注明反应类型:
③__(反应类型__)。
④__(反应类型__)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
【详解】A.乙醇与钠反应生成乙醇钠和氢气的反应属于置换反应,A不符合题意;
B.乙烯与溴单质反应生成1,2-二溴乙烷的反应为加成反应,B符合题意;
C.乙酸与乙醇反应生成乙酸乙酯和水的反应为酯化反应,酯化反应属于取代反应,C不符合题意;
D.甲烷与氯气反应生成一氯甲烷和氯化氢的反应为取代反应,D不符合题意;
故合理选项是B。
2.B
【详解】A.装置A应先加入乙醇,然后再沿烧瓶内壁缓慢加入浓硫酸,故A错误;
B.浓硫酸和乙醇在140℃会生成乙醚,因此制取乙烯时,应迅速升温到170℃,并控制温度保持不变,故B正确;
C.乙烯容易被酸性KMnO4溶液氧化,因此装置B洗气瓶中不能装入酸性KMnO4溶液,故C错误;
D.乙醇和乙醚是互溶的,则乙醇和乙醚的混合物不可以采用分液的方法,故D错误;
本题答案B。
3.D
【详解】A.苯是一种良好的有机溶剂,既能溶解溴单质,又能溶解三溴苯酚,因此在苯酚的苯溶液中加浓溴水是不能除去苯酚的,正确的方法是加入适量的NaOH溶液,使苯酚和NaOH溶液反应生成溶于水的苯酚钠,再用分液的方法分离,选项A错误;
B.碳碳双键、-CHO均能与溴水反应而使溴水褪色,不能证明丙烯醛中含有碳碳双键,选项B错误;
C.将铁锈溶于浓盐酸,反应所得溶液中含有氯离子,滴入溶液,高锰酸钾也能氧化氯离子而紫色褪去,不能证明铁锈中是否含有二价铁,选项C错误;
D.溶液不足,AgCl转化为更难溶的AgI,由实验操作和现象可知,,选项D正确;
答案选D。
4.B
【详解】与Br2发生1,4加成反应产生;
与Br2发生1,2加成反应可能产生、,而不可能反应产生;
故合理选项是B。
5.D
【详解】A.乙烯的分子式为C2H4,分子中碳原子与碳原子通过两对共用电子对相连接,碳原子与氢原子通过一对共用电子对相连接,其电子式为,故A错误;
B.是丙烷的球棍模型,丙烷主链有3个碳原子,氢原子数为8个,比例模型为:,故B错误;
C.二氧化碳为直线型结构,且碳原子半径大于氧原子,所以比例模型为,故C错误;
D.乙醇的结构简式为CH3CH2OH,所以分子式为C2H6O,故D正确;
综上所述答案为D。
6.A
【详解】A.H2O2分子结构式为H-O-O-H,故A正确;
B.氮气的电子式为,故B错误;
C.比例模型能够体现原子的大小关系,原子半径:Cl>C>H,故能表示CH4的比例模型但不能表示CCl4的比例模型,故C错误;
D.为乙烯的球棍模型,不是比例模型,故D错误;
答案选A。
7.A
【详解】A.乙烯和环丁烷(C4H8)的最简式均是CH2,28 g乙烯和环丁烷(C4H8)的混合气体中CH2的物质的量是2mol,含有的碳原子数为2NA,A正确;
B.在密闭容器中加入l.5 mol H2和0.5 mol N2,充分反应后由于可逆反应,因此可得到NH3分子数小于NA,B错误;
C.4.6 g有机物C2H6O的物质的量是0.1mol,分子中含有的C-H键数目不一定为0.5NA,如果是二甲醚,含有的C-H键数目定为0.6NA,C错误;
D.甲烷和Cl2的反应属于取代反应,乙烯和Br2的反应属于加成反应,D错误;
答案选A。
8.A
【详解】A.和分子中氢原子均有四类,其一溴代物均有4种(不考虑立体异构),A正确;
B.碳碳双键是平面形结构,CH3CH=CHCH3分子中的四个碳原子不可能在同一直线上,但可位于同一个平面上,与同一个碳碳双键的碳相连的部分均不相同,存在顺反异构,B错误;
C.按系统命名法,化合物的名称是2,3,4,4-四甲基己烷,C错误;
D.烯烃和氢气发生加成反应生成烷烃,则反过来,烷烃分子中相邻的碳原子上如果各自去掉个氢原子,就可以形成碳碳双键。根据该烷烃的结构简式可知,烯烃可能的结构有种,其中碳碳双键的位置分别是,D错误;
答案选A。
【点睛】判断有机物的取代产物的种类,可通过等效氢的判断方法确定,如果分子结构中有3种等效氢,则一元取代产物的种类就是3种,常见判断等效氢原子的方法是:①分子中同一甲基上连接的氢原子等效,②同一碳原子所连的氢原子等效,同一碳原子所连甲基上的氢原子等效,③处于镜面对称位置上的氢原子等效。
9.C
【详解】A.a分子中含有14个键,2个键,A项错误;
B.a的分子式为,苯的分子式为,二者不互为同分异构体,B项错误;
C.b中含有碳碳双键,与溴发生加成反应时,键断裂,C项正确;
D.b分子中有6种不同化学环境的氢原子,则b的一氯代物有6种,D项错误。
故选:C。
10.A
【详解】A.生成乙炔中混有硫化氢等均可被酸性高锰酸钾氧化,硫酸铜溶液除去杂质,高锰酸钾溶液褪色,能证明乙炔的还原性,选项A正确;
B.导管在碳酸钠溶液的液面下,可发生倒吸,应将导管在液面上,选项B错误;
C.乙醇在170℃发生消去反应生成乙烯,则温度计应测定液体的温度,温度计水银球插入溶液中,选项C错误;
D.酒精和水互溶,不能分液分离,应选蒸馏法,选项D错误;
答案选A。
11.A
【详解】A.桶烯分子中存在饱和碳原子,所以桶烯分子中所有原子不可能在同一平面内,故A错误;
B.根据桶烯的结构简式可知桶烯的分子式为C8H8,0.1 mol桶烯完全燃烧需要消耗氧气的物质的量为0.1 mol×(8+)=1 mol,在标准状况下的体积为22.4 L,故B正确;
C.桶烯和苯乙烯的分子式相同,都是C8H8,但桶烯和苯乙烯的结构不同,所以二者互为同分异构体,故C正确;
D.桶烯是对称结构,只有两种不同化学环境的氢原子,所以桶烯中的一个氢原子被氯原子取代,所得产物只有两种,故D正确;
故选A。
12. (CH3)2CHCH(CH2CH3)2 (CH3)3CCH(CH2CH3)CH2CH2CH2CH3 CH2=C(CH3)CH(CH3)2
【详解】(1)2-甲基-3-乙基戊烷属于烷烃,结构简式为(CH3)2CHCH(CH2CH3)2;
(2)2,2-二甲基-3-乙基庚烷属于烷烃,结构简式为(CH3)3CCH(CH2CH3)CH2CH2CH2CH3;
(3)2,3-二甲基-1-丁烯属于烯烃,结构简式为CH2=C(CH3)CH(CH3)2;
(4)2,4,6-三硝基甲苯的结构简式为;
(5)聚乙烯是乙烯加聚得到的高分子化合物,结构简式为;
(6)聚2-甲基-1,3-丁二烯是2-甲基-1,3-丁二烯加聚得到的高分子化合物,结构简式为。
13.(1)CH3CH2OH CH2=CH2↑ +H2O
(2) abad 如果第2瓶品红溶液不褪色,酸性高锰酸钾溶液褪色,则确定生成了乙烯
(3) 防倒吸 氢氧化钠溶液 吸收乙烯 在浓溴水洗气瓶之后,再连接一个盛有稀溴水的洗剂瓶,若不褪色则证明乙烯已除尽
【分析】本实验为通过无水乙醇与浓硫酸加热到170℃制取乙烯的并验证的过程,据此分析回答问题。
(1)
实验室通过无水乙醇与浓硫酸加热到170℃制取乙烯,化学反应方程式为CH3CH2OH CH2=CH2 +H2O;
(2)
①由题干可知溶液变黑时生成了C,C与浓硫酸反应生成SO2、CO2和H2O,二氧化硫与溴水、酸性高锰酸钾溶液反应,所以反应中先通入品红溶液验证二氧化硫,之后通过氢氧化钠除去二氧化硫,再通过品红溶液验证二氧化硫是否除尽,若品红不褪色,则证明二氧化硫已除尽,最后通过酸性高锰酸钾溶液,酸性高锰酸钾溶液与乙烯发生氧化还原反应而褪色,故顺序依次是abad;
②由以上分析可知,如果第2瓶品红溶液不褪色,酸性高锰酸钾溶液褪色,则确定生成了乙烯;
(3)
①如果酒精灯熄灭导致温度降低,装置内大气压小于外界大气压,会引起倒吸现象,所以装置a的作用是防倒吸;
②二氧化硫和二氧化碳可以和强碱溶液反应,所以装置b中应该盛放的试剂是氢氧化钠溶液;
③反应过程中生成的乙烯也可以燃烧生成二氧化碳和水,会影响一氧化碳的鉴别,故浓溴水的作用是吸收乙烯;
④验证乙烯是否除尽,可以在浓溴水洗气瓶之后,再连接一个盛有稀溴水的洗剂瓶,若不褪色则证明乙烯已除尽。
14. CH2=CH2 CH3CH3 CH3CH2Cl CH3CH2OH CH2=CH2+H2O CH3CH2OH 加成反应 nCH2=CH2 加聚反应
【分析】根据题意可知:A是乙烯:CH2=CH2;A与H2在Ni作催化剂时发生加成反应得到B:乙烷CH3CH3;A与H2O在稀硫酸作用下发生加成反应得到D乙醇:CH3CH2OH;与HCl在一定条件下发生加成反应得到C氯乙烷:CH3CH2Cl;B乙烷与Cl2在光照下发生取代反应得到氯乙烷:CH3CH2Cl;乙烯在催化剂作用下还可发生加聚反应生产E,E为聚乙烯: ,据此分析解答。
【详解】(1)根据分析,A是乙烯,结构简式为:CH2=CH2;B是乙烷,结构简式为:CH3CH3;C是氯乙烷,结构简式为:CH3CH2Cl;D是乙醇,结构简式为:CH3CH2OH;
(2)反应③为乙烯与H2O在稀硫酸作用下发生加成反应得到乙醇,化学反应方程式为:CH2=CH2+H2O CH3CH2OH;
反应④乙烯在催化剂作用下还可发生加聚反应生产聚乙烯,化学反应方程式为:nCH2=CH2。
答案第1页,共2页
答案第1页,共2页
1.下列反应属于加成反应的是
A.乙醇与钠反应生成乙醇钠和氢气 B.乙烯与溴单质反应生成1,2-二溴乙烷
C.乙酸与乙醇反应生成乙酸乙酯和水 D.甲烷与氯气反应生成一氯甲烷和氯化氢
2.兴趣小组用乙醇和浓硫酸制取乙烯,并验证乙烯气体的生成,所用实验装置如图所示。下列说法正确的是
A.装置A烧瓶中应加入浓硫酸、再沿烧瓶内壁缓慢加入乙醇
B.反应时应迅速升温到170℃,并控制温度保持不变
C.为除去乙烯中混有的SO2杂质,装置B洗气瓶中应装入酸性KMnO4溶液
D.实验中有少量副产物乙醚生成,分离乙醇和乙醚的混合物可以采用分液的方法
3.下列说法正确的是
A.除去苯中含有的少量苯酚,可向其中加入溴水,然后分液
B.向丙烯醛中加入溴水,溴水褪色,证明丙烯醛中含有碳碳双键
C.将铁锈溶于浓盐酸,滴入溶液,紫色褪去,证明铁锈中含有二价铁
D.向盛有2mL0.1mol/LNaCl溶液的试管中,滴加2滴0.1mol/L溶液,振荡,然后继续滴加4滴0.1mol/LKI溶液,观察到白色沉淀转化为黄色,说明(AgCl)>(AgI)
4.已知1,3-丁二烯可发生反应:CH2=CH-CH=CH2+Br2→BrCH2-CH=CH-CH2Br。有机物能使溴水褪色,它与溴发生等物质的量加成反应时生成物不可能是
A. B.
C. D.
5.下列化学用语表达正确的是( )
A.乙烯的电子式: B.丙烷分子的比例模型:
C.CO2分子球棍模型: D.乙醇的分子式:C2H6O
6.下列化学用语或模型表示正确的是( )
A.H2O2分子结构式:H-O-O-H
B.氮气的电子式:
C.比例模型:可以表示甲烷分子,也可以表示四氯化碳分子
D.C2H4分子比例模型:
7.用NA表示阿伏加德罗常数的值。下列与有机物的结构、性质有关的叙述正确的是
A.28g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA
B.在密闭容器中加入1.5mol H2和0.5molN2,充分反应后可得到NH3分子数为NA
C.4.6g有机物C2H6O的分子中含有的C-H键数目一定为0.5NA
D.甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应
8.下列说法正确的是
A. 的一溴代物和的一溴代物都有4种(不考虑立体异构)
B.分子中的4个碳原子在同一直线上,且存在顺反异构体
C.按系统命名法,化合物的名称是2,3,4-三甲基-2-乙基戊烷
D.由单烯烃和氢气加成制得,则对应的单烯烃有5种
9.已知有机物a和b的结构简式分别为和。下列说法正确的是(不考虑立体异构)
A.a分子中含有6个键,2个键 B.a与苯互为同分异构体
C.b可使溴水褪色,反应时键断裂 D.b的一氯代物有5种
10.下列实验装置或操作正确的是
A.验证乙炔的还原性 B.实验室制取乙酸乙酯 C.实验室制乙烯 D.分离酒精和水
A.A B.B C.C D.D
11.桶烯(Barrelene)键线式如图所示,下列有关说法不正确的是
A.桶烯分子中所有原子在同一平面内
B.0.1 mol桶烯完全燃烧需要消耗氧气22.4 L(标准状况)
C.桶烯与苯乙烯(C6H5CH=CH2)互为同分异构体
D.桶烯中的一个氢原子被氯原子取代,所得产物只有两种
12.写出下列有机物的结构简式
(1)2-甲基-3-乙基戊烷________________;
(2)2,2-二甲基-3-乙基庚烷________________;
(3)2,3-二甲基-1-丁烯________________;
(4)2,4,6-三硝基甲苯________________;
(5)聚乙烯________________;
(6)聚2-甲基-1,3-丁二烯________________。
13.实验室制取乙烯的装置如图Ⅰ所示。根据实验及有关操作回答下列问题。
(1)甲同学按照如图Ⅰ所示的实验装置进行了实验。当温度升至170℃左右时,有大量气体产生,产生的气体通入溴水中,溴水的颜色迅速褪去。甲同学认为达到了实验目的,写出烧瓶中发生反应的化学方程式:___。
(2)乙同学仔细考察了甲同学的整个实验过程,发现当温度升到100℃左右时,无色液体开始变色,到160℃左右时,混合液全呈黑色,在超过170℃后生成气体速度明显加快,生成的气体有刺激性气味。由此他推出,产生的气体中应有某杂质,可能影响乙烯的检验,必须除去。乙同学设计了如图Ⅱ所示的实验装置进行实验。请回答:
①Ⅱ装置abcd中可盛放的试剂的顺序依次是____(填序号)。
a.品红溶液 b.NaOH溶液 c.浓硫酸 d.酸性KMnO4溶液
②乙设计的实验中能确定生成了乙烯的现象是____。
(3)丙同学根据甲、乙同学的分析,认为还可能有CO、CO2两种气体产生。为证明CO的存在,他设计了如图Ⅲ所示过程(假设该过程可把实验中产生的有机产物除净),发现最后气体经点燃产生蓝色火焰,确认有一氧化碳生成。
①图Ⅲ中装置a的作用是____。
②为除去混合气中的SO2和CO2,装置b中应该盛放的试剂是____。
③浓溴水的作用是____。
④丙同学认为该装置还需添加一个装置验证杂质气体是否除净,该操作是____。
14.某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应.
根据如图回答下列问题:
(1)写出A、B、C、D的结构简式:
A__,B__,C__,D__。
(2)写出③④两步反应的化学方程式,并注明反应类型:
③__(反应类型__)。
④__(反应类型__)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
【详解】A.乙醇与钠反应生成乙醇钠和氢气的反应属于置换反应,A不符合题意;
B.乙烯与溴单质反应生成1,2-二溴乙烷的反应为加成反应,B符合题意;
C.乙酸与乙醇反应生成乙酸乙酯和水的反应为酯化反应,酯化反应属于取代反应,C不符合题意;
D.甲烷与氯气反应生成一氯甲烷和氯化氢的反应为取代反应,D不符合题意;
故合理选项是B。
2.B
【详解】A.装置A应先加入乙醇,然后再沿烧瓶内壁缓慢加入浓硫酸,故A错误;
B.浓硫酸和乙醇在140℃会生成乙醚,因此制取乙烯时,应迅速升温到170℃,并控制温度保持不变,故B正确;
C.乙烯容易被酸性KMnO4溶液氧化,因此装置B洗气瓶中不能装入酸性KMnO4溶液,故C错误;
D.乙醇和乙醚是互溶的,则乙醇和乙醚的混合物不可以采用分液的方法,故D错误;
本题答案B。
3.D
【详解】A.苯是一种良好的有机溶剂,既能溶解溴单质,又能溶解三溴苯酚,因此在苯酚的苯溶液中加浓溴水是不能除去苯酚的,正确的方法是加入适量的NaOH溶液,使苯酚和NaOH溶液反应生成溶于水的苯酚钠,再用分液的方法分离,选项A错误;
B.碳碳双键、-CHO均能与溴水反应而使溴水褪色,不能证明丙烯醛中含有碳碳双键,选项B错误;
C.将铁锈溶于浓盐酸,反应所得溶液中含有氯离子,滴入溶液,高锰酸钾也能氧化氯离子而紫色褪去,不能证明铁锈中是否含有二价铁,选项C错误;
D.溶液不足,AgCl转化为更难溶的AgI,由实验操作和现象可知,,选项D正确;
答案选D。
4.B
【详解】与Br2发生1,4加成反应产生;
与Br2发生1,2加成反应可能产生、,而不可能反应产生;
故合理选项是B。
5.D
【详解】A.乙烯的分子式为C2H4,分子中碳原子与碳原子通过两对共用电子对相连接,碳原子与氢原子通过一对共用电子对相连接,其电子式为,故A错误;
B.是丙烷的球棍模型,丙烷主链有3个碳原子,氢原子数为8个,比例模型为:,故B错误;
C.二氧化碳为直线型结构,且碳原子半径大于氧原子,所以比例模型为,故C错误;
D.乙醇的结构简式为CH3CH2OH,所以分子式为C2H6O,故D正确;
综上所述答案为D。
6.A
【详解】A.H2O2分子结构式为H-O-O-H,故A正确;
B.氮气的电子式为,故B错误;
C.比例模型能够体现原子的大小关系,原子半径:Cl>C>H,故能表示CH4的比例模型但不能表示CCl4的比例模型,故C错误;
D.为乙烯的球棍模型,不是比例模型,故D错误;
答案选A。
7.A
【详解】A.乙烯和环丁烷(C4H8)的最简式均是CH2,28 g乙烯和环丁烷(C4H8)的混合气体中CH2的物质的量是2mol,含有的碳原子数为2NA,A正确;
B.在密闭容器中加入l.5 mol H2和0.5 mol N2,充分反应后由于可逆反应,因此可得到NH3分子数小于NA,B错误;
C.4.6 g有机物C2H6O的物质的量是0.1mol,分子中含有的C-H键数目不一定为0.5NA,如果是二甲醚,含有的C-H键数目定为0.6NA,C错误;
D.甲烷和Cl2的反应属于取代反应,乙烯和Br2的反应属于加成反应,D错误;
答案选A。
8.A
【详解】A.和分子中氢原子均有四类,其一溴代物均有4种(不考虑立体异构),A正确;
B.碳碳双键是平面形结构,CH3CH=CHCH3分子中的四个碳原子不可能在同一直线上,但可位于同一个平面上,与同一个碳碳双键的碳相连的部分均不相同,存在顺反异构,B错误;
C.按系统命名法,化合物的名称是2,3,4,4-四甲基己烷,C错误;
D.烯烃和氢气发生加成反应生成烷烃,则反过来,烷烃分子中相邻的碳原子上如果各自去掉个氢原子,就可以形成碳碳双键。根据该烷烃的结构简式可知,烯烃可能的结构有种,其中碳碳双键的位置分别是,D错误;
答案选A。
【点睛】判断有机物的取代产物的种类,可通过等效氢的判断方法确定,如果分子结构中有3种等效氢,则一元取代产物的种类就是3种,常见判断等效氢原子的方法是:①分子中同一甲基上连接的氢原子等效,②同一碳原子所连的氢原子等效,同一碳原子所连甲基上的氢原子等效,③处于镜面对称位置上的氢原子等效。
9.C
【详解】A.a分子中含有14个键,2个键,A项错误;
B.a的分子式为,苯的分子式为,二者不互为同分异构体,B项错误;
C.b中含有碳碳双键,与溴发生加成反应时,键断裂,C项正确;
D.b分子中有6种不同化学环境的氢原子,则b的一氯代物有6种,D项错误。
故选:C。
10.A
【详解】A.生成乙炔中混有硫化氢等均可被酸性高锰酸钾氧化,硫酸铜溶液除去杂质,高锰酸钾溶液褪色,能证明乙炔的还原性,选项A正确;
B.导管在碳酸钠溶液的液面下,可发生倒吸,应将导管在液面上,选项B错误;
C.乙醇在170℃发生消去反应生成乙烯,则温度计应测定液体的温度,温度计水银球插入溶液中,选项C错误;
D.酒精和水互溶,不能分液分离,应选蒸馏法,选项D错误;
答案选A。
11.A
【详解】A.桶烯分子中存在饱和碳原子,所以桶烯分子中所有原子不可能在同一平面内,故A错误;
B.根据桶烯的结构简式可知桶烯的分子式为C8H8,0.1 mol桶烯完全燃烧需要消耗氧气的物质的量为0.1 mol×(8+)=1 mol,在标准状况下的体积为22.4 L,故B正确;
C.桶烯和苯乙烯的分子式相同,都是C8H8,但桶烯和苯乙烯的结构不同,所以二者互为同分异构体,故C正确;
D.桶烯是对称结构,只有两种不同化学环境的氢原子,所以桶烯中的一个氢原子被氯原子取代,所得产物只有两种,故D正确;
故选A。
12. (CH3)2CHCH(CH2CH3)2 (CH3)3CCH(CH2CH3)CH2CH2CH2CH3 CH2=C(CH3)CH(CH3)2
【详解】(1)2-甲基-3-乙基戊烷属于烷烃,结构简式为(CH3)2CHCH(CH2CH3)2;
(2)2,2-二甲基-3-乙基庚烷属于烷烃,结构简式为(CH3)3CCH(CH2CH3)CH2CH2CH2CH3;
(3)2,3-二甲基-1-丁烯属于烯烃,结构简式为CH2=C(CH3)CH(CH3)2;
(4)2,4,6-三硝基甲苯的结构简式为;
(5)聚乙烯是乙烯加聚得到的高分子化合物,结构简式为;
(6)聚2-甲基-1,3-丁二烯是2-甲基-1,3-丁二烯加聚得到的高分子化合物,结构简式为。
13.(1)CH3CH2OH CH2=CH2↑ +H2O
(2) abad 如果第2瓶品红溶液不褪色,酸性高锰酸钾溶液褪色,则确定生成了乙烯
(3) 防倒吸 氢氧化钠溶液 吸收乙烯 在浓溴水洗气瓶之后,再连接一个盛有稀溴水的洗剂瓶,若不褪色则证明乙烯已除尽
【分析】本实验为通过无水乙醇与浓硫酸加热到170℃制取乙烯的并验证的过程,据此分析回答问题。
(1)
实验室通过无水乙醇与浓硫酸加热到170℃制取乙烯,化学反应方程式为CH3CH2OH CH2=CH2 +H2O;
(2)
①由题干可知溶液变黑时生成了C,C与浓硫酸反应生成SO2、CO2和H2O,二氧化硫与溴水、酸性高锰酸钾溶液反应,所以反应中先通入品红溶液验证二氧化硫,之后通过氢氧化钠除去二氧化硫,再通过品红溶液验证二氧化硫是否除尽,若品红不褪色,则证明二氧化硫已除尽,最后通过酸性高锰酸钾溶液,酸性高锰酸钾溶液与乙烯发生氧化还原反应而褪色,故顺序依次是abad;
②由以上分析可知,如果第2瓶品红溶液不褪色,酸性高锰酸钾溶液褪色,则确定生成了乙烯;
(3)
①如果酒精灯熄灭导致温度降低,装置内大气压小于外界大气压,会引起倒吸现象,所以装置a的作用是防倒吸;
②二氧化硫和二氧化碳可以和强碱溶液反应,所以装置b中应该盛放的试剂是氢氧化钠溶液;
③反应过程中生成的乙烯也可以燃烧生成二氧化碳和水,会影响一氧化碳的鉴别,故浓溴水的作用是吸收乙烯;
④验证乙烯是否除尽,可以在浓溴水洗气瓶之后,再连接一个盛有稀溴水的洗剂瓶,若不褪色则证明乙烯已除尽。
14. CH2=CH2 CH3CH3 CH3CH2Cl CH3CH2OH CH2=CH2+H2O CH3CH2OH 加成反应 nCH2=CH2 加聚反应
【分析】根据题意可知:A是乙烯:CH2=CH2;A与H2在Ni作催化剂时发生加成反应得到B:乙烷CH3CH3;A与H2O在稀硫酸作用下发生加成反应得到D乙醇:CH3CH2OH;与HCl在一定条件下发生加成反应得到C氯乙烷:CH3CH2Cl;B乙烷与Cl2在光照下发生取代反应得到氯乙烷:CH3CH2Cl;乙烯在催化剂作用下还可发生加聚反应生产E,E为聚乙烯: ,据此分析解答。
【详解】(1)根据分析,A是乙烯,结构简式为:CH2=CH2;B是乙烷,结构简式为:CH3CH3;C是氯乙烷,结构简式为:CH3CH2Cl;D是乙醇,结构简式为:CH3CH2OH;
(2)反应③为乙烯与H2O在稀硫酸作用下发生加成反应得到乙醇,化学反应方程式为:CH2=CH2+H2O CH3CH2OH;
反应④乙烯在催化剂作用下还可发生加聚反应生产聚乙烯,化学反应方程式为:nCH2=CH2。
答案第1页,共2页
答案第1页,共2页
