3.3-1 金属晶体 课件(共21张PPT) 2022-2023学年高二下学期化学人教版(2019)选择性必修2
文档属性
| 名称 | 3.3-1 金属晶体 课件(共21张PPT) 2022-2023学年高二下学期化学人教版(2019)选择性必修2 |  | |
| 格式 | zip | ||
| 文件大小 | 2.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-23 15:38:14 | ||
图片预览





文档简介
(共21张PPT)
3.3 金属晶体与离子晶体
3.3-1 金属晶体
2
学习目标
1、了解金属键的含义,
2、能用金属键理论解释金属的物理性质
1
金属键与金属晶体
(一)金属键
1.电子气理论
①金属原子最外层电子脱落形成自由电子。
2.金属键
(1)定义:
金属阳离子和自由电子之间的较强作用(静电作用)
(2)特征:
无方向性与饱和性。
③电子在整个金属中自由移动。形成“电子气”把金属阳离子维系在一起。
②金属中存在粒子为:
(3)强弱判断:
金属离子所带电荷越多、半径越小,金属键越强
金属阳离子与自由电子。
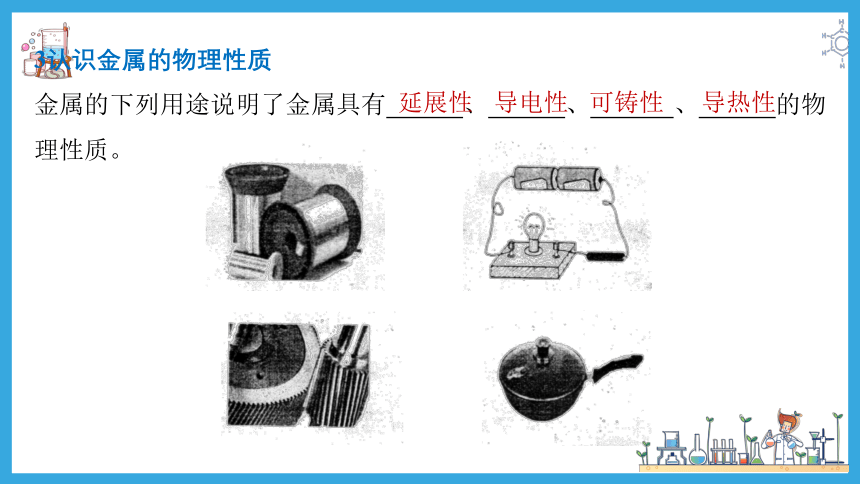
3认识金属的物理性质
金属的下列用途说明了金属具有 、 、 、 的物理性质。
延展性
导电性
可铸性
导热性
3、物理特性与结构的关系
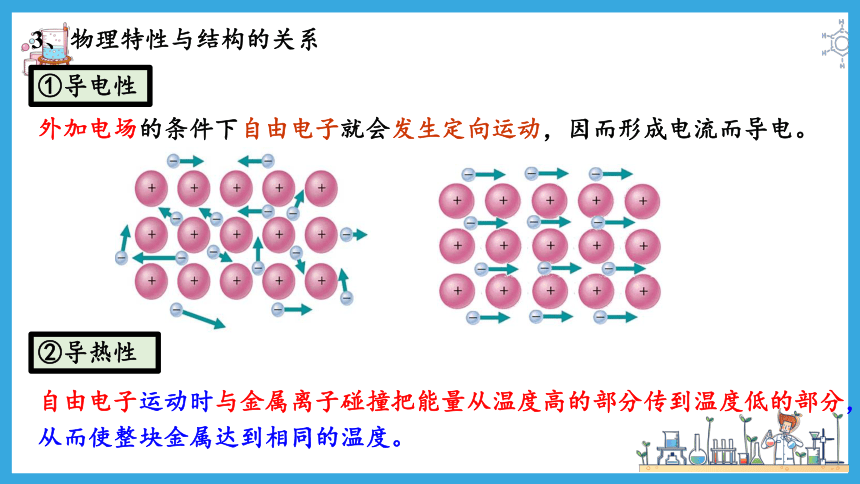
①导电性
外加电场的条件下自由电子就会发生定向运动,因而形成电流而导电。
②导热性
自由电子运动时与金属离子碰撞把能量从温度高的部分传到温度低的部分,从而使整块金属达到相同的温度。
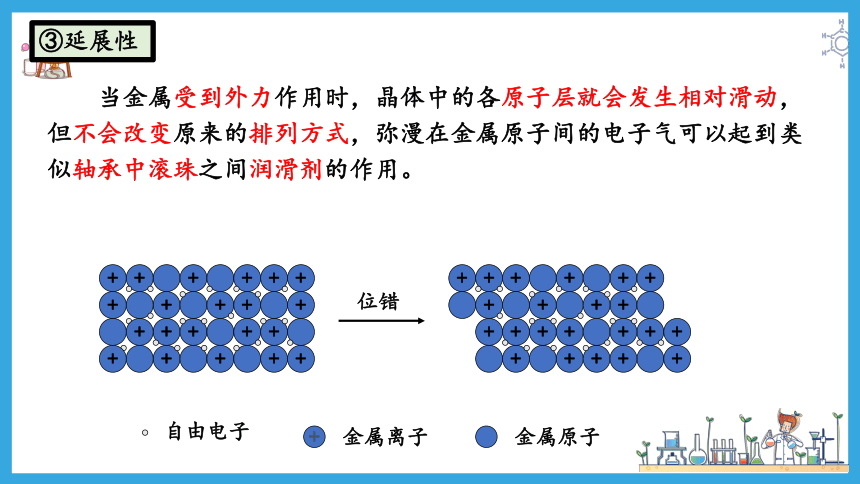
③延展性
当金属受到外力作用时,晶体中的各原子层就会发生相对滑动,但不会改变原来的排列方式,弥漫在金属原子间的电子气可以起到类似轴承中滚珠之间润滑剂的作用。
自由电子
+
金属离子
金属原子
位错
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
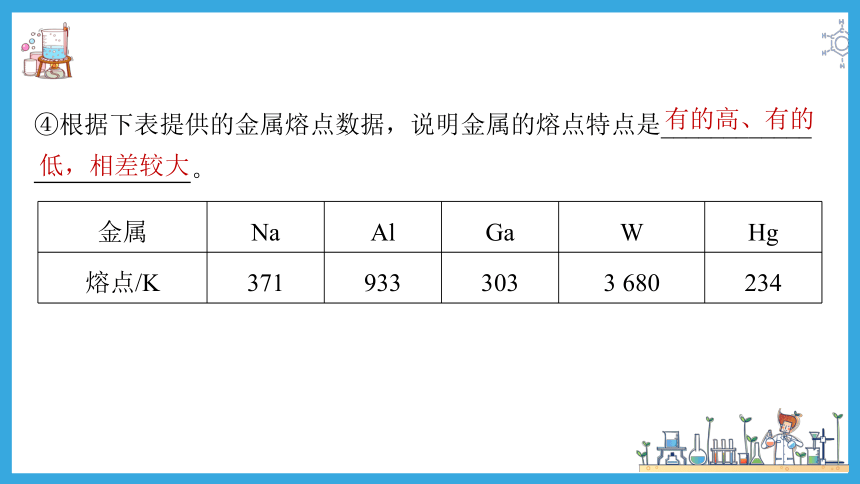
④根据下表提供的金属熔点数据,说明金属的熔点特点是____________
。
有的高、有的
低,相差较大
金属 Na Al Ga W Hg
熔点/K 371 933 303 3 680 234
1.用“电子气理论”解释金属晶体的下列性质。
(1)延展性
深度思考
提示 当金属受到外力作用时,晶体中的各原子层就会发生相对滑动,但排列方式不变,金属离子与自由电子形成的金属键没有被破坏,所以金属具有良好的延展性。
(2)导电性
提示 在外加电场的作用下,金属晶体中的自由电子做定向移动形成电流,呈现良好的导电性。
(3)导热性
提示 电子气中的自由电子在热的作用下与金属原子碰撞,从而引起两者能量的交换。
2.影响金属键强弱的因素有哪些?金属键的强弱对物质的性质有哪些影响?
提示 金属键的强弱与离子半径、离子所带电荷数有关。离子半径越小,离子所带的电荷数越多,则金属键越强,金属的熔点越高、硬度越大。
3.比较镁和铝的熔点高低,并用原子结构与金属键理论加以解释?
提示 铝的熔点比镁高。因为铝的原子半径小、价电子数多,金属键强。
1、金属晶体:金属单质、金属晶体
2、金属晶体中含有金属阳离子、电子、但无阴离子
3、金属晶体导电原因与电解质溶液不同。
4、微粒间作用力:金属键
组成粒子:金属阳离子和自由电子
5、影响金属键强弱的影响因素:
一般情况下,金属晶体熔点由金属键强弱决定:
金属阳离子半径越小,所带电荷越多,自由电子越多,金属键越强,熔点就相应越高,硬度也越大。
注 意:
晶体类型 电解质 金属晶体
导电时的状态
导电粒子
导电时发生的变化
导电能力随温度的变化
水溶液或熔融状态下
晶体状态
自由移动的离子
自由电子
电解质在熔化状态或溶于水能导电与金属导电的异同
化学变化
物理变化
增强
减弱
1、已知碱金属元素的熔沸点随原子序数增大而递减,试用金属键理论加以解释。
同主族元素价电子数相同(阳离子所带电荷数相同),从上到下,原子(离子)半径依次增大,则单质中所形成金属键依次减弱,故碱金属元素的熔沸点随原子序数的增大而递减。
新思想在线
2、试判断钠、镁、铝三种金属熔沸点和硬度的大小
同周期元素,从左到右,价电子数依次增大,原子(离子)半径依次减弱,则单质中所形成金属键依次增强,故钠、镁、铝三种金属熔沸点和硬度的大小顺序是:钠<镁<铝。
3
当堂训练
1.下列有关金属键的叙述错误的是
A.金属键没有饱和性和方向性
B.金属键是金属阳离子和自由电子间的强烈的静电吸引作用
C.自由电子属于整块金属
D.金属的物理性质和金属固体的形成都与金属键有关
√
2.“神九”载人飞船上使用了锂镁合金和锂铝合金等合金材料,下列有关叙述不正确的是
A.飞船使用的合金材料,一般具有质量轻、强度高的特点
B.锂铝合金中铝、锂的金属性不如钠强
C.锂镁合金和锂铝合金性质相当稳定,不会与酸发生化学反应
D.锂镁合金是一种具有金属特性的物质,易导热、导电
√
3.石墨烯是从石墨材料中剥离出来的由碳原子组成的只有一层原子厚度的二维晶体。其结构如图:
下列有关说法正确的是
A.石墨烯中碳原子的杂化方
式为sp3杂化
B.石墨烯中平均每个六元碳
环含有3个碳原子
C.从石墨中剥离石墨烯需要破坏化学键
D.石墨烯具有导电性
√
返回
4.下列关于金属键的叙述不正确的是
A.金属键是金属阳离子和自由电子这两种带异性电荷的微粒间的强烈相
互作用,其实质与离子键类似,也是一种电性作用
B.金属键可以看作是许多原子共用许多电子所形成的强烈的相互作用,
所以与共价键类似,也有方向性和饱和性
C.金属键是带异性电荷的金属阳离子和自由电子间的相互作用,故金属
键无饱和性和方向性
D.构成金属键的自由电子在整个金属内部的三维空间中做自由运动
√
11.回答下列问题:
(1)根据下列叙述,判断一定为金属晶体的是_____(填字母,下同)。
A.由分子间作用力形成,熔点很低
B.由共价键结合形成网状晶体,熔点很高
C.固体有良好的导电性、导热性和延展性
解析 A项属于分子晶体;
B项属于原子晶体;
而C项是金属的通性。
C
综合强化
返回
(2)下列有关金属晶体的叙述正确的是________。
A.常温下,金属单质都以金属晶体形式存在
B.钙的熔、沸点高于钾
C.金属具有良好的导热性能,是因为自由电子在受热后,加快了运动速
率,自由电子通过与金属原子发生碰撞,传递了能量
D.金属具有良好的导电性,是因为在金属晶体中共享了金属原子的价电
子,形成了“电子气”,在外电场的作用下自由电子定向移动便形成
了电流,所以金属易导电
E.温度越高,金属的导电性越好
F.金属晶体具有良好的延展性,是因为金属晶体中的原子层可以滑动而
不破坏金属键
BCDF
学习小结
返回
3.3 金属晶体与离子晶体
3.3-1 金属晶体
2
学习目标
1、了解金属键的含义,
2、能用金属键理论解释金属的物理性质
1
金属键与金属晶体
(一)金属键
1.电子气理论
①金属原子最外层电子脱落形成自由电子。
2.金属键
(1)定义:
金属阳离子和自由电子之间的较强作用(静电作用)
(2)特征:
无方向性与饱和性。
③电子在整个金属中自由移动。形成“电子气”把金属阳离子维系在一起。
②金属中存在粒子为:
(3)强弱判断:
金属离子所带电荷越多、半径越小,金属键越强
金属阳离子与自由电子。
3认识金属的物理性质
金属的下列用途说明了金属具有 、 、 、 的物理性质。
延展性
导电性
可铸性
导热性
3、物理特性与结构的关系
①导电性
外加电场的条件下自由电子就会发生定向运动,因而形成电流而导电。
②导热性
自由电子运动时与金属离子碰撞把能量从温度高的部分传到温度低的部分,从而使整块金属达到相同的温度。
③延展性
当金属受到外力作用时,晶体中的各原子层就会发生相对滑动,但不会改变原来的排列方式,弥漫在金属原子间的电子气可以起到类似轴承中滚珠之间润滑剂的作用。
自由电子
+
金属离子
金属原子
位错
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
④根据下表提供的金属熔点数据,说明金属的熔点特点是____________
。
有的高、有的
低,相差较大
金属 Na Al Ga W Hg
熔点/K 371 933 303 3 680 234
1.用“电子气理论”解释金属晶体的下列性质。
(1)延展性
深度思考
提示 当金属受到外力作用时,晶体中的各原子层就会发生相对滑动,但排列方式不变,金属离子与自由电子形成的金属键没有被破坏,所以金属具有良好的延展性。
(2)导电性
提示 在外加电场的作用下,金属晶体中的自由电子做定向移动形成电流,呈现良好的导电性。
(3)导热性
提示 电子气中的自由电子在热的作用下与金属原子碰撞,从而引起两者能量的交换。
2.影响金属键强弱的因素有哪些?金属键的强弱对物质的性质有哪些影响?
提示 金属键的强弱与离子半径、离子所带电荷数有关。离子半径越小,离子所带的电荷数越多,则金属键越强,金属的熔点越高、硬度越大。
3.比较镁和铝的熔点高低,并用原子结构与金属键理论加以解释?
提示 铝的熔点比镁高。因为铝的原子半径小、价电子数多,金属键强。
1、金属晶体:金属单质、金属晶体
2、金属晶体中含有金属阳离子、电子、但无阴离子
3、金属晶体导电原因与电解质溶液不同。
4、微粒间作用力:金属键
组成粒子:金属阳离子和自由电子
5、影响金属键强弱的影响因素:
一般情况下,金属晶体熔点由金属键强弱决定:
金属阳离子半径越小,所带电荷越多,自由电子越多,金属键越强,熔点就相应越高,硬度也越大。
注 意:
晶体类型 电解质 金属晶体
导电时的状态
导电粒子
导电时发生的变化
导电能力随温度的变化
水溶液或熔融状态下
晶体状态
自由移动的离子
自由电子
电解质在熔化状态或溶于水能导电与金属导电的异同
化学变化
物理变化
增强
减弱
1、已知碱金属元素的熔沸点随原子序数增大而递减,试用金属键理论加以解释。
同主族元素价电子数相同(阳离子所带电荷数相同),从上到下,原子(离子)半径依次增大,则单质中所形成金属键依次减弱,故碱金属元素的熔沸点随原子序数的增大而递减。
新思想在线
2、试判断钠、镁、铝三种金属熔沸点和硬度的大小
同周期元素,从左到右,价电子数依次增大,原子(离子)半径依次减弱,则单质中所形成金属键依次增强,故钠、镁、铝三种金属熔沸点和硬度的大小顺序是:钠<镁<铝。
3
当堂训练
1.下列有关金属键的叙述错误的是
A.金属键没有饱和性和方向性
B.金属键是金属阳离子和自由电子间的强烈的静电吸引作用
C.自由电子属于整块金属
D.金属的物理性质和金属固体的形成都与金属键有关
√
2.“神九”载人飞船上使用了锂镁合金和锂铝合金等合金材料,下列有关叙述不正确的是
A.飞船使用的合金材料,一般具有质量轻、强度高的特点
B.锂铝合金中铝、锂的金属性不如钠强
C.锂镁合金和锂铝合金性质相当稳定,不会与酸发生化学反应
D.锂镁合金是一种具有金属特性的物质,易导热、导电
√
3.石墨烯是从石墨材料中剥离出来的由碳原子组成的只有一层原子厚度的二维晶体。其结构如图:
下列有关说法正确的是
A.石墨烯中碳原子的杂化方
式为sp3杂化
B.石墨烯中平均每个六元碳
环含有3个碳原子
C.从石墨中剥离石墨烯需要破坏化学键
D.石墨烯具有导电性
√
返回
4.下列关于金属键的叙述不正确的是
A.金属键是金属阳离子和自由电子这两种带异性电荷的微粒间的强烈相
互作用,其实质与离子键类似,也是一种电性作用
B.金属键可以看作是许多原子共用许多电子所形成的强烈的相互作用,
所以与共价键类似,也有方向性和饱和性
C.金属键是带异性电荷的金属阳离子和自由电子间的相互作用,故金属
键无饱和性和方向性
D.构成金属键的自由电子在整个金属内部的三维空间中做自由运动
√
11.回答下列问题:
(1)根据下列叙述,判断一定为金属晶体的是_____(填字母,下同)。
A.由分子间作用力形成,熔点很低
B.由共价键结合形成网状晶体,熔点很高
C.固体有良好的导电性、导热性和延展性
解析 A项属于分子晶体;
B项属于原子晶体;
而C项是金属的通性。
C
综合强化
返回
(2)下列有关金属晶体的叙述正确的是________。
A.常温下,金属单质都以金属晶体形式存在
B.钙的熔、沸点高于钾
C.金属具有良好的导热性能,是因为自由电子在受热后,加快了运动速
率,自由电子通过与金属原子发生碰撞,传递了能量
D.金属具有良好的导电性,是因为在金属晶体中共享了金属原子的价电
子,形成了“电子气”,在外电场的作用下自由电子定向移动便形成
了电流,所以金属易导电
E.温度越高,金属的导电性越好
F.金属晶体具有良好的延展性,是因为金属晶体中的原子层可以滑动而
不破坏金属键
BCDF
学习小结
返回
