2023年高三化学实验专题——物质制备型实验 课件(共20张PPT)
文档属性
| 名称 | 2023年高三化学实验专题——物质制备型实验 课件(共20张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 17.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-24 00:00:00 | ||
图片预览


文档简介
(共20张PPT)
高三化学实验专题——物质制备型实验
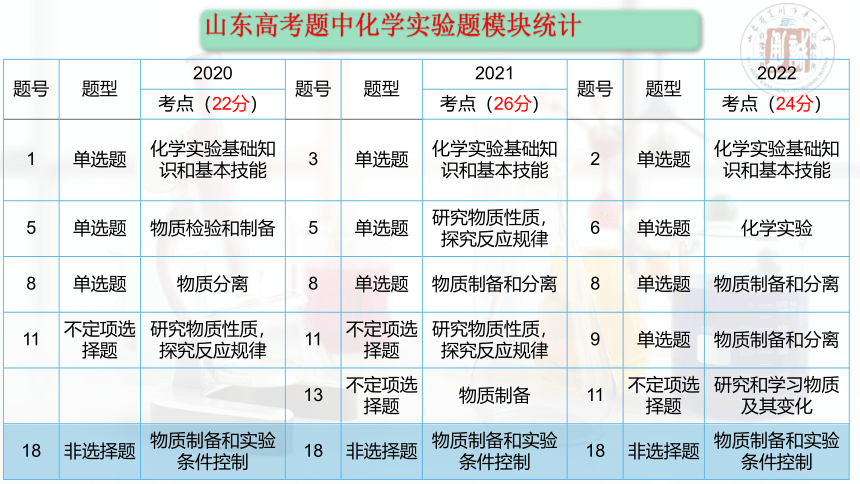
山东高考题中化学实验题模块统计
题号 题型 2020 题号 题型 2021 题号 题型 2022
考点(22分) 考点(26分) 考点(24分)
1 单选题 化学实验基础知识和基本技能 3 单选题 化学实验基础知识和基本技能 2 单选题 化学实验基础知识和基本技能
5 单选题 物质检验和制备 5 单选题 研究物质性质,探究反应规律 6 单选题 化学实验
8 单选题 物质分离 8 单选题 物质制备和分离 8 单选题 物质制备和分离
11 不定项选择题 研究物质性质,探究反应规律 11 不定项选择题 研究物质性质,探究反应规律 9 单选题 物质制备和分离
13 不定项选择题 物质制备 11 不定项选择题 研究和学习物质及其变化
18 非选择题 物质制备和实验条件控制 18 非选择题 物质制备和实验条件控制 18 非选择题 物质制备和实验条件控制
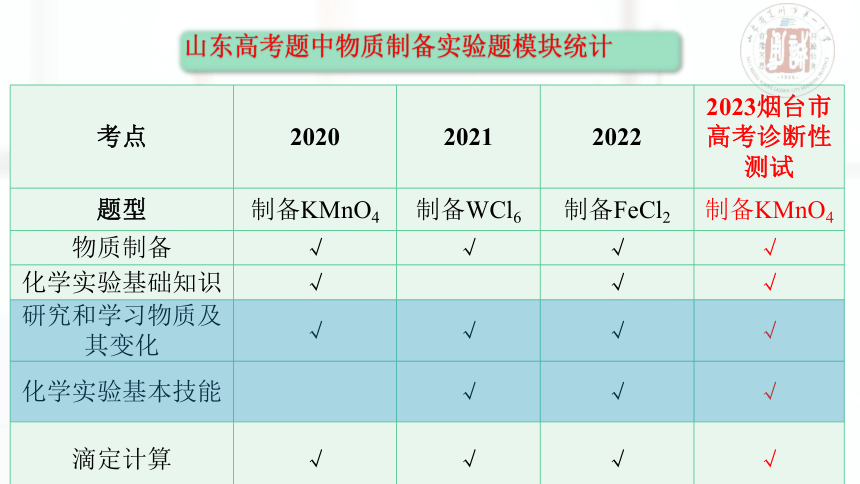
考点 2020 2021 2022 2023烟台市高考诊断性测试
题型 制备KMnO4 制备WCl6 制备FeCl2 制备KMnO4
物质制备 √ √ √ √
化学实验基础知识 √ √ √
研究和学习物质及其变化 √ √ √ √
化学实验基本技能 √ √ √
滴定计算 √ √ √ √
山东高考题中物质制备实验题模块统计
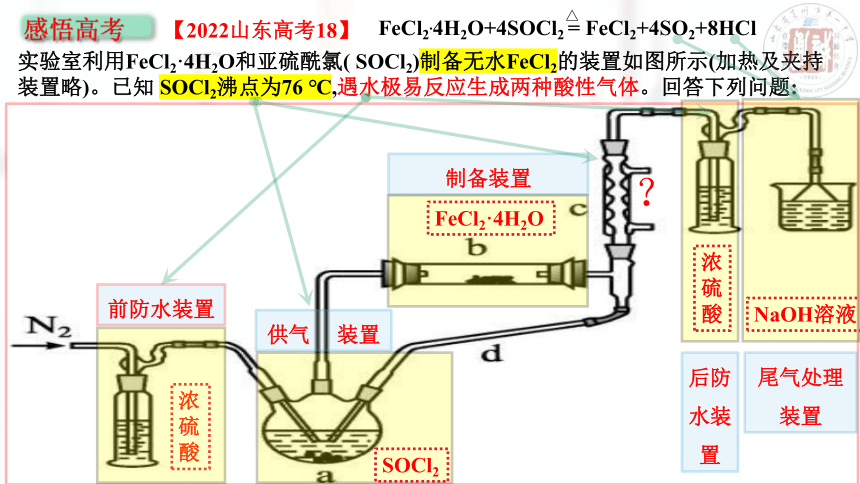
【2022山东高考18】
实验室利用FeCl2·4H2O和亚硫酰氯( SOCl2)制备无水FeCl2的装置如图所示(加热及夹持装置略)。已知 SOCl2沸点为76 ℃,遇水极易反应生成两种酸性气体。回答下列问题:
供气 装置
浓硫酸
SOCl2
制备装置
后防水装置
尾气处理装置
FeCl2.4H2O+4SOCl2 = FeCl2+4SO2+8HCl
FeCl2·4H2O
浓硫酸
NaOH溶液
?
△
感悟高考
前防水装置
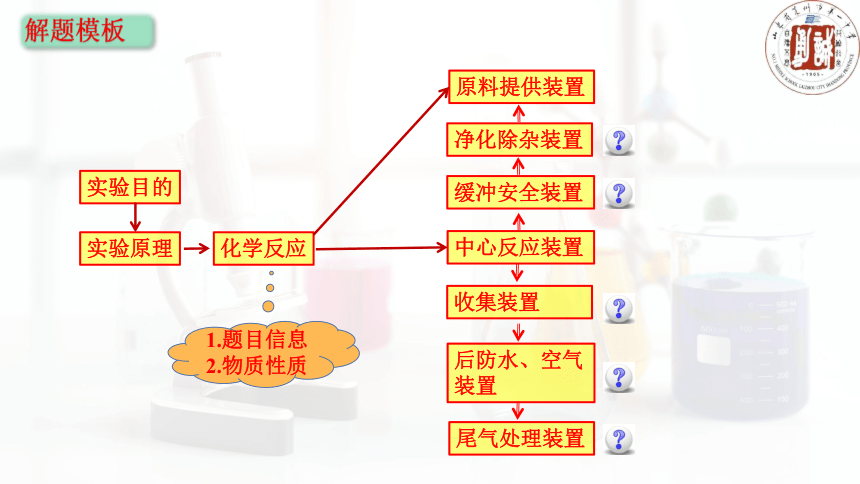
原料提供装置
缓冲安全装置
净化除杂装置
中心反应装置
后防水、空气装置
尾气处理装置
实验目的
实验原理
化学反应
1.题目信息
2.物质性质
收集装置
解题模板
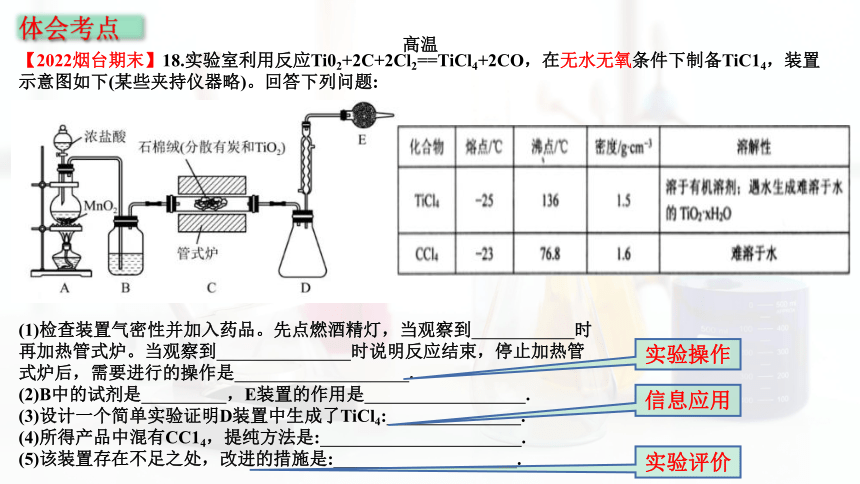
【2022烟台期末】18.实验室利用反应Ti02+2C+2Cl2==TiCl4+2CO,在无水无氧条件下制备TiC14,装置示意图如下(某些夹持仪器略)。回答下列问题:
高温
(1)检查装置气密性并加入药品。先点燃酒精灯,当观察到 时 再加热管式炉。当观察到 时说明反应结束,停止加热管式炉后,需要进行的操作是 .
(2)B中的试剂是 ,E装置的作用是 .
(3)设计一个简单实验证明D装置中生成了TiCl4: .
(4)所得产品中混有CC14,提纯方法是: .
(5)该装置存在不足之处,改进的措施是: .
体会考点
实验操作
实验评价
信息应用
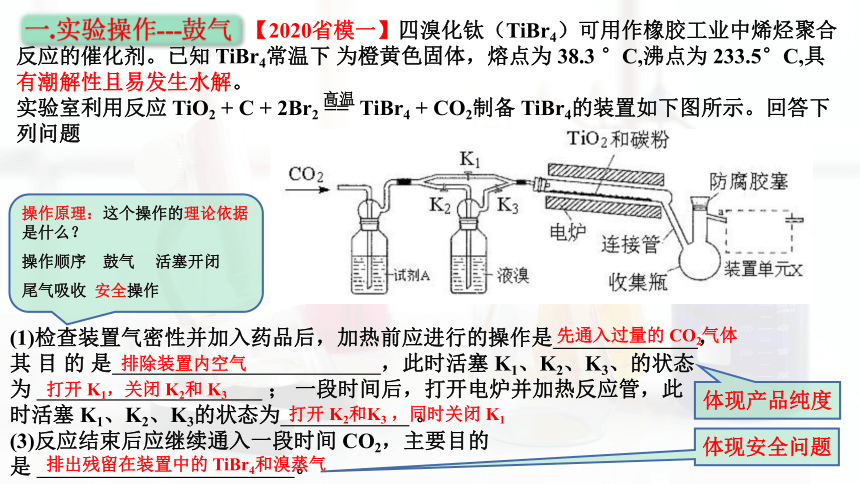
【2020省模一】四溴化钛(TiBr4)可用作橡胶工业中烯烃聚合反应的催化剂。已知 TiBr4常温下 为橙黄色固体,熔点为 38.3 °C,沸点为 233.5°C,具有潮解性且易发生水解。
实验室利用反应 TiO2 + C + 2Br2 == TiBr4 + CO2制备 TiBr4的装置如下图所示。回答下列问题
高温
(1)检查装置气密性并加入药品后,加热前应进行的操作是 , 其 目 的 是 ,此时活塞 K1、K2、K3、的状态为 ; 一段时间后,打开电炉并加热反应管,此时活塞 K1、K2、K3的状态为 。
(3)反应结束后应继续通入一段时间 CO2,主要目的是 。
先通入过量的 CO2气体
打开 K2和K3 ,同时关闭 K1
打开 K1,关闭 K2和 K3
排出残留在装置中的 TiBr4和溴蒸气
操作原理:这个操作的理论依据是什么?
操作顺序 鼓气 活塞开闭
尾气吸收 安全操作
一.实验操作---鼓气
体现产品纯度
体现安全问题
排除装置内空气
体现安全问题
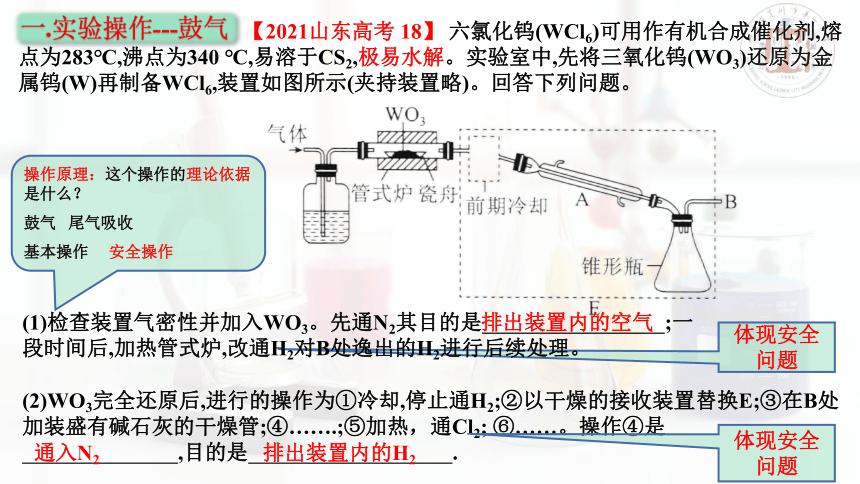
(1)检查装置气密性并加入WO3。先通N2其目的是 ;一段时间后,加热管式炉,改通H2对B处逸出的H2进行后续处理。
(2)WO3完全还原后,进行的操作为①冷却,停止通H2;②以干燥的接收装置替换E;③在B处加装盛有碱石灰的干燥管;④…….;⑤加热,通Cl2; ⑥……。操作④是
,目的是 .
排出装置内的空气
通入N2
排出装置内的H2
【2021山东高考 18】 六氯化钨(WCl6)可用作有机合成催化剂,熔点为283℃,沸点为340 ℃,易溶于CS2,极易水解。实验室中,先将三氧化钨(WO3)还原为金属钨(W)再制备WCl6,装置如图所示(夹持装置略)。回答下列问题。
操作原理:这个操作的理论依据是什么?
鼓气 尾气吸收
基本操作 安全操作
体现安全问题
一.实验操作---鼓气
知识升华
归纳总结:反应前通入X2排空气作用:
归纳总结:反应中鼓入某气,
归纳总结:反应后鼓入某气,
鼓气操作
排出装置内空气,防止空气中O2、CO2、H2O对实验的影响。
1.Cl2等带颜色的气体:整套装置内充满黄绿色气体
2.H2等易燃气体:收集末端气体验纯
3.CO2等:末端通入澄清石灰水中,产生白色沉淀
4.N2等:一段时间后,导气管末端出现连续稳定的气泡
目的是为了将反应中产生的气体,全部转入后续装置并完全吸收。
1.鼓入“难溶”气体“稀释”溶解度较大的气体,
2.鼓入“某气”气体“稀释”浓度较大时易爆的气体(ClO2),
目的是:
1.为了将反应中产生的有害气体或者有害反应物(如Br2、Cl2、SO2等),全部转入尾气吸收装置完全吸收,
2.冷却固体。
防止吸收该气体时产生倒吸。
防止产品爆炸。
消除拆卸装置时可能造成的污染。
【2022烟台期末】18.实验室利用反应Ti02+2C+2Cl2==TiCl4+2CO,在无水无氧条件下制备TiC14,装置示意图如下(某些夹持仪器略)。回答下列问题:
高温
(1)检查装置气密性并加入药品。先点燃酒精灯,当观察到 时再加热管式炉。
当观察到 时说明反应结束,停止加热管式炉后,需要进行的操作是 .
体会考点
实验操作
装置内充满黄绿色气体
球形冷凝管没有液体滴下
继续通一段时间C12
【2021湖北18】
由三氯化锑(SbCl3)制备HSbF6的反应如下:
SbCl3+ Cl2 = SbCl5
80°
物质 熔点/℃ 沸点/℃ 性质
SbCl3 73.4 220.3 极易水解
SbCl5 3.5 79℃/2.9kPa 140℃分解,极易水解
二.信息应用---装置作用
(1)实验装置中两个冷凝管 (填“能”或“不能”)交换使用。
(2)试剂X的作用为 、 。
(3)反应完成后,关闭活塞a、打开活塞b,减压转移 (填仪器名称)中生成的至双口烧瓶中。用真空泵抽气减压蒸馏前,必须关闭的活塞是 (填“a”或“b”);用减压蒸馏而不用常压蒸馏的主要原因是 。
不能
吸收氯气 防止空气中的水蒸气进入
b
防止SbCl5分解
三颈烧瓶
体现安全和条件
体现条件控制
【2021烟台一模】已知磺酰氯(SOCl2)是一种无色液体,熔点—54.1℃,沸点69.1℃,遇水发生剧烈水解,且产生白雾。某学习小组依据SO2(g)+Cl2(g)===SOC12(g)△H<0,利用下列装置制备磺酰氯(部分夹持装置咯)。
(3)仪器甲的名称为_ _______﹐仪器乙的作用是 .
(4)制备时,D 中的三颈烧瓶宜浸入冰水浴中的原因是 .
球形冷凝管
吸收Cl2和SO2,并防止水蒸气进入三颈烧瓶中
降低温度,有利于SO2(g)+Cl2(g)===SOC12(g)平衡右移,提高产率
体现信息运用
体现安全和条件
二.信息应用---装置作用
控制条件
前后都加气体净化/干燥装置
增加防氧化装置
控制温度装置
调控洗涤剂(醇洗)
装置原理
题目信息
焦性没食子酸
苯
决定
易水解
有杂质
易氧化
易分解
易挥发
反应能量变化
溶解性
决定
决定
决定
思维建模
【2021烟台二模】硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]是一种蓝绿色的无机复盐,易溶于水,不溶于乙醇。在水中的溶解度比FeSO4和(NH4)2SO4都要小。某同学设计如图实验装置制备硫酸亚铁铵晶体。
实验步骤如下。
①用30%的 NaOH, 溶液和铁屑(含有Fe2O3、FeS等杂质)混合、煮沸、冷却、分离,将分离出的NaOH溶液装入c中。
②在B中用①处理过的铁屑和稀H2SO4反应制取FeSO4.
③将②制得的FeSO4溶液与(NH4)2SO4溶液混合。
④将A中混合液蒸发浓缩、自然冷却、过滤、洗涤、干燥得到硫酸亚铁铵晶体。
(4)过滤后的品体用乙醇洗涤而不用蒸馏水洗涤原因是 。
硫酸亚铁铵易溶于水,不溶于乙醇,减少损耗
【2022烟台期末】18.实验室利用反应Ti02+2C+2Cl2==TiCl4+2CO,在无水无氧条件下制备TiC14,装置示意图如下(某些夹持仪器略)。回答下列问题:
高温
(2)B中的试剂是 ,E装置的作用是 .
(3)设计一个简单实验证明D装置中生成了TiCl4: .
(4)所得产品中混有CC14,提纯方法是: .
体会考点
信息应用
浓硫酸
吸收Cl2、HCl,并防止空气中的水蒸气进入装置
取少量产品溶于水中,产生浑浊,证明有TiCl4生成
蒸馏
Cl2、HCl、H2O
装置缺陷
根据反应原理--反应物性质:浓盐酸易挥发、锰酸钾碱性条件稳定。利用信息、 实验评价的角度
三.实验评价---装置缺陷
【2020山东卷】某同学利用C12氧化K2MnO4制备KMnO4的装置如下图所示(夹持装置略);已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:3MnO42-+2H2O= 2MnO4-+MnO2↓+4OH-
(2)上述装置存在一处缺陷,会导致KMnO4产率降低,改进的方法是 。
在装置A、B之间加装盛有饱和食盐水的洗气瓶
装置缺陷
在XX装置之间,
添加一个装有XX试剂的XX装置(干燥管,洗气瓶等)
思维建模
解决方案
切入点:产品纯度,安全,产率
1. ,有副反应
2. ,污染环境
5. ,氧化产品等
3. ,安全
4. ,产品发生反应
未除杂或干燥
未吸收尾气
未防倒吸或未防止爆炸
未防空气中的水蒸汽等进入装置
未屏蔽氧气
【2022烟台期末】18.实验室利用反应Ti02+2C+2Cl2==TiCl4+2CO,在无水无氧条件下制备TiC14,装置示意图如下(某些夹持仪器略)。回答下列问题:
高温
(5)该装置存在不足之处,改进的措施是: .
体会考点
实验评价
在E装置后接吸收CO的装置或接气球或接玻璃尖嘴点燃
Cl2、HCl、H2O
浓硫酸
原料提供装置
缓冲安全装置
净化除杂装置
中心反应装置
后防水、空气装置
尾气处理装置
实验目的
实验原理
化学反应
1.题目信息
2.物质性质
收集装置
知识整合
实验操作
信息利用
实验评价
体现产品纯度,实验安全,实验效率的综合化学素养。
实验评价---实验装置的缺陷
一条主线
三个应用
【2022烟台期末】18.实验室利用反应Ti02+2C+2Cl2==TiCl4+2CO,在无水无氧条件下制备TiC14,装置示意图如下(某些夹持仪器略)。回答下列问题:
高温
(1)检查装置气密性并加入药品。先点燃酒精灯,当观察到时 再加热管式炉。当观察到 时说明反应结束,停止加热管式炉后,需要进行的操作是 .
(2)B中的试剂是 ,E装置的作用是 .
(3)设计一个简单实验证明D装置中生成了TiCl4: 。
(4)所得产品中混有CC14,提纯方法是: .
(5)该装置存在不足之处,改进的措施是: .
装置内充满黄绿色气体
球形冷凝管没有液体滴下
继续通一段时间C12
浓硫酸
吸收Cl2、HCl,并防止空气中的水蒸气进入装置
取少量产品溶于水中,产生浑浊,证明有TiCl4生成
蒸馏
在E装置后接吸收CO的装置或接气球或接玻璃尖嘴点燃
学习评价
实验评价
信息应用
实验操作
高三化学实验专题——物质制备型实验
山东高考题中化学实验题模块统计
题号 题型 2020 题号 题型 2021 题号 题型 2022
考点(22分) 考点(26分) 考点(24分)
1 单选题 化学实验基础知识和基本技能 3 单选题 化学实验基础知识和基本技能 2 单选题 化学实验基础知识和基本技能
5 单选题 物质检验和制备 5 单选题 研究物质性质,探究反应规律 6 单选题 化学实验
8 单选题 物质分离 8 单选题 物质制备和分离 8 单选题 物质制备和分离
11 不定项选择题 研究物质性质,探究反应规律 11 不定项选择题 研究物质性质,探究反应规律 9 单选题 物质制备和分离
13 不定项选择题 物质制备 11 不定项选择题 研究和学习物质及其变化
18 非选择题 物质制备和实验条件控制 18 非选择题 物质制备和实验条件控制 18 非选择题 物质制备和实验条件控制
考点 2020 2021 2022 2023烟台市高考诊断性测试
题型 制备KMnO4 制备WCl6 制备FeCl2 制备KMnO4
物质制备 √ √ √ √
化学实验基础知识 √ √ √
研究和学习物质及其变化 √ √ √ √
化学实验基本技能 √ √ √
滴定计算 √ √ √ √
山东高考题中物质制备实验题模块统计
【2022山东高考18】
实验室利用FeCl2·4H2O和亚硫酰氯( SOCl2)制备无水FeCl2的装置如图所示(加热及夹持装置略)。已知 SOCl2沸点为76 ℃,遇水极易反应生成两种酸性气体。回答下列问题:
供气 装置
浓硫酸
SOCl2
制备装置
后防水装置
尾气处理装置
FeCl2.4H2O+4SOCl2 = FeCl2+4SO2+8HCl
FeCl2·4H2O
浓硫酸
NaOH溶液
?
△
感悟高考
前防水装置
原料提供装置
缓冲安全装置
净化除杂装置
中心反应装置
后防水、空气装置
尾气处理装置
实验目的
实验原理
化学反应
1.题目信息
2.物质性质
收集装置
解题模板
【2022烟台期末】18.实验室利用反应Ti02+2C+2Cl2==TiCl4+2CO,在无水无氧条件下制备TiC14,装置示意图如下(某些夹持仪器略)。回答下列问题:
高温
(1)检查装置气密性并加入药品。先点燃酒精灯,当观察到 时 再加热管式炉。当观察到 时说明反应结束,停止加热管式炉后,需要进行的操作是 .
(2)B中的试剂是 ,E装置的作用是 .
(3)设计一个简单实验证明D装置中生成了TiCl4: .
(4)所得产品中混有CC14,提纯方法是: .
(5)该装置存在不足之处,改进的措施是: .
体会考点
实验操作
实验评价
信息应用
【2020省模一】四溴化钛(TiBr4)可用作橡胶工业中烯烃聚合反应的催化剂。已知 TiBr4常温下 为橙黄色固体,熔点为 38.3 °C,沸点为 233.5°C,具有潮解性且易发生水解。
实验室利用反应 TiO2 + C + 2Br2 == TiBr4 + CO2制备 TiBr4的装置如下图所示。回答下列问题
高温
(1)检查装置气密性并加入药品后,加热前应进行的操作是 , 其 目 的 是 ,此时活塞 K1、K2、K3、的状态为 ; 一段时间后,打开电炉并加热反应管,此时活塞 K1、K2、K3的状态为 。
(3)反应结束后应继续通入一段时间 CO2,主要目的是 。
先通入过量的 CO2气体
打开 K2和K3 ,同时关闭 K1
打开 K1,关闭 K2和 K3
排出残留在装置中的 TiBr4和溴蒸气
操作原理:这个操作的理论依据是什么?
操作顺序 鼓气 活塞开闭
尾气吸收 安全操作
一.实验操作---鼓气
体现产品纯度
体现安全问题
排除装置内空气
体现安全问题
(1)检查装置气密性并加入WO3。先通N2其目的是 ;一段时间后,加热管式炉,改通H2对B处逸出的H2进行后续处理。
(2)WO3完全还原后,进行的操作为①冷却,停止通H2;②以干燥的接收装置替换E;③在B处加装盛有碱石灰的干燥管;④…….;⑤加热,通Cl2; ⑥……。操作④是
,目的是 .
排出装置内的空气
通入N2
排出装置内的H2
【2021山东高考 18】 六氯化钨(WCl6)可用作有机合成催化剂,熔点为283℃,沸点为340 ℃,易溶于CS2,极易水解。实验室中,先将三氧化钨(WO3)还原为金属钨(W)再制备WCl6,装置如图所示(夹持装置略)。回答下列问题。
操作原理:这个操作的理论依据是什么?
鼓气 尾气吸收
基本操作 安全操作
体现安全问题
一.实验操作---鼓气
知识升华
归纳总结:反应前通入X2排空气作用:
归纳总结:反应中鼓入某气,
归纳总结:反应后鼓入某气,
鼓气操作
排出装置内空气,防止空气中O2、CO2、H2O对实验的影响。
1.Cl2等带颜色的气体:整套装置内充满黄绿色气体
2.H2等易燃气体:收集末端气体验纯
3.CO2等:末端通入澄清石灰水中,产生白色沉淀
4.N2等:一段时间后,导气管末端出现连续稳定的气泡
目的是为了将反应中产生的气体,全部转入后续装置并完全吸收。
1.鼓入“难溶”气体“稀释”溶解度较大的气体,
2.鼓入“某气”气体“稀释”浓度较大时易爆的气体(ClO2),
目的是:
1.为了将反应中产生的有害气体或者有害反应物(如Br2、Cl2、SO2等),全部转入尾气吸收装置完全吸收,
2.冷却固体。
防止吸收该气体时产生倒吸。
防止产品爆炸。
消除拆卸装置时可能造成的污染。
【2022烟台期末】18.实验室利用反应Ti02+2C+2Cl2==TiCl4+2CO,在无水无氧条件下制备TiC14,装置示意图如下(某些夹持仪器略)。回答下列问题:
高温
(1)检查装置气密性并加入药品。先点燃酒精灯,当观察到 时再加热管式炉。
当观察到 时说明反应结束,停止加热管式炉后,需要进行的操作是 .
体会考点
实验操作
装置内充满黄绿色气体
球形冷凝管没有液体滴下
继续通一段时间C12
【2021湖北18】
由三氯化锑(SbCl3)制备HSbF6的反应如下:
SbCl3+ Cl2 = SbCl5
80°
物质 熔点/℃ 沸点/℃ 性质
SbCl3 73.4 220.3 极易水解
SbCl5 3.5 79℃/2.9kPa 140℃分解,极易水解
二.信息应用---装置作用
(1)实验装置中两个冷凝管 (填“能”或“不能”)交换使用。
(2)试剂X的作用为 、 。
(3)反应完成后,关闭活塞a、打开活塞b,减压转移 (填仪器名称)中生成的至双口烧瓶中。用真空泵抽气减压蒸馏前,必须关闭的活塞是 (填“a”或“b”);用减压蒸馏而不用常压蒸馏的主要原因是 。
不能
吸收氯气 防止空气中的水蒸气进入
b
防止SbCl5分解
三颈烧瓶
体现安全和条件
体现条件控制
【2021烟台一模】已知磺酰氯(SOCl2)是一种无色液体,熔点—54.1℃,沸点69.1℃,遇水发生剧烈水解,且产生白雾。某学习小组依据SO2(g)+Cl2(g)===SOC12(g)△H<0,利用下列装置制备磺酰氯(部分夹持装置咯)。
(3)仪器甲的名称为_ _______﹐仪器乙的作用是 .
(4)制备时,D 中的三颈烧瓶宜浸入冰水浴中的原因是 .
球形冷凝管
吸收Cl2和SO2,并防止水蒸气进入三颈烧瓶中
降低温度,有利于SO2(g)+Cl2(g)===SOC12(g)平衡右移,提高产率
体现信息运用
体现安全和条件
二.信息应用---装置作用
控制条件
前后都加气体净化/干燥装置
增加防氧化装置
控制温度装置
调控洗涤剂(醇洗)
装置原理
题目信息
焦性没食子酸
苯
决定
易水解
有杂质
易氧化
易分解
易挥发
反应能量变化
溶解性
决定
决定
决定
思维建模
【2021烟台二模】硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]是一种蓝绿色的无机复盐,易溶于水,不溶于乙醇。在水中的溶解度比FeSO4和(NH4)2SO4都要小。某同学设计如图实验装置制备硫酸亚铁铵晶体。
实验步骤如下。
①用30%的 NaOH, 溶液和铁屑(含有Fe2O3、FeS等杂质)混合、煮沸、冷却、分离,将分离出的NaOH溶液装入c中。
②在B中用①处理过的铁屑和稀H2SO4反应制取FeSO4.
③将②制得的FeSO4溶液与(NH4)2SO4溶液混合。
④将A中混合液蒸发浓缩、自然冷却、过滤、洗涤、干燥得到硫酸亚铁铵晶体。
(4)过滤后的品体用乙醇洗涤而不用蒸馏水洗涤原因是 。
硫酸亚铁铵易溶于水,不溶于乙醇,减少损耗
【2022烟台期末】18.实验室利用反应Ti02+2C+2Cl2==TiCl4+2CO,在无水无氧条件下制备TiC14,装置示意图如下(某些夹持仪器略)。回答下列问题:
高温
(2)B中的试剂是 ,E装置的作用是 .
(3)设计一个简单实验证明D装置中生成了TiCl4: .
(4)所得产品中混有CC14,提纯方法是: .
体会考点
信息应用
浓硫酸
吸收Cl2、HCl,并防止空气中的水蒸气进入装置
取少量产品溶于水中,产生浑浊,证明有TiCl4生成
蒸馏
Cl2、HCl、H2O
装置缺陷
根据反应原理--反应物性质:浓盐酸易挥发、锰酸钾碱性条件稳定。利用信息、 实验评价的角度
三.实验评价---装置缺陷
【2020山东卷】某同学利用C12氧化K2MnO4制备KMnO4的装置如下图所示(夹持装置略);已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:3MnO42-+2H2O= 2MnO4-+MnO2↓+4OH-
(2)上述装置存在一处缺陷,会导致KMnO4产率降低,改进的方法是 。
在装置A、B之间加装盛有饱和食盐水的洗气瓶
装置缺陷
在XX装置之间,
添加一个装有XX试剂的XX装置(干燥管,洗气瓶等)
思维建模
解决方案
切入点:产品纯度,安全,产率
1. ,有副反应
2. ,污染环境
5. ,氧化产品等
3. ,安全
4. ,产品发生反应
未除杂或干燥
未吸收尾气
未防倒吸或未防止爆炸
未防空气中的水蒸汽等进入装置
未屏蔽氧气
【2022烟台期末】18.实验室利用反应Ti02+2C+2Cl2==TiCl4+2CO,在无水无氧条件下制备TiC14,装置示意图如下(某些夹持仪器略)。回答下列问题:
高温
(5)该装置存在不足之处,改进的措施是: .
体会考点
实验评价
在E装置后接吸收CO的装置或接气球或接玻璃尖嘴点燃
Cl2、HCl、H2O
浓硫酸
原料提供装置
缓冲安全装置
净化除杂装置
中心反应装置
后防水、空气装置
尾气处理装置
实验目的
实验原理
化学反应
1.题目信息
2.物质性质
收集装置
知识整合
实验操作
信息利用
实验评价
体现产品纯度,实验安全,实验效率的综合化学素养。
实验评价---实验装置的缺陷
一条主线
三个应用
【2022烟台期末】18.实验室利用反应Ti02+2C+2Cl2==TiCl4+2CO,在无水无氧条件下制备TiC14,装置示意图如下(某些夹持仪器略)。回答下列问题:
高温
(1)检查装置气密性并加入药品。先点燃酒精灯,当观察到时 再加热管式炉。当观察到 时说明反应结束,停止加热管式炉后,需要进行的操作是 .
(2)B中的试剂是 ,E装置的作用是 .
(3)设计一个简单实验证明D装置中生成了TiCl4: 。
(4)所得产品中混有CC14,提纯方法是: .
(5)该装置存在不足之处,改进的措施是: .
装置内充满黄绿色气体
球形冷凝管没有液体滴下
继续通一段时间C12
浓硫酸
吸收Cl2、HCl,并防止空气中的水蒸气进入装置
取少量产品溶于水中,产生浑浊,证明有TiCl4生成
蒸馏
在E装置后接吸收CO的装置或接气球或接玻璃尖嘴点燃
学习评价
实验评价
信息应用
实验操作
同课章节目录
