河南省驻马店市2022-2023学年高一上学期期末考试化学试题(含答案)
文档属性
| 名称 | 河南省驻马店市2022-2023学年高一上学期期末考试化学试题(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 589.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-24 00:00:00 | ||
图片预览


文档简介
驻马店市2022-2023学年高一上学期期末考试
化学试题
可能用到的相对原子质量:H1 C12 N14 O16 Na23 S32 Fe56 Ba137
第Ⅰ卷(选择题共45分)
一、选择题:本题共15小题,每小题3分,共55分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.下列说法不正确的是( )
A.侯德榜发明联合制碱法,为我国化学工业发展作出重要贡献
B.我国化学家徐光宪院士在稀土元素的分离及应用中作出了重要贡献
C.英国科学家道尔顿提出分子是构成物质的基本粒子,是不可再分的实心球,为近代化学的发展奠定了坚实的基础
D.俄国化学家门捷列夫发现了元素周期律,使化学的研究变得有规律可循
2.2022年诺贝尔化学奖授予了三位在“点击化学”及其应用方面做出了重大贡献的三位化学家——卡罗琳·贝尔托西、莫滕桦尔达和巴里·夏普莱斯。卡罗琳·贝尔托西将“点击化学”运用在生物学领域,并开创了“正交化学”,她的研究中需要对糖类进行示踪和定位。在很多研究糖类的实验中,会选用具有放射性的进行示踪研究。以下有关同位素的说法正确的是( )
A.、互为同位素
B.D、T发生核聚变成为其它元素,属于化学反应
C.、的质子数相同,电子数不同
D.同一元素各核素的近似相对原子质量不同,但它们的化学性质几乎完全相同
3.下图是一种具有磁性的“纳米药物”,可利用磁性引导该药物到达人体内的病变部位。该技术可大大提高治疗效果。下列有关说法不正确的是( )
A.该“纳米药物分子车"属于混合物
B.葡萄糖等这类含碳化合物属于有机物
C.该“纳米约物分子车”分散于水中可得胶体
D.该“纳米药物分子车”中的四氧化三铁中铁的价态为+2、+3价
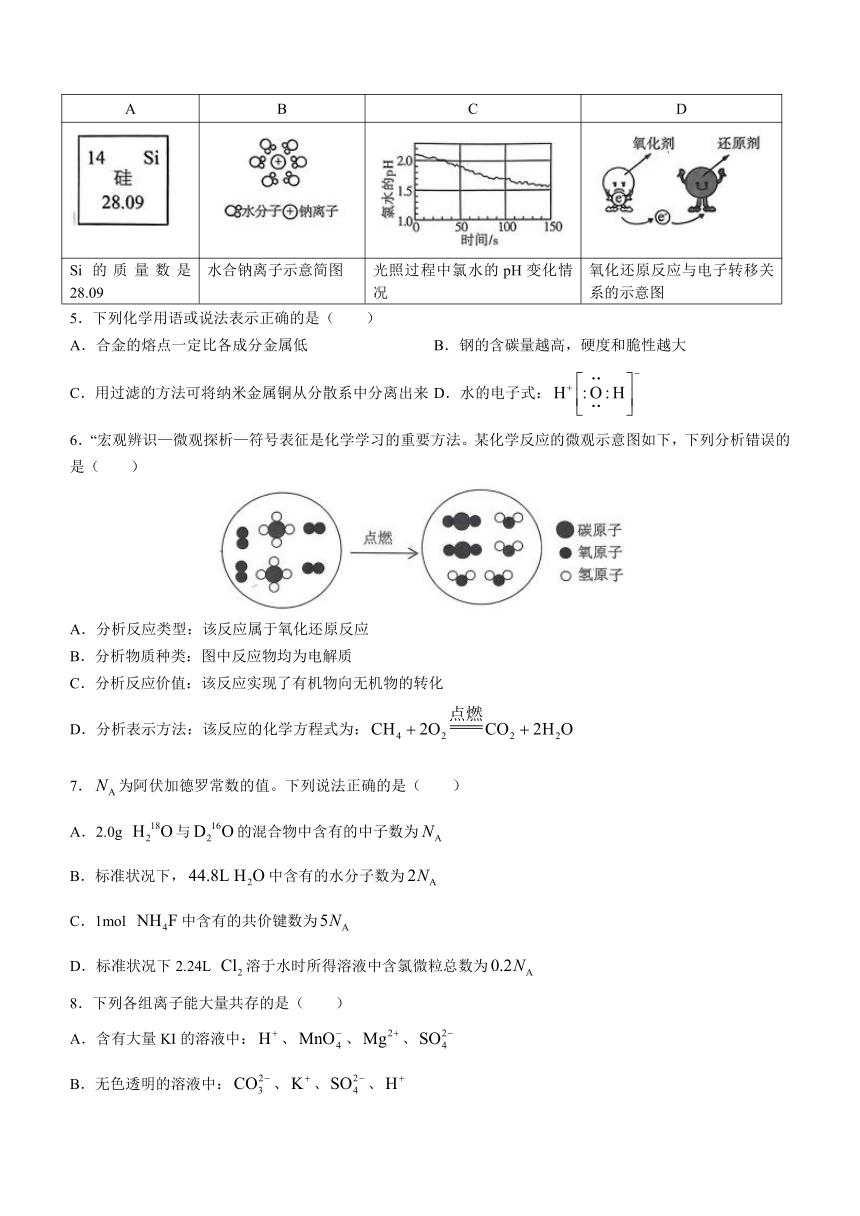
4.用示意图或图示的方法能够直观形象地将化学知识传授给学生,下列示意图或者说法正确的是( )
A B C D
Si的质量数是28.09 水合钠离子示意简图 光照过程中氯水的pH变化情况 氧化还原反应与电子转移关系的示意图
5.下列化学用语或说法表示正确的是( )
A.合金的熔点一定比各成分金属低 B.钢的含碳量越高,硬度和脆性越大
C.用过滤的方法可将纳米金属铜从分散系中分离出来 D.水的电子式:
6.“宏观辨识—微观探析—符号表征是化学学习的重要方法。某化学反应的微观示意图如下,下列分析错误的是( )
A.分析反应类型:该反应属于氧化还原反应
B.分析物质种类:图中反应物均为电解质
C.分析反应价值:该反应实现了有机物向无机物的转化
D.分析表示方法:该反应的化学方程式为:
7.为阿伏加德罗常数的值。下列说法正确的是( )
A.2.0g 与的混合物中含有的中子数为
B.标准状况下,中含有的水分子数为
C.1mol 中含有的共价键数为
D.标准状况下2.24L 溶于水时所得溶液中含氯微粒总数为
8.下列各组离子能大量共存的是( )
A.含有大量KI的溶液中:、、、
B.无色透明的溶液中:、、、
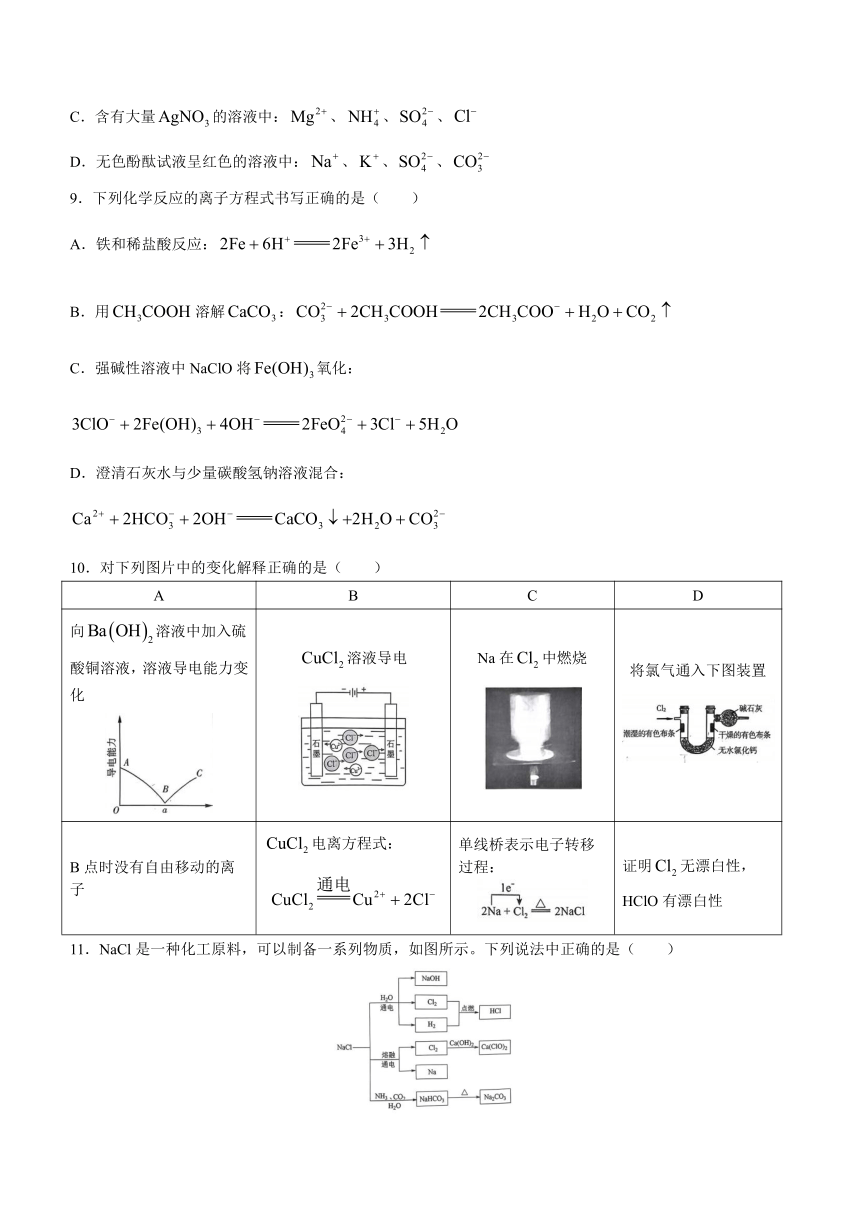
C.含有大量的溶液中:、、、
D.无色酚酞试液呈红色的溶液中:、、、
9.下列化学反应的离子方程式书写正确的是( )
A.铁和稀盐酸反应:
B.用溶解:
C.强碱性溶液中NaClO将氧化:
D.澄清石灰水与少量碳酸氢钠溶液混合:
10.对下列图片中的变化解释正确的是( )
A B C D
向溶液中加入硫酸铜溶液,溶液导电能力变化 溶液导电 Na在中燃烧 将氯气通入下图装置
B点时没有自由移动的离子 电离方程式: 单线桥表示电子转移过程: 证明无漂白性,HClO有漂白性
11.NaCl是一种化工原料,可以制备一系列物质,如图所示。下列说法中正确的是( )
A.同浓度的溶液的碱性强于溶液
B.工业上可用石灰乳与反应制取漂白粉
C.和在点燃的条件下安静燃烧,产生淡蓝色火焰
D.如图所示转化反应都是氧化还原反应
12.有A、B、C、D四种元素,质子数均小于18。A元素原子的最外层电子数是其电子层数的3倍;B元素的原子失去1个电子,所得到的微粒具有与氖原子相同的电子层结构;C元素是地壳中含量最多的金属元素;D元素的原子M层电子数是K层的3倍,下列说法不正确的是( )
A.A元素可以形成多种同素异形体 B.简单气态氢化物的稳定性:A>D
C.最高价氧化物对应的水化物的碱性:B>C D.离子半径:B13.根据元素周期表与元素周期律,下列推断不合理的是( )
A.第六周期0族元素的原子序数为86 B.第37号元素的最高化合价是+1
C.第53号元素的单质在常温常压下是固态 D.位于第四周期第ⅤA族的元素为金属元素
14.硫化氢的转化是资源利用和环境保护的重要研究课题。将和空气的混合气体通入、和的混合溶液中回收S,其转化如下图所示(CuS不溶于水)。下列说法中,不正确的是( )
A.过程①中,生成CuS的反应为全分解反应
B.过程②中,发生的反应为
C.过程③中,当有1mol 参与反应,转移个电子
D.过程②中为氧化剂,过程③中为氧化产物
15.向一定量的Cu、FeO、的混合物中加入100mL 的盐酸,恰好使混合物完全溶解,所得溶液中加入KSCN溶液无红色出现。若用足量的CO在高温下还原相同质量的此混合物,固体质量减少为( )
A.1.6g B.2.4g C.3.8g D.无法计算
第Ⅱ卷(非选择题,共55分)
二、非选择题:本题共4小题,共55分。
16.(14分)现有下列9种物质:① ②淀粉液 ③ ④ ⑤ ⑥Al ⑦纯醋酸 ⑧NaOH溶液 ⑨ ⑩,根据所学知识回答下列问题:
(1)以上物质属于电解质的是______(填写序号)。
(2)标准状况下,若④和⑤混合气体相对于氢气的密度为14.5,则④和⑤物质的量之比为______。标准状况下,VL 溶入100mL (1g/mL)中,溶液密度为g/mL,则氨水物质的量浓度表达式为______mol/L。
(3)物质⑥对应的氧化物为______(填“酸”、“碱”或“两性”)性氧化物,其与⑧反应的化学方程式为______。
(4)根据世界环保联盟的要求,⑩将逐渐取代成为水的消毒剂。工业上常用和溶液混合并加入稀酸化后制得,反应的离子方程式为:
______。
17.(16分)I.配制480mL 1.00mol/L碳酸钠溶液。下图是一些关键步骤和操作。
a b c d e f
(1)配制过程所需的玻璃仪器有烧杯、玻璃棒、量筒、______。
(2)配制过程的先后顺序是______(用字母序号填写)。
(3)某同学用晶体来配制此溶液,需要用托盘天平称量______g晶体。
(4)①如定容时仰视,配制的溶液的浓度会______(填“偏高”、“偏低”、“不变”)
②如晶体已经部分失去结晶水,配制的溶液的浓度会______(填“偏高”、偏低”、“不变”。)
Ⅱ.某小组利用下列装置继续对和的性质进行探究(夹持装置已略去,气密性已检验)。
(5)方框中试剂a为饱和溶液,其作用为______。
(6)请将该洗气装置补充完整______。
(7)实验持续一段时间后,观察到饱和溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因______。
0℃ 10℃ 20℃ 30℃ 40℃
的溶解度(g) 7.1 12.5 21.5 39.7 49.0
的溶解度(g) 6.9 8.1 9.6 11.1 12.7
18.(12分)铜和三氧化一铁在工农业生产中用途广泛,用黄铜矿(主要成分为,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示
已知:
(1)高温焙烧时发生的反应是,该反应中,氧化产物是______;1mol 参加反应时,反应中转移电子______mol。
(2)具有较强的氧化生,具有较强的还原性,当把通入滤液A中,检验产物中是否有生成的试剂最好为______(写化学式)。
(3)某同学想用酸性溶液检验溶液B中是否还有,你认为是否合适______(填“是”或“否”)。请简述理由______。
(4)经检验后溶液B中无,向溶液B中通入后发生反应的离子方程式为______。
19.(13分)溶液A中可能含有如下离子中的若干种:、、、、、、、。所含离子浓度均相同。为确定其组成,某实验小组按如下流程进行了实验:
已知:(NO为无色气体)
(1)溶液A中各离子的物质的量浓度为______。
(2)溶液A中一定存在的离子是______。
(3)溶液A中一定不存在的离子是和______,请结合数据简述判断理由为______。
(4)为确定溶液A中是否存在,请写出简要的实验步骤:______。
高一化学试题参考答案
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.C 2.D 3.C 4.C 5.B 6.B 7.A 8.D 9.C 10.D 11.B 12.D 13.D 14.C 15.B
二、非选择题:本题共4小题,共55分。(除注明外,每空2分)
16.(14分)
(1)①③⑦⑨(3分)
(2)4:5 (3分)
(3)两性
(4)
17.(16分)(1)500mL容量瓶、胶头滴管 (2)dbcafe
(3)143.0 (4)偏低 偏高
(5)除去中HCl (6)
(7)
18.(12分(1) 6 (2)KSCN溶液
(3)否 根据题给已知信息,可将溶液B中的氧化而褪色,干扰了的检验,故不合适
(4)或
19.(1)(13分)
(2)、、、(4分)
(3) 根据题意,溶液C中加入过量溶液,生成的白色沉淀D为,物质的量为,溶液A中加入的物质的量为0.02mol,则A中含有为0.01mol,因有存在,则A中一定不含(3分)
(4)用洁净的铁丝或铂丝 取待测液,在酒精灯外焰上灼烧,若火焰呈黄色则存在,反之则不存在。答案也可为:取少量溶液A,加入过量溶液,过滤,往滤液中滴加溶液,若有白色沉淀生成,证明溶液A中含有,根据溶液呈电中性原则,则一定含有,否则不含有。
化学试题
可能用到的相对原子质量:H1 C12 N14 O16 Na23 S32 Fe56 Ba137
第Ⅰ卷(选择题共45分)
一、选择题:本题共15小题,每小题3分,共55分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.下列说法不正确的是( )
A.侯德榜发明联合制碱法,为我国化学工业发展作出重要贡献
B.我国化学家徐光宪院士在稀土元素的分离及应用中作出了重要贡献
C.英国科学家道尔顿提出分子是构成物质的基本粒子,是不可再分的实心球,为近代化学的发展奠定了坚实的基础
D.俄国化学家门捷列夫发现了元素周期律,使化学的研究变得有规律可循
2.2022年诺贝尔化学奖授予了三位在“点击化学”及其应用方面做出了重大贡献的三位化学家——卡罗琳·贝尔托西、莫滕桦尔达和巴里·夏普莱斯。卡罗琳·贝尔托西将“点击化学”运用在生物学领域,并开创了“正交化学”,她的研究中需要对糖类进行示踪和定位。在很多研究糖类的实验中,会选用具有放射性的进行示踪研究。以下有关同位素的说法正确的是( )
A.、互为同位素
B.D、T发生核聚变成为其它元素,属于化学反应
C.、的质子数相同,电子数不同
D.同一元素各核素的近似相对原子质量不同,但它们的化学性质几乎完全相同
3.下图是一种具有磁性的“纳米药物”,可利用磁性引导该药物到达人体内的病变部位。该技术可大大提高治疗效果。下列有关说法不正确的是( )
A.该“纳米药物分子车"属于混合物
B.葡萄糖等这类含碳化合物属于有机物
C.该“纳米约物分子车”分散于水中可得胶体
D.该“纳米药物分子车”中的四氧化三铁中铁的价态为+2、+3价
4.用示意图或图示的方法能够直观形象地将化学知识传授给学生,下列示意图或者说法正确的是( )
A B C D
Si的质量数是28.09 水合钠离子示意简图 光照过程中氯水的pH变化情况 氧化还原反应与电子转移关系的示意图
5.下列化学用语或说法表示正确的是( )
A.合金的熔点一定比各成分金属低 B.钢的含碳量越高,硬度和脆性越大
C.用过滤的方法可将纳米金属铜从分散系中分离出来 D.水的电子式:
6.“宏观辨识—微观探析—符号表征是化学学习的重要方法。某化学反应的微观示意图如下,下列分析错误的是( )
A.分析反应类型:该反应属于氧化还原反应
B.分析物质种类:图中反应物均为电解质
C.分析反应价值:该反应实现了有机物向无机物的转化
D.分析表示方法:该反应的化学方程式为:
7.为阿伏加德罗常数的值。下列说法正确的是( )
A.2.0g 与的混合物中含有的中子数为
B.标准状况下,中含有的水分子数为
C.1mol 中含有的共价键数为
D.标准状况下2.24L 溶于水时所得溶液中含氯微粒总数为
8.下列各组离子能大量共存的是( )
A.含有大量KI的溶液中:、、、
B.无色透明的溶液中:、、、
C.含有大量的溶液中:、、、
D.无色酚酞试液呈红色的溶液中:、、、
9.下列化学反应的离子方程式书写正确的是( )
A.铁和稀盐酸反应:
B.用溶解:
C.强碱性溶液中NaClO将氧化:
D.澄清石灰水与少量碳酸氢钠溶液混合:
10.对下列图片中的变化解释正确的是( )
A B C D
向溶液中加入硫酸铜溶液,溶液导电能力变化 溶液导电 Na在中燃烧 将氯气通入下图装置
B点时没有自由移动的离子 电离方程式: 单线桥表示电子转移过程: 证明无漂白性,HClO有漂白性
11.NaCl是一种化工原料,可以制备一系列物质,如图所示。下列说法中正确的是( )
A.同浓度的溶液的碱性强于溶液
B.工业上可用石灰乳与反应制取漂白粉
C.和在点燃的条件下安静燃烧,产生淡蓝色火焰
D.如图所示转化反应都是氧化还原反应
12.有A、B、C、D四种元素,质子数均小于18。A元素原子的最外层电子数是其电子层数的3倍;B元素的原子失去1个电子,所得到的微粒具有与氖原子相同的电子层结构;C元素是地壳中含量最多的金属元素;D元素的原子M层电子数是K层的3倍,下列说法不正确的是( )
A.A元素可以形成多种同素异形体 B.简单气态氢化物的稳定性:A>D
C.最高价氧化物对应的水化物的碱性:B>C D.离子半径:B
A.第六周期0族元素的原子序数为86 B.第37号元素的最高化合价是+1
C.第53号元素的单质在常温常压下是固态 D.位于第四周期第ⅤA族的元素为金属元素
14.硫化氢的转化是资源利用和环境保护的重要研究课题。将和空气的混合气体通入、和的混合溶液中回收S,其转化如下图所示(CuS不溶于水)。下列说法中,不正确的是( )
A.过程①中,生成CuS的反应为全分解反应
B.过程②中,发生的反应为
C.过程③中,当有1mol 参与反应,转移个电子
D.过程②中为氧化剂,过程③中为氧化产物
15.向一定量的Cu、FeO、的混合物中加入100mL 的盐酸,恰好使混合物完全溶解,所得溶液中加入KSCN溶液无红色出现。若用足量的CO在高温下还原相同质量的此混合物,固体质量减少为( )
A.1.6g B.2.4g C.3.8g D.无法计算
第Ⅱ卷(非选择题,共55分)
二、非选择题:本题共4小题,共55分。
16.(14分)现有下列9种物质:① ②淀粉液 ③ ④ ⑤ ⑥Al ⑦纯醋酸 ⑧NaOH溶液 ⑨ ⑩,根据所学知识回答下列问题:
(1)以上物质属于电解质的是______(填写序号)。
(2)标准状况下,若④和⑤混合气体相对于氢气的密度为14.5,则④和⑤物质的量之比为______。标准状况下,VL 溶入100mL (1g/mL)中,溶液密度为g/mL,则氨水物质的量浓度表达式为______mol/L。
(3)物质⑥对应的氧化物为______(填“酸”、“碱”或“两性”)性氧化物,其与⑧反应的化学方程式为______。
(4)根据世界环保联盟的要求,⑩将逐渐取代成为水的消毒剂。工业上常用和溶液混合并加入稀酸化后制得,反应的离子方程式为:
______。
17.(16分)I.配制480mL 1.00mol/L碳酸钠溶液。下图是一些关键步骤和操作。
a b c d e f
(1)配制过程所需的玻璃仪器有烧杯、玻璃棒、量筒、______。
(2)配制过程的先后顺序是______(用字母序号填写)。
(3)某同学用晶体来配制此溶液,需要用托盘天平称量______g晶体。
(4)①如定容时仰视,配制的溶液的浓度会______(填“偏高”、“偏低”、“不变”)
②如晶体已经部分失去结晶水,配制的溶液的浓度会______(填“偏高”、偏低”、“不变”。)
Ⅱ.某小组利用下列装置继续对和的性质进行探究(夹持装置已略去,气密性已检验)。
(5)方框中试剂a为饱和溶液,其作用为______。
(6)请将该洗气装置补充完整______。
(7)实验持续一段时间后,观察到饱和溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因______。
0℃ 10℃ 20℃ 30℃ 40℃
的溶解度(g) 7.1 12.5 21.5 39.7 49.0
的溶解度(g) 6.9 8.1 9.6 11.1 12.7
18.(12分)铜和三氧化一铁在工农业生产中用途广泛,用黄铜矿(主要成分为,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示
已知:
(1)高温焙烧时发生的反应是,该反应中,氧化产物是______;1mol 参加反应时,反应中转移电子______mol。
(2)具有较强的氧化生,具有较强的还原性,当把通入滤液A中,检验产物中是否有生成的试剂最好为______(写化学式)。
(3)某同学想用酸性溶液检验溶液B中是否还有,你认为是否合适______(填“是”或“否”)。请简述理由______。
(4)经检验后溶液B中无,向溶液B中通入后发生反应的离子方程式为______。
19.(13分)溶液A中可能含有如下离子中的若干种:、、、、、、、。所含离子浓度均相同。为确定其组成,某实验小组按如下流程进行了实验:
已知:(NO为无色气体)
(1)溶液A中各离子的物质的量浓度为______。
(2)溶液A中一定存在的离子是______。
(3)溶液A中一定不存在的离子是和______,请结合数据简述判断理由为______。
(4)为确定溶液A中是否存在,请写出简要的实验步骤:______。
高一化学试题参考答案
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.C 2.D 3.C 4.C 5.B 6.B 7.A 8.D 9.C 10.D 11.B 12.D 13.D 14.C 15.B
二、非选择题:本题共4小题,共55分。(除注明外,每空2分)
16.(14分)
(1)①③⑦⑨(3分)
(2)4:5 (3分)
(3)两性
(4)
17.(16分)(1)500mL容量瓶、胶头滴管 (2)dbcafe
(3)143.0 (4)偏低 偏高
(5)除去中HCl (6)
(7)
18.(12分(1) 6 (2)KSCN溶液
(3)否 根据题给已知信息,可将溶液B中的氧化而褪色,干扰了的检验,故不合适
(4)或
19.(1)(13分)
(2)、、、(4分)
(3) 根据题意,溶液C中加入过量溶液,生成的白色沉淀D为,物质的量为,溶液A中加入的物质的量为0.02mol,则A中含有为0.01mol,因有存在,则A中一定不含(3分)
(4)用洁净的铁丝或铂丝 取待测液,在酒精灯外焰上灼烧,若火焰呈黄色则存在,反之则不存在。答案也可为:取少量溶液A,加入过量溶液,过滤,往滤液中滴加溶液,若有白色沉淀生成,证明溶液A中含有,根据溶液呈电中性原则,则一定含有,否则不含有。
同课章节目录
