化学人教版(2019)必修第二册7.3.2乙酸(共21张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第二册7.3.2乙酸(共21张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-23 00:00:00 | ||
图片预览





文档简介
(共21张PPT)
喝点醋能解酒
第七章 有机化合物
第三节 乙醇与乙酸
第2课时 乙酸
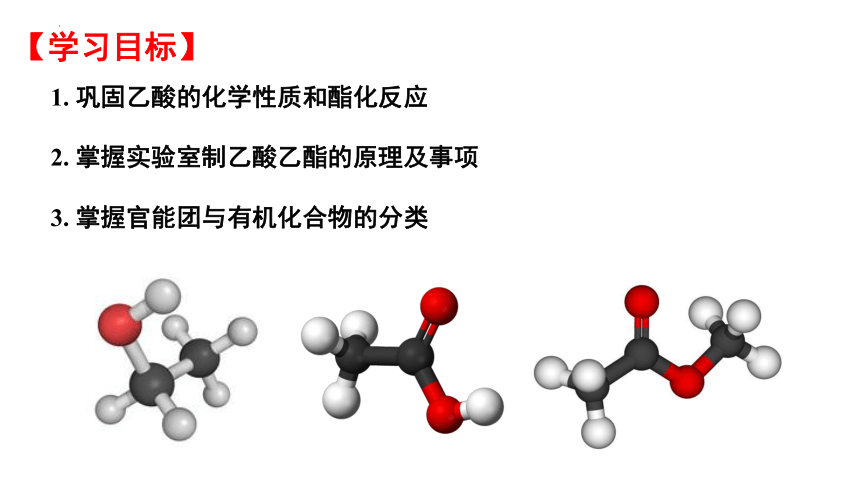
1. 巩固乙酸的化学性质和酯化反应
2. 掌握实验室制乙酸乙酯的原理及事项
3. 掌握官能团与有机化合物的分类
【学习目标】
1. 制备乙酸乙酯的原理
3. 如何加快制备乙酸乙酯的反应速率?
2. 制备乙酸乙酯药品的滴加顺序?
4. 饱和的Na2CO3溶液的作用?
【问题导学1】
一、乙酸乙酯的实验室制备
【实验7-6】在一支试管中加入3mL乙醇,然后边振荡试管边加慢慢加入2mL浓硫酸,和2mL 乙酸,再加入几片碎瓷片。连接好装置,用酒精灯小心加热,将产生的蒸汽经导管通入饱和碳酸钠液面之上,观察现象。
现象:
1. 碳酸钠液面分层,上层有无色油状液体;
2. 可闻到香味。(果香味)
【点拨精讲1】
反应原理和过程分析
CH3COOH + HOC2H5 H2O + CH3COOC2H5
浓H2SO4
反应特点
②可逆反应
③生成的乙酸乙酯和H2O如果留在反应液里会抑制反应向正方向进行。
①常温下几乎不反应,需加热和催化剂
④乙醇沸点(78.5℃)和乙酸沸点(117.8℃)都较低,当乙酸乙酯形成蒸气被导出时,其中会混有少量乙醇和乙酸蒸气。冷却后的乙酸乙酯和乙醇、乙酸都互溶而难于分离。
冰醋酸 无水乙醇 乙酸乙酯
防止倒吸
增大受热面积
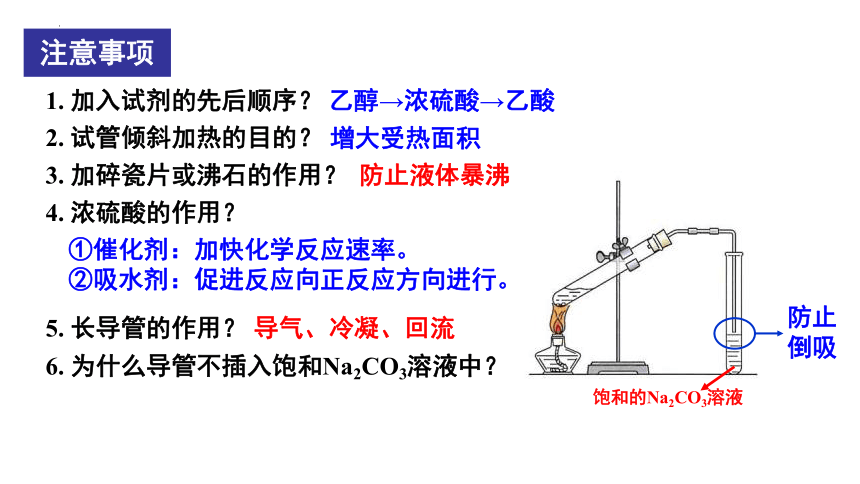
乙醇→浓硫酸→乙酸
2. 试管倾斜加热的目的?
3. 加碎瓷片或沸石的作用?
防止液体暴沸
4. 浓硫酸的作用?
①催化剂:加快化学反应速率。 ②吸水剂:促进反应向正反应方向进行。
6. 为什么导管不插入饱和Na2CO3溶液中?
导气、冷凝、回流
5. 长导管的作用?
1. 加入试剂的先后顺序?
饱和的Na2CO3溶液
注意事项
8. 能否用氢氧化钠溶液代替饱和Na2CO3溶液?
NaOH溶液能使生成的酯水解,故不可能用。
CH3COOC2H5+NaOH CH3COONa+C2H5 OH
9. 如何提高乙酸的转化率?
①过量的乙醇增大反应进行的程度;
②浓硫酸的吸水性增大反应进行的程度;
③及时分离生成物等。
7. 饱和Na2CO3溶液作用?
中和乙酸,溶解乙醇,降低乙酸乙酯的溶解度,
提高水溶液的密度以加速乙酸乙酯与水溶液的分层
饱和Na2CO3溶液
CH3 C O H + H O C2H5 CH3 C O C2H5+H O H
CH3 C O H + H O C2H5 CH3 C O C2H5 +H O H
O
O
浓H2SO4
方式一:
O
O
方式二:
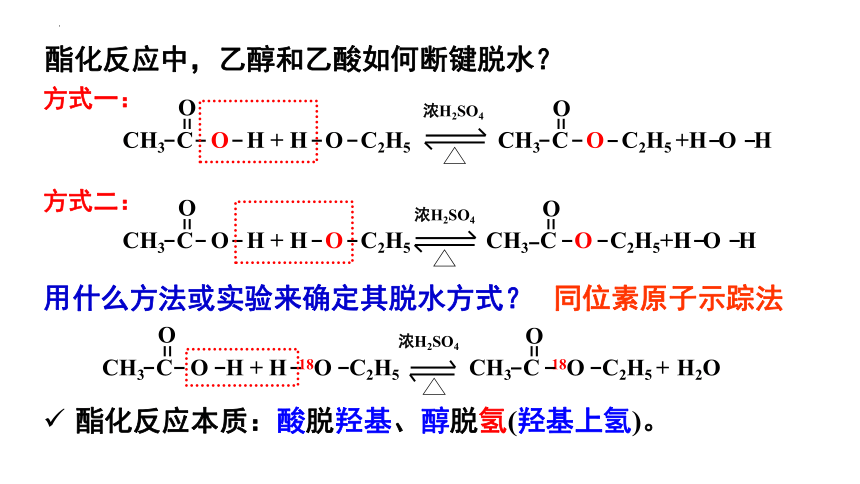
用什么方法或实验来确定其脱水方式?
酯化反应中,乙醇和乙酸如何断键脱水?
浓H2SO4
同位素原子示踪法
浓H2SO4
CH3 C O H + H 18O C2H5 CH3 C 18O C2H5 + H2O
O
O
酯化反应本质:酸脱羟基、醇脱氢(羟基上氢)。
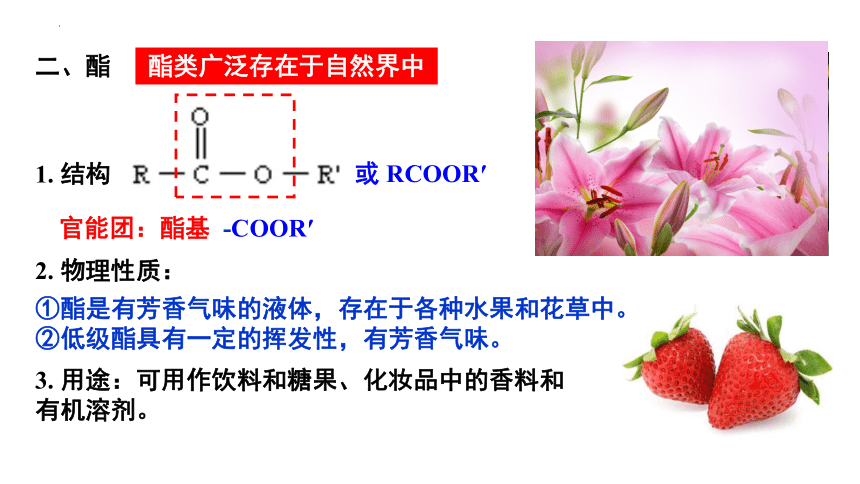
酯类广泛存在于自然界中
①酯是有芳香气味的液体,存在于各种水果和花草中。
②低级酯具有一定的挥发性,有芳香气味。
3. 用途:可用作饮料和糖果、化妆品中的香料和有机溶剂。
二、酯
1. 结构
或 RCOOR′
官能团:酯基 -COOR′
2. 物理性质:
4. 酯化反应产物命名:
某酸某酯
【练习】写出下列酯化反应的方程式,并把生成的酯命名
②CH3OH与CH3COOH
乙酸甲酯
①CH3OH与HCOOH
甲酸甲酯
C
O
OH
H
+ HO-CH3
C
O
O-CH3
H
浓H2SO4
C
O
OH
CH3
+ HO-CH3
C
O
O-CH3
CH3
浓H2SO4
+ H2O
+ H2O
阅读课本80页,回答下列问题:
1. 常见的官能团有哪些?代表物?
2. 认识有机物的一般思路?
【问题导学2】
官能团与有机化合物的分类
通过对乙烯、乙醇和乙酸性质的学习,我们认识到官能团对有机物的性质具有决定作用,含有相同官能团的有机物在性质上具有相似之处。因此我们可以根据有机物分子中所含官能团的不同,从结构和性质上对数量庞大的有机物进行分类(如表7-2)。
【点拨精讲2】
有机物的主要类别、官能团及典型代表物
类别 官能团的结构和名称 典型代表物的
名称和结构简式
烃
乙烯 CH2=CH2
甲烷 CH4
碳碳双键
碳碳三键
乙炔 CH≡CH
苯
不饱和烃
饱和烃
烷烃
环烷烃
环丙烷
烯烃
炔烃
芳香烃
类别 官能团的结构和名称 典型代表物的
名称和结构简式
烃 的 衍 生 物
CH3CH2Br
—X( F、Cl、Br、I)
(醇)羟基
—OH
CH3CH2OH
乙醇
酯基
醛基
羧基
乙酸
乙酸乙酯
R是烃基
—CHO
—COOH
—COOR
CH3CHO
CH3COOH
CH3COOC2H5
碳卤键
溴乙烷
乙醛
卤代烃
醇
醛
羧酸
酯
【方法引导】
认识有机化合物的一般思路
认识一种有机物,可先从结构入手,分析其碳骨架和官能团,了解它所属的有机物类别;再结合这类有机物的一般性质,推测该有机物可能具有的性质,并通过实验进行验证;在此基础上进一步了解该有机物的用途。另外,还可以根据有机物发生的化学反应,了解其在有机物转化(有机合成)中的作用。与认识无机物类似,认识有机物也体现了“结构决定性质”的观念。各类有机物在结构和性质上具有的明显规律性,有助于我们更好地认识有机物。
一、乙酸乙酯的实验室制备
1. 实验原理:
CH3COOH + HOC2H5 H2O+CH3COOC2H5
浓H2SO4
2. 注意事项
二、酯
酯的密度一般小于水,并难溶于水,易溶于乙醇和乙醚等有机溶剂。
三、官能团与有机化合物的分类
【课堂小结】
1.除去乙酸乙酯中含有的乙酸,最好的处理和操作是
A.蒸馏 B.水洗后分液
C.用过量饱和碳酸钠溶液洗涤后分液
D.用过量氢氧化钠溶液洗涤后分液
2.实验室用乙酸、乙醇、浓H2SO4制取乙酸乙酯,加热蒸馏后,在饱和Na2CO3溶液的上面得到无色油状液体,当振荡混合时,有气泡产生,原因是
A.产品中有被蒸馏出的H2SO4
B.有部分未反应的乙醇被蒸馏出来
C.有部分未反应的乙酸被蒸馏出来
D.有部分乙醇跟浓H2SO4作用生成乙烯
【当堂检测】
C
C
3.某学习小组在实验室制取乙酸乙酯的主要步骤如下:
①配制2 mL浓硫酸、3 mL乙醇(含18O)和2 mL乙酸的混合溶液。
②按如图连接好装置并加入混合液,用小火均匀加热3~5 min。
③待试管乙收集到一定量产物后停止加热,撤出试管乙用力振荡,然后静置待分层。
④分离出乙酸乙酯,洗涤、干燥。
回答问题:
(1)装置中球形干燥管,除起冷凝作用外,另一重要作用是_________。
(2)步骤②安装好实验装置,加入药品前还应检查_______________。
防止倒吸
装置的气密性
(4)上述实验中饱和碳酸钠溶液的作用是______(填字母)。
a. 中和乙酸并吸收乙醇
b. 中和乙酸和乙醇
c. 减少乙酸乙酯的溶解
d. 加速酯的生成,提高其产率
(5)步骤③所观察到的现象是________________________________
________________________________________________________;
(3)反应中浓硫酸的作用是________________。
催化剂、吸水剂
ac
试管乙中的液体分成上下两层,
上层无色,下层为红,色液体,振荡后下层液体的红色变浅
(3)巴豆酸与金属钠溶液反应的化学方程式为
____________________________________________________________;
巴豆酸与溴水发生加成反应的化学方程式为
____________________________________________________________;
巴豆酸跟乙醇在浓硫酸催化下发生酯化反应的化学方程式为
____________________________________________________________。
(2)现有①氯化氢②溴水③纯碱溶液④乙醇⑤酸性高锰酸钾溶液,在一定条件下能与巴豆酸反应的物质是____________________。
4.巴豆酸的结构简式为:
(1)巴豆酸的分子中含有__________和________两种官能团(写名称);
①②③④⑤
碳碳双键 羧基
5.有机物A的结构简式为 ,取1molA,分别与
足量的Na、NaOH、NaHCO3反应,消耗三种物质的物质的量之比为
A. 2:1:1 B. 1:1:1 C. 4:2:1 D. 4:4:1
CH2OH
CH3
CH2COOH
A
6.在同温同压下,某有机物和过量Na反应得到V1L氢气,另一份等量的该有机物和足量的NaHCO3反应得到V2L二氧化碳,若V1=V2≠0,则该有机物可能是
A. CH3CHCOOH B. HOOC-COOH C. HOCH2CH2OH D. CH3COOH
OH
A
喝点醋能解酒
第七章 有机化合物
第三节 乙醇与乙酸
第2课时 乙酸
1. 巩固乙酸的化学性质和酯化反应
2. 掌握实验室制乙酸乙酯的原理及事项
3. 掌握官能团与有机化合物的分类
【学习目标】
1. 制备乙酸乙酯的原理
3. 如何加快制备乙酸乙酯的反应速率?
2. 制备乙酸乙酯药品的滴加顺序?
4. 饱和的Na2CO3溶液的作用?
【问题导学1】
一、乙酸乙酯的实验室制备
【实验7-6】在一支试管中加入3mL乙醇,然后边振荡试管边加慢慢加入2mL浓硫酸,和2mL 乙酸,再加入几片碎瓷片。连接好装置,用酒精灯小心加热,将产生的蒸汽经导管通入饱和碳酸钠液面之上,观察现象。
现象:
1. 碳酸钠液面分层,上层有无色油状液体;
2. 可闻到香味。(果香味)
【点拨精讲1】
反应原理和过程分析
CH3COOH + HOC2H5 H2O + CH3COOC2H5
浓H2SO4
反应特点
②可逆反应
③生成的乙酸乙酯和H2O如果留在反应液里会抑制反应向正方向进行。
①常温下几乎不反应,需加热和催化剂
④乙醇沸点(78.5℃)和乙酸沸点(117.8℃)都较低,当乙酸乙酯形成蒸气被导出时,其中会混有少量乙醇和乙酸蒸气。冷却后的乙酸乙酯和乙醇、乙酸都互溶而难于分离。
冰醋酸 无水乙醇 乙酸乙酯
防止倒吸
增大受热面积
乙醇→浓硫酸→乙酸
2. 试管倾斜加热的目的?
3. 加碎瓷片或沸石的作用?
防止液体暴沸
4. 浓硫酸的作用?
①催化剂:加快化学反应速率。 ②吸水剂:促进反应向正反应方向进行。
6. 为什么导管不插入饱和Na2CO3溶液中?
导气、冷凝、回流
5. 长导管的作用?
1. 加入试剂的先后顺序?
饱和的Na2CO3溶液
注意事项
8. 能否用氢氧化钠溶液代替饱和Na2CO3溶液?
NaOH溶液能使生成的酯水解,故不可能用。
CH3COOC2H5+NaOH CH3COONa+C2H5 OH
9. 如何提高乙酸的转化率?
①过量的乙醇增大反应进行的程度;
②浓硫酸的吸水性增大反应进行的程度;
③及时分离生成物等。
7. 饱和Na2CO3溶液作用?
中和乙酸,溶解乙醇,降低乙酸乙酯的溶解度,
提高水溶液的密度以加速乙酸乙酯与水溶液的分层
饱和Na2CO3溶液
CH3 C O H + H O C2H5 CH3 C O C2H5+H O H
CH3 C O H + H O C2H5 CH3 C O C2H5 +H O H
O
O
浓H2SO4
方式一:
O
O
方式二:
用什么方法或实验来确定其脱水方式?
酯化反应中,乙醇和乙酸如何断键脱水?
浓H2SO4
同位素原子示踪法
浓H2SO4
CH3 C O H + H 18O C2H5 CH3 C 18O C2H5 + H2O
O
O
酯化反应本质:酸脱羟基、醇脱氢(羟基上氢)。
酯类广泛存在于自然界中
①酯是有芳香气味的液体,存在于各种水果和花草中。
②低级酯具有一定的挥发性,有芳香气味。
3. 用途:可用作饮料和糖果、化妆品中的香料和有机溶剂。
二、酯
1. 结构
或 RCOOR′
官能团:酯基 -COOR′
2. 物理性质:
4. 酯化反应产物命名:
某酸某酯
【练习】写出下列酯化反应的方程式,并把生成的酯命名
②CH3OH与CH3COOH
乙酸甲酯
①CH3OH与HCOOH
甲酸甲酯
C
O
OH
H
+ HO-CH3
C
O
O-CH3
H
浓H2SO4
C
O
OH
CH3
+ HO-CH3
C
O
O-CH3
CH3
浓H2SO4
+ H2O
+ H2O
阅读课本80页,回答下列问题:
1. 常见的官能团有哪些?代表物?
2. 认识有机物的一般思路?
【问题导学2】
官能团与有机化合物的分类
通过对乙烯、乙醇和乙酸性质的学习,我们认识到官能团对有机物的性质具有决定作用,含有相同官能团的有机物在性质上具有相似之处。因此我们可以根据有机物分子中所含官能团的不同,从结构和性质上对数量庞大的有机物进行分类(如表7-2)。
【点拨精讲2】
有机物的主要类别、官能团及典型代表物
类别 官能团的结构和名称 典型代表物的
名称和结构简式
烃
乙烯 CH2=CH2
甲烷 CH4
碳碳双键
碳碳三键
乙炔 CH≡CH
苯
不饱和烃
饱和烃
烷烃
环烷烃
环丙烷
烯烃
炔烃
芳香烃
类别 官能团的结构和名称 典型代表物的
名称和结构简式
烃 的 衍 生 物
CH3CH2Br
—X( F、Cl、Br、I)
(醇)羟基
—OH
CH3CH2OH
乙醇
酯基
醛基
羧基
乙酸
乙酸乙酯
R是烃基
—CHO
—COOH
—COOR
CH3CHO
CH3COOH
CH3COOC2H5
碳卤键
溴乙烷
乙醛
卤代烃
醇
醛
羧酸
酯
【方法引导】
认识有机化合物的一般思路
认识一种有机物,可先从结构入手,分析其碳骨架和官能团,了解它所属的有机物类别;再结合这类有机物的一般性质,推测该有机物可能具有的性质,并通过实验进行验证;在此基础上进一步了解该有机物的用途。另外,还可以根据有机物发生的化学反应,了解其在有机物转化(有机合成)中的作用。与认识无机物类似,认识有机物也体现了“结构决定性质”的观念。各类有机物在结构和性质上具有的明显规律性,有助于我们更好地认识有机物。
一、乙酸乙酯的实验室制备
1. 实验原理:
CH3COOH + HOC2H5 H2O+CH3COOC2H5
浓H2SO4
2. 注意事项
二、酯
酯的密度一般小于水,并难溶于水,易溶于乙醇和乙醚等有机溶剂。
三、官能团与有机化合物的分类
【课堂小结】
1.除去乙酸乙酯中含有的乙酸,最好的处理和操作是
A.蒸馏 B.水洗后分液
C.用过量饱和碳酸钠溶液洗涤后分液
D.用过量氢氧化钠溶液洗涤后分液
2.实验室用乙酸、乙醇、浓H2SO4制取乙酸乙酯,加热蒸馏后,在饱和Na2CO3溶液的上面得到无色油状液体,当振荡混合时,有气泡产生,原因是
A.产品中有被蒸馏出的H2SO4
B.有部分未反应的乙醇被蒸馏出来
C.有部分未反应的乙酸被蒸馏出来
D.有部分乙醇跟浓H2SO4作用生成乙烯
【当堂检测】
C
C
3.某学习小组在实验室制取乙酸乙酯的主要步骤如下:
①配制2 mL浓硫酸、3 mL乙醇(含18O)和2 mL乙酸的混合溶液。
②按如图连接好装置并加入混合液,用小火均匀加热3~5 min。
③待试管乙收集到一定量产物后停止加热,撤出试管乙用力振荡,然后静置待分层。
④分离出乙酸乙酯,洗涤、干燥。
回答问题:
(1)装置中球形干燥管,除起冷凝作用外,另一重要作用是_________。
(2)步骤②安装好实验装置,加入药品前还应检查_______________。
防止倒吸
装置的气密性
(4)上述实验中饱和碳酸钠溶液的作用是______(填字母)。
a. 中和乙酸并吸收乙醇
b. 中和乙酸和乙醇
c. 减少乙酸乙酯的溶解
d. 加速酯的生成,提高其产率
(5)步骤③所观察到的现象是________________________________
________________________________________________________;
(3)反应中浓硫酸的作用是________________。
催化剂、吸水剂
ac
试管乙中的液体分成上下两层,
上层无色,下层为红,色液体,振荡后下层液体的红色变浅
(3)巴豆酸与金属钠溶液反应的化学方程式为
____________________________________________________________;
巴豆酸与溴水发生加成反应的化学方程式为
____________________________________________________________;
巴豆酸跟乙醇在浓硫酸催化下发生酯化反应的化学方程式为
____________________________________________________________。
(2)现有①氯化氢②溴水③纯碱溶液④乙醇⑤酸性高锰酸钾溶液,在一定条件下能与巴豆酸反应的物质是____________________。
4.巴豆酸的结构简式为:
(1)巴豆酸的分子中含有__________和________两种官能团(写名称);
①②③④⑤
碳碳双键 羧基
5.有机物A的结构简式为 ,取1molA,分别与
足量的Na、NaOH、NaHCO3反应,消耗三种物质的物质的量之比为
A. 2:1:1 B. 1:1:1 C. 4:2:1 D. 4:4:1
CH2OH
CH3
CH2COOH
A
6.在同温同压下,某有机物和过量Na反应得到V1L氢气,另一份等量的该有机物和足量的NaHCO3反应得到V2L二氧化碳,若V1=V2≠0,则该有机物可能是
A. CH3CHCOOH B. HOOC-COOH C. HOCH2CH2OH D. CH3COOH
OH
A
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
