9.3钢铁的锈蚀与防护同步练习(含答案)—2022-2023学年九年级化学鲁教版下册
文档属性
| 名称 | 9.3钢铁的锈蚀与防护同步练习(含答案)—2022-2023学年九年级化学鲁教版下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 421.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-24 00:00:00 | ||
图片预览

文档简介
9.3钢铁的锈蚀与防护
同步练习
一、单选题
1.保护环境人人有责,做好垃圾分类是我们每个人的责任和义务。废旧金属属于
A.可回收物 B.其他垃圾
C.厨余垃圾 D.有害垃圾
2.为了延缓袋装食品变质,包装时不宜采用
A.充入空气 B.真空包装
C.放入一小包生石灰 D.放入一小包铁粉
3.下列有关资源及能源的说法正确的是( )
A.地球表面约有96.5%被水覆盖,但可利用的淡水资源是有限的
B.目前使用最多的金属材料是铝
C.煤、石油、沼气等化石能源储量有限,且不能再生
D.空气中稀有气体约占空气体积的0.94%
4.下列生活中的做法正确的是( )
A.用汽油除去衣服上的油污
B.将养鱼池中的水喷向空中,可以增大水与空气的接触面积,增加氧气的溶解度
C.用喷漆的方法防止自行车链条锈蚀
D.用铝作人造卫星和宇宙飞船的天线
5.下列生活中的做法合理的是
A.炒菜时油锅中的油着火,用水浇灭
B.食品包装袋内放一包铁粉,用来吸收袋内空气中的水和氧气
C.用煤炉取暖,在煤炉上放一壶水以防止CO中毒
D.煮肉后的铝锅,可用钢丝球反复擦洗干净
6.下列与金属相关的说法正确的是
A.生铁和钢性能完全相同
B.炼铁过程只发生物理变化
C.常温下所有金属均为固态
D.铁在潮湿的空气中易生锈
7.下列有关说法错误的是
A.回收废旧金属是保护金属资源的重要途径
B.人呼出的气体主要成分是二氧化碳,只能用向上排空气法收集
C.自然界中的水经过沉降、过滤、吸附等净化处理后,硬度不会明显降低
D.天然气的主要成分是甲烷
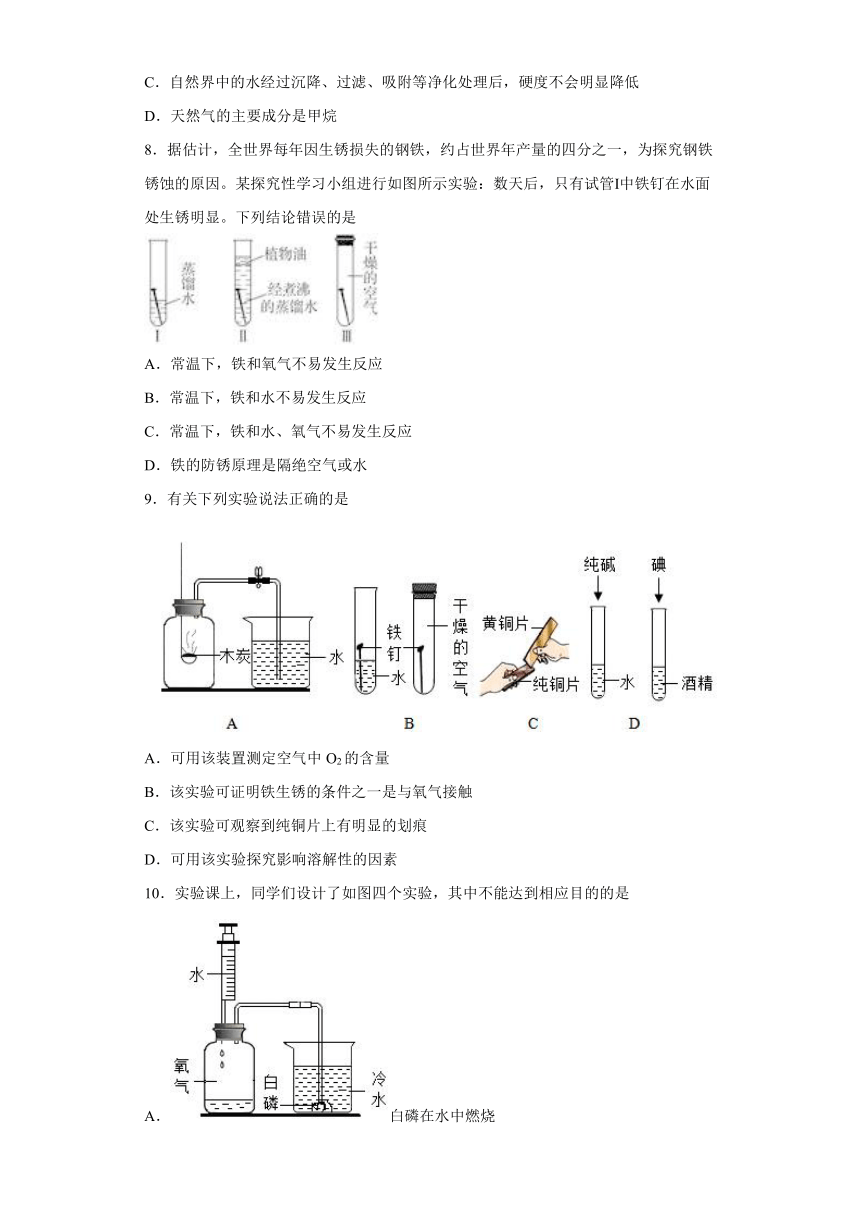
8.据估计,全世界每年因生锈损失的钢铁,约占世界年产量的四分之一,为探究钢铁锈蚀的原因。某探究性学习小组进行如图所示实验:数天后,只有试管Ⅰ中铁钉在水面处生锈明显。下列结论错误的是
A.常温下,铁和氧气不易发生反应
B.常温下,铁和水不易发生反应
C.常温下,铁和水、氧气不易发生反应
D.铁的防锈原理是隔绝空气或水
9.有关下列实验说法正确的是
A.可用该装置测定空气中O2的含量
B.该实验可证明铁生锈的条件之一是与氧气接触
C.该实验可观察到纯铜片上有明显的划痕
D.可用该实验探究影响溶解性的因素
10.实验课上,同学们设计了如图四个实验,其中不能达到相应目的的是
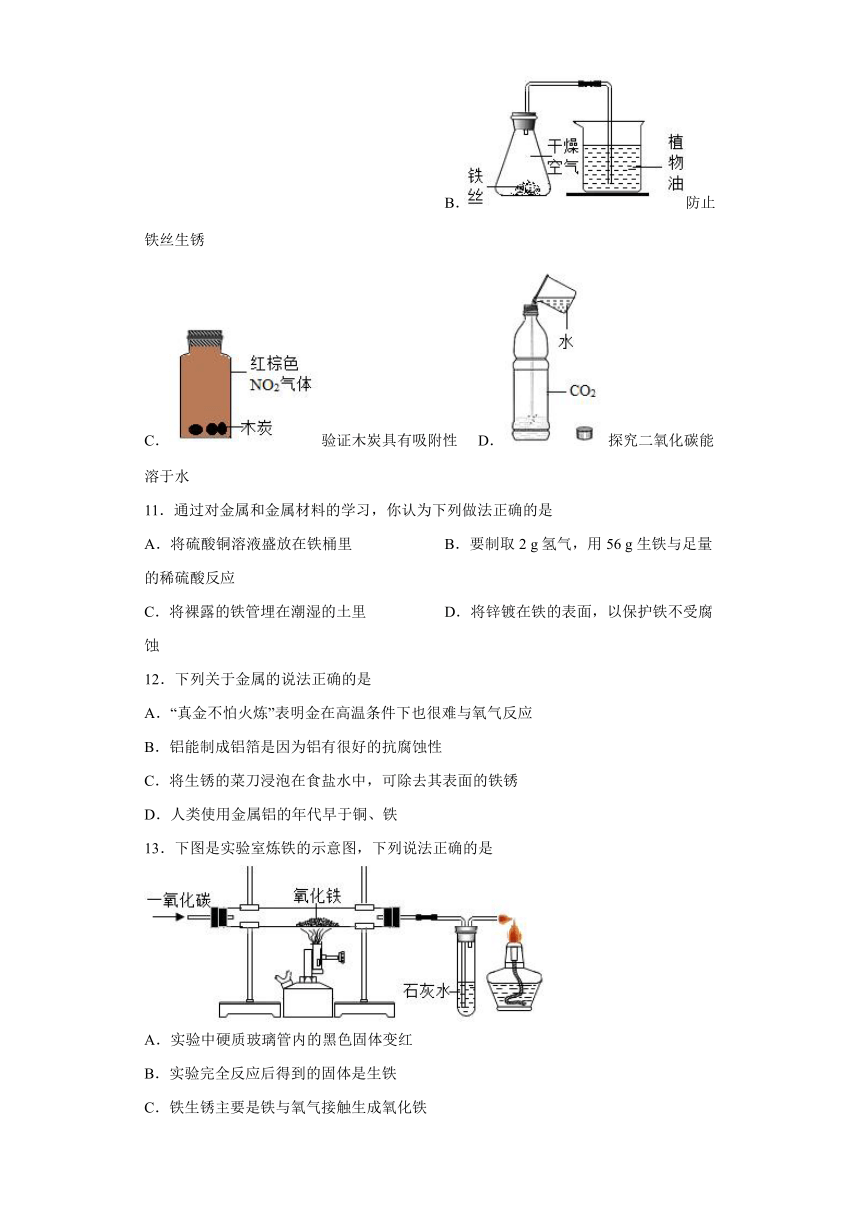
A.白磷在水中燃烧 B.防止铁丝生锈
C.验证木炭具有吸附性 D.探究二氧化碳能溶于水
11.通过对金属和金属材料的学习,你认为下列做法正确的是
A.将硫酸铜溶液盛放在铁桶里 B.要制取2 g氢气,用56 g生铁与足量的稀硫酸反应
C.将裸露的铁管埋在潮湿的土里 D.将锌镀在铁的表面,以保护铁不受腐蚀
12.下列关于金属的说法正确的是
A.“真金不怕火炼”表明金在高温条件下也很难与氧气反应
B.铝能制成铝箔是因为铝有很好的抗腐蚀性
C.将生锈的菜刀浸泡在食盐水中,可除去其表面的铁锈
D.人类使用金属铝的年代早于铜、铁
13.下图是实验室炼铁的示意图,下列说法正确的是
A.实验中硬质玻璃管内的黑色固体变红
B.实验完全反应后得到的固体是生铁
C.铁生锈主要是铁与氧气接触生成氧化铁
D.该反应的原理为
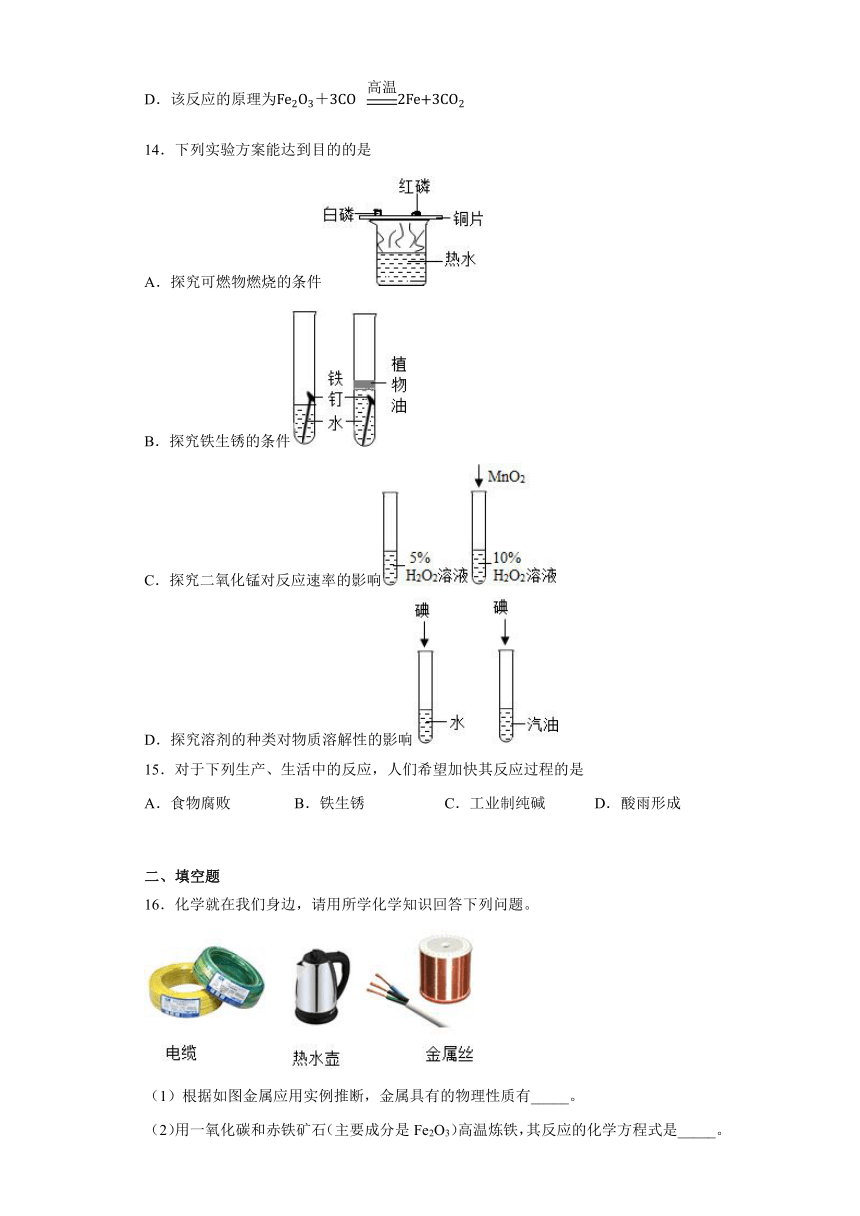
14.下列实验方案能达到目的的是
A.探究可燃物燃烧的条件
B.探究铁生锈的条件
C.探究二氧化锰对反应速率的影响
D.探究溶剂的种类对物质溶解性的影响
15.对于下列生产、生活中的反应,人们希望加快其反应过程的是
A.食物腐败 B.铁生锈 C.工业制纯碱 D.酸雨形成
二、填空题
16.化学就在我们身边,请用所学化学知识回答下列问题。
(1)根据如图金属应用实例推断,金属具有的物理性质有_____。
(2)用一氧化碳和赤铁矿石(主要成分是Fe2O3)高温炼铁,其反应的化学方程式是_____。
(3)保护金属资源,防止腐蚀是关键。日常生活中如何防止铁锅锈蚀_____。
17.金属材料在生产、生活、化学实验中有着广泛应用。
(1)下列属于金属材料的是___(填序号)。
A.水泥 B.硬铝 C.纯铜 D.玻璃
(2)《天工开物》中记载“凡金箔每七寸造方寸金一千片”,体现金具有的物理性质是___。
(3)《淮南万毕术》有“曾青(硫酸铜溶液)得铁则化为铜”的湿法炼铜工艺,有关反应的化学方程式为______。
(4)2022年3月29日,我国首型固体捆绑中型运载火箭“长征六号改”首飞,标志着我国新一代运载火箭家族再添新成员。火箭中运用了大量合金,下列有关合金的说法不正确的是___(填序号)。
A.合金的抗腐蚀性能比组成它们的纯金属好 B.合金中一定含非金属元素
C.生铁是比钢含碳量高的铁合金 D.合金的熔点比组成它们的纯金属高
(5)金属资源的保护格外重要。下列做法不能有效保护金属资源的是___(填序号)。
A.寻找,开发金属的代用品 B.在金属栏杆表面刷漆防锈
C.任意开采金属矿物 D.回收废旧金属
18.金属材料与人类的生产和生活密切相关。
(1)唐太宗曾说:“以铜为镜,可以正衣冠;以史为镜,可以知兴替;以人为镜,可以明得失。”铜之所以能为镜是因为 (填字母)
A.铜有金属光泽 B.铜能导热 C.铜能导电 D.铜不容易生锈
(2)铁是目前世界上年产量最高的金属,工业上采用赤铁矿炼铁的反应原理是_______(用化学方程式表示)。
(3)世界每年因腐蚀而报废的金属相当于年产量的20%-40%,为探究铁生锈的原因,化学兴趣小组同学设计如图实验通过对比试管①②中的现象,可说明铁生锈与____________有关。
19.铁是生产、生活中应用很广泛的一种金属。如图是与铁的性质有关的部分实验图,请回答下列问题。
(1)A中细铁丝燃烧时集气瓶中水的作用______。
(2)B中铁钉最易生锈的部位是______(填“a”、“b”或“c”)。
(3)C中铁和硫酸铜溶液反应的化学方程式为______。
20.金属的用途广,我们应该节约和保护金属资源。
“沉睡数千年,一醒惊天下”。自1929年至今,我国有计划地对四川三星堆遗址进行的13次挖掘,共出土金面具残片、巨青铜面具、鸟型金饰片、青铜神树、精美牙雕残件等重要文物500余件,作为公元前16世纪至公元前14世纪世界青铜文明的重要代表,被誉为“堪比兵马俑的第九大奇迹”。
(1)如图是三星堆出土的青铜面具。青铜是一种铜锡合金,由此推断青铜比铜的硬度______(选填“大”或“小”);则出土时,青铜因腐蚀常有Cu2(OH)3Cl覆盖在其表面,其中铜元素的化合价为______价。
(2)金属元素位于元素周期表中的______(选填“左下”或“右上”),因其原子在化学反应中易______(选填“失去”或“得到”)最外层电子而导致绝大部分金属在自然界中以化合物的状态存在。工业炼铁就是把铁从它的化合物中再还原出来,写出一氧化碳还原氧化铁的化学方程式______,在这个反应中铁元素的化合价变化情况是______。
(3)以下是三种防止钢铁锈蚀的方法①在金属表面涂油②在金属表面“烤蓝”③改变金属的组成和结构,从使用角度看,最耐用的方法是______(选填数字序号)。
(4)X、Y、Z是三种金属。已知①X+H2SO4=XSO4+H2↑②Y+2ZNO3=Y(NO3)2+2Z③Y与稀硫酸不反应,根据金属活动性顺序表判断,符合要求的X、Y、Z是______(选填字母序号)。
A.Cu、Hg、Ag B.Fe、Cu、Ag C.Mg、Cu、Fe
三、实验题
21.化学是以实验为基础的学科,根据下列实验回答问题。
实验一 实验二
(1)实验一:
①实验室用高锰酸钾制取氧气应选用的装置是________,(填字母),发生反应的化学方程式为________。
②装置C、D是收集到的两瓶氧气,若进行铁丝在氧气中燃烧的实验,应选用的一瓶是________(填字母);实验中可观察到铁丝剧烈燃烧,________。
(2)实验二:三天后,观察到序号为________的试管中铁钉明显生锈。对照实验①和③,可知铁锈蚀与______有关。
参考答案:
1.A2.A3.D4.A5.B6.D7.B8.C9.C10.A11.D12.A13.D14.D15.C
16. 导电性、导热性、延展性 保持干燥(防水)或表面涂油(隔绝氧气)(其它合理答案均可)
17.(1)BC
(2)黄金具有良好的延展性
(3)
(4)AC
(5)C
18.(1)A
(2)
(3)氧气
19. 防止高温熔化物溅落炸裂瓶底 b
20. 大 +2 左下 失去
+3价到0价 ③ B
21. A D 火星四射,生成黑色固体,放出热量 ③ 水
同步练习
一、单选题
1.保护环境人人有责,做好垃圾分类是我们每个人的责任和义务。废旧金属属于
A.可回收物 B.其他垃圾
C.厨余垃圾 D.有害垃圾
2.为了延缓袋装食品变质,包装时不宜采用
A.充入空气 B.真空包装
C.放入一小包生石灰 D.放入一小包铁粉
3.下列有关资源及能源的说法正确的是( )
A.地球表面约有96.5%被水覆盖,但可利用的淡水资源是有限的
B.目前使用最多的金属材料是铝
C.煤、石油、沼气等化石能源储量有限,且不能再生
D.空气中稀有气体约占空气体积的0.94%
4.下列生活中的做法正确的是( )
A.用汽油除去衣服上的油污
B.将养鱼池中的水喷向空中,可以增大水与空气的接触面积,增加氧气的溶解度
C.用喷漆的方法防止自行车链条锈蚀
D.用铝作人造卫星和宇宙飞船的天线
5.下列生活中的做法合理的是
A.炒菜时油锅中的油着火,用水浇灭
B.食品包装袋内放一包铁粉,用来吸收袋内空气中的水和氧气
C.用煤炉取暖,在煤炉上放一壶水以防止CO中毒
D.煮肉后的铝锅,可用钢丝球反复擦洗干净
6.下列与金属相关的说法正确的是
A.生铁和钢性能完全相同
B.炼铁过程只发生物理变化
C.常温下所有金属均为固态
D.铁在潮湿的空气中易生锈
7.下列有关说法错误的是
A.回收废旧金属是保护金属资源的重要途径
B.人呼出的气体主要成分是二氧化碳,只能用向上排空气法收集
C.自然界中的水经过沉降、过滤、吸附等净化处理后,硬度不会明显降低
D.天然气的主要成分是甲烷
8.据估计,全世界每年因生锈损失的钢铁,约占世界年产量的四分之一,为探究钢铁锈蚀的原因。某探究性学习小组进行如图所示实验:数天后,只有试管Ⅰ中铁钉在水面处生锈明显。下列结论错误的是
A.常温下,铁和氧气不易发生反应
B.常温下,铁和水不易发生反应
C.常温下,铁和水、氧气不易发生反应
D.铁的防锈原理是隔绝空气或水
9.有关下列实验说法正确的是
A.可用该装置测定空气中O2的含量
B.该实验可证明铁生锈的条件之一是与氧气接触
C.该实验可观察到纯铜片上有明显的划痕
D.可用该实验探究影响溶解性的因素
10.实验课上,同学们设计了如图四个实验,其中不能达到相应目的的是
A.白磷在水中燃烧 B.防止铁丝生锈
C.验证木炭具有吸附性 D.探究二氧化碳能溶于水
11.通过对金属和金属材料的学习,你认为下列做法正确的是
A.将硫酸铜溶液盛放在铁桶里 B.要制取2 g氢气,用56 g生铁与足量的稀硫酸反应
C.将裸露的铁管埋在潮湿的土里 D.将锌镀在铁的表面,以保护铁不受腐蚀
12.下列关于金属的说法正确的是
A.“真金不怕火炼”表明金在高温条件下也很难与氧气反应
B.铝能制成铝箔是因为铝有很好的抗腐蚀性
C.将生锈的菜刀浸泡在食盐水中,可除去其表面的铁锈
D.人类使用金属铝的年代早于铜、铁
13.下图是实验室炼铁的示意图,下列说法正确的是
A.实验中硬质玻璃管内的黑色固体变红
B.实验完全反应后得到的固体是生铁
C.铁生锈主要是铁与氧气接触生成氧化铁
D.该反应的原理为
14.下列实验方案能达到目的的是
A.探究可燃物燃烧的条件
B.探究铁生锈的条件
C.探究二氧化锰对反应速率的影响
D.探究溶剂的种类对物质溶解性的影响
15.对于下列生产、生活中的反应,人们希望加快其反应过程的是
A.食物腐败 B.铁生锈 C.工业制纯碱 D.酸雨形成
二、填空题
16.化学就在我们身边,请用所学化学知识回答下列问题。
(1)根据如图金属应用实例推断,金属具有的物理性质有_____。
(2)用一氧化碳和赤铁矿石(主要成分是Fe2O3)高温炼铁,其反应的化学方程式是_____。
(3)保护金属资源,防止腐蚀是关键。日常生活中如何防止铁锅锈蚀_____。
17.金属材料在生产、生活、化学实验中有着广泛应用。
(1)下列属于金属材料的是___(填序号)。
A.水泥 B.硬铝 C.纯铜 D.玻璃
(2)《天工开物》中记载“凡金箔每七寸造方寸金一千片”,体现金具有的物理性质是___。
(3)《淮南万毕术》有“曾青(硫酸铜溶液)得铁则化为铜”的湿法炼铜工艺,有关反应的化学方程式为______。
(4)2022年3月29日,我国首型固体捆绑中型运载火箭“长征六号改”首飞,标志着我国新一代运载火箭家族再添新成员。火箭中运用了大量合金,下列有关合金的说法不正确的是___(填序号)。
A.合金的抗腐蚀性能比组成它们的纯金属好 B.合金中一定含非金属元素
C.生铁是比钢含碳量高的铁合金 D.合金的熔点比组成它们的纯金属高
(5)金属资源的保护格外重要。下列做法不能有效保护金属资源的是___(填序号)。
A.寻找,开发金属的代用品 B.在金属栏杆表面刷漆防锈
C.任意开采金属矿物 D.回收废旧金属
18.金属材料与人类的生产和生活密切相关。
(1)唐太宗曾说:“以铜为镜,可以正衣冠;以史为镜,可以知兴替;以人为镜,可以明得失。”铜之所以能为镜是因为 (填字母)
A.铜有金属光泽 B.铜能导热 C.铜能导电 D.铜不容易生锈
(2)铁是目前世界上年产量最高的金属,工业上采用赤铁矿炼铁的反应原理是_______(用化学方程式表示)。
(3)世界每年因腐蚀而报废的金属相当于年产量的20%-40%,为探究铁生锈的原因,化学兴趣小组同学设计如图实验通过对比试管①②中的现象,可说明铁生锈与____________有关。
19.铁是生产、生活中应用很广泛的一种金属。如图是与铁的性质有关的部分实验图,请回答下列问题。
(1)A中细铁丝燃烧时集气瓶中水的作用______。
(2)B中铁钉最易生锈的部位是______(填“a”、“b”或“c”)。
(3)C中铁和硫酸铜溶液反应的化学方程式为______。
20.金属的用途广,我们应该节约和保护金属资源。
“沉睡数千年,一醒惊天下”。自1929年至今,我国有计划地对四川三星堆遗址进行的13次挖掘,共出土金面具残片、巨青铜面具、鸟型金饰片、青铜神树、精美牙雕残件等重要文物500余件,作为公元前16世纪至公元前14世纪世界青铜文明的重要代表,被誉为“堪比兵马俑的第九大奇迹”。
(1)如图是三星堆出土的青铜面具。青铜是一种铜锡合金,由此推断青铜比铜的硬度______(选填“大”或“小”);则出土时,青铜因腐蚀常有Cu2(OH)3Cl覆盖在其表面,其中铜元素的化合价为______价。
(2)金属元素位于元素周期表中的______(选填“左下”或“右上”),因其原子在化学反应中易______(选填“失去”或“得到”)最外层电子而导致绝大部分金属在自然界中以化合物的状态存在。工业炼铁就是把铁从它的化合物中再还原出来,写出一氧化碳还原氧化铁的化学方程式______,在这个反应中铁元素的化合价变化情况是______。
(3)以下是三种防止钢铁锈蚀的方法①在金属表面涂油②在金属表面“烤蓝”③改变金属的组成和结构,从使用角度看,最耐用的方法是______(选填数字序号)。
(4)X、Y、Z是三种金属。已知①X+H2SO4=XSO4+H2↑②Y+2ZNO3=Y(NO3)2+2Z③Y与稀硫酸不反应,根据金属活动性顺序表判断,符合要求的X、Y、Z是______(选填字母序号)。
A.Cu、Hg、Ag B.Fe、Cu、Ag C.Mg、Cu、Fe
三、实验题
21.化学是以实验为基础的学科,根据下列实验回答问题。
实验一 实验二
(1)实验一:
①实验室用高锰酸钾制取氧气应选用的装置是________,(填字母),发生反应的化学方程式为________。
②装置C、D是收集到的两瓶氧气,若进行铁丝在氧气中燃烧的实验,应选用的一瓶是________(填字母);实验中可观察到铁丝剧烈燃烧,________。
(2)实验二:三天后,观察到序号为________的试管中铁钉明显生锈。对照实验①和③,可知铁锈蚀与______有关。
参考答案:
1.A2.A3.D4.A5.B6.D7.B8.C9.C10.A11.D12.A13.D14.D15.C
16. 导电性、导热性、延展性 保持干燥(防水)或表面涂油(隔绝氧气)(其它合理答案均可)
17.(1)BC
(2)黄金具有良好的延展性
(3)
(4)AC
(5)C
18.(1)A
(2)
(3)氧气
19. 防止高温熔化物溅落炸裂瓶底 b
20. 大 +2 左下 失去
+3价到0价 ③ B
21. A D 火星四射,生成黑色固体,放出热量 ③ 水
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
