6.3金属矿物与冶炼同步练习(含答案)-2022-2023学年九年级化学科粤版下册
文档属性
| 名称 | 6.3金属矿物与冶炼同步练习(含答案)-2022-2023学年九年级化学科粤版下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 71.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-24 00:00:00 | ||
图片预览


文档简介
6.3 金属矿物与冶炼
同步练习
一、单选题
1.工业上通过反应 SiO2+2CSi+2CO↑将自然界中二氧化硅转化为硅,该反应中( )
A.一氧化碳作还原剂 B.二氧化硅发生了氧化反应
C.二氧化硅是氧化剂 D.碳发生了还原反应
2.金属是重要的资源。下列有关金属的说法错误的是
A.“湿法炼铜”的化学原理可以表示为:
B.金属与金属、金属与非金属都可能形成合金
C.工业上用一氧化碳还原氧化铁制备铁,该反应属于置换反应
D.金属钠和镁化学性质不同是由于最外层电子数不同
3.下列有关实验现象描述正确的是
A.细铁丝在氧气中燃烧,火星四射,生成白色固体
B.红磷在空气中燃烧产生大量白色烟雾
C.将一氧化碳通入灼热的氧化铁粉末,一段时间,黑色粉末变红
D.将铜丝放入硝酸银溶液中,溶液由无色变为蓝色
4.兴趣小组同学利用如图所示装置模拟工业炼铁。下列说法错误的是
A.赤铁矿的主要成分是Fe2O3
B.实验时应先通入CO再点燃酒精灯
C.充分加热后,a处固体由红棕色变为黑色
D.可用水吸收尾气中的CO
5.为适应火车提速,沪宁线上原有的短轨全部接为超长轨。在焊接过程中,工程技术人员点燃铝热剂(铝粉和氧化铁的混合物)能释放大量的能量,生成熔融状态的铁可用来连接铁轨,反应的化学方程式为,其中的还原剂为
A. B. C. D.
6.下列用途中,主要利用物质物理性质的是
A.焦炭用于炼铁 B.食品包装袋中充入氮气
C.氢气作高能燃料 D.竹炭除冰箱中的异味
7.化学研究的目的就是帮助人们认识、改造和应用物质,把金属矿物冶炼成金属就是人们利用化学方法实现物质改造的典型范例.下表中不同的金属被开发和利用的年代不同,从化学反应的角度看,决定这一年代先后顺序的关键因素是
A.金属的活动性 B.金属的导电性
C.金属的延展性 D.地壳中金属元素的含量
8.下列做法正确的是( )
A.洒出的酒精在桌面上燃烧起来,赶快用水浇灭
B.一氧化碳还原氧化铁的实验中,可以将气体直接排放到空气中
C.发现家中天然气泄漏时,立即打开排风扇
D.发生火灾逃生时,用湿毛巾捂住口鼻,蹲下沿墙壁逃离火灾区域
9.将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是(已知:A、B、C在生成物中均为+2价)
A.放出H2的质量是B>A>C
B.金属活动性顺序是A>B>C
C.反应速率最大的是A
D.相对原子质量是C>B>A
10.Fe2O3、CuO的混合粉末8g,高温下与足量CO充分反应后,得到固体的质量可能为( )
A.6g B.5.6g C.6.4g D.8g
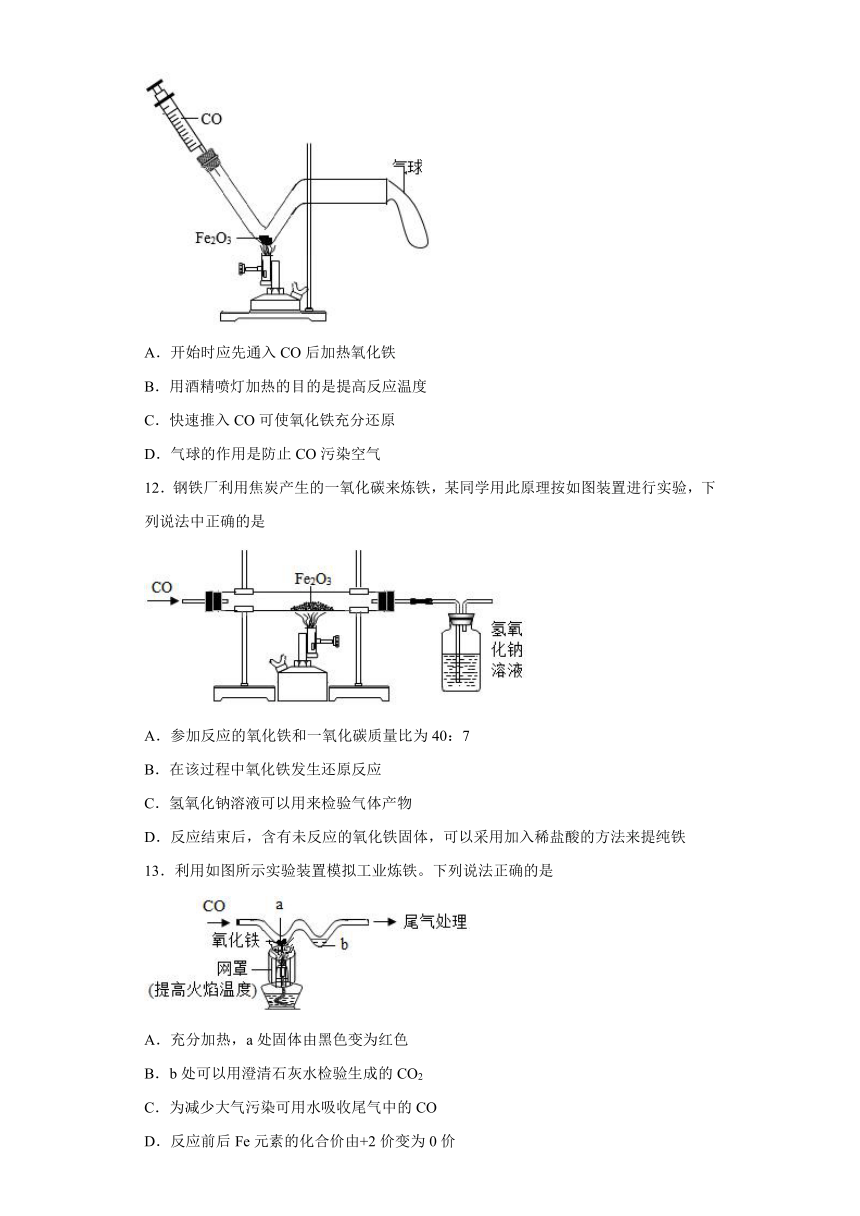
11.如图为一氧化碳还原氧化铁实验。下列说法不正确的是
A.开始时应先通入CO后加热氧化铁
B.用酒精喷灯加热的目的是提高反应温度
C.快速推入CO可使氧化铁充分还原
D.气球的作用是防止CO污染空气
12.钢铁厂利用焦炭产生的一氧化碳来炼铁,某同学用此原理按如图装置进行实验,下列说法中正确的是
A.参加反应的氧化铁和一氧化碳质量比为40:7
B.在该过程中氧化铁发生还原反应
C.氢氧化钠溶液可以用来检验气体产物
D.反应结束后,含有未反应的氧化铁固体,可以采用加入稀盐酸的方法来提纯铁
13.利用如图所示实验装置模拟工业炼铁。下列说法正确的是
A.充分加热,a处固体由黑色变为红色
B.b处可以用澄清石灰水检验生成的CO2
C.为减少大气污染可用水吸收尾气中的CO
D.反应前后Fe元素的化合价由+2价变为0价
14.下列指定反应的化学方程式正确的是
A.实验室用双氧水制氧气:
B.铜在潮湿的空气中生锈:
C.工业炼铁中一氧化碳的产生:
D.用石灰石浆处理二氧化硫:
15.在高温下,氧化铜和氧化铁的混合物3.2g与足量的一氧化碳充分反应后,固体质量减少了0.8g,则原混合物中氧化铁的质量为
A.0.8g B.1.12g C.1.6g D.2.4g
二、填空题
16.化学就在我们身边,一些物质在生产、生活中有重要的用途。现有①干冰②焦炭③氮气④氧气⑤金刚石,选择适当的物质填空(填序号)。 .
(1)可用于高温炼铁的是______________;
(2)可作高档装饰品的是______________;
(3)用于抢救病人的是______________;
(4) 可充入食品包装袋中以防腐的是______________。
17.铁元素与人类关系密切.
(1)铁是年产量最高的_________元素.
(2)元素周期表中铁元素的信息如图所示其原子的核外电子数为 ________ .
(3)铁元素在自然界中主要以Fe2O3和Fe3O4形式存在,它们属于________ .(填字母序号)
A.单质 B.氧化物 C.酸 D.碱 E.盐
(4)用磁铁矿炼铁的反应原理为(写化学方程式)________ .
(5)铁制成铁锅,主要是利用铁的延展性和________ 性.
18.按要求写出下列反应的化学方程式:
(1) 炼铁高炉内焦炭与二氧化碳反应生成一氧化碳:_________;
(2) 铁丝在氧气中剧烈燃烧:______________;
(3) 汽车尾气中有害气体主要是CO和NO,通过安装尾气催化转化器可将其转化为空气中两种无毒的气体:_____________;
(4) 氢氧化亚铁[Fe(OH)2]在潮湿的空气中会化合生成氢氧化铁[Fe(OH)3]:________。
19.高安古浮桥横亘于锦江之上,承载了一代又一代高安人的记忆。
(1)浮桥边上卖烤红薯的烤炉里飘出阵阵香味,从微观角度分析能闻到红薯香味的原因是_______________。
(2)被水冲洗的码头石块的主要成分是碳酸钙,其中所含的阳离子符号为_______________。
(3)滋滋作响的浮桥伴随着汩汩锦江水弹出美丽的乐谱,检验锦江水是硬水还是软水的方法是_______________。
(4)浮桥是由数十只木船用铁链连接起来,并将铁锚沉入水底固定而成的。请写出工业上用赤铁矿炼铁的化学方程式:_______________。
20.金属材料在工农业和人们日常生活中有着广泛的应用。回答下列各题。
(1)我国自主设计的大型客机成功试飞,首艘国产航母正式下水,标志着我国合金制造技术取得重大突破。根据所学知识回答。
①生铁和钢都是铁合金,其中含碳量较高的是_____。
②我国的钢铁产量居世界第一。写出用赤铁矿(主要成分为Fe2O3)炼铁的化学方程式:_____。
③探究铝与酸的反应前,用砂纸打磨铝条,是为了除去_____(填化学式)。
(2)在相同条件下取相同状态的Sc和Zn分别与同一种稀硫酸反应,Sc产生气泡的速率明显比Zn快,则两种金属的活动性:Sc_____(填“>”或“<”)Zn。结合上述结论判断,下列说法不正确的是_____(填字母序号)。
A.将打磨了的Sc伸入CuCl2溶液中,无明显现象
B.用Fe(NO3)2溶液、Sc(NO3)3溶液、Ag做实验,能验证Fe和Sc的金属活动性强弱
C.Sc的金属活动性强于Fe
三、实验题
21.化学小组同学用如图所示装置模拟工业炼铁,请回答下列问题:
(1)写出如图装置中玻璃管A内发生反应的现象_______,化学方程式______。
(2)从环保角度考虑,对以上装置的改进措施是______。
(3)实验加热前先通一氧化碳的目的_______。
参考答案:
1.C2.C3.D4.D5.B6.D7.A8.D9.D10.A11.C12.B13.B14.D15.C
16. ② ⑤ ④ ③
17. 金属; 26; B; 2Fe3O4+4CO3Fe+4CO2; 导热
18. CO2+C2CO 3Fe+2O2Fe3O4 2CO+2NON2+2CO2 4 Fe(OH)2+2H2O+O2═4 Fe(OH)3
19.(1)分子在不断地运动
(2)Ca2+
(3)加入肥皂水
(4)
20.(1) 生铁 3CO+Fe2O32Fe+3CO2 Al2O3
(2) > AB/BA
21.(1) 红色粉末变成黑色
(2)增加尾气处理装置(答案合理即可)
(3)排出装置中的空气,防止一氧化碳和空气混合,发生爆炸
同步练习
一、单选题
1.工业上通过反应 SiO2+2CSi+2CO↑将自然界中二氧化硅转化为硅,该反应中( )
A.一氧化碳作还原剂 B.二氧化硅发生了氧化反应
C.二氧化硅是氧化剂 D.碳发生了还原反应
2.金属是重要的资源。下列有关金属的说法错误的是
A.“湿法炼铜”的化学原理可以表示为:
B.金属与金属、金属与非金属都可能形成合金
C.工业上用一氧化碳还原氧化铁制备铁,该反应属于置换反应
D.金属钠和镁化学性质不同是由于最外层电子数不同
3.下列有关实验现象描述正确的是
A.细铁丝在氧气中燃烧,火星四射,生成白色固体
B.红磷在空气中燃烧产生大量白色烟雾
C.将一氧化碳通入灼热的氧化铁粉末,一段时间,黑色粉末变红
D.将铜丝放入硝酸银溶液中,溶液由无色变为蓝色
4.兴趣小组同学利用如图所示装置模拟工业炼铁。下列说法错误的是
A.赤铁矿的主要成分是Fe2O3
B.实验时应先通入CO再点燃酒精灯
C.充分加热后,a处固体由红棕色变为黑色
D.可用水吸收尾气中的CO
5.为适应火车提速,沪宁线上原有的短轨全部接为超长轨。在焊接过程中,工程技术人员点燃铝热剂(铝粉和氧化铁的混合物)能释放大量的能量,生成熔融状态的铁可用来连接铁轨,反应的化学方程式为,其中的还原剂为
A. B. C. D.
6.下列用途中,主要利用物质物理性质的是
A.焦炭用于炼铁 B.食品包装袋中充入氮气
C.氢气作高能燃料 D.竹炭除冰箱中的异味
7.化学研究的目的就是帮助人们认识、改造和应用物质,把金属矿物冶炼成金属就是人们利用化学方法实现物质改造的典型范例.下表中不同的金属被开发和利用的年代不同,从化学反应的角度看,决定这一年代先后顺序的关键因素是
A.金属的活动性 B.金属的导电性
C.金属的延展性 D.地壳中金属元素的含量
8.下列做法正确的是( )
A.洒出的酒精在桌面上燃烧起来,赶快用水浇灭
B.一氧化碳还原氧化铁的实验中,可以将气体直接排放到空气中
C.发现家中天然气泄漏时,立即打开排风扇
D.发生火灾逃生时,用湿毛巾捂住口鼻,蹲下沿墙壁逃离火灾区域
9.将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是(已知:A、B、C在生成物中均为+2价)
A.放出H2的质量是B>A>C
B.金属活动性顺序是A>B>C
C.反应速率最大的是A
D.相对原子质量是C>B>A
10.Fe2O3、CuO的混合粉末8g,高温下与足量CO充分反应后,得到固体的质量可能为( )
A.6g B.5.6g C.6.4g D.8g
11.如图为一氧化碳还原氧化铁实验。下列说法不正确的是
A.开始时应先通入CO后加热氧化铁
B.用酒精喷灯加热的目的是提高反应温度
C.快速推入CO可使氧化铁充分还原
D.气球的作用是防止CO污染空气
12.钢铁厂利用焦炭产生的一氧化碳来炼铁,某同学用此原理按如图装置进行实验,下列说法中正确的是
A.参加反应的氧化铁和一氧化碳质量比为40:7
B.在该过程中氧化铁发生还原反应
C.氢氧化钠溶液可以用来检验气体产物
D.反应结束后,含有未反应的氧化铁固体,可以采用加入稀盐酸的方法来提纯铁
13.利用如图所示实验装置模拟工业炼铁。下列说法正确的是
A.充分加热,a处固体由黑色变为红色
B.b处可以用澄清石灰水检验生成的CO2
C.为减少大气污染可用水吸收尾气中的CO
D.反应前后Fe元素的化合价由+2价变为0价
14.下列指定反应的化学方程式正确的是
A.实验室用双氧水制氧气:
B.铜在潮湿的空气中生锈:
C.工业炼铁中一氧化碳的产生:
D.用石灰石浆处理二氧化硫:
15.在高温下,氧化铜和氧化铁的混合物3.2g与足量的一氧化碳充分反应后,固体质量减少了0.8g,则原混合物中氧化铁的质量为
A.0.8g B.1.12g C.1.6g D.2.4g
二、填空题
16.化学就在我们身边,一些物质在生产、生活中有重要的用途。现有①干冰②焦炭③氮气④氧气⑤金刚石,选择适当的物质填空(填序号)。 .
(1)可用于高温炼铁的是______________;
(2)可作高档装饰品的是______________;
(3)用于抢救病人的是______________;
(4) 可充入食品包装袋中以防腐的是______________。
17.铁元素与人类关系密切.
(1)铁是年产量最高的_________元素.
(2)元素周期表中铁元素的信息如图所示其原子的核外电子数为 ________ .
(3)铁元素在自然界中主要以Fe2O3和Fe3O4形式存在,它们属于________ .(填字母序号)
A.单质 B.氧化物 C.酸 D.碱 E.盐
(4)用磁铁矿炼铁的反应原理为(写化学方程式)________ .
(5)铁制成铁锅,主要是利用铁的延展性和________ 性.
18.按要求写出下列反应的化学方程式:
(1) 炼铁高炉内焦炭与二氧化碳反应生成一氧化碳:_________;
(2) 铁丝在氧气中剧烈燃烧:______________;
(3) 汽车尾气中有害气体主要是CO和NO,通过安装尾气催化转化器可将其转化为空气中两种无毒的气体:_____________;
(4) 氢氧化亚铁[Fe(OH)2]在潮湿的空气中会化合生成氢氧化铁[Fe(OH)3]:________。
19.高安古浮桥横亘于锦江之上,承载了一代又一代高安人的记忆。
(1)浮桥边上卖烤红薯的烤炉里飘出阵阵香味,从微观角度分析能闻到红薯香味的原因是_______________。
(2)被水冲洗的码头石块的主要成分是碳酸钙,其中所含的阳离子符号为_______________。
(3)滋滋作响的浮桥伴随着汩汩锦江水弹出美丽的乐谱,检验锦江水是硬水还是软水的方法是_______________。
(4)浮桥是由数十只木船用铁链连接起来,并将铁锚沉入水底固定而成的。请写出工业上用赤铁矿炼铁的化学方程式:_______________。
20.金属材料在工农业和人们日常生活中有着广泛的应用。回答下列各题。
(1)我国自主设计的大型客机成功试飞,首艘国产航母正式下水,标志着我国合金制造技术取得重大突破。根据所学知识回答。
①生铁和钢都是铁合金,其中含碳量较高的是_____。
②我国的钢铁产量居世界第一。写出用赤铁矿(主要成分为Fe2O3)炼铁的化学方程式:_____。
③探究铝与酸的反应前,用砂纸打磨铝条,是为了除去_____(填化学式)。
(2)在相同条件下取相同状态的Sc和Zn分别与同一种稀硫酸反应,Sc产生气泡的速率明显比Zn快,则两种金属的活动性:Sc_____(填“>”或“<”)Zn。结合上述结论判断,下列说法不正确的是_____(填字母序号)。
A.将打磨了的Sc伸入CuCl2溶液中,无明显现象
B.用Fe(NO3)2溶液、Sc(NO3)3溶液、Ag做实验,能验证Fe和Sc的金属活动性强弱
C.Sc的金属活动性强于Fe
三、实验题
21.化学小组同学用如图所示装置模拟工业炼铁,请回答下列问题:
(1)写出如图装置中玻璃管A内发生反应的现象_______,化学方程式______。
(2)从环保角度考虑,对以上装置的改进措施是______。
(3)实验加热前先通一氧化碳的目的_______。
参考答案:
1.C2.C3.D4.D5.B6.D7.A8.D9.D10.A11.C12.B13.B14.D15.C
16. ② ⑤ ④ ③
17. 金属; 26; B; 2Fe3O4+4CO3Fe+4CO2; 导热
18. CO2+C2CO 3Fe+2O2Fe3O4 2CO+2NON2+2CO2 4 Fe(OH)2+2H2O+O2═4 Fe(OH)3
19.(1)分子在不断地运动
(2)Ca2+
(3)加入肥皂水
(4)
20.(1) 生铁 3CO+Fe2O32Fe+3CO2 Al2O3
(2) > AB/BA
21.(1) 红色粉末变成黑色
(2)增加尾气处理装置(答案合理即可)
(3)排出装置中的空气,防止一氧化碳和空气混合,发生爆炸
