第九单元金属测试题(含答案) ---2022-2023学年九年级化学鲁教版下册
文档属性
| 名称 | 第九单元金属测试题(含答案) ---2022-2023学年九年级化学鲁教版下册 |
|
|
| 格式 | docx | ||
| 文件大小 | 257.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-25 00:00:00 | ||
图片预览



文档简介
第九单元《金属》测试题
一、单选题
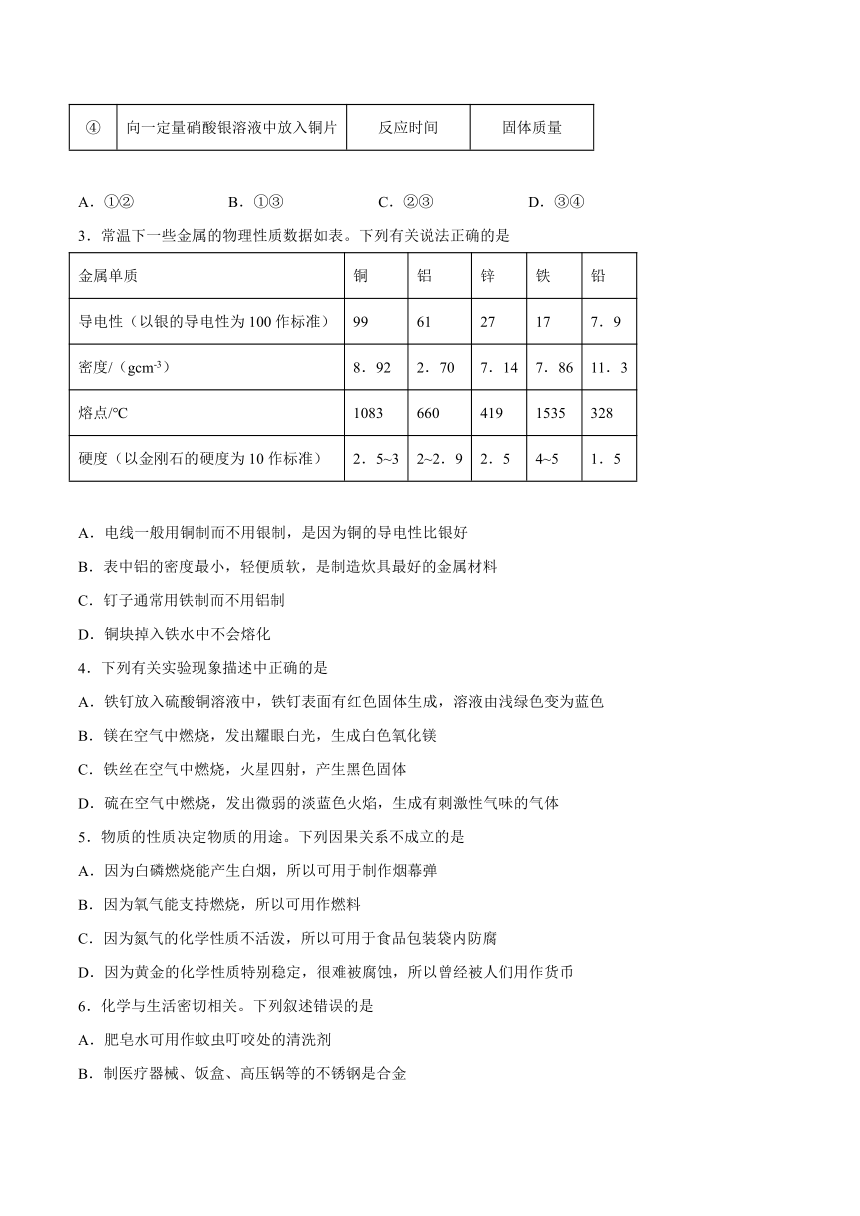
1.如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响)。则滴管和烧瓶中所用试剂可能是
甲 乙
A 稀硫酸和铜片 水和 CO2
B 双氧水和MnO2 NaOH溶液和CO2
C BaCl2溶液和稀硫酸 NaOH溶液和SO2
D H2O和NH3 硝酸银溶液和HCl
A.A B.B C.C D.D
2.下列实验内容符合坐标图所示变化趋势的是
序号 实验内容 横坐标表示的量 纵坐标表示的量
① 用过量红磷测定空气中氧气含量 时间 红磷的质量
② 过氧化氢溶液与二氧化锰制氧气 时间 二氧化锰的质量
③ 生锈铁钉放入一定量稀盐酸 加入盐酸的质量 剩余固体的质量
④ 向一定量硝酸银溶液中放入铜片 反应时间 固体质量
A.①② B.①③ C.②③ D.③④
3.常温下一些金属的物理性质数据如表。下列有关说法正确的是
金属单质 铜 铝 锌 铁 铅
导电性(以银的导电性为100作标准) 99 61 27 17 7.9
密度/(gcm-3) 8.92 2.70 7.14 7.86 11.3
熔点/℃ 1083 660 419 1535 328
硬度(以金刚石的硬度为10作标准) 2.5~3 2~2.9 2.5 4~5 1.5
A.电线一般用铜制而不用银制,是因为铜的导电性比银好
B.表中铝的密度最小,轻便质软,是制造炊具最好的金属材料
C.钉子通常用铁制而不用铝制
D.铜块掉入铁水中不会熔化
4.下列有关实验现象描述中正确的是
A.铁钉放入硫酸铜溶液中,铁钉表面有红色固体生成,溶液由浅绿色变为蓝色
B.镁在空气中燃烧,发出耀眼白光,生成白色氧化镁
C.铁丝在空气中燃烧,火星四射,产生黑色固体
D.硫在空气中燃烧,发出微弱的淡蓝色火焰,生成有刺激性气味的气体
5.物质的性质决定物质的用途。下列因果关系不成立的是
A.因为白磷燃烧能产生白烟,所以可用于制作烟幕弹
B.因为氧气能支持燃烧,所以可用作燃料
C.因为氮气的化学性质不活泼,所以可用于食品包装袋内防腐
D.因为黄金的化学性质特别稳定,很难被腐蚀,所以曾经被人们用作货币
6.化学与生活密切相关。下列叙述错误的是
A.肥皂水可用作蚊虫叮咬处的清洗剂
B.制医疗器械、饭盒、高压锅等的不锈钢是合金
C.活性炭具有除异味和杀菌作用
D.碘酒溶液常用于消毒
7.下列每组对比实验不能达到实验目的是
选项 实验设计 实验目的
实验一 实验二
A 将带火星的木条伸入装有5mL5%的过氧化氢溶液的试管中 将带火星的木条伸入装有少量红砖粉和5mL5%的过氧化氢溶液的试管中 催化剂对化学反应速率的影响
B 将铁钉放入干燥的试管中并将试管口密封 将铁钉放入装有水的试管中,使铁钉一半被水淹没 铁生锈是水和氧气共同作用的结果
C 将铁丝放入2mL10%的硫酸铜溶液中 将银丝放入2mL10%的硫酸铜溶液中 探究铁、铜、银三种金属的活动性顺序
D 将植物嫩叶浸泡在10mL蒸馏水中 取10mL蒸馏水,通入过量二氧化硫气体,再将植物嫩叶浸泡其中 酸雨危害的模拟实验
A.A B.B C.C D.D
8.下列有关金属的说法不正确的是( )
A.多数合金的抗腐蚀性能比组成它们的纯金属更好
B.防止金属锈蚀是保护金属资源的有效途径
C.回收废旧金属有利于保护环境
D.铝制品不需要涂保护层来防腐蚀,因为常温下铝不与氧气反应
9.下列物质的性质与用途对应关系正确的是
选项 性质 用途
A 镁具有银白色金属光泽 用于制作照明弹
B 一氧化碳具有可燃性 用于冶炼金属
C 武德合金熔点低 用于制作电路保险丝
D 二氧化碳不能支持燃烧 用作气体肥料
A.A B.B C.C D.D
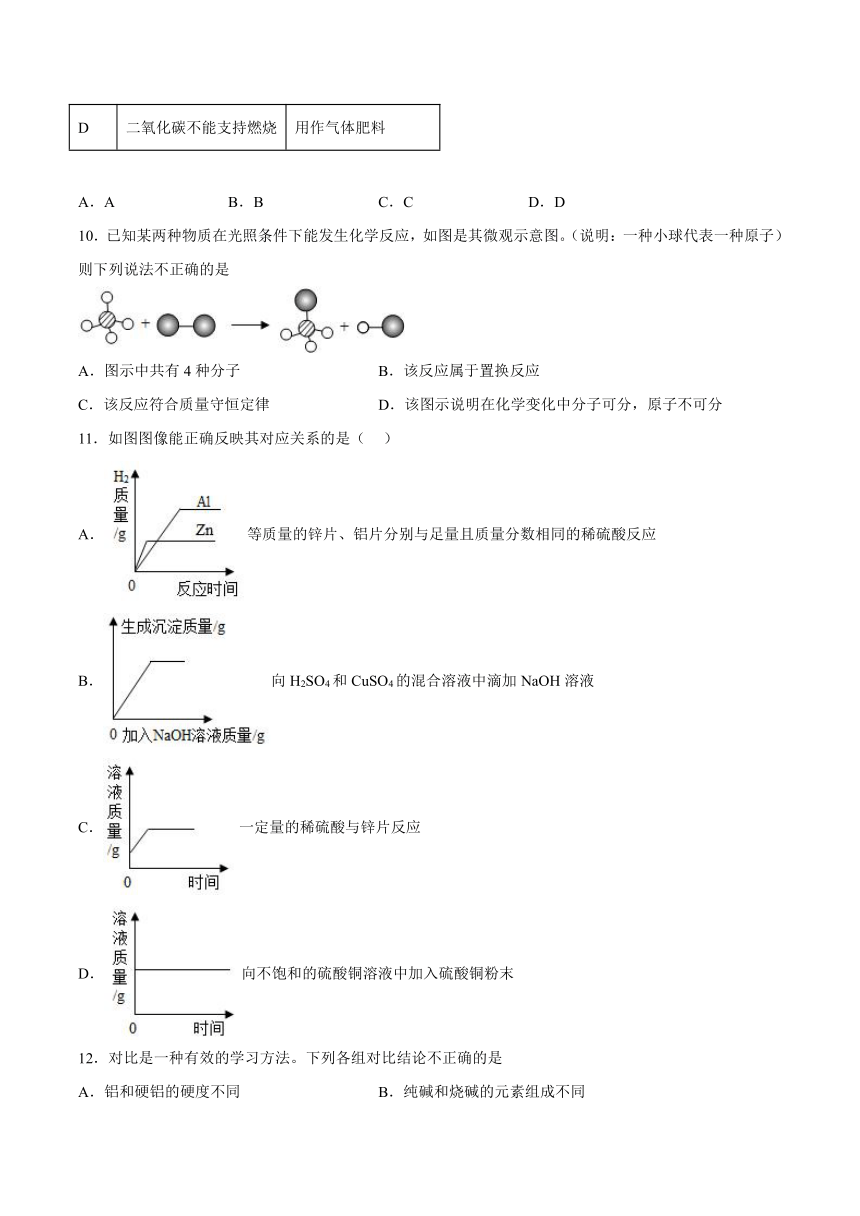
10.已知某两种物质在光照条件下能发生化学反应,如图是其微观示意图。(说明:一种小球代表一种原子)则下列说法不正确的是
A.图示中共有4种分子 B.该反应属于置换反应
C.该反应符合质量守恒定律 D.该图示说明在化学变化中分子可分,原子不可分
11.如图图像能正确反映其对应关系的是( )
A.等质量的锌片、铝片分别与足量且质量分数相同的稀硫酸反应
B.向H2SO4和CuSO4的混合溶液中滴加NaOH溶液
C.一定量的稀硫酸与锌片反应
D.向不饱和的硫酸铜溶液中加入硫酸铜粉末
12.对比是一种有效的学习方法。下列各组对比结论不正确的是
A.铝和硬铝的硬度不同 B.纯碱和烧碱的元素组成不同
C.石墨和金刚石完全燃烧的产物不同 D.浓盐酸和浓硫酸的挥发性不同
二、填空题
13.我国是钢铁大国,粗钢产量占世界的一半。工业炼铁炼钢的主要流程如下图所示:
高炉中可能发生的化学反应有:①CaCO3CaO + CO2↑ ②C+CO22CO ③C+O2CO2④3C+2Fe2O34Fe +3CO2↑ ⑤Fe2O3+3CO2Fe+3CO2
(1)反应⑤中作为还原剂的物质是____。
(2)上述反应中,属于置换反应的是(填序号)____;
(3)从以上反应中可以分析得知碳元素的化合价有____种;
(4)在转炉中将生铁转化成钢,主要利用了上述反应中的(填序号)____。
(5)月饼盒中常有一小纸包,上面标明“双吸剂”,其中盛有极细的铁粉,防止食品受潮和变质,主要是铁粉生锈时与水和____发生反应。
14.2021年5月15日,中国“天问一号”探测器成功着陆火星,它应用的新型镁锂合金材料是由西安四方超轻材料有限公司自主研发。回答下列问题:
(1)镁锂合金硬度比其纯金属的硬度___________(填“大”或“小”)。
(2)锂原子(Li)在反应中易失去1个电子形成离子,写出锂离子的符号:___________。
(3)下图1为镁在元素周期表中的部分信息,则镁的相对原子质量为________。下图2为几种粒子的结构示意图,其中属于同种元素的是_______(填序号)。与镁元素化学性质相似的是_______(填序号)。
15.过氧化氢溶液常用作消毒剂。
(1)过氧化氢溶液中起消毒作用的成分为_______(填化学式)。
(2)过氧化氢不稳定,易分解。过氧化氢常温下分解的化学方程式为_______。
(3)用3%的过氧化氢溶液对不同金属进行腐蚀性实验,结果如下:
金属种类 不锈钢 铝片 铜片
腐蚀速率(mg/h) 0.001 0.01 0.404
下列金属制品用该溶液消毒时,最容易被腐蚀的是_____(填序号)。
a.不锈钢锅 b.铝饭盒 c.铜火锅
三、推断题
16.A、B、C、D、E为初中化学常见的物质,其中A、C为金属单质,E为非金属单质,下图是它们之间的相互转化关系。请回答:
(1)反应①的基本反应类型是______。
(2)写出反应②的化学方程式______。
(3)E的化学式是______,产生无色气体E的原因是______。
(4)金属C在______的条件下容易生锈;保护金属资源的有效途径是______(只写一条)。
17.A、B、C、D、E、F、G、H、I为初中化学常见的物质,其中A是一种红棕色固体,B是能与血液中的血红蛋白结合使人中毒的气体,如图是它们之间的相互转化关系。请回答:
(1)物质D的化学式为___________,写出其中的一种用途___________。
(2)写出反应①的化学方程式 ___________ 。
(3)写出反应②的化学方程式 ___________ 。其基本反应类型是___________ 。
(4)金属C在 ___________ 的条件下容易生锈;保护金属资源的有效途径是___________(任写一条)。
四、实验题
18.为探究Fe、Cu、Ag的金属活动性强弱,某兴趣小组做了如下实验:
(1)实验前需将金属丝打磨,目的是_____。
(2)甲实验中发生反应的化学方程式为_____;乙实验中观察到的现象为_____。
(3)通过甲、乙实验探究,可得出三种金属活动性由强到弱的顺序为_____。
(4)若采用丙实验方案也可得出相同结论,则金属C是_____,A溶液与B溶液分别是_____和_____。
(5)如果只用两种金属丝和一种溶液,来探究三种金属的活动性强弱,则所需要的金属和溶液分别是_____。
19.明代宋应星所著《天工开物》中记载了我国古代的炼铁方法。现代工业利用高炉炼铁,其主要反应原理是一氧化碳与氧化铁的反应。实验室模拟高炉炼铁的实验装置如图所示。点燃酒精喷灯前,先通入一段时间CO的原因是_____;B装置中的实验现象为_____;C装置的作用是检验反应生成的气体产物,发生反应的化学方程式为_____;CO有毒,尾气的处理方法是_____。
五、计算题
20.往盛有 10g 某黄铜(Cu-Zn 合金)样品的烧杯中加入足量的稀硫酸 50g,一段时间后,发现烧杯 中剩余物质的质量为 59.8g,则:
(1)生成氢气的质量为 g;
(2)该黄铜样品中铜的质量分数(写出计算过程)。
参考答案:
1.B 2.B 3.C 4.D 5.B 6.C 7.B 8.D 9.C 10.B 11.C 12.C
13.(1)CO/一氧化碳
(2) ④
(3)3/三
(4) ③
(5)氧气/O2
14.(1)大
(2)Li+
(3) 24.31 ①④ ③
15.(1)
(2)
(3)c
16. 化合反应 H2 铁与过量稀硫酸反应产生氢气(或反应②中稀硫酸过量) 潮湿的空气中(或与空气和水同时接触) 防止金属腐蚀(或回收利用废旧金属、合理有效地开采矿物、寻找金属的代用品等)
17.(1) CO2 灭火、化工原料、植物光合作用(任写一个)
(2)
(3) 或 置换反应
(4) O2和H2O 喷漆、涂油、电镀、搪瓷等(合理即可)
18. 除去金属表面的氧化膜 Cu+2AgNO3=2Ag+Cu(NO3)2 铁丝的表面有一层红色物质,溶液由蓝色逐渐变为浅绿色 Fe>Cu>Ag Cu 硫酸亚铁溶液 硝酸银溶液 铁丝、银丝和硫酸铜溶液
19. 排尽装置中的空气,防止加热时发生爆炸 红棕色固体逐渐变为黑色 将尾气点燃(或用气球收集)
20.(1)0.2g;
(2)解:设该黄铜样品中锌的质量为x。
,x=6.5g
该黄铜样品中铜的质量分数为:=35%
一、单选题
1.如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响)。则滴管和烧瓶中所用试剂可能是
甲 乙
A 稀硫酸和铜片 水和 CO2
B 双氧水和MnO2 NaOH溶液和CO2
C BaCl2溶液和稀硫酸 NaOH溶液和SO2
D H2O和NH3 硝酸银溶液和HCl
A.A B.B C.C D.D
2.下列实验内容符合坐标图所示变化趋势的是
序号 实验内容 横坐标表示的量 纵坐标表示的量
① 用过量红磷测定空气中氧气含量 时间 红磷的质量
② 过氧化氢溶液与二氧化锰制氧气 时间 二氧化锰的质量
③ 生锈铁钉放入一定量稀盐酸 加入盐酸的质量 剩余固体的质量
④ 向一定量硝酸银溶液中放入铜片 反应时间 固体质量
A.①② B.①③ C.②③ D.③④
3.常温下一些金属的物理性质数据如表。下列有关说法正确的是
金属单质 铜 铝 锌 铁 铅
导电性(以银的导电性为100作标准) 99 61 27 17 7.9
密度/(gcm-3) 8.92 2.70 7.14 7.86 11.3
熔点/℃ 1083 660 419 1535 328
硬度(以金刚石的硬度为10作标准) 2.5~3 2~2.9 2.5 4~5 1.5
A.电线一般用铜制而不用银制,是因为铜的导电性比银好
B.表中铝的密度最小,轻便质软,是制造炊具最好的金属材料
C.钉子通常用铁制而不用铝制
D.铜块掉入铁水中不会熔化
4.下列有关实验现象描述中正确的是
A.铁钉放入硫酸铜溶液中,铁钉表面有红色固体生成,溶液由浅绿色变为蓝色
B.镁在空气中燃烧,发出耀眼白光,生成白色氧化镁
C.铁丝在空气中燃烧,火星四射,产生黑色固体
D.硫在空气中燃烧,发出微弱的淡蓝色火焰,生成有刺激性气味的气体
5.物质的性质决定物质的用途。下列因果关系不成立的是
A.因为白磷燃烧能产生白烟,所以可用于制作烟幕弹
B.因为氧气能支持燃烧,所以可用作燃料
C.因为氮气的化学性质不活泼,所以可用于食品包装袋内防腐
D.因为黄金的化学性质特别稳定,很难被腐蚀,所以曾经被人们用作货币
6.化学与生活密切相关。下列叙述错误的是
A.肥皂水可用作蚊虫叮咬处的清洗剂
B.制医疗器械、饭盒、高压锅等的不锈钢是合金
C.活性炭具有除异味和杀菌作用
D.碘酒溶液常用于消毒
7.下列每组对比实验不能达到实验目的是
选项 实验设计 实验目的
实验一 实验二
A 将带火星的木条伸入装有5mL5%的过氧化氢溶液的试管中 将带火星的木条伸入装有少量红砖粉和5mL5%的过氧化氢溶液的试管中 催化剂对化学反应速率的影响
B 将铁钉放入干燥的试管中并将试管口密封 将铁钉放入装有水的试管中,使铁钉一半被水淹没 铁生锈是水和氧气共同作用的结果
C 将铁丝放入2mL10%的硫酸铜溶液中 将银丝放入2mL10%的硫酸铜溶液中 探究铁、铜、银三种金属的活动性顺序
D 将植物嫩叶浸泡在10mL蒸馏水中 取10mL蒸馏水,通入过量二氧化硫气体,再将植物嫩叶浸泡其中 酸雨危害的模拟实验
A.A B.B C.C D.D
8.下列有关金属的说法不正确的是( )
A.多数合金的抗腐蚀性能比组成它们的纯金属更好
B.防止金属锈蚀是保护金属资源的有效途径
C.回收废旧金属有利于保护环境
D.铝制品不需要涂保护层来防腐蚀,因为常温下铝不与氧气反应
9.下列物质的性质与用途对应关系正确的是
选项 性质 用途
A 镁具有银白色金属光泽 用于制作照明弹
B 一氧化碳具有可燃性 用于冶炼金属
C 武德合金熔点低 用于制作电路保险丝
D 二氧化碳不能支持燃烧 用作气体肥料
A.A B.B C.C D.D
10.已知某两种物质在光照条件下能发生化学反应,如图是其微观示意图。(说明:一种小球代表一种原子)则下列说法不正确的是
A.图示中共有4种分子 B.该反应属于置换反应
C.该反应符合质量守恒定律 D.该图示说明在化学变化中分子可分,原子不可分
11.如图图像能正确反映其对应关系的是( )
A.等质量的锌片、铝片分别与足量且质量分数相同的稀硫酸反应
B.向H2SO4和CuSO4的混合溶液中滴加NaOH溶液
C.一定量的稀硫酸与锌片反应
D.向不饱和的硫酸铜溶液中加入硫酸铜粉末
12.对比是一种有效的学习方法。下列各组对比结论不正确的是
A.铝和硬铝的硬度不同 B.纯碱和烧碱的元素组成不同
C.石墨和金刚石完全燃烧的产物不同 D.浓盐酸和浓硫酸的挥发性不同
二、填空题
13.我国是钢铁大国,粗钢产量占世界的一半。工业炼铁炼钢的主要流程如下图所示:
高炉中可能发生的化学反应有:①CaCO3CaO + CO2↑ ②C+CO22CO ③C+O2CO2④3C+2Fe2O34Fe +3CO2↑ ⑤Fe2O3+3CO2Fe+3CO2
(1)反应⑤中作为还原剂的物质是____。
(2)上述反应中,属于置换反应的是(填序号)____;
(3)从以上反应中可以分析得知碳元素的化合价有____种;
(4)在转炉中将生铁转化成钢,主要利用了上述反应中的(填序号)____。
(5)月饼盒中常有一小纸包,上面标明“双吸剂”,其中盛有极细的铁粉,防止食品受潮和变质,主要是铁粉生锈时与水和____发生反应。
14.2021年5月15日,中国“天问一号”探测器成功着陆火星,它应用的新型镁锂合金材料是由西安四方超轻材料有限公司自主研发。回答下列问题:
(1)镁锂合金硬度比其纯金属的硬度___________(填“大”或“小”)。
(2)锂原子(Li)在反应中易失去1个电子形成离子,写出锂离子的符号:___________。
(3)下图1为镁在元素周期表中的部分信息,则镁的相对原子质量为________。下图2为几种粒子的结构示意图,其中属于同种元素的是_______(填序号)。与镁元素化学性质相似的是_______(填序号)。
15.过氧化氢溶液常用作消毒剂。
(1)过氧化氢溶液中起消毒作用的成分为_______(填化学式)。
(2)过氧化氢不稳定,易分解。过氧化氢常温下分解的化学方程式为_______。
(3)用3%的过氧化氢溶液对不同金属进行腐蚀性实验,结果如下:
金属种类 不锈钢 铝片 铜片
腐蚀速率(mg/h) 0.001 0.01 0.404
下列金属制品用该溶液消毒时,最容易被腐蚀的是_____(填序号)。
a.不锈钢锅 b.铝饭盒 c.铜火锅
三、推断题
16.A、B、C、D、E为初中化学常见的物质,其中A、C为金属单质,E为非金属单质,下图是它们之间的相互转化关系。请回答:
(1)反应①的基本反应类型是______。
(2)写出反应②的化学方程式______。
(3)E的化学式是______,产生无色气体E的原因是______。
(4)金属C在______的条件下容易生锈;保护金属资源的有效途径是______(只写一条)。
17.A、B、C、D、E、F、G、H、I为初中化学常见的物质,其中A是一种红棕色固体,B是能与血液中的血红蛋白结合使人中毒的气体,如图是它们之间的相互转化关系。请回答:
(1)物质D的化学式为___________,写出其中的一种用途___________。
(2)写出反应①的化学方程式 ___________ 。
(3)写出反应②的化学方程式 ___________ 。其基本反应类型是___________ 。
(4)金属C在 ___________ 的条件下容易生锈;保护金属资源的有效途径是___________(任写一条)。
四、实验题
18.为探究Fe、Cu、Ag的金属活动性强弱,某兴趣小组做了如下实验:
(1)实验前需将金属丝打磨,目的是_____。
(2)甲实验中发生反应的化学方程式为_____;乙实验中观察到的现象为_____。
(3)通过甲、乙实验探究,可得出三种金属活动性由强到弱的顺序为_____。
(4)若采用丙实验方案也可得出相同结论,则金属C是_____,A溶液与B溶液分别是_____和_____。
(5)如果只用两种金属丝和一种溶液,来探究三种金属的活动性强弱,则所需要的金属和溶液分别是_____。
19.明代宋应星所著《天工开物》中记载了我国古代的炼铁方法。现代工业利用高炉炼铁,其主要反应原理是一氧化碳与氧化铁的反应。实验室模拟高炉炼铁的实验装置如图所示。点燃酒精喷灯前,先通入一段时间CO的原因是_____;B装置中的实验现象为_____;C装置的作用是检验反应生成的气体产物,发生反应的化学方程式为_____;CO有毒,尾气的处理方法是_____。
五、计算题
20.往盛有 10g 某黄铜(Cu-Zn 合金)样品的烧杯中加入足量的稀硫酸 50g,一段时间后,发现烧杯 中剩余物质的质量为 59.8g,则:
(1)生成氢气的质量为 g;
(2)该黄铜样品中铜的质量分数(写出计算过程)。
参考答案:
1.B 2.B 3.C 4.D 5.B 6.C 7.B 8.D 9.C 10.B 11.C 12.C
13.(1)CO/一氧化碳
(2) ④
(3)3/三
(4) ③
(5)氧气/O2
14.(1)大
(2)Li+
(3) 24.31 ①④ ③
15.(1)
(2)
(3)c
16. 化合反应 H2 铁与过量稀硫酸反应产生氢气(或反应②中稀硫酸过量) 潮湿的空气中(或与空气和水同时接触) 防止金属腐蚀(或回收利用废旧金属、合理有效地开采矿物、寻找金属的代用品等)
17.(1) CO2 灭火、化工原料、植物光合作用(任写一个)
(2)
(3) 或 置换反应
(4) O2和H2O 喷漆、涂油、电镀、搪瓷等(合理即可)
18. 除去金属表面的氧化膜 Cu+2AgNO3=2Ag+Cu(NO3)2 铁丝的表面有一层红色物质,溶液由蓝色逐渐变为浅绿色 Fe>Cu>Ag Cu 硫酸亚铁溶液 硝酸银溶液 铁丝、银丝和硫酸铜溶液
19. 排尽装置中的空气,防止加热时发生爆炸 红棕色固体逐渐变为黑色 将尾气点燃(或用气球收集)
20.(1)0.2g;
(2)解:设该黄铜样品中锌的质量为x。
,x=6.5g
该黄铜样品中铜的质量分数为:=35%
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
